基于网络药理学探讨健脾化浊调脂方治疗动脉粥样硬化合并肠道菌群失调的机制
2022-12-04黄浪浪王建安刘言薇刘中勇
黄浪浪, 徐 驲, 王建安, 刘言薇*, 万 强, 刘中勇*
(1.江西中医药大学,江西 南昌 330004;2.江西中医药大学附属医院,江西 南昌 330006)
动脉粥样硬化是多种心脑血管疾病的病理基础,其主要病理特点是脂质池和纤维帽的粥样硬化斑块的形成。斑块本身不仅可以堵塞血管腔引起大中动脉的缺血性改变,还能因突然破裂诱发血栓导致急性心脑血管事件,在全球引起较高的死亡率和社会压力[1]。解释动脉粥样硬化的发病机制学说存在多种,包括脂质浸润学说、炎症反应学说、氧化应激学说等[2],但任何学说均无法单独全面地解释动脉粥样硬化的形成机制。肠道菌群的组分和功能稳定对于维持肠道正常生理功能及机体免疫防御有着重要作用[3]。越来越多证据表明,肠道菌群失调能通过参与调节人体胆固醇代谢、氧化应激和炎症等方面,影响着动脉粥样硬化的发生与发展。因此,积极研究动脉粥样硬化的形成机制,开发有效防治动脉粥样硬化的药物,仍是研究热点。
健脾化浊调脂方是江西中医药大学附属医院心血管病科专科经验方,由刘中勇教授基于“浊”的理论精心研制而成,运用于临床二十余年,具有健脾理气、运化痰浊、活血祛瘀之效,已获得国家专利(专利号ZL201510430075.8)。课题组前期研究表明,健脾化浊调脂方能通过改善血脂、降低血清炎性因子、抑制血管平滑肌增殖、保护血管内皮细胞、改变肠道菌群结构等,达到抗动脉粥样硬化的作用[4-7]。该方临床疗效确切,不良反应低,具有较好的应用前景,但其对于调节肠道菌群失调所致动脉粥样硬化的分子机制尚不十分清楚。
网络药理学能进一步系统的理解中药的潜在作用机制,从而了解药物对疾病的影响情况,与中医的整体观念相吻合[8]。本研究通过网络药理学的方法,探讨健脾化浊调脂方活性成分,构建健脾化浊调脂方治疗肠道菌群失调引起的动脉粥样硬化的多层次生物信息网络,筛选出关键靶点和通路,同时借助分子对接技术和高胆碱饮食诱导的动脉粥样硬化小鼠模型验证,为进一步开展健脾化浊调脂方治疗肠道菌群失调引起的动脉粥样硬化的药理作用机制提供研究基础和理论依据。
1 材料与方法
1.1 活性成分筛选 采用中药系统药理学分析平台(TCMSP,http://tcmspw.com/tcmsp.php)、BATMAN-TCM数据库(http://bionet.ncpsb.org/batman-tcm/),以“党参”“白术”“茯苓”“陈皮”“荷叶”“薏苡仁”“丝瓜络”“木香”“砂仁”“丹参”“麦芽”“山楂”“泽泻”为关键词,获取活性成分信息。将TCMSP数据库毒药物动力学(ADME)参数设置为口服生物利用度(OB)≥30%、类药性(DL)≥0.18,BATMAN-TCM数据库参数设置为score cutoff≥20、adjustedP-value<0.05,获取活性成分群。
1.2 作用靶点及动脉粥样硬化、肠道菌群疾病靶点预测 采用TCMSP、BATMAN-TCM、DrugBank(https://www.drugbank.ca/)和Uniport(https://www.uniprot.org/)数据库,预测并筛选出符合“1.1”项下标准的作用靶点,并将其蛋白和基因信息标准化为相应基因简称。采用GeneCards(https://www.genecards.org/)数据库,以“atherosclerosis”“intestinal flora”为关键词检索动脉粥样硬化和肠道菌群的靶点基因,再采用Venny平台筛选出药物活性成分与疾病的共同靶点,得到健脾化浊调脂方治疗动脉粥样硬化合并肠道菌群失调的靶点。
1.3 活性成分-疾病靶点网络、蛋白互作网络构建及关键靶点筛选 将活性成分与疾病靶点导入Cytoscape 3.8.1软件(http://www.cytoscape.org/),构建靶点网络,并将结果可视化。将“1.2”项下共同靶点输入STRING数据库(https://string-db.org/),物种设置为“Homosapiens”,构建靶点蛋白-蛋白相互作用(PPI)网络图。采用Cytoscape软件中的CytoNCA插件对PPI网络进行拓扑学参数分析,根据介度中心性(betweeness centrality,BC)、接近中心性(closeness centrality,CC)、度中心性(degree centrality,DC)、特征向量中心性(eigenvector centrality,EC)、网络中心性(network centrality,NC)、局部边连通性(LAC)进行筛选,筛选标准为6个参数数值均大于所有节点中位数,连续筛选2次后得到的靶点作为关键靶点。
1.4 关键靶点富集分析 采用DAVID数据库(https://david.ncifcrf.gov/)上传健脾化浊调脂方对动脉粥样硬化合并肠道菌群失调作用的靶点基因名称列表,经数据库检索和转化操作进行GO富集(包括分子功能、生物过程和细胞成分)和KEGG通路富集分析。
1.5 关键靶点分子对接验证 分别从PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)、RCSB PDB数据库(http://www.rcsb.org/)中获取排名前3的活性成分3D结构及所需靶标蛋白的受体SDF格式文件,采用AutoDockTools 1.5.6软件对受体进行去水、加氢处理,并计算其电荷,最后转换为pdbqt格式。利用Pymol软件进行蛋白小分子结构处理,最后由AutoDock vina软件完成分子对接。
1.6 动物实验验证
1.6.1 动物 8周龄SPF级雄性C57BL/6J小鼠20只、ApoE-/-小鼠60只,体质量(20±2)g,购于邳州市东方养殖有限公司,实验动物生产许可证号SCXK(苏)2017-0003,饲养条件为温度20~26 ℃,相对湿度40%~70%,自由饮食饮水。本研究获得江西中医药大学动物实验伦理委员会批准同意。
1.6.2 试剂与仪器 健脾化浊调脂组方药材饮片由江西中医药大学附属医院提供,经江西中医药大学附属医院刘中勇主任中医师鉴定为正品,符合2020年版《中国药典》标准,按常规方法制成混合浓缩药液,生药量2 g/mL,保存于4 ℃冰箱中。氯化胆碱(美国Sigma公司,批号C7017);氨苄青霉素、硫酸新霉素、万古霉素、甲硝唑(上海源叶生物科技有限公司,批号S17018、S17028、S17059、S17078);IL-1β(北京博奥森生物技术有限公司,批号bs-0812R);PTGS2抗体、c-Jun 抗体(美国Affinity公司,批号AF7003、AF6090);β-肌动蛋白(β-actin)抗体、辣根酶标记山羊抗兔IgG(H+L)(北京中杉金桥生物技术有限公司,批号ATRDE0701、ZB-2301);苏木素(武汉博士德生物工程有限公司,批号AR1180-1);DAB显色试剂盒、中性树脂、BCA蛋白定量试剂盒(北京康为世纪生物科技有限公司,批号CW0125、CW0136、CW0014S)。显微镜(日本Olympus公司);蛋白垂直电泳仪(北京六一生物科技有限公司);超高灵敏度化学发光成像系统(美国Bio-Rad公司)。
史东门风格图案的特点是主要表现真实的美国西部风情,人物的表情动态、动物的毛发和植物组合刻画得都要求精细写实。
1.6.3 造模、分组与给药 ApoE-/-小鼠在基础饮食的同时,给予1%胆碱以建立动脉粥样硬化合并肠道菌群失调动物模型。将20只C57BL/6J小鼠随机分为空白对照组、氯化胆碱对照组,每组10只,空白对照组给予基础饲料,氯化胆碱对照组在基础饲料基础上灌胃给予1%氯化胆碱;将60只ApoE-/-小鼠随机分为ApoE-/-对照组(基础饲料),模型组(基础饲料+灌胃给予1%氯化胆碱),抗生素组(基础饲料+灌胃给予1%氯化胆碱和广谱抗生素),健脾化浊调脂方低、中、高剂量组(基础饲料+灌胃给予1%氯化胆碱和健脾化浊调脂方药液9.49、18.98、37.96 g/kg),造模周期16周,其中广谱抗生素配方为0.5 g/L万古霉素、1.0 g/L氨苄青霉素、1.0 g/L甲硝唑、1.0 g/L 硫酸新霉素,健脾化浊调脂方中剂量根据人和动物体表面积换算临床等效剂量。
1.6.4 免疫组织化学法检测IL-1β表达 ApoE-/-小鼠主动脉石蜡切片经烤片、脱蜡、水化后,加入柠檬酸缓冲液进行抗原修复,3%双氧水去除内源性过氧化物酶,滴加一抗IL-1β(1∶200)在4 ℃下孵育过夜,加二抗(1∶200)在室温下孵育30 min,DAB显色后苏木精复染,脱水,透明,封片,在显微镜下观察,并记录实验结果。
1.6.5 蛋白免疫印迹法检测PTGS2、c-Jun蛋白表达 取ApoE-/-小鼠主动脉适量,加入蛋白裂解液,充分研磨,离心后采用BCA蛋白定量测定法对上清液蛋白浓度进行检测,样品经10% SDS-PAGE电泳分离,转至PVDF膜,5%脱脂奶粉封闭2 h,加入一抗在4 ℃下孵育过夜,TBST洗膜3次,加入二抗(1∶2 000)在室温下孵育2 h,膜上滴加ECL曝光液,在凝胶成像系统中曝光。以β-actin蛋白为参照,采用Image J软件分析各抗体条带灰度值。

2 结果
2.1 活性成分筛选 从TCMSP、BATMAN-TCM数据库平台中共获得1 042种活性成分,经筛选后得到212种,其中党参21种,白术7种,茯苓15种,陈皮5种,荷叶15种,薏苡仁9种,丝瓜络1种,木香6种,砂仁10种,丹参65种,麦芽18种,山楂30种,泽泻10种,去除重复值后最终得到144种。
2.2 作用靶点筛选 在TCMSP、BATMAN-TCM、Uniport数据库平台上继续查询活性成分靶点信息,去除重复值后得到649个靶点。根据GeneCards人类基因组数据库检索与人类相关的动脉粥样硬化、肠道菌群失调的治疗靶点,分别得到4 481、354个,采用Venny平台对相关靶点取交集,最终得到46个,见图1。
2.3 活性成分-疾病靶点网络 图2显示,144种活性成分通过调控46个靶点来治疗动脉粥样硬化合并肠道菌群失调,其中quercetin可作用于ESR1、ESR2等21个靶点,而ESR1又能与quercetin、beta-sitosterol等124个化合物相连接,表明健脾化浊调脂方治疗本病时具有多重效应。
2.5 GO功能及KEGG通路富集分析 以P<0.05为筛选条件,共得到2 095个GO条目、144条KEGG通路,其中GO条目包括生物过程(biological process,BP)1 971条、细胞成分(cell component,CC)18条、分子功能(molecular function,MF)106条,各取显著性排名前10者制作柱状图,见图5,可知靶点生物过程主要涉及活性氧代谢过程、类固醇代谢过程、炎症反应的调节等;细胞成分主要与膜筏、膜微域等有关;分子功能主要涉及血红素结合、四吡咯结合、RNA聚合酶Ⅱ转录因子结合等。KEGG通路富集主要涉及Th17细胞分化、IL-17信号通路、催乳素信号通路、T细胞受体信号通路、肿瘤坏死因子信号通路等,取显著性排名前30者制作气泡图,见图6。
2.6 核心活性成分与关键靶点的分子对接 将方中作用最强(即为核心)的6种活性成分quercetin(槲皮素)、methylheptenone(甲基庚烯酮)、luteolin(木犀草素)、kaempferol(山柰酚)、tanshinone iia(丹参酮ⅡA)、beta-sitosterol(β-谷甾醇)和关键靶标蛋白(IL10、JUN、INS、TP53、PTGS2、TNF)进行分子对接,结果见表1、图7。图7显示,5种成分与PTGS2的结合活性最好,而β-谷甾醇与TNF的结合活性最好。再取与每个关键靶标蛋白结合最强的活性成分进行可视化处理,结果见图8。
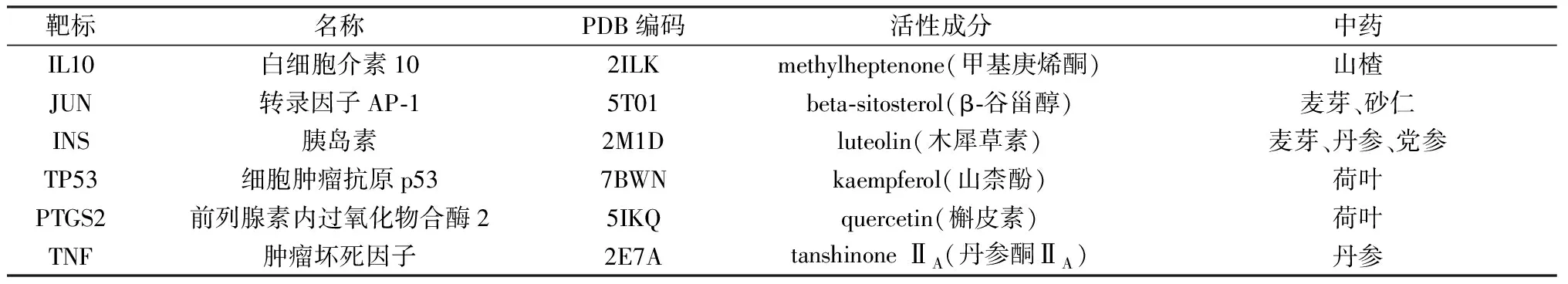
表1 核心活性成分与关键靶点的相关信息
2.7 健脾化浊调脂方对ApoE-/-小鼠主动脉IL-1β表达的影响 与空白对照组比较,模型组ApoE-/-小鼠主动脉IL-1β表达升高(P<0.01);与模型组比较,抗生素组、健脾化浊调脂方各剂量组ApoE-/-小鼠主动脉IL-1β表达降低(P<0.01);与健脾化浊调脂方低剂量组比较,健脾化浊调脂方高剂量组ApoE-/-小鼠主动脉IL-1β表达降低(P<0.01),见图9。
2.8 健脾化浊调脂方对ApoE-/-小鼠主动脉PTGS2、c-Jun表达的影响 与空白对照组比较,模型组ApoE-/-小鼠主动脉PTGS2、c-Jun表达升高(P<0.01);与模型组比较,抗生素组、健脾化浊调脂方各剂量组ApoE-/-小鼠主动脉PTGS2、c-Jun表达降低(P<0.01),见图10。
3 讨论
中医无“动脉粥样硬化”病名,根据其临床症状、病理变化等,可归属于“脉痹”等范畴。本病病位在心,但与脾脏密切相关。脾主运化,为气血生化之源,脾气旺则外邪难侵,脾的正常生理功能和抗邪能力与肠道菌群调节机体代谢和免疫防御功能相似;此外,肠道中的微生物直接参与水谷精微的消化吸收,因而维持肠道微生物稳态是“脾主运化”功能正常的重要体现。脾虚气弱,气血、水谷精微输布障碍,致痰瘀互结,浊毒内生,日久则引起动脉粥样硬化的发生。健脾化浊调脂方由异功散加减而成,具有醒脾助运,化浊祛瘀,补而不滞的优点。方中党参、白术、茯苓、薏苡仁等健脾药物中所含有的多糖,可促进肠道内益生菌生长,进而维持肠道菌群的稳态[9]。
本研究采用网络药理学筛选得到,健脾化浊调脂方活性成分144个,对应作用靶点46个。其中,槲皮素不仅能通过抑制脂质过氧化、蛋白质氧化和酶促反应,抑制氧化应激反应的发生;还能通过增加肠道短链脂肪酸的浓度,调节Firmicutes和Actinobacteria的丰度来降低动脉粥样硬化脂质代谢产物的水平,从而抑制动脉粥样硬化的进展[10-11]。木犀草素是一种常见的类黄酮,具有扩张血管和保护血管的双重生物活性,能有效保护血管内皮免受氧化应激损伤,还能通过抑制信号转导和转录激活因子3减少oxLDL诱导的炎症反应[12]。丹参酮ⅡA可以下调CD36和MKK4/JNK2信号通路,从而抑制血小板活化,防止血栓形成[13]。此外,还有一些尚未被报道的生物过程和活性成分,这些生物过程和活性成分的功效将成为未来研究健脾化浊调脂方对动脉粥样硬化合并肠道菌群失调影响的潜在方向。
通过对46个靶点的PPI网络进行拓扑分析,IL10、JUN、INS、TP53、PTGS2、TNF等靶点是健脾化浊调脂方治疗动脉粥样硬化合并肠道菌群失调的关键靶点。肠道菌群通过在体内参与蛋白质、膳食纤维、胆碱等营养物质的代谢,产生氧化三甲胺(TMAO)、短链脂肪酸(SCFAs)和胆汁酸(BAs)等代谢物影响动脉粥样硬化的发生发展。TMAO能上调巨噬细胞清道夫受体,导致巨噬细胞胆固醇积累和泡沫细胞形成,促进血管斑块的形成,并通过释放炎性细胞因子,诱导血管炎性反应;还能影响胰岛素抵抗,增强血小板高反应性,促进血小板聚集,增加血栓形成[14-17]。SCFAs主要是乙酸、丙酸和丁酸,可以通过激活细胞上的G蛋白偶联受体41和43,或通过抑制组蛋白去乙酰化,调节激素分泌,影响机体脂质代谢和炎症反应[18-19]。研究表明,丁酸可以调节肠道紧密连接蛋白Occludin和ZO-1的表达,减少血液循环中内毒素和IL-1β等炎症因子的水平,抑制动脉粥样硬化斑块形成[20]。胆汁酸是内源性G蛋白偶联受体5(TGR5)的配体,通过调控脂肪、糖、能量的代谢及炎症反应,在动脉粥样硬化发生发展中扮演了重要角色。巨噬细胞上的TGR5受体被激活,通过TGR5-cAMP信号通路抑制IκB激酶的磷酸化,降低NF-κB的活性,增加IL-10的产生,抑制单核细胞与内皮细胞粘附[21]。以上研究结果表明,肠道菌群可以通过NF-κB信号通路、cAMP信号通路等影响动脉粥样硬化的形成。通过KEGG通路分析发现,健脾化浊调脂方治疗动脉粥样硬化合并肠道菌群失调的相关靶点皆可富集到上述通路,说明健脾化浊调脂方可能通过调节相关通路,从而发挥抑制肠道菌群失调所致动脉粥样硬化的功效。
为了验证网络药理学分析结果,采用动物实验验证IL-1β和分子对接结果较好的PTGS2以及JUN蛋白表达,旨在说明健脾化浊调脂方能通过调节肠道菌群、抑制炎症反应等信号通路干预动脉粥样硬化形成。本研究利用网络药理学的方法初步从健脾化浊调脂方中筛选出活性成分、作用靶点、以及治疗疾病的关键通路,并对关键靶点进行实验验证,可为研究探索健脾化浊调脂方调节肠道菌群失调、抗动脉粥样硬化的作用机制提供依据。
