心宝丸质量标准的提高
2022-12-03吴丽琼林琼英庄伟洪蔡荣钦
吴丽琼 林琼英 庄伟洪 蔡荣钦
(广东心宝药业科技有限公司, 广东 广州510535)
心宝丸是由洋金花、人参、肉桂、附子、鹿茸、冰片、人工麝香、三七、蟾酥9 味药材组成的中药制剂,临床上广泛用于病态窦房结综合征、慢性心功能不全、心肌缺血、心率失常等心脏疾病的治疗,效果显著,不良反应少,深受医师和患者认可[1],近年来研究发现,该制剂联合西药治疗慢性心力衰竭合并心动过缓时具有理想疗效[2⁃8],并且临床上辅以综合护理[9]或联用功能相近的中成药时也能提高药物临床疗效[10⁃11],在社会老龄化趋势下其市场潜力和应用前景突出。然而,现阶段心宝丸执行标准仅设置【性状】、【鉴别】、【检查】 等质量控制项目,缺少含量测定项,而且随着2020 年版《中国药典》对相关药材质控要求的提高,上述标准部分鉴别项相对滞后,专属性差,无法对该制剂质量进行有效控制[12⁃14],亟待提高。
国家食品药品监督管理局数据库信息显示,心宝丸共有2 个国药准字,即Z44021843(广东心宝药业科技有限公司)、Z44022728(广东太安堂药业股份有限公司),故本实验以上述2 家公司产品为研究对象,通过TLC、GC、HPLC 法进行定性鉴别和含量测定,以期为该制剂质量标准提高提供参考。
1 材料
GC⁃2014 气相色谱仪(配置氢火焰离子检测器)、LC⁃20AT 高效液相色谱仪(日本岛津公司);Agilent 1260 高效液相色谱仪,配置Agilent Open LAB 色谱工作站(版本号2.1.0)(美国Agilent 公司);AL204、MS105DU、ME303电子分析天平(瑞士梅特勒⁃托利多公司);HNY⁃350 L 超声波清洗器(华南超声设备有限公司)。聚乙二醇(PEG⁃20M)Rtx®⁃Wax 毛细管柱(30 m×0.25 mm×0.25 μm);Phenomenex Gemini C18色谱柱(250 mm×4.6 mm,5 μm);中普红RD⁃C18色谱柱(250 mm×4.6 mm,5 μm);Agilent EC⁃C18色谱柱(150 mm×4.6 mm,4 μm)。预制硅胶G 薄层板(青岛海洋化工有限公司、德国Macherey⁃Nagel 公司);硅胶G 薄层板(自制)。乙腈为色谱纯;其他试剂均为分析纯;水为超纯水。
硫酸阿托品(批号100040⁃200510)、氢溴酸东莨菪碱(批号100049⁃201009)、龙脑(批号110881⁃201508)、麝香酮(批号110719⁃201215)、桂皮醛(批号110710⁃201720)、人参皂苷Rg1(批号110703⁃201731)、人参皂苷Re(批号110754⁃201626)、人参皂苷Rb1(批号110704⁃201726)对照品及洋金花对照药材(批号121058⁃200503)(中国食品药品检定研究院)。洋金花、冰片、肉桂、人工麝香阴性样品(批号20191217)及人参、三七阴性样品(批号20171217)(广东心宝药业科技有限公司)。心宝丸(批号20180301、20180501、20190702、20190901、20190902、20190903、20190904、20190905、20190907、20190908,用于TLC 定性鉴别;批号20171004、20180301、20180501、20190701、20190702、20190901、20190902、20190903、20190904、20190907,用于GC 定性鉴别;批号20160101、20160803、20160909、20161009、20170405、20170810、20171004、20171005、20171006、20180301,用于HPLC 含量测定,均由广东心宝药业科技有限公司生产。批号C20170105、C20170712、C20171104、C20180104、C20180501、C20180901、C20181202、C20190101、C20190607、C20191216,用于TLC、GC 定性鉴别;批号C20180203、C20180602、C20181108、C20190204、C20190602、C20190801、C20191008、C2002003、C2005052、C2005053,用于HPLC 含量测定,均由广东太安堂药业股份有限公司生产)。
2 方法与结果
2.1 定性鉴别
2.1.1 TLC 法(洋金花)
2.1.1.1 供试品溶液制备 取本品2 g,研细,加乙酸乙酯⁃无水乙醇⁃氨水(100∶5∶1)25 mL,超声(400 W、40 kHz)处理30 min,滤过,滤液蒸干,加1 mL 甲醇溶解,即得。
2.1.1.2 对照药材溶液制备 取洋金花对照药材1 g,加乙酸乙酯⁃无水乙醇⁃氨 水(100∶5∶1)25 mL,超 声(400 W、40 kHz)处理30 min,滤过,滤液蒸干,加1 mL甲醇溶解,即得。
2.1.1.3 对照品溶液制备 取硫酸阿托品、氢溴酸东莨菪碱对照品适量,加甲醇制成每1 mL 含两者各4 mg 的溶液,即得。
2.1.1.4 阴性样品溶液制备 取缺洋金花的阴性样品2 g,按“2.1.1.2”项下方法制备,即得。
2.1.1.5 结果分析 吸取对照药材溶液5 μL,对照品溶液各1 μL,供试品、阴性样品溶液各10 μL,分别点于同一硅胶G 薄层板上,以乙酸乙酯⁃甲醇⁃氨水(17∶2∶1)为展开剂,展开后取出,晾干,于日光下检视,结果见图1。由此可知,供试品溶液在对照药材、对照品溶液相应位置上显相同颜色斑点,阴性无干扰,表明该方法专属性良好。
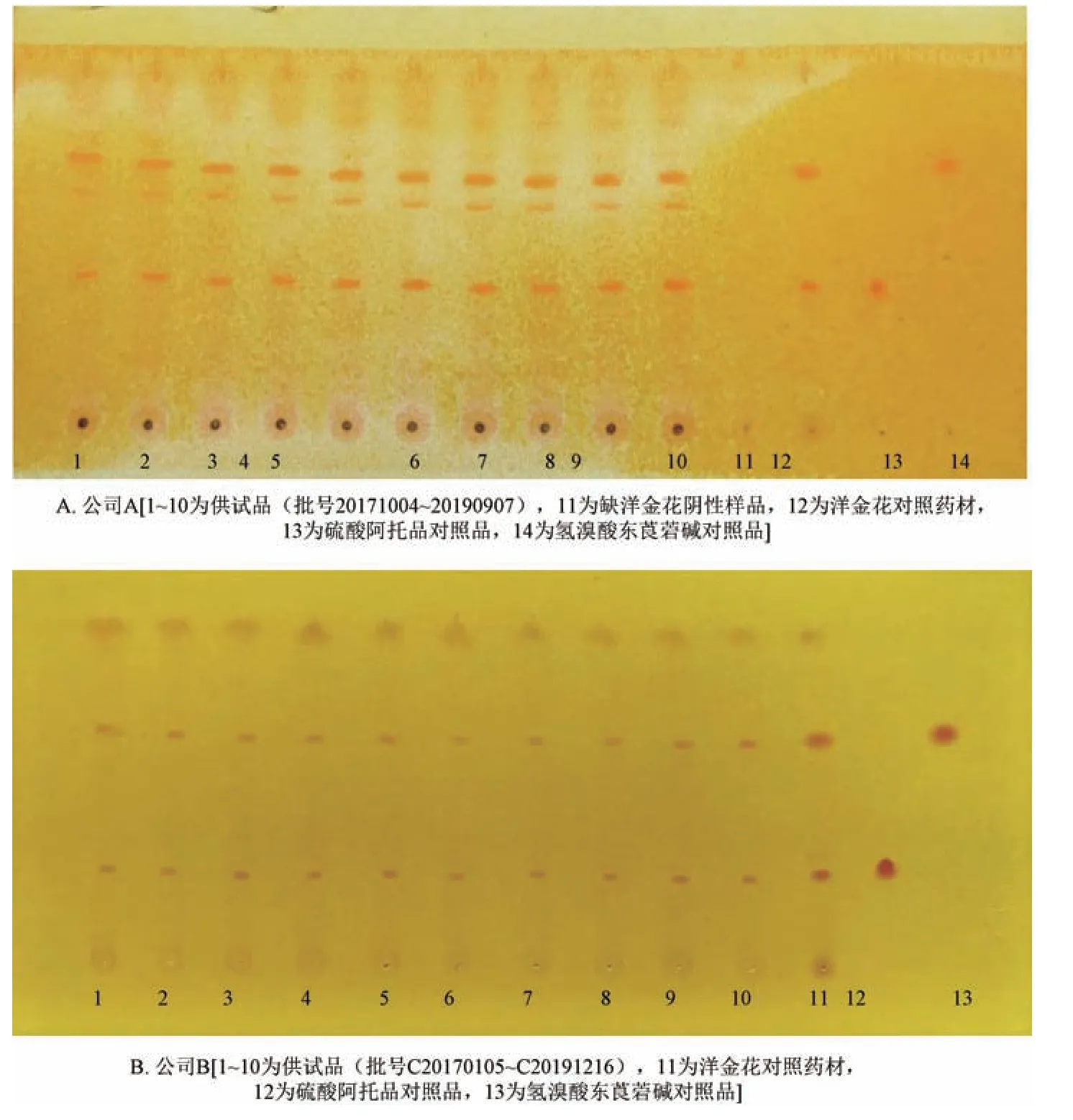
图1 2 家公司洋金花TLC 色谱图
2.1.2 GC 法(冰片、人工麝香、肉桂)
2.1.2.1 色谱条件与系统适应性考察 聚乙二醇(PEG⁃20M)Rtx® ⁃Wax 毛细管柱(30 m×0.25 mm×0.25 μm);程序升温(初始80 ℃,保持5 min,以5 ℃/min 升至180 ℃,保持10 min);进样口温度210 ℃;检测器温度250 ℃;分流比10∶1;载气体积流量1.59 mL/min。理论塔板数按龙脑峰计,应不低于10 000。
2.1.2.2 对照品溶液制备 精密称取龙脑、麝香酮、桂皮醛对照品适量,加乙酸乙酯制成每1 mL 分别含三者0.1、0.02、0.1 mg 的溶液,即得。
2.1.2.3 供试品溶液制备 取本品适量,研磨后取细粉约5 g,精密称定,置于具塞锥形瓶中,精密加入乙酸乙酯20 mL,称定质量,超声(400 W、40 kHz)处理10 min,取出,放冷,乙酸乙酯补足减失的质量,摇匀,滤过,即得。
2.1.2.4 阴性样品溶液制备 取缺冰片、肉桂、人工麝香的阴性样品,按“2.1.2.3”项下方法制备,即得。
2.1.2.5 结果分析 精密量取对照品、供试品溶液各1 μL,在“2.1.2.1”项色谱条件下进样测定,结果见图2。由此可知,供试品溶液呈现与对照品溶液保留时间一致的色谱峰,阴性无干扰,表明该方法专属性良好。
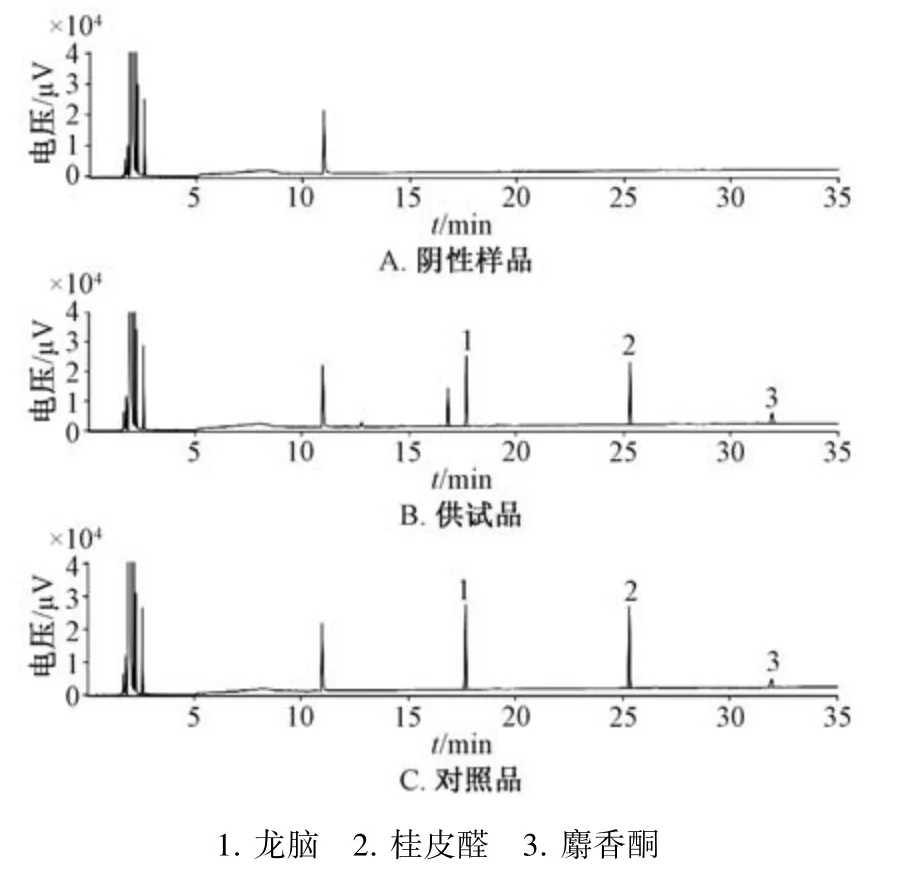
图2 各成分GC 色谱图
2.2 HPLC 含量测定(人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1)
2.2.1 色谱条件与系统适应性考察 以十八烷基硅烷键合硅胶为填充剂;流动相乙腈(A)⁃水(B),梯度洗脱,程序见表1;体积流量1.0 mL/min;检测波长203 nm。理论塔板数按人参皂苷Rg1计,应不低于6 000。

表1 梯度洗脱程序
2.2.2 对照品溶液制备 精密称取人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1对照品适量,甲醇制成每1 mL 分别含三者0.6、0.15、0.7 mg 的溶液,摇匀,即得。
2.2.3 供试品溶液制备 取本品适量,研细后取约1 g,精密称定,置于具塞锥形瓶中,精密加入水饱和的正丁醇50 mL,称定质量,加热回流提取1.5 h,放冷,水饱和正丁醇补足减失的质量,摇匀,滤过。精密量取续滤液20 mL,置于蒸发皿中蒸干,残渣加50%甲醇溶解,转移至10 mL 量瓶中,50% 甲醇稀释至刻度,滤过,取续滤液,即得。
2.2.4 阴性样品溶液制备 取缺人参、三七的阴性样品,按“2.2.3”项下方法制备,即得。
2.2.5 方法学考察
2.2.5.1 线性关系考察 精密称取各对照品适量,甲醇溶解并制成每1 mL 分别含人参皂苷Rg1190.4、380.8、565.3、775.9、992.1 μg,人参皂苷 Re 51.1、99.8、149.8、199.7、234.9 μg,人参皂苷Rb1370.6、605.8、785.4、975.1、1 179.5 μg 的溶液,在“2.2.1”项色谱条件下各进样10 μL 测定。以对照品峰面积为纵坐标(Y),进样量为横坐标(X)进行回归,结果见表2。由此可知,各人参皂苷在各自范围内呈良好的线性关系。

表2 各人参皂苷线性关系
2.2.5.2 专属性试验 吸取对照品、供试品、阴性样品溶液各10 μL,在“2.2.1”项色谱条件下进样测定,结果见图3。由此可知,阴性无干扰,表明该方法专属性良好。
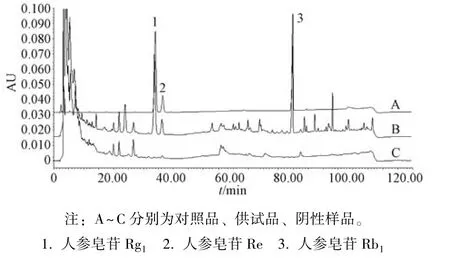
图3 各人参皂苷HPLC 色谱图
2.2.5.3 精密度试验 取“2.2.2”项下对照品溶液适量,在“2.2.1”项色谱条件下进样测定6次,测得人参皂苷Rg1、人 参皂苷Re、人参皂 苷Rb1峰面积RSD 分别为0.5%、0.6%、0.5%,表明仪器精密度良好。
2.2.5.4 重复性试验 取本品(批号20170905)6份,每份约1 g,精密称定,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,测得人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1含量RSD 分别为0.5%、0、0.3%,表明该方法重复性良好。
2.2.5.5 稳定性试验 取本品(批号20170905)适量,按“2.2.3”项下方法制备供试品溶液,于0、8、16、24、36、48 h在“2.2.1”项色谱条件下进样测定,测得人参皂苷Rg1、人 参皂苷Re、人参皂 苷Rb1峰面积RSD 分别为0.4%、0.5%、1.3%,表明溶液在48 h 内稳定性良好。
2.2.5.6 加样回收率试验 精密称取同一批本品(批号20170405,含人参皂苷Rg10.761 mg/丸、人参皂苷Re 0.172 mg/丸、人参皂苷Rb10.777 mg/丸)9份,置于具塞锥形瓶中,每3 份1组,分别精密加入50%水平(含人参皂苷Rg10.059 mg/mL、人参皂苷Re 0.013 mg/mL、人参皂苷Rb10.061 mg/mL)、100%水平(含人参皂苷Rg10.120 mg/mL、人参皂苷Re 0.027 mg/mL、人参皂苷Rb10.121 mg/mL)、150%水平(含人参皂苷Rg10.189 mg/mL、人参皂苷Re 0.040 mg/mL、人参皂苷Rb10.182 mg/mL)对照品溶液(溶剂为水饱和正丁醇)各50 mL,称定质量,加热回流提取1.5 h,放冷,水饱和正丁醇补足减失的质量,摇匀,滤过,精密量取续滤液20 mL,置于蒸发皿中蒸干,残渣加50%甲醇溶解,转移至10 mL 量瓶中,50% 甲醇稀释至刻度,滤过,取续滤液,在“2.2.1”项色谱条件下进样测定,计算回收率,结果见表3。
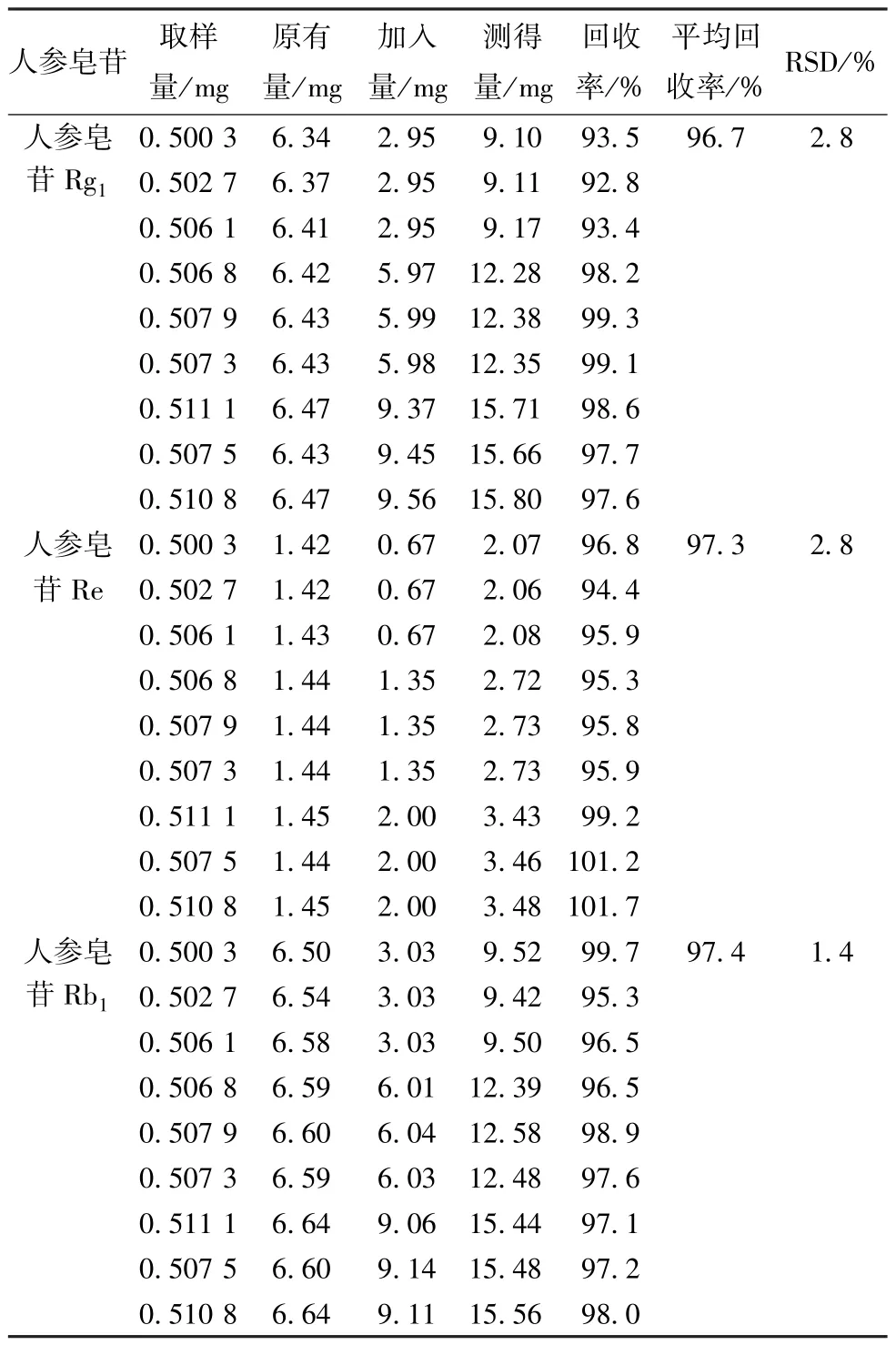
表3 各人参皂苷加样回收试验结果(n=9)
2.2.5.7 色谱柱考察 取本品(批号20180301)适量,按“2.2.3”项下方法制备供试品溶液,分别采用Phenomenex Gemini C18(250 mm× 4.6 mm,5 μm)、中普红RD⁃C18(250 mm × 4.6 mm,5 μm)、Agilent EC⁃C18(150 mm ×4.6 mm,4 μm)色谱柱,在“2.2.1”项色谱条件下进样测定。结果,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1分离度良好,三者含量RSD 分别为0.5%、4.4%、4.5%,表明不同色谱柱对测定无明显影响。
2.2.5.8 仪器考察 取本品(批号20170905)适量,按“2.2.3”项下方法制备供试品溶液,在Phenomenex Gemini C18色谱柱(250 mm×4.6 mm,5 μm)上分别采用LC⁃20AT、Agilent 1260 高效液相色谱仪,在“2.2.1”项色谱条件下进样测定。结果,人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1分离度良好,三者含量RSD 分别为0、2.2%、1.9%,表明不同仪器对测定无明显影响。
2.2.6 样品含量测定 取20 批样品,按“2.2.3”项下方法制备供试品溶液,在“2.2.1”项色谱条件下进样测定,计算人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1总含量,结果见表4。
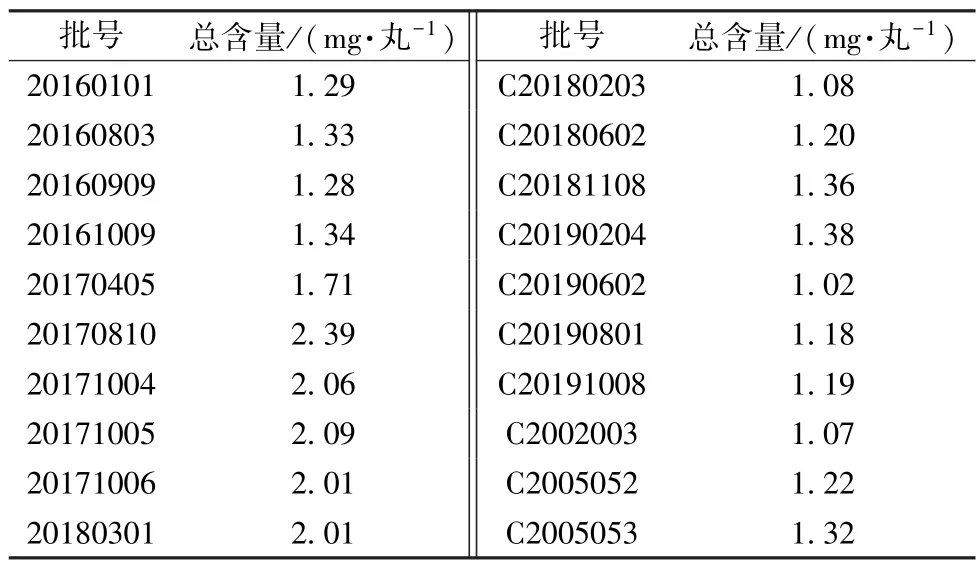
表4 人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1 总含量测定结果
3 讨论
3.1 显微鉴别 本实验对心宝丸原标准中的显微鉴别项进行药材归属,发现三七为树脂道碎片含黄色油滴状或块状分泌物;鹿茸为不规则碎块灰黄色,稍具光泽,充塞灰黑色微细颗粒。
3.2 GC 定性鉴别 心宝丸原标准中的部分鉴别项存在一定缺陷,如升华法鉴别冰片时因温度难以控制,导致结果重复性差;TLC 法鉴别人工麝香、鹿茸时,由于2020 年版《中国药典》中指标成分更新,存在阴性干扰现象。本实验建立的GC 法专属性强,可对冰片、人工麝香进行定性鉴别。
3.3 检测波长选择 本实验采用DAD 检测器对对照品溶液进行全波长扫描,发现当检测波长为203 nm时,各人参皂苷色谱图基线平稳,具有良好的紫外吸收,峰形稳定,杂质干扰小,分离度较好。
3.4 供试品溶液制备方法筛选 本实验考察了提取溶剂(水饱和正丁醇、70%甲醇、50%甲醇)、提取方法(回流、超声)、提取时间(15、30、45、60、90、120 min)、取样量(1.0、3.0 g)对各人参皂苷提取率的影响,最终确定为“2.2.3”项下方法,此时提取效果最好。
3.5 含量限度制定 研究表明,人参皂苷具有抗氧化、改善血流动力学、调节血管功能、抗血栓形成、保护心肌缺血再灌注等药理活性,对多种心血管疾病都有着显著的治疗作用[15⁃16],而三七、人参作为心宝丸主要药味,富含人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1等活性成分[17⁃19],其中人参是贵重药材,不同厂家在制备过程中其投料差异在很大程度上影响到产品质量,故有必要制定该类成分含量限度,以保证产品有效性。本实验测定2 个厂家各10 批心宝丸中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1总含量,以其平均值的70%为下限来制订限度,最终确定每丸含人参、三七以三者总含量计,不得少于1.0 mg。
4 结论
心血管疾病作为全球发病率和致死率最高的疾病之一,严重威胁人类生命健康。心宝丸作为治疗多种心血管疾病的名优产品,是在补肾壮阳药基础上加益气、活血、通络等药物形成特色组方,不仅表现出高效低毒的优势特征,而且联合其他中西药物使用能增强疗效,在社会老龄化趋势下具有广阔的应用前景,但该制剂组方药材多,也在一定程度上增加了其质量控制的难度。现行心宝丸标准大多采用传统手段,存在阴性干扰、重复性差等问题,而且缺少含量测定项,不利于产品质量控制。本实验基于2020 年版《中国药典》对心宝丸药材指标成分的更新,建立TLC法定性鉴别洋金花,GC 法定性鉴别冰片、人工麝香、肉桂,HPLC 测定人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1总含量,大大提高了该制剂质量的安全性和可控性,从而为建立其更全面的质量标准提供有力保证。
