基于TLR4/MyD88/NF⁃κB 信号通路探讨龙牡安神颗粒对慢性束缚应激小鼠焦虑行为的影响
2022-12-03赵建军彭晓明李婷婷朱鑫磊王伟龙漆哲宁刘立
赵建军 彭晓明 李婷婷 朱鑫磊 王伟龙 漆哲宁刘立∗
(1.甘肃中医药大学, 甘肃 兰州730000; 2.甘肃中医药大学附属医院, 甘肃 兰州730000)
焦虑症是最常见的精神障碍,核心特征包括过度恐惧和焦虑,恐惧是由迫在眉睫的威胁产生,而焦虑是对未来威胁的一种预期状态[1]。流行病学显示,我国焦虑症的12 个月患病率为5.0%,终生患病率为7.6%[2]。目前,抗抑郁药物选择性5⁃羟色胺(5⁃HT)再摄取抑制剂(SSRIs)是治疗焦虑症的一线用药,但其常伴有头痛、失眠、性功能下降等不良反应[3]。因此,从多角度阐明焦虑症的病理机制,发现新的药物作用靶点和寻找更有效的抗焦虑方法无疑是值得探索的方向。
近年来,应激诱导的神经炎症在焦虑症病理过程中的作用逐渐受到专家学者的关注。其中,Toll样受体4(TLR4)在应激诱导的神经炎症中扮演极其重要的角色[4],其可通过髓样分化因子88(MyD88)依赖途径激活核转录因子⁃κB(NF⁃κB),刺激促炎细胞因子的释放。研究表明,通过调节TLR4/NF⁃κB 信号通路,可逆转束缚应激诱导的小鼠焦虑行为[5⁃6]。龙牡安神颗粒是临床经验处方,具有安神定惊、养心健脾功效。前期研究发现,龙牡安神颗粒在临床上治疗焦虑症疗效确切,但其具体作用机制尚不明确[7]。因此,本实验采用慢性束缚应激诱导焦虑模型,通过观察龙牡安神颗粒对焦虑模型小鼠行为学及TLR4/MyD88/NF⁃κB 信号通路的影响,探讨其发挥抗焦虑作用的可能机制。
1 材料
1.1 动物 SPF 级雄性昆明小鼠,8 周龄,体质量(20±2)g,购自甘肃中医药大学实验动物中心,动物质量合格证号62001000000621,实验动物生产许可证号SCXK(甘)2020⁃0001。小鼠饲养于温度(22 ± 2)℃,相对湿度(60±5)%,12 h/12 h 明暗交替的SPF 环境中,实验动物使用许可证号 SYXK(甘)2020⁃0009,所有实验均在09:00至15:00 之间进行。
1.2 试剂与药物 龙牡安神颗粒(龙骨30 g、牡蛎30 g、磁石30 g、珍珠母30 g、远志9 g、酸枣仁15 g、合欢皮10 g、首乌藤10 g、甘草10 g、浮小麦30 g、大枣6 g、茯苓12 g、太子参10 g、桂枝6 g、生姜6 g、石菖蒲6 g)为广东一方制药有限公司生产的中药配方颗粒,批号分别为1060433、1052093、1080083、0123753、1105103、1033643、1055633、1035763、1080933、1012623、1081343、1050723、1030843、1045483、1020733、1052113。盐酸帕罗西汀片(乐友,浙江华海药业股份有限公司,国药准字H20031106,20 mg/片,批号0000012020)。BCA 蛋白定量试剂盒(北京索莱宝科技有限公司,批号20210814);TNF⁃α、IL⁃1β、IL⁃6 ELISA 试剂盒(江苏麦莎实业有限公司,批 号 202201、202201、202201);TLR4抗体、MyD88 抗体、NF⁃κB 抗体、p⁃NF⁃κB 抗体(北京博奥森生物技术有限公司,批号 BA08313887、AH10163311、BA07072298、BA09108701);GAPDH抗体(英国Abcam 公司,批号GR303514⁃13);辣根过氧化物酶标记羊抗兔免疫球蛋白(Ig)G(北京中杉金桥生物技术有限公司,批号210060240);反转录试剂盒(上海翊圣生物科技有限公司,批号HB170809)。
1.3 仪器 iMark 酶标仪(美国Bio⁃Rad 公司);5424R 型高速冷冻离心机(德国Eppendorf 公司);DNP⁃9022 型恒温培养箱(上海精宏实验设备有限公司);实时荧光定量PCR 仪(美国Thermo 公司);DYCZ⁃25D 型Western blot 电泳仪(北京六一生物科技有限公司);DM2500 型显微镜(德国Leica 公司)。
2 方法
2.1 模型建立 48 只雄性昆明小鼠随机选取8 只作为空白组,其余40 只作为造模组。空白组不束缚,造模组小鼠参考文献[5,8] 报道,采用慢性束缚应激法复制焦虑小鼠模型,将小鼠放入改造过的50 mL 离心管中(管壁有供动物呼吸的气孔),每日束缚2 h,持续35 d,束缚时间在09:00~15:00 时间段内随机安排。造模第14 天行高架十字迷宫实验,与空白组比较,若慢性束缚应激造模组小鼠进入开臂次数、开臂停留时间减少,则说明造模成功。
2.2 分组及给药 造模成功的小鼠按体质量随机分为模型组、盐酸帕罗西汀组(阳性药)和龙牡安神颗粒高、中、低剂量组,每组8 只。按照成人和动物体表面积折算,盐酸帕罗西汀灌胃剂量为2.6 mg/kg,龙牡安神颗粒 高、中、低剂量为4.16、2.08、1.04 g/kg(临床等效剂量的2、1、0.5 倍)。从第15 天开始,每天束缚结束后0.5 h,给药组灌胃给予相应剂量药物(10 mL/kg),空白组和模型组灌胃给予等量蒸馏水,每天1次,连续21 d。末次给药后,各组小鼠进行行为学检测(高架十字迷宫、旷场实验),行为学实验结束后,断头取全脑,冰上迅速分离海马。
2.3 检测指标
2.3.1 高架十字迷宫实验 高架十字迷宫距离地面50 cm,由2 个开臂(30 cm×5 cm×0.6 cm)和2个闭臂(30 cm×5 cm×15 cm)经中央平台(5 cm×5 cm)垂直交叉组成。测试时,将小鼠置于中央平台,头朝开臂,记录5 min 内小鼠进入开臂和闭臂的次数及在各臂停留的时间。每次实验后用75%乙醇擦拭迷宫,再将下一只小鼠放入。
2.3.2 旷场实验 旷场箱(30 cm×30 cm)分为周围和中央两个区域,中央区大小为15 cm×15 cm的小正方形。测试时,将小鼠置于旷场箱的中央,记录5 min 内小鼠进入中央区域的次数及停留时间。每次实验后用75%乙醇溶液彻底清洁旷场箱,再进行下一只小鼠的实验。
2.3.3 ELISA 法检测海马组织TNF⁃α、IL⁃1β、IL⁃6 水平 制备10%小鼠海马组织匀浆,离心后取上清液,采用ELISA 试剂盒检测上清液中炎症因子TNF⁃α、IL⁃1β、IL⁃6 水平,操作过程遵循试剂盒说明书进行。
2.3.4 RT⁃qPCR 法检测海马组织TLR4、MyD88、NF⁃κBmRNA 表达 按照RNA 提取试剂盒说明书提取小鼠海马组织总RNA,然后根据HifairⅢ1st Strand cDNA Synthesis 试剂盒逆转录为cDNA,通过Real⁃time PCR 仪进行扩增,以GAPDH为内参,采用2-ΔΔCT法计算TLR4、MyD88、NF⁃κBmRNA 相对表达量。引物序列见表1。

表1 引物序列Tab.1 Primer sequences
2.3.5 Western blot 法检测海马组织TLR4、MyD88、NF⁃κB 蛋白表达 冰上提取海马组织总蛋白,BCA法测定蛋白浓度,经电泳、转膜、脱脂奶粉封闭后,加入一抗TLR4、MyD88、NF⁃κB、GAPDH(1∶1 000),4 ℃孵育过夜,次日TBST 洗膜后加入二抗(1∶6 000),显影后使用Image Pro Plus 图像处理软件分析蛋白相对表达量。
2.3.6 免疫组化法检测海马组织p⁃NF⁃κB 蛋白表达 组织切片经脱蜡处理后,柠檬酸钠修复2次,3%过氧化氢孵育15 min,PBS 冲洗3次,用p⁃NF⁃κB 抗体(1 ︰ 100)4 ℃过夜,二抗37 ℃孵育,DAB 显色,苏木素复染1 min,中性树胶封片,显微镜下拍照,使用Image Pro Plus 图像处理软件分析p⁃NF⁃κB 蛋白表达。
2.4 统计学分析 通过SPSS 25.0 软件进行处理,计量资料以()表示,符合正态性及方差齐性的数据,多组间比较采用单因素方差分析,2 组间比较采用LSD 法;方差不齐则用Dunnett’s T3 检验。P<0.05 表示差异有统计学意义。
3 结果
3.1 龙牡安神颗粒对慢性束缚应激小鼠高架十字迷宫实验的影响 与空白组比较,模型组小鼠进入开臂次数、开臂停留时间和进入开臂次数百分比均减少(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒高、中剂量组小鼠进入开臂次数、开臂停留时间和进入开臂次数百分比均增加(P<0.05,P<0.01),见表2。
表2 龙牡安神颗粒对慢性束缚应激小鼠高架十字迷宫实验的影响(,n=8)Tab.2 Effects of Longmu Anshen Granules on mice exposed to chronic restraint stress in the elevated plus maze test(,n=8)
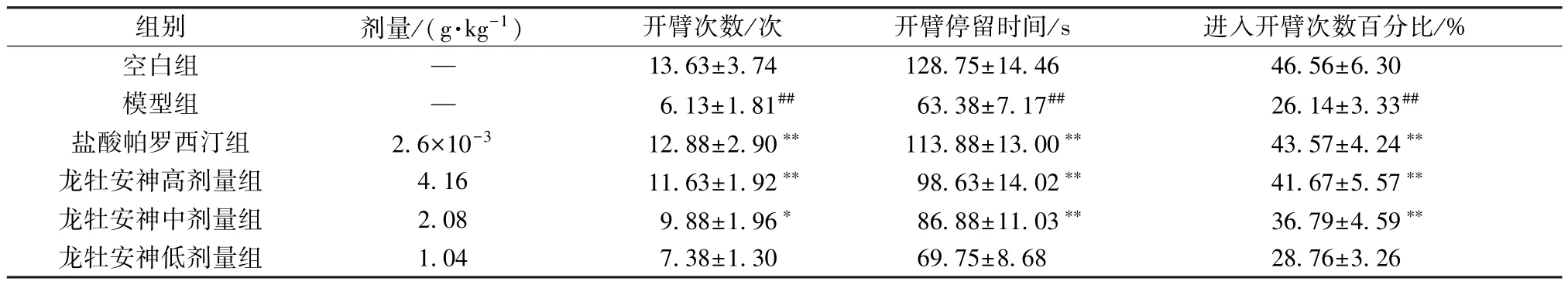
表2 龙牡安神颗粒对慢性束缚应激小鼠高架十字迷宫实验的影响(,n=8)Tab.2 Effects of Longmu Anshen Granules on mice exposed to chronic restraint stress in the elevated plus maze test(,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01。
3.2 龙牡安神颗粒对慢性束缚应激小鼠旷场实验的影响 与空白组比较,模型组小鼠进入中央区域次数及停留时间减少(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒高、中剂量组小鼠进入中央区域次数及停留时间均增加(P<0.01),见表3。
表3 龙牡安神颗粒对慢性束缚应激小鼠旷场实验的影响(,n=8)Tab.3 Effects of Longmu Anshen Granules on mice exposed to chronic restraint stress in the open field test(,n=8)

表3 龙牡安神颗粒对慢性束缚应激小鼠旷场实验的影响(,n=8)Tab.3 Effects of Longmu Anshen Granules on mice exposed to chronic restraint stress in the open field test(,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗∗P<0.01。
3.3 龙牡安神颗粒对慢性束缚应激小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平的影响 与空白组比较,模型组小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平升高(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒高、中剂量组小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平降低(P<0.01),龙牡安神颗粒低剂量组小鼠海马组织IL⁃6 水平降低(P<0.01),见表4。
表4 龙牡安神颗粒对慢性束缚应激小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平的影响(ng/L,,n=8)Tab.4 Effects of Longmu Anshen Granules on hippocampus TNF⁃α,IL⁃1β and IL⁃6 levels of mice exposed to chronic restraint stress(ng/L,,n=8)

表4 龙牡安神颗粒对慢性束缚应激小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平的影响(ng/L,,n=8)Tab.4 Effects of Longmu Anshen Granules on hippocampus TNF⁃α,IL⁃1β and IL⁃6 levels of mice exposed to chronic restraint stress(ng/L,,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗∗P<0.01。
3.4 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、MyD88、NF⁃κBmRNA 表达的影响 与空白组比较,模型组小鼠海马组织TLR4、MyD88、NF⁃κBmRNA 表达升高(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒高、中剂量组小鼠海马组织中TLR4、MyD88、NF⁃κBmRNA 表达降低(P<0.05,P<0.01),见表5。
表5 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、 MyD88、 NF⁃κB mRNA 表达的影响(,n=8)Tab.5 Effects of Longmu Anshen Granules on hippocampus mRNA expressions of TLR4,MyD88 and NF⁃κB of mice exposed to chronic restraint stress(,n=8)
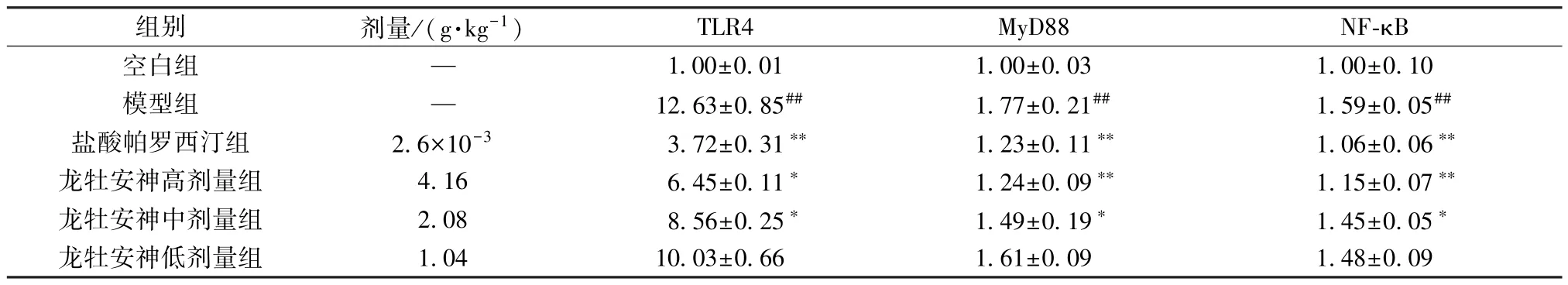
表5 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、 MyD88、 NF⁃κB mRNA 表达的影响(,n=8)Tab.5 Effects of Longmu Anshen Granules on hippocampus mRNA expressions of TLR4,MyD88 and NF⁃κB of mice exposed to chronic restraint stress(,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01。
3.5 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、MyD88、NF⁃κB 蛋白表达的影响 与空白组比较,模型组小鼠海马组织TLR4、MyD88、NF⁃κB 蛋白表达升高(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒各剂量组小鼠海马组织TLR4、MyD88、NF⁃κB 表达降低(P<0.05,P<0.01),见表6、图1。
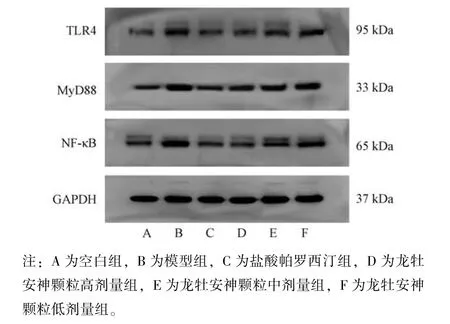
图1 各组小鼠海马组织TLR4、MyD88、NF⁃κB 蛋白条带图Fig.1 TLR4,MyD88 and NF⁃κB protein bands in mouse hippocampus of each group
表6 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、MyD88、NF⁃κB 蛋白表达的影响(,n=8)Tab.6 Effects of Longmu Anshen Granules on hippocampus protein expressions of TLR4,MyD88 and NF⁃κB of mice exposed to chronic restraint stress(,n=8)

表6 龙牡安神颗粒对慢性束缚应激小鼠海马组织TLR4、MyD88、NF⁃κB 蛋白表达的影响(,n=8)Tab.6 Effects of Longmu Anshen Granules on hippocampus protein expressions of TLR4,MyD88 and NF⁃κB of mice exposed to chronic restraint stress(,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01。
3.6 龙牡安神颗粒对慢性束缚应激小鼠海马组织p⁃NF⁃κB 蛋白表达的影响 与空白组比较,模型组小鼠海马组织p⁃NF⁃κB 蛋白表达升高(P<0.01);与模型组比较,盐酸帕罗西汀组及龙牡安神颗粒高、中剂量组小鼠海马组织p⁃NF⁃κB 蛋白表达降低(P<0.05,P<0.01),见图2、表7。
表7 龙牡安神颗粒对慢性束缚应激小鼠海马组织p⁃NF⁃κB 蛋白表达的影响(,n=8)Tab.7 Effects of Longmu Anshen Granules on hippocampus expression of p⁃NF⁃κB protein of mice exposed to chronic restraint stress(,n=8)

表7 龙牡安神颗粒对慢性束缚应激小鼠海马组织p⁃NF⁃κB 蛋白表达的影响(,n=8)Tab.7 Effects of Longmu Anshen Granules on hippocampus expression of p⁃NF⁃κB protein of mice exposed to chronic restraint stress(,n=8)
注:与空白组比较,##P<0.01;与模型组比较,∗P<0.05,∗∗P<0.01。
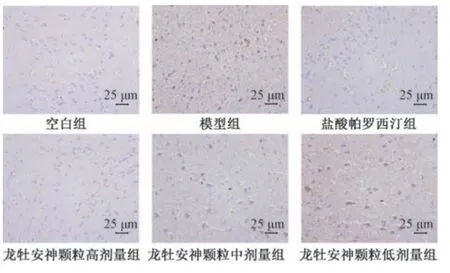
图2 各组小鼠海马组织p⁃NF⁃κB 蛋白免疫组化染色图(×400)Fig.2 Immunohistochemistry of p⁃NF⁃κB protein in mouse hippocampus of each group(×400)
4 讨论
焦虑症是一种常见的与各种应激源相关的神经精神疾病,急性和慢性应激暴露均可诱发焦虑症[9]。慢性束缚应激是诱导啮齿动物出现焦虑样行为的可靠方法,能够模拟慢性压力对人类病理生理的影响,在抗焦虑药物的研究中被广泛使用。高架十字迷宫实验和旷场实验是评价抗焦虑药物效果的经典方法。本实验发现,与空白组比较,慢性束缚应激造模14 d后,小鼠进入开臂次数、开臂停留时间均减少,说明慢性束缚应激焦虑模型复制成功;与模型组比较,使用龙牡安神颗粒干预21 d后,小鼠进入开臂次数、开臂停留时间、进入旷场中央区域次数和中央区域停留时间均增加,提示龙牡安神颗粒具有改善慢性束缚应激小鼠焦虑行为的作用。
应激反应可激活中枢及外周免疫系统,共同促进神经炎症的产生。研究发现,反复社会挫败应激可激活先天免疫系统,招募外周促炎单核细胞进入中枢,增加中枢及外周循环中促炎细胞因子的释放,导致神经炎症的发生[10⁃12]。此外,外周循环中的促炎细胞因子也可以利用迷走神经和特定的细胞因子转运体等多种途径通过血脑屏障,进一步加强中枢神经炎症信号[13]。有研究发现,腹膜注射TNF⁃α 和IL⁃6 抑制剂可改善大鼠的焦虑样行为和认知功能[14];海马区IL⁃1β 基因敲除可减轻脂多糖(LPS)诱导的神经炎症及焦虑行为[15]。现代药理研究表明,远志、酸枣仁、甘草、小麦、大枣均具有降低中枢促炎细胞因子水平,保护神经元细胞的作用[16⁃18]。本研究结果显示,模型组小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6 水平升高;龙牡安神颗粒干预后,小鼠海马组织TNF⁃α、IL⁃1β、IL⁃6水平降低。以上结果提示,龙牡安神颗粒改善慢性束缚应激小鼠焦虑行为可能与减少海马组织TNF⁃α、IL⁃1β、IL⁃6 水平有关。
TLR4 是激活先天免疫系统的重要受体,在神经炎症的产生和小胶质细胞活化中发挥重要作用[19]。NF⁃κB 通常以P65 和P50 形成的异二聚体存在于细胞质中,静息状态下无活性,MyD88 是TLR4 向下转导激活NF⁃κB 的关键衔接蛋白,TLR4可通过MyD88 依赖途径激活下游NF⁃κB,活化后NF⁃κB 被转运进细胞核,参与促炎细胞因子的转录与释放[4,20]。本研究结果表明,与空白组比较,持续的慢性束缚应激诱导可使模型组小鼠海马组织中TLR4、MyD88、NF⁃κB mRNA及蛋白表达升高,说明慢性束缚应激激活了TLR4/MyD88/NF⁃κB 信号通路,通过龙牡安神颗粒干预后,小鼠海马组织中TLR4、MyD88、NF⁃κB mRNA 及蛋白表达均有不同程度降低,提示龙牡安神颗粒发挥抗焦虑作用的机制可能与抑制TRL4/MyD88/NF⁃κB 信号通路,减少炎性介质的释放和表达有关。
综上所述,龙牡安神颗粒能改善慢性束缚应激小鼠的焦虑行为,其机制可能与抑制TRL4/MyD88/NF⁃κB 信号通路,减少促炎介质的释放和表达有关。
