简化模型分类 突破转化率问题
2022-11-30湖北杨世全邱亚明
湖北 杨世全 邱亚明
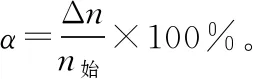
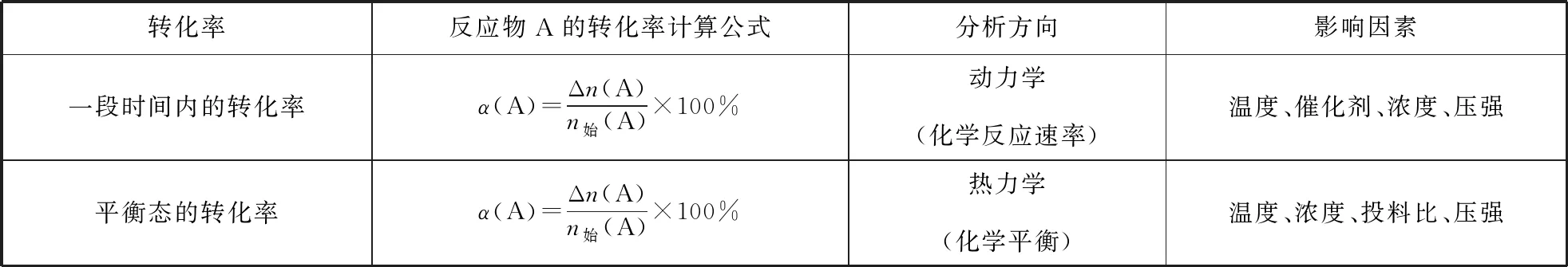
表1 转化率的类型及影响因素
在以“真实情境”为命题原则的情况下,新高考试题中对转化率的考查属于热点问题。在2022年高考化学卷中,全国卷和多个地区的高考卷均考查了转化率,主要涉及转化率的计算和转化率变化趋势的判断。高考试题对转化率的考查,倾向于融入学科核心素养和关键能力的考查。例如,2022年6月浙江卷,需要阅读试题的信息,依靠获取的信息进行分析判断,不仅考查了对转化率知识的掌握,还考查了信息的获取能力和推理判断能力。在陌生情境中,遇到与转化率有关的问题,建议构建思维模型解决问题,不能过于依靠总结的结论进行判断。
一、一段时间内的转化率分析
通常分析一段时间内的转化率的变化基本思路如图1所示。

图1 一段时间内的转化率分析思路
【例1】(2022年6月浙江卷,29(2)④题)热解H2S制H2。根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:



投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释;常压,不同温度下反应相同时间后,测得H2和CS2体积分数如表2所示:
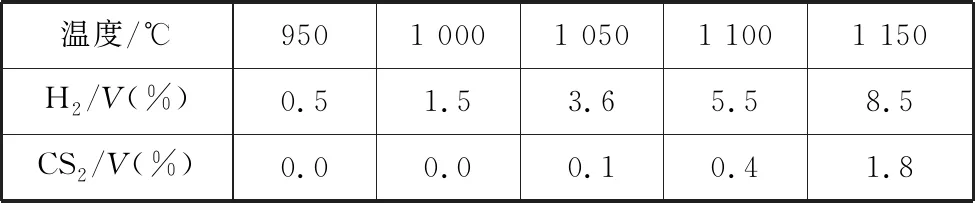
表2
在1 000℃,常压下,保持通入的H2S体积分数不变,提高投料比[V(H2S)∶V(CH4)],H2S的转化率不变,原因是__________________________________________________________________________。
【分析】阅读题目中给定的条件“一边进料,另一边出料”“反应相同时间”可知,本题分析的H2S的转化率属于一段时间内的转化率,需要从反应速率的角度分析。根据表格中的信息可知,1 000℃时CS2的体积分数为0,说明此温度下并没有发生反应Ⅱ,CH4没有参与反应。常压下,当H2S体积分数不变时,说明H2S的分压是定值,即H2S的浓度为定值,与投料比无关,因此在其余外界条件相同的情况下,浓度一定,则反应速率相同,一段时间内的转化量也相同,所以转化率不变。
通过对该例题的分析可以总结出,对于“一段时间内的转化率”分析模型如图2。
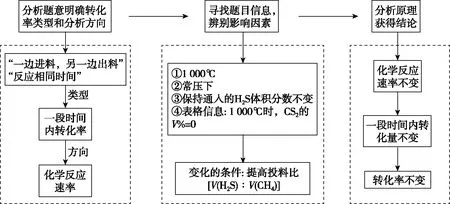
图2 一段时间内的转化率分析模型
可以看出该试题以真实的化工生产为情境,需要考虑反应物投入的实际情况(恒压、氮气施压等),是基于真实问题解决进行的考查。在解答这类试题的过程中应注意题目信息的获取、信息的整合,将陌生的问题简化为熟悉的问题,结合原理的分析,考虑工业的实际生产过程最终可形成完整的作答。
【例2】(2020年江苏卷,20(1)题)CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。
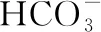
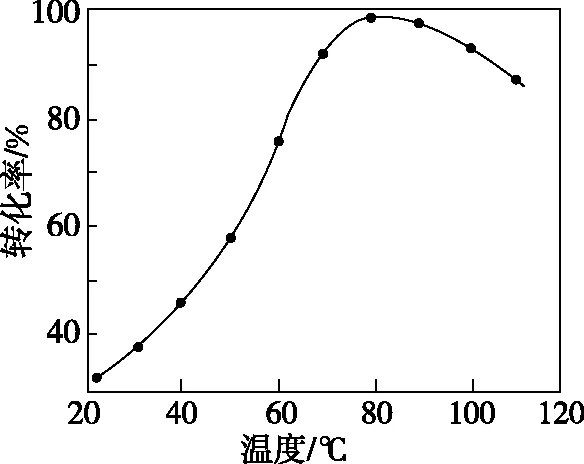
图3

二、平衡态转化率分析
当遇到平衡态转化率的判断时,分析思路如图4所示。
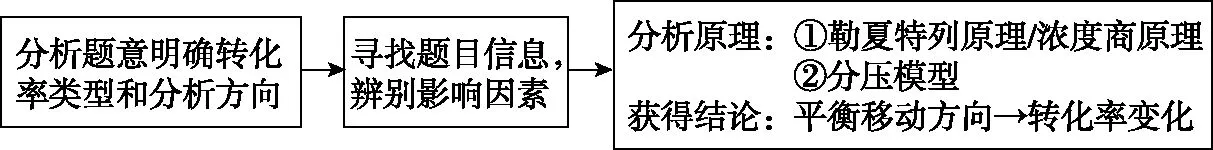
图4 平衡态转化率的分析思路
总结出的平衡态转化率变化规律如表3所示。
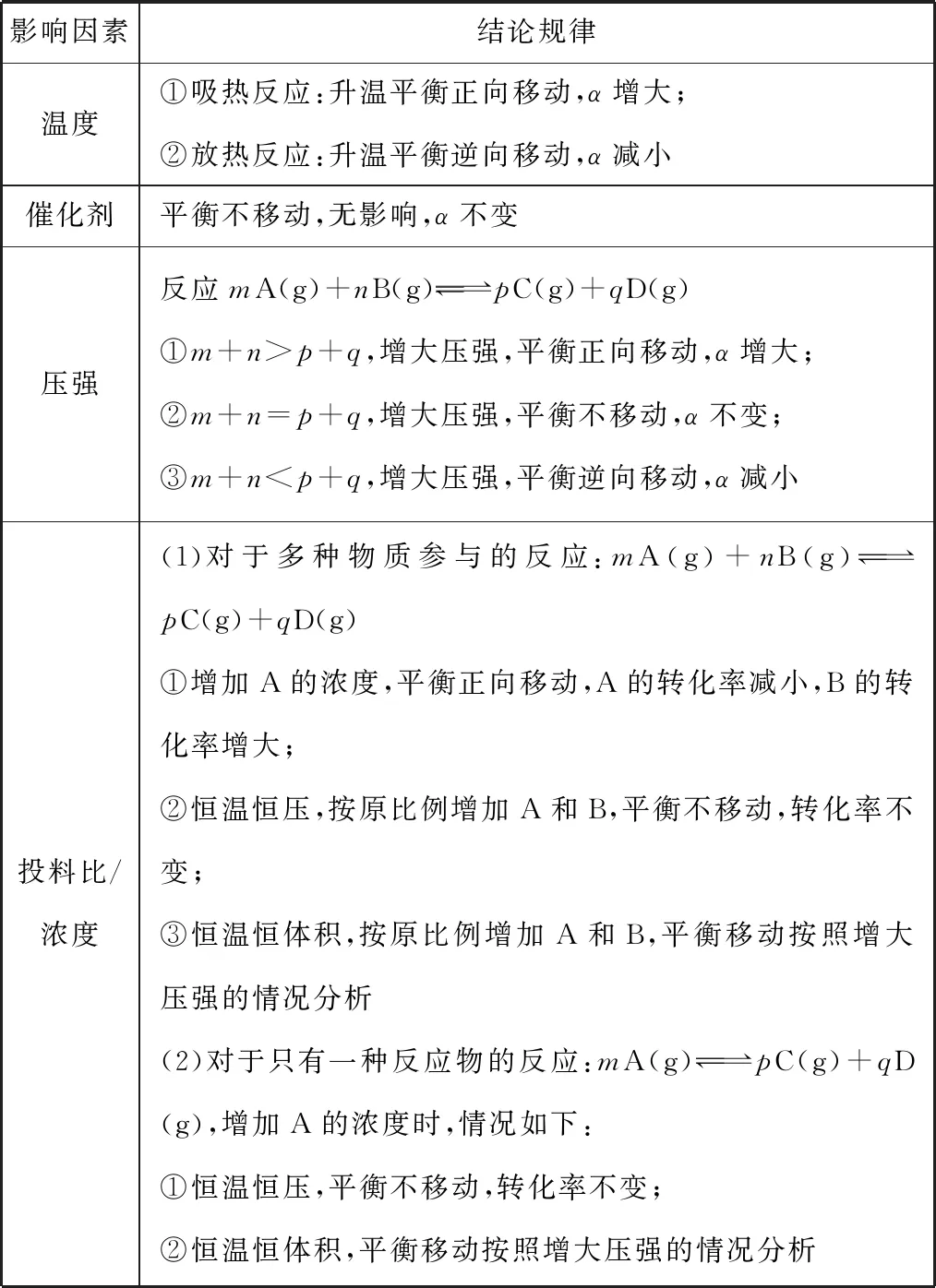
表3 平衡态转化率变化规律

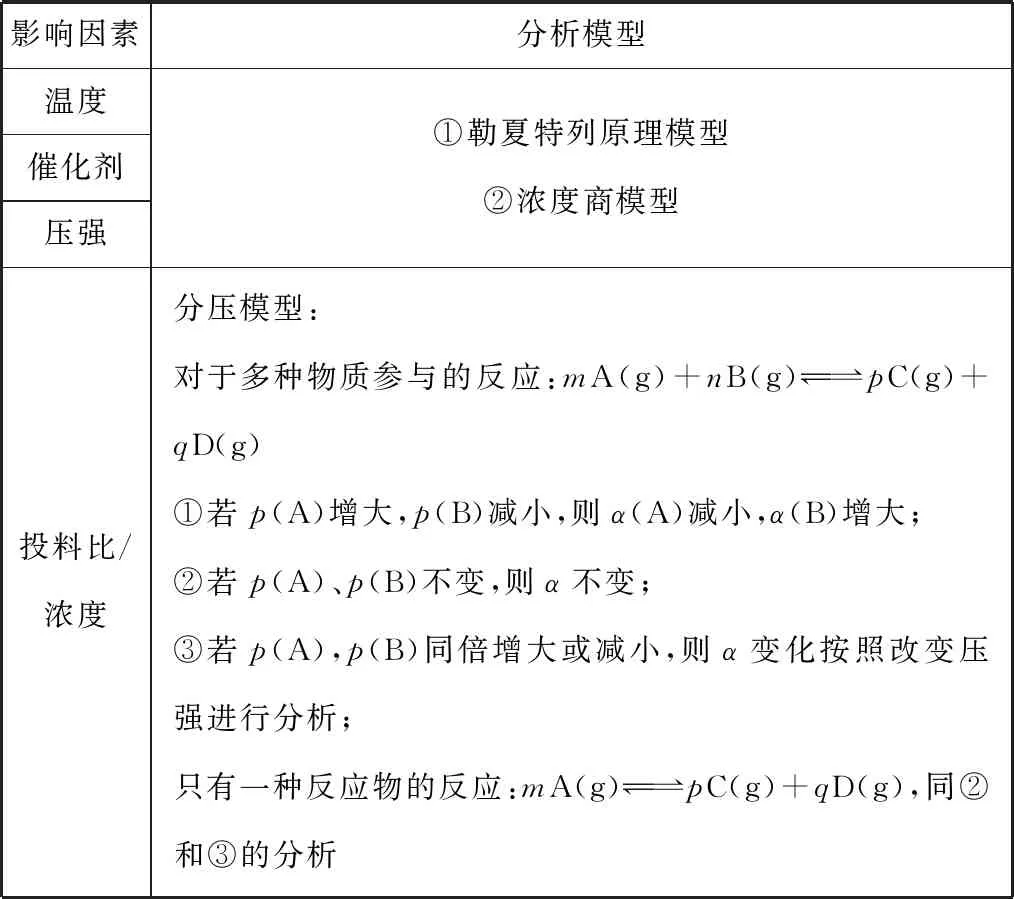
表4 平衡态转化率变化分析模型
【例3】(2022年全国乙卷,28(4)①题改编)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
已知下列反应的热化学方程式:




在实际生产作业中,也发生过由于人为因素或者设备故障导致集卡旋锁开闭不到位,造成桥吊在起吊集装箱时发生连箱带车一起起吊的安全事故,造成财产损失。
在1 373 K、100 kPa反应条件下,对于n(H2S)∶n(Ar)分别为4∶1、1∶1、1∶4、1∶9、1∶19的H2S-Ar混合气,热分解反应过程中H2S转化率随时间的变化如图5所示。
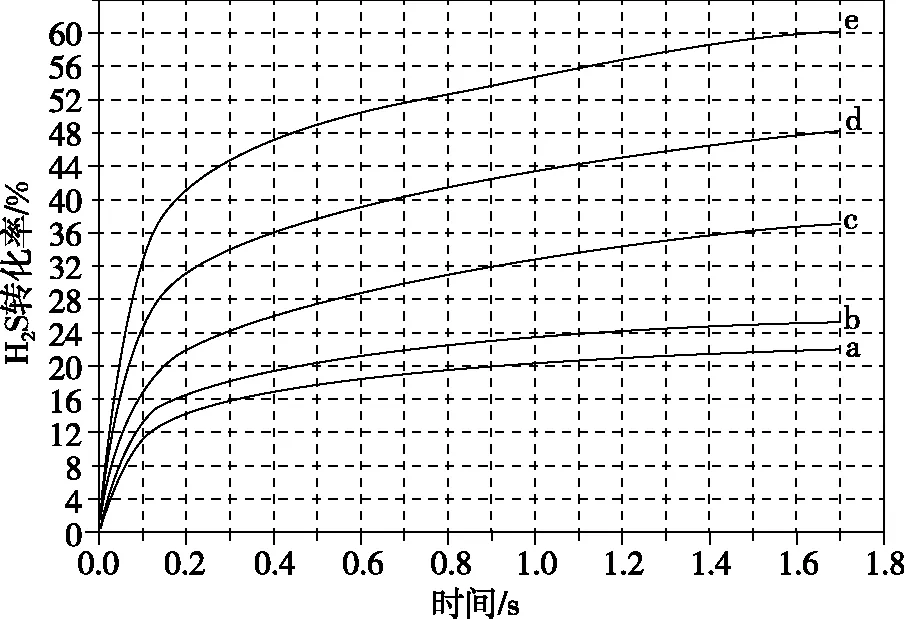
图5
n(H2S)∶n(Ar)越小,H2S平衡转化率________,理由是_____________________________________。
【分析】本题考查H2S平衡转化率,分析的方向为平衡移动,影响因素为投料比。当条件为恒温、总压恒定时,由于H2S所占的比例不同,导致其分压不同。因此不能当作恒压情况(恒压等效)进行处理。实际此处的分析可以看成恒体积情况下,H2S浓度不同进行处理。
思路一:K判定法。在恒温、恒压条件下,假设起始H2S分压为p1,达到平衡态,此时转化率为α,平衡常数为Kp,三段式如下:

起始p10 0
转化αp10.5αp1αp1
若起始H2S分压变为p2,假设某时刻转化率达到了α,根据此时的转化率列出三段式如下:

起始p20 0
转化αp20.5αp2αp2
某时刻 (1-α)p20.5αp2αp2
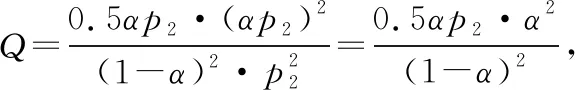
思路二:等效法。假设容器Ⅰ中投入1 mol H2S和容器Ⅱ中投入2 mol H2S(如图6),对比容器Ⅰ和Ⅱ中的平衡态。可以假设容器Ⅲ,设定的容器Ⅲ投入量为2 mol H2S,体积为2V,则容器Ⅰ和Ⅲ中所达到的平衡态相同,转化率αⅠ=αⅢ。由容器Ⅲ的平衡态变为容器Ⅱ,需要压缩体积,根据勒夏特列原理,平衡往系数小的方向移动,即逆向移动,则H2S的转化率减小,αⅢ>αⅡ,最终推出αⅠ>αⅡ,得出当投入量减小,H2S的转化率增大。
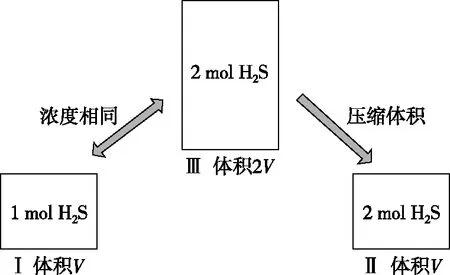
图6
思路三:H2S分压减小,分解反应中只有H2S一种反应物,因此相当于减压,依据勒夏特列原理,平衡向系数增大的方向移动,即平衡正向移动,H2S的平衡转化率增大。
通过以上的例题可以认识到,在高考试题中,对转化率的考查主要分为2种形式:①转化率的计算;②转化率变化的判断及解释。转化率的计算方法为三段式法,通常考查平衡态的转化率计算,只需要寻找题目给出的信息,列出三段式,利用三段式中的数据进行计算即可。在学习中需要注意练习寻找数据,注重题目数据之间的关系,能够熟练使用阿伏加德罗定律及其推论进行数据之间的转化。
从全国乙卷的转化率判断可以看出,在恒温恒压条件下,由于反应物只有一个,随着n(H2S)∶n(Ar)比例的减小,投入的H2S量减少,若错认为应按照表3中(2)的规律分析,则会得到平衡不移动,转化率不变的结论,与正确答案不一致。若从分压的角度分析,则不会出现误解的情况。因此,将原有的分析模型转变成分压的分析模型一方面可以简化分类,便于记忆理解;另一方面与实际的生产更贴合,可以将复杂的情境转变为简单的模型,使用更加方便更易于理解。

回答下列问题:
(1)恒温、恒压条件下,在密闭容器中,投料比n(SO2)∶n(空气)=1∶3时,若容器1中投入1 mol SO2,容器2中投入2 mol SO2,则两容器中SO2的转化率α大小为α1________(填“>”“<”或“=”)α2。
(2)恒温、恒压条件下,增大n(SO2)∶n(空气)的比例,则SO2的平衡转化率会________(填“增大”“不变”或“减小”)。
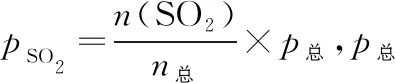
(2)恒温、恒压条件下,增大n(SO2)∶n(空气)的比例,则pSO2增大,pO2减小,相当于增大了SO2的量,则α(SO2)减小。
【例4】(2020年山东卷,18(3)题改编)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:



回答下列问题:
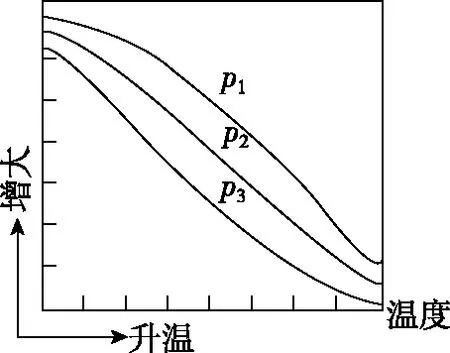
不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。
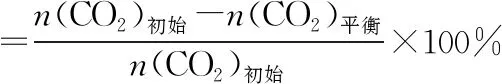
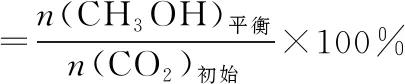
其中纵坐标表示CO2平衡转化率的是图________(填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为________;图乙中T1温度时,三条曲线几乎交于一点的原因是__________________________________________________________________________。
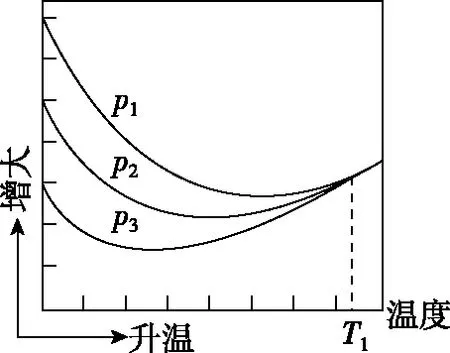
图乙
【分析】本题中需要分析的是平衡转化率,影响因素为温度。根据题意CO2参与了多个平衡,因此需要综合考虑多个平衡的移动。升温时,反应Ⅰ逆向移动,CO2转化量减少;反应Ⅲ正向移动,CO2转化量增多,直接分析不易判断CO2转化率的变化。若分析CH3OH的平衡产率,通过反应Ⅰ和Ⅱ可以分析出,升温两个反应均逆向移动,则CH3OH的平衡产率降低,因此图甲对应的是CH3OH的平衡产率,则图乙对应的是CO2的平衡转化率。从图像可以看出,CO2平衡转化率先降低后升高,结合反应Ⅰ和Ⅲ的移动情况,在升温的过程中前一阶段以反应Ⅰ为主,后一阶段以反应Ⅲ为主。分析思路如图7所示。
图甲
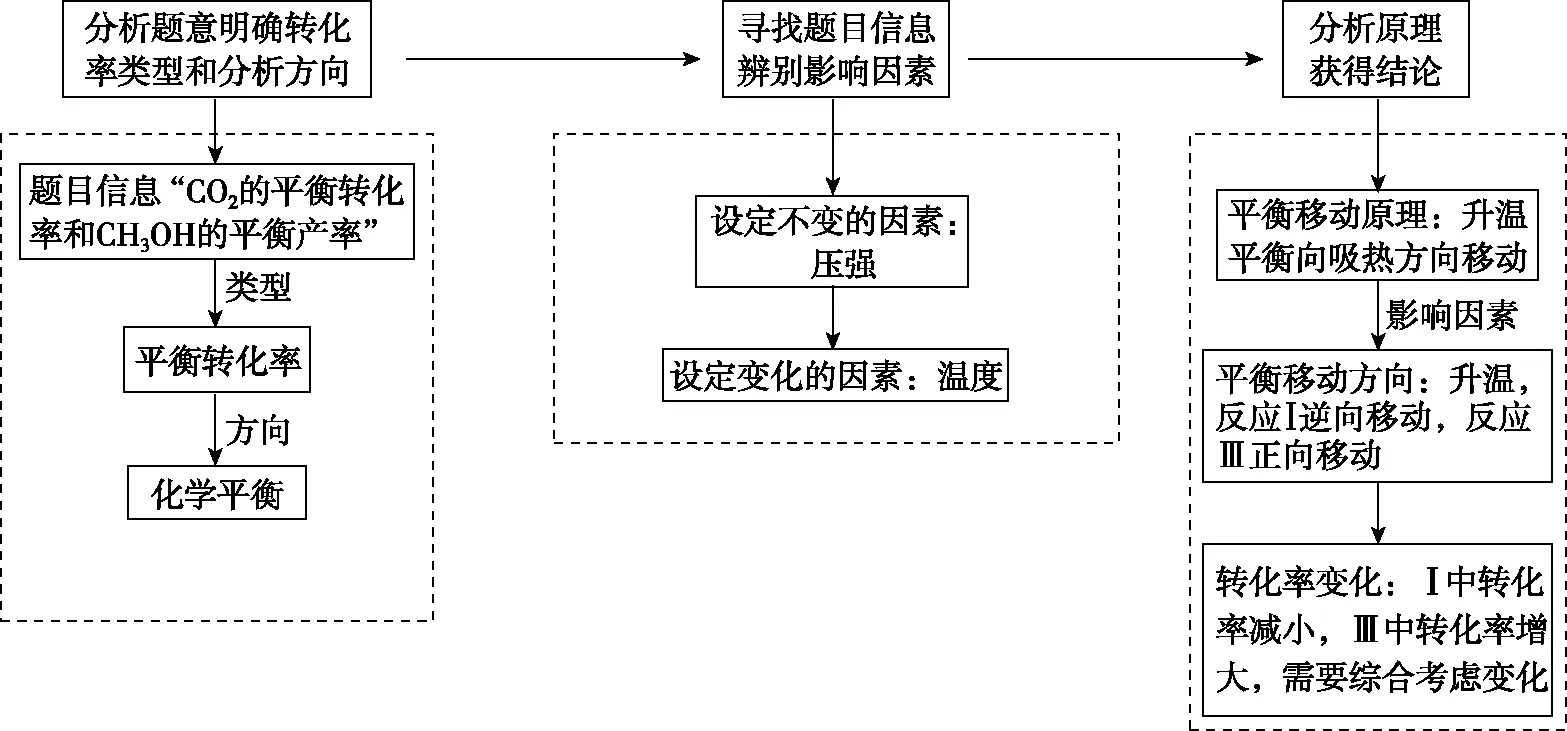
图7 平衡转化率的分析思路
压强增大反应Ⅰ和Ⅱ平衡正向移动,反应Ⅲ平衡不受压强影响,因此压强越大则CO2转化率越大,所以p1>p2>p3。当温度升高到一定程度,主要发生的反应为反应Ⅲ,压强对反应Ⅲ的平衡无影响,因此三条线在T1时几乎交于一点。
从新高考的考查方向和考查方式看,高考试题要选拔合适的人才,做到有效的区分度,会更加注重考查学生对信息的整合、对原因的分析和对结论的评价。高考试题对转化率的分析通常设置成主观性文字型的描述题,提升了考查难度,因此,复习过程中,应培养以“证据推理与模型认知”的学科核心素养为导向的能力指标,注重逻辑思维和综合分析能力的培养,形成高阶思维模型。抓住问题的本质,建立多样的分析模式,形成发散性的多种思维方式,让学生知其然,也知其所以然。总之,在复习备考中应适应新高考的变化,以能力培养为目标,注重对过程的分析和理解,才能真正地完成知识的升华。
