转录组与蛋白组关联分析探讨草酸钙结石晶体对HK-2细胞基因表达的影响
2022-11-25张圣平张建文
张圣平,邓 琼,张 颖,张建文,梁 辉,王 铸
(南方医科大学附属深圳龙华医院泌尿外科,广东深圳 518109)
肾结石在中国成年人中很常见,大约每17名成年人中就有1人遭受尿路结石困扰[1],其中草酸钙结石占尿路结石发病率的65%以上[2]。草酸钙晶体造成肾小管上皮细胞适应性改变并表达多种调节大分子,从而影响草酸钙结晶的粘附、聚集和生长,在肾结石的形成过程中起重要作用[3]。草酸钙结石晶体的形成造成了肾小管上皮细胞蛋白组和转录组表达谱的改变[4-5],对肾脏功能存在显著的影响。但是这些研究未能揭示蛋白组和转录组表达水平不一致的差异基因表达谱及其在肾结石形成和肾小管损伤过程中参与的调控通路。
本研究首次采用转录组与蛋白组关联分析探讨草酸钙结石晶体对人近曲肾小管上皮细胞的影响,重点分析了转录组与蛋白组差异表达基因,初步探讨差异表达基因在草酸钙结石造成的肾损伤过程中的作用。
1 材料与方法
1.1 实验材料本研究采用的人近曲肾小管上皮细胞HK-2(目录号SCSP-511)购自中国科学院典型培养物保藏委员会细胞库(https://www.cellbank.org.cn/)。本研究中使用的草酸钙结石样本来自深圳市龙华区人民医院泌尿外科,标本使用符合医学伦理相关规定,且征得患者的知情同意。
1.2 实验方法
1.2.1样品制备 人近曲肾小管上皮细胞HK-2采用K-SFM(Invitrogen,17005-042)培养液培养,其中包含两个组分:基础培养液1瓶(货号10724-011)+生长因子2管(货号37000-015),在37 ℃、体积分数为5%的CO2、饱和湿度的环境下恒温培养。
草酸钙结石样品经过无菌水冲洗、UV照射并充分干燥后研磨成粉末,经过结石成分分析确认[一水草酸钙(calcium oxalate monohydrate,COM)含量>99%]后使用K-SFM培养基配制成浓度为100 μg/ mL的草酸钙结石晶体悬浮液。按照1×105个/孔的密度将HK-2细胞接种到6孔板,在细胞密度达到70%~80%的汇合度时加入配制好的草酸钙晶体悬浮液,以加入等量K-SFM培养基作为对照组,培养48 h后用于下一步实验研究。
1.2.2转录组与蛋白组关联分析 将制备好的样本分别由Macrogen(www.macrogencn.com)完成转录组测序分析,由美吉生物(www.majorprotein.com)完成蛋白组分析。采用InterProScan(http://www.ebi.ac.uk/interpro/)将差异蛋白注释为3个大类,即生物进程、细胞组成、分子功能。采用KEGG Mapper(http://www.kegg.jp/kegg/mapper.html)进行通路富集分析,P<0.05为差异有统计学意义。转录组定量结果通过差异分析得到各个比较组中转录组相对表达量log2FC和差异统计学检验P值。由于转录组差异分析数据量较大,为了进一步降低假阳性率,对P值做了BH校验。当log2FC>1且校验后的P<0.05时,为显著差异表达上调转录本;log2FC<-1且校验后的P<0.05时,为显著差异表达下调转录本。蛋白质组定量结果通过差异分析得到各个比较组中蛋白相对表达量比值和差异统计学检验P值。由于差异表达蛋白数据量相对转录组较小,这里不需要对P值做进一步的错误发现率(false discovery rate,FDR)校验。当比值>1.2且P<0.05时,为显著差异表达上调蛋白;比值< 1/1.2且P<0.05时,为显著差异表达下调蛋白。
1.2.3实验组与对照组差异蛋白互作网络分析 将筛选出的差异表达基因集合导入STRING(http://string-db.org/)。除了从实验数据和各种数据库中挖掘数据外,还从染色体临近、基因融合、系统进化和基于芯片数据的基因共表达等方面进行综合打分(0.4~1.0分),从而预测出蛋白分子间的相互作用网络。网络中每个节点代表一个蛋白分子,连线表示蛋白之间的相互作用关系,连线越宽表示得分越高,连线越窄表示得分越低,本研究选择默认得分最小值0.4为中等得分。
2 结 果
2.1 转录组与蛋白组定量比较分析本项目通过转录组与蛋白组定量研究分别定量到57 833个转录本和6 407个蛋白。通过比较转录组与蛋白组的定量情况,我们发现有6 144个基因在转录组和蛋白组水平都定量。蛋白组与转录组差异分析结果表明,在蛋白水平有464个分子发生显著下调,有699个分子发生显著上调表达;在转录组水平,有11个分子下调表达,有14个分子上调表达(图1A)。采用以转录本ID为标准的韦恩图分析表明,有681个蛋白发生了上调,455个蛋白发生下调表达(图1B)。

A:不同比较组中蛋白(左)与转录本(右)定量火山图;B:差异表达蛋白与差异表达转录本比较分析韦恩图。
2.2 转录组与蛋白组差异蛋白的功能富集分析通过转录组与蛋白组定量比较分析将蛋白或转录本分为多种不同类型的表达情况,每种表达情况可以对应一种调控关系。差异蛋白的KEGG和GO富集分析结果表明:在蛋白组下调-转录组无差异这个集合中缬氨酸、亮氨酸和异亮氨酸降解,初级胆汁酸生物合成以及DNA的非同源末端链接为最显著的KEEG通路(图2A);在蛋白组上调-转录组无差异的集合中维生素B6代谢,硫中继系统以及糖胺聚糖生物合成为最显著的KEEG通路(图2B)。GO分析结果表明,在蛋白组下调-转录组无差异的集合中线粒体衍生囊泡与腺嘌呤跨膜转运体活性富集指数最高(图3A);在蛋白组上调-转录组无差异snRNA的细胞核输出以及中心粒周围异染色质组装具有最高的富集指数(图3B)。

A:蛋白组下调-转录组无差异组;B:蛋白组上调-转录组无差异组。
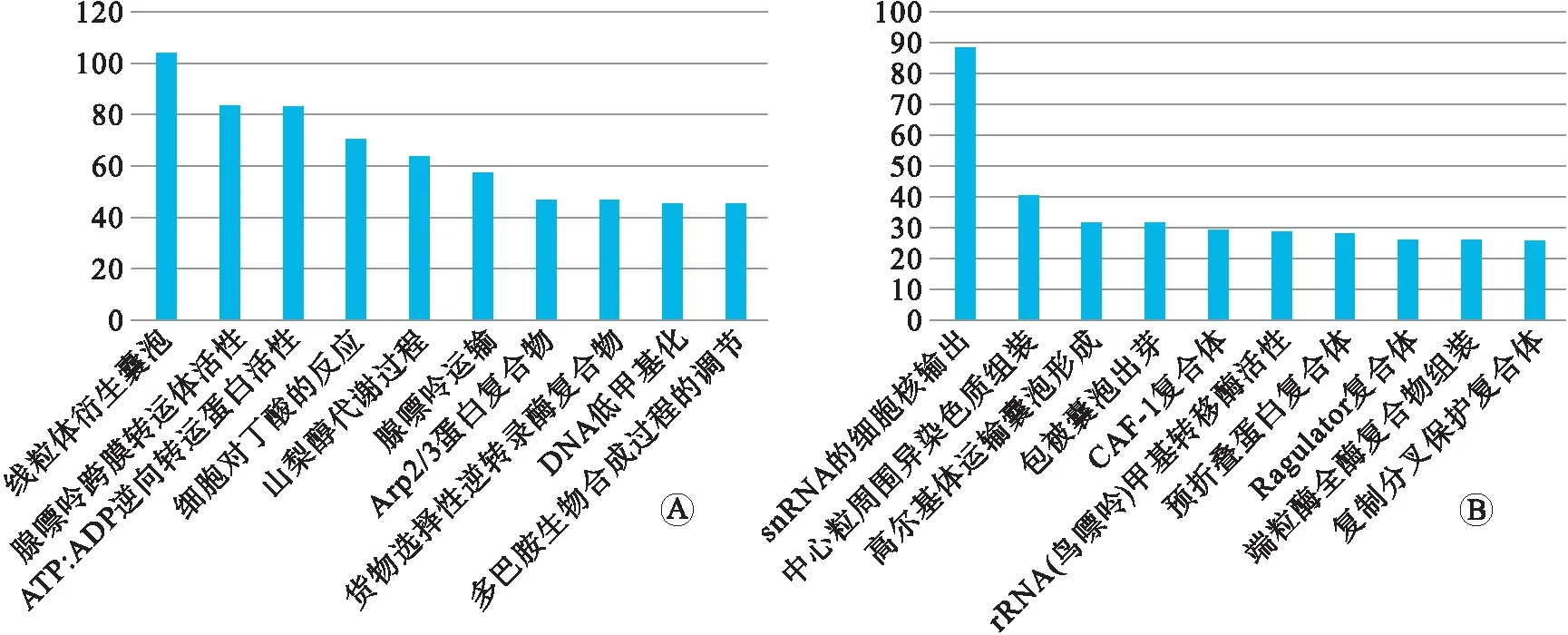
A:蛋白组下调-转录组无差异组;B:蛋白组上调-转录组无差异组。
2.3 差异蛋白互作网络分析STRING分析显示在草酸钙晶体处理后HK-2细胞差异表达基因MYH9、MYH14、MYH1、MYL12A、ACTB、ARPC1A、ARPC2、ANXA2、CFL1、PRDX1及PRDX2之间具有最为密切的相互作用(图4)。其相互作用网络节点为39,边数34,平均节点度1.74,平均局部聚类系数为0.39,预期边数为9,PPI富集P<0.001。
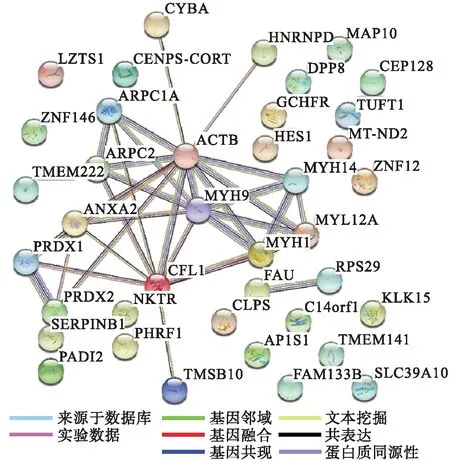
图4 差异表达蛋白相互作用网络分析
3 讨 论
肾结石的形成是一个异常复杂的过程,经典的结石形成机制包括晶核形成、尿液过饱和、晶体成长、晶体聚集等一连串的生物化学过程[6-7]。越来越多的研究关注到肾结石晶体对肾小管细胞造成的病理以及基因表达层面的损伤[8],结石晶体与肾脏细胞之间的相互作用研究对揭示结石起源及其造成的肾功能损害具有重要意义。
本研究通过构建结石晶体与近曲肾小管上皮细胞相互作用模型,采用转录组与蛋白组关联分析的方法,揭示了结石晶体对HK-2细胞蛋白组以及转录组的改变。发现了蛋白组和转录组差异表达的基因集合,差异表达基因主要集中在蛋白组改变-转录组无差异的集合,表明差异基因蛋白表达水平调控很可能与转录后调控有关[5, 9-10]。另外,本研究发现蛋白组上调-转录组无差异的基因681个,蛋白组下调-转录组无差异的基因455个。GO功能富集分析显示,差异基因主要涉及线粒体衍生囊泡、腺嘌呤跨膜转运、snRNA的细胞核输出以及中心粒周围异染色质组装等功能。证据表明肾小管上皮细胞线粒体功能障碍与草酸钙晶体形成、聚集以及Randall斑块的形成有关,是肾结石形成的重要机制[11]。KEEG富集分析显示差异表达基因主要影响缬氨酸、亮氨酸和异亮氨酸降解,维生素B6代谢、硫中继系统以及糖胺聚糖生物合成和DNA非同源末端链接等信号通路。研究发现维生素B6作为丙氨酸-乙醛酸转氨酶的辅助因子,可通过减少肝脏中草酸的生成来减少草酸的排泄,与肾结石的形成密切相关[12]。有研究表明乙醛酸和二羧酸代谢,甘氨酸、丝氨酸和苏氨酸代谢,苯丙氨酸代谢,柠檬酸循环4种代谢途径都与肾结石密切相关[13-14]。因此,本研究发现缬氨酸、亮氨酸和异亮氨酸降解通路可能为蛋白质/氨基酸代谢在肾结石形成中的作用提供新的见解,其确切作用及机制有待进一步研究。运用STRING构建差异基因相互作用网络后,发现ACTB、MYH9、MYH14、CFL1等11个关键节点基因。ACTB和CFL1参与细胞运动、结构、完整性和细胞间信号传导,在细胞骨架以及细胞形状维持中发挥重要作用[15];研究发现MYH9、MYH10以及MYH14与肾小球滤过功能密切相关,赋予肾单位片段特异性膜转运特性[16]。由此可见草酸钙晶体对近曲肾小管上皮细胞功能和形态具有显著影响。
综上所述,本研究通过转录组与蛋白组关联分析揭示草酸钙结石晶体对人肾近曲小管上皮细胞基因表达的影响,发现了肾结石形成过程中可能涉及的关键通路及关键基因,为肾结石形成机制的阐明及防治策略研究提供了新线索。本研究采用高通量技术以及生物信息学分析,研究方法存在一定局限性,相关基因及通路还需要细胞实验及临床样本进一步验证。