一种三维多孔Au/N/C的合成策略及其在双酚A电化学传感中的应用
2022-11-24郭晨宇吴逸阳巩斯曼李晓宇姬柳迪
朱 敏, 郭晨宇, 吴逸阳, 巩斯曼, 李晓宇*, 姬柳迪
(1.武汉纺织大学电子与电气工程学院,新型纺织品微纳加工技术研究中心,湖北武汉 430200; 2.湖北科技学院,辐射化学与功能材料湖北省重点实验室,湖北咸宁 437100)
碳材料由于其良好的稳定性与导电性,在电化学领域具有广阔的应用前景,一直备受研究者青睐[1 - 3]。近来年,为改善碳材料反应活性以提高其电化学性能,研究者们提出了化学官能团功能化[4]、制备复合碳材料[5]和掺杂多种杂原子[6]的方法。其中,化学掺杂被认为是调节其电子结构和电荷分布的有效方法,特别是通过共掺杂或者共负载的方式引入两种或两种以上杂原子,可以制备出具有独特电子结构的新型功能碳纳米材料[7,8]。Zhou等人利用生物还原法制备了直径约20 nm的纳米Au颗粒,并将其负载于N掺杂碳纳米片上,该Au/N/C三元复合材料表现出优异的电催化性能[9]。Chen等人制备了金属Ni与N元素共掺杂的碳纳米材料,对于葡萄糖氧化表现出了超高活性,成功构筑了无酶型葡萄糖电化学传感器[10]。因此,如何避免掺杂元素的团聚,实现其在碳基底上均匀分布,提高合成材料的性能具有十分重要的意义。多孔碳具有极大的比表面积、独特的多孔贯通结构、可控的孔隙率和适当的孔径。同时多孔碳还具有优异的导电性,大量易于接近的活性位点,畅通无阻的离子传输途径,一直被认为是一种性能优异的电化学敏感材料[11,12]。然而,常用来制备多孔碳的方法是纳米SiO2硬模板法。这种方法不仅耗时长、成本高,并且需要使用剧毒和强腐蚀性HF来去除SiO2模板,这也使得该方法难以在现实中广泛使用。因此,开发一种简便、经济、有效且绿色的方法来制备具有良好电化学活性的金属/N元素共掺杂多孔碳材料是很有必要的。
本研究以绿色无害的NaCl为模板,聚乙烯吡咯烷酮(PVP)为前驱体,氯金酸为金属源,采用自生长策略合成了Au/N负载多孔碳(Au/N/C)。使用多种技术对材料进行表征,发现其形成了具有丰富的微孔和高比表面积的三维多孔结构,且微量Au和N元素分散掺杂到整个三维多孔碳骨架中,为电化学传感提供了大量的催化活性位点。进而,研究了典型探针分子K3[Fe(CN)6]和常见的环境污染物双酚A(BPA)在不同材料表面的电化学行为,发现Au/N/C表现出良好的电化学性能和显著的信号增强效应。基于此,成功构建了一种新型的具有高灵敏度的BPA电化学传感平台,将构建的电化学方法用于污水样品的检测,采用标准加入法进行回收率实验,回收率在98%~105.2%之间,相对标准偏差均小于5%。
1 实验部分
1.1 仪器和试剂
所有电化学测试实验均在CHI 660E电化学工作站(上海辰华仪器有限公司)上完成,采用三电极体系:直径3 mm的裸玻碳电极(GCE)或修饰电极为工作电极,铂柱电极为对电极,饱和甘汞电极为参比电极。X射线衍射(XRD)测量在PANalytical X'Pert PRO光谱仪(PANalytical,荷兰)上进行。材料的形貌和结构表征来自于日本日立有限公司的SU8010扫描电子显微镜(SEM),荷兰FEI公司的Tecnai G2 F30高分辨率透射电子显微镜(HRTEM)。
NaCl、聚乙烯吡咯烷酮(PVP)、HAuCl4·3H2O、双酚A(BPA)均购于美国Sigma Aldrich公司。以乙醇为溶剂,制备BPA储备溶液(1 mg/mL),存储于4 ℃冰箱保存。实验中用到的所有化学试剂均为分析纯。实验用水为MilliQ纯净水系统中所得电阻率为18.2 MΩ·cm的超纯水。
1.2 Au/N/C复合材料的制备
采用有机溶剂诱导重结晶方法对NaCl粉末进行前处理。即将80 g NaCl粉体完全溶解在250 mL超纯水中,然后在混合溶液中加入250 mL乙醇并不断搅拌。由于有机溶剂的加入会使NaCl溶解度急剧下降,从而析出大量白色的NaCl晶体。最后经过抽滤、干燥、仔细研磨,得到最终使用的NaCl模板。利用过量NaCl模板配制饱和NaCl溶液,并取上清液待用。首先将1 g PVP完全溶解在15 mL饱和NaCl溶液中,然后分三次加入50 μL的0.1 mg/mL氯金酸溶液并搅拌均匀。随后,将制备的混合溶液在-80 ℃冰箱中真空冷冻干燥,直至混合溶液中的水完全升华。继而将冷冻干燥的产物仔细研磨后,放入瓷舟并置于管式炉中于N2气氛下800 ℃煅烧2 h(升温速度5 ℃/min),得到黑色固体。然后,用超纯水反复超声清洗所得黑色固体粉末以去除NaCl模板。最后在60 ℃鼓风干燥箱中干燥,得到最终产物Au/N/C。为了对比,在不添加氯金酸的前提下,重复上述步骤制备具有不含纳米Au颗粒的三维多孔N/C。
1.3 BPA电化学传感平台的构建
准确称量1 g所制备Au/N/C或N/C,将其溶解于1 mL N,N-二甲基甲酰胺中,超声20 min以混合均匀。将所得混合溶液滴涂于打磨光滑并清洗干净的GCE表面即可得到修饰电极。电化学测试以pH=4.6的HAc-NaAc缓冲溶液(0.1 mol/L)为支持电解质溶液,在0.3 V电位下搅拌富集90 s后,采用差分脉冲伏安法(DPV)采集信号。仪器条件:扫描速率为40 mV/s,振幅为50 mV,宽度为40 ms,记录0.65 V处的氧化峰信号,作为BPA的检测信号。
2 结果与讨论
2.1 Au/N/C的合成策略
如图1所示,用重结晶法得到的立方体NaCl晶体配制饱和NaCl溶液,再将水溶性的聚合物PVP完全溶解在饱和NaCl溶液中,接着加入一定量的HAuCl4溶液并搅拌均匀。在-80 ℃条件下对混合溶液进行冷冻干燥,由于水中溶解的NaCl的量远大于其他两种物质,NaCl晶体最先析出,析出的PVP和纳米Au会在其表面形成自组装的团聚体,最终得到表面被PVP-Au包覆的NaCl材料。然后,在800 ℃ N2气氛下对其进行煅烧碳化。最后,用水反复超声清洗可以轻易去除材料中的NaCl模板,得到负载纳米Au的三维多孔网络材料Au/N/C。

图1 Au/N/C合成过程示意图Fig.1 Illustration of the synthesis process of the Au/N/C
2.2 Au/N/C的形貌与结构
采用X射线衍射(XRD)研究了PVP、800 ℃煅烧后未去除NaCl模板的Au/N/C前驱体、Au/N/C和N/C的晶体结构特性。如图2所示,Au/N/C前驱体在2θ分别为27.3°、31.9°、45.5°、54.0°、56.5°、66.3°、75.2°处出现了明显的衍射峰,分别对应于NaCl粉末的(111)、(200)、(220)、(311)、(222)、(400)、(420)晶面。这些衍射峰都呈现尖锐的峰形和高强度,说明冷冻干燥形成NaCl结晶在800 ℃煅烧后依然保持良好的晶相。在N/C的XRD曲线中可以在2θ26°处明显看到归属于碳材料(002)晶面的衍射峰,而在Au/N/C的曲线中新增了在38.1°、43.9°、64.5°、77.5°处的衍射峰,分别归属于纳米Au颗粒的(111)、(200)、(220)、(311)晶面,证明Au/N/C复合材料成功合成。
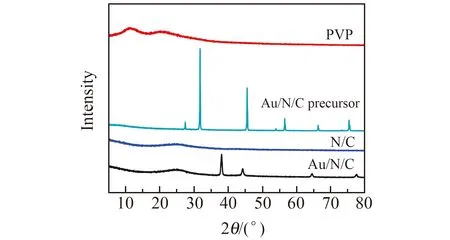
图2 PVP、去除NaCl模板前的Au/N/C前驱体、N/C以及Au/N/C的XRD图谱Fig.2 XRD patterns of PVP,the precursor of Au/N/C before NaCl removing,N/C and Au/N/C
为深入了解所得材料的形貌结构和化学组成,采用扫描电子显微镜(SEM)和高倍透射电镜(HRTEM)对制备的N/C和Au/N/C进行了系统表征。如图3a~b所示,可以看到N/C由大量类石墨烯的超薄壁相互贯通、相互折叠形成了三维多孔形态,这也为纳米Au颗粒的负载提供了良好的支撑骨架。从图3c~f中可以看出,加入的HAuCl4溶液最终形成了大量的纳米Au颗粒,且分散在整个三维多孔碳结构之中。同时,从能谱图(图3g~j)中可以清楚的看到N元素与C元素分布均匀且高度重合,而在碳基底上还有零散分布的纳米Au,说明成功得到了表面分布着丰富纳米Au颗粒的N掺杂碳纳米材料。丰富的褶皱和孔洞结构可以提供更大的反应活性面积,有利于反应物的吸附与富集,而Au、N等异质元素的引入,则有望赋予其更高的电化学催化活性,增强电子转移能力。
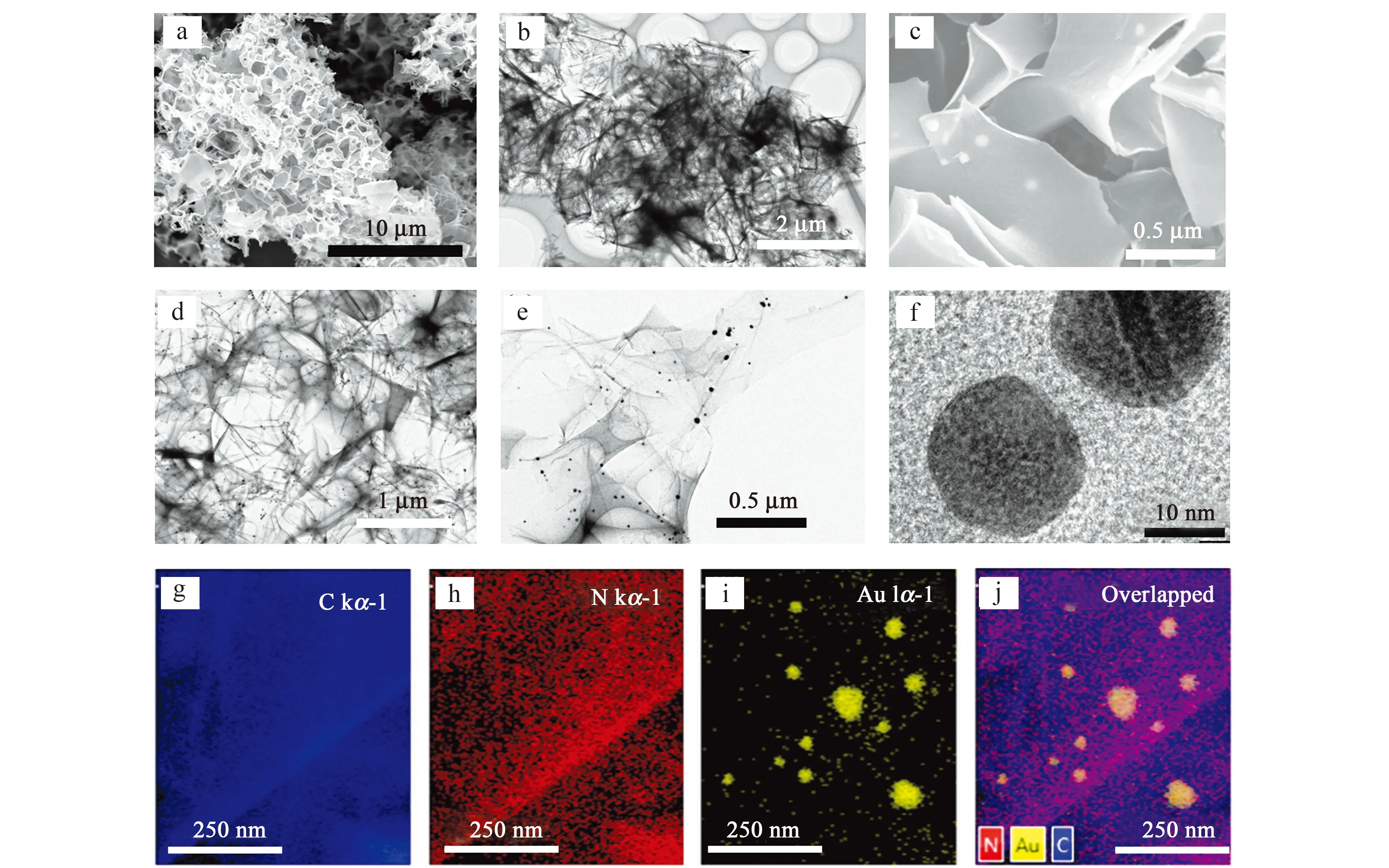
图3 N/C的SEM图(a)和HRTEM图(b),Au/N/C的SEM图(c)和HRTEM图(d~f),Au/N/C的EDX(g~j)Fig.3 SEM image (a) and HRTEM image (b) of N/C,SEM image (c) and HRTEM images (d-f) of Au/N/C and EDX element mapping images (g-j) of Au/N/C
2.3 Au/N/C的增敏效应
利用循环伏安法(CV)和电化学阻抗法(EIS)研究了不同合成材料的电化学性能。图4a为GCE、N/C和Au/N/C在5 mmol/L K3[Fe(CN)6]溶液(1 mol/L KCl)中的CV图。如图所示,相比于GCE,N/C和Au/N/C修饰电极上K3[Fe(CN)6]的氧化还原峰电流明显增大,说明修饰电极具有更高的电化学活性。而与N/C相比,Au/N/C具有更高的氧化峰电流,更小的氧化还原峰电位差,同时K3[Fe(CN)6]氧化还原峰峰形也变得更为尖锐和对称,说明纳米Au的引入进一步提高了材料的电化学活性。图4b为不同电极在5 mmol/L K3/K4[Fe(CN)6]溶液(1 mol/L KCl)中的阻抗图。在修饰了N/C和Au/N/C材料之后,图中曲线的Rct值急剧减小,这可能是由于N/C和Au/N/C丰富的三维多孔结构和异质结构大大提升了传质效率和电子传输能力。Au/N/C比N/C具有更小的Rct值,这意味着Au/N/C具有最优的电子传递效率,这个结果也与之前CV法的结果相一致。
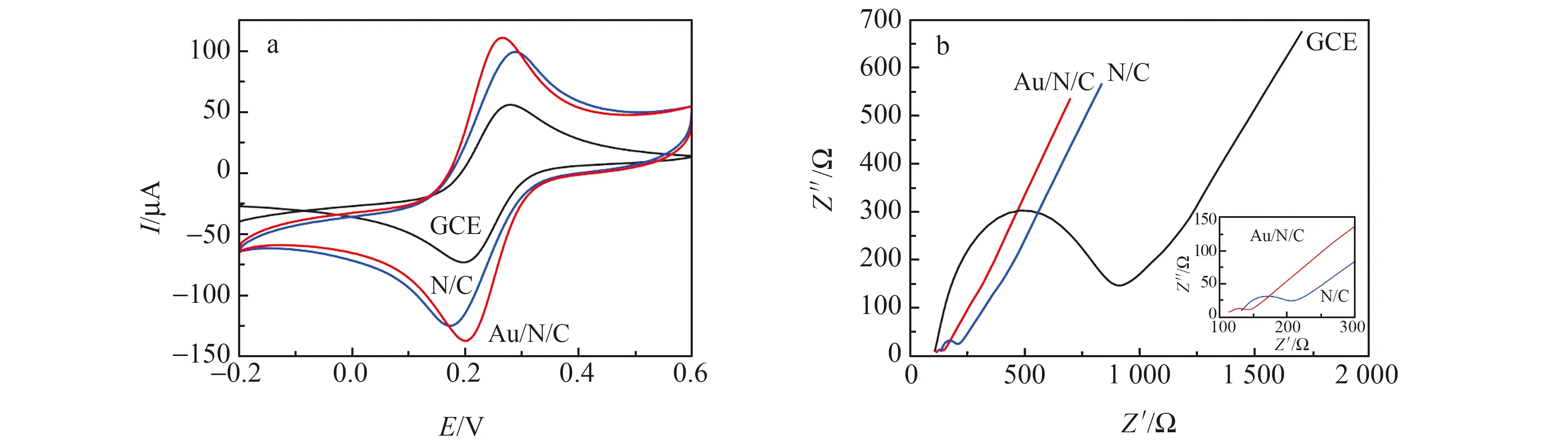
图4 (a)GCE、N/C、Au/N/C在含有5 mmol/L K3[Fe(CN)6]的1 mol/L KCl溶液中于扫速100 mV/s的循环伏安图;(b)GCE、N/C、Au/N/C在含有5 mmol/L K3/K4[Fe(CN)6]的1 mol/L KCl溶液中的阻抗图(频率范围:0.01 Hz~100 kHz)Fig.4 (a) Cyclic voltammograms of GCE,N/C and Au/N/C in 5 mmol/L K3[Fe(CN)6] (1 mol/L KCl) at 100 mV/s;(b) Nyquist plots of GCE,N/C,Au/N/C in 5 mmol/L K3/K4[Fe(CN)6](1 mol/L KCl)(frequency range:0.01 Hz to 100 kHz)
为了进一步验证其电化学增敏效应,分别用循环伏安法(CV)和差分脉冲伏安法(DPV)研究了高浓度和低浓度BPA在不同电极材料上的电化学行为,其支持电解质为0.1 mol/L的HAc-NaAc缓冲溶液(pH=4.6)。如图5a所示,在0.5 g/L BPA溶液中,GCE表面可以观测到一个微弱的氧化峰,但在N/C和Au/N/C表面,BPA的氧化峰电流均出现了显著增强,且氧化峰位置也发生了明显负移,并且Au/N/C表面具有最大的氧化峰电流和最负的氧化峰电位,说明Au/N/C对BPA的电化学氧化具有明显的增敏作用。在低浓度(1 mg/L)的BPA溶液中,利用DPV法再次确认了Au/N/C良好的电化学表现,从图中可以看到,在0.65 V处Au/N/C表面出现了一个明显的氧化峰(图5b)。与N/C和GCE表面的氧化峰相比,其具有明显增大的峰电流,同时峰形也更为尖锐,更便于观测。上述现象进一步确认了合成的Au/N/C具有良好的电化学增敏能力,可以显著提升BPA的电化学传感信号。

图5 (a)GCE、N/C、Au/N/C在0.5 g/L的BPA溶液中于扫速100 mV/s的循环伏安图;(b)GCE、N/C、Au/N/C在1 mg/L的BPA溶液中的差分脉冲图线(缓冲溶液:0.1 mol/L HAc-NaAc缓冲溶液(pH=4.6)Fig.5 (a)Cyclic voltammograms of GCE,N/C and Au/N/C in 0.5 g/L BPA at 100 mV/s;(b) DPV of GCE,N/C and Au/N/C in 1 mg/L BPA(supporting electrolyte:0.1 mol/L HAc-NaAc buffer,pH=4.6)
2.4 BPA电化学传感平台的构建
为了构建高灵敏的BPA电化学传感平台,在1 mg/L BPA溶液中,对实验中的一些重要参数(富集电位、富集时间和Au/N/C修饰用量)进行了优化。从图6a中可以看到,从0.0 V开始,随着富集电位的增加,BPA的氧化峰电流逐渐增加,到0.3 V时达到最大峰电流,然后随着富集电位的增加开始出现峰电流的降低。在0.3 V的富集电位下,我们探究了富集时间的影响,结果如图6b所示。当富集时间从30 s增加到90 s的过程中,氧化峰电流逐渐增大,这可能是因为富集时间的延长增加了Au/N/C的多孔结构中BPA的吸附量,带来了更强的响应信号,但是在90 s之后,BPA的氧化峰电流出现了显著的降低。如图6c所示,当Au/N/C修饰量从2 μL增加至4 μL时,BPA的氧化峰电流逐渐增加,而当修饰量继续增加时,氧化峰电流开始下降。因此,最终选择的测试条件为富集电位:0.3 V;富集时间:90 s;Au/N/C修饰用量:4 μL。

图6 富集电位(a)、富集时间(b)和Au/N/C修饰量(c)对BPA氧化峰电流的影响Fig.6 Effects of accumulation potential (a),accumulation time (b) and the modified amount of Au/N/C on the oxidation peak current of BPA
2.5 BPA电化学传感器平台的分析性能
在最优条件下,采用DPV法检测不同浓度BPA在0.65 V产生的氧化峰电流值。如图7a所示,BPA的氧化峰电流随其浓度的增加而增大,且其浓度和对应氧化峰电流在0.05~5 mg/L内表现出了良好的线性关系,线性方程为:I(μA)=1.118c(mg/L),相关系数r=0.9999。计算出其检出限(S/N=3)为0.014 mg/L(约为60 nmol/L)。

图7 (a)Au/N/C在不同浓度BPA中的DPV图;(b)BPA氧化峰电流与浓度的线性拟合曲线Fig.7 (a) DPV of Au/N/C in BPA with different concentration;(b) Linear fitting curve of BPA peak currents and the corresponding concentration
本检测方法与目前已有报道的BPA电化学传感器相比,具有更优或者相当的检出限[13 - 16](表1)。

表1 不同电化学传感平台测定BPA性能比较Table 1 Performance comparison of different electrochemical platforms for the detection of bisphenol A
为了测试所构建的电化学检测平台的重复性,我们将7支Au/N/C修饰电极置于含有1 mg/L BPA的0.1 mol/L pH=4.6的HAc-NaAc溶液中进行DPV扫描,记录所有观测到的BPA氧化峰电流值并计算相对标准偏差(4.7%),验证了该方法具有很好的重现性。
此外,稳定性也是评估电化学传感平台性能的一个重要指标。首先实验记录Au/N/C修饰电极分别在0.2 mg/L、0.5 mg/L和1 mg/L BPA溶液中的DPV曲线,然后将修饰电极直接放置在室温空气环境中,在第7天时重新测量,发现在3种不同浓度的BPA溶液中其氧化峰电流响应值分别保留了原始值的94.1%、93.9%和96.6%,验证了该电化学传感器具有良好的稳定性。
同时,实验研究了一些潜在的干扰物对BPA测定结果的影响。实验考察了一些可能与BPA共存的酚类污染物的影响,结果发现20 mg/L对苯二酚、邻苯二酚和对硝基酚,10 mg/L苯酚和对氨基酚对0.5 mg/L BPA的测定几乎没有影响(电流信号变化小于5%)。
2.6 实际样品检测
为了评估构建的电化学传感器在实际样品检测中的应用潜力,我们将其用于本地工厂实际污水样品检测,采用标准加入法评判该方法的准确性。在测量前,首先用0.22 μm的微孔滤膜过滤工业废水,然后取5 mL过滤后的清液加入5 mL 0.1 mol/L的HAc-NaAc缓冲溶液(pH=4.6)中,按照前述测量条件,记录其DPV曲线以及在0.65 V处氧化峰电流值。每份样品均平行检测3次,测得氧化峰电流值的RSD均小于5%。实验结果如表2所示,实际污水样品的加标回收率值在98.0%~105.2%范围内,表明构建的BPA电化学传感器具有较高的检测准确度,有应用于实际污水检测的潜在价值。

表2 实际污水样品中BPA的测定Table 2 Determination of BPA in industry wastewater samples
3 结论
本文提出了一种绿色环保的方法,制备得到了表面均匀负载纳米Au的三维多孔氮碳材料(Au/N/C)。一方面,三维多孔结构可以提供良好的传质途径以及富集性能;另一方面,Au纳米颗粒与N元素的掺杂能改变电子结构,提供丰富的电化学反应活性位点。得益于Au/N/C优异的电化学性质,它对双酚A的电化学氧化表现出了显著的信号增强效应。基于此,成功构建了一种快速、简便、灵敏的BPA电化学传感平台,并运用于实际样品检测。更进一步的,考虑到金属元素和异质元素的多样性,本文提出的策略对于制备其他具有良好性能的多孔碳杂化材料合成具有参考意义。
