离子色谱法同时测定燃料电池车用氢气中氯化氢和甲酸含量
2022-11-22郝逍瑶王少军凌凤香
韩 博,郝逍瑶,王少军,凌凤香
(中石化(大连)石油化工研究院有限公司,辽宁 大连 116045)
0 引 言
目前,全球汽车保有量正以每年 3 000 万辆的速度递增,我国汽车保有量已达3.07亿辆,居全球首位。基于能源枯竭危机和尾气排放造成的环境污染日趋严峻,新燃料汽车越来越受到世界各国政府、汽车厂商和相关研究机构的普遍重视和青睐。作为2l 世纪最有发展前景的新能源环保型汽车——氢燃料电池汽车,在全球范围内已迈入示范运行。
作为新能源环保型汽车燃料的氢气,其产品的纯度和所含杂质的种类及含量对氢燃料电池的放电性能和寿命具有重要作用,对燃料电池汽车产业的健康发展有重要影响。甲酸是一种严重影响燃料电池性能的毒物,易吸附在燃料电池催化剂表面,特别是在燃料电池阳极催化剂量少时,很容易使催化剂中毒、降低催化效能[1];氯碱生产过程和氢气生产中所用的制冷剂和清洁剂等引入的卤化物在电池阴极上的竞争吸附则会引起燃料电池产生不可逆的劣化[2]。
国家标准GB/T 37244—2018《质子交换膜燃料电池汽车用燃料氢气》[3]于2019年7月1日起开始实施,该标准规定了质子交换膜燃料电池(PEMFC)汽车用燃料氢气中14种杂质的限量要求及其分析试验方法等。其中规定了甲酸含量要低于 0.2 µmol·mol-1,总卤化物(按卤离子计)要低于0.05 µmol·mol-1。分析甲酸常用的方法有傅里叶变换红外光谱法[4]和离子色谱法[5]等,分析卤化物常用的方法有离子色谱法[6]和气相色谱法[7]等。离子色谱价格相对低,且操作简单,常用于测定大气[8]、土壤[9]和水[10]中的各类阴、阳离子。GB/T 37244附录中规定了采用离子色谱法测定氢气中总卤化物的方法,但该方法中对氢气的富集用气量较大,且针对痕量级的物质分析,方法中应用的湿式气体流量计精度无法满足要求。由于甲酸根离子同样可通过离子色谱柱分离检测,且与卤离子峰不重叠,所以本文拟采用高精度质量流量计,通过正交实验等对吸收富集条件进行优化,用同一份吸收富集样品建立同时测定燃料电池车用氢气中氯化氢和甲酸的离子色谱方法。应用该方法节省用气量,加快分析时间,提升测试结果准确度。
1 实验部分
1.1 仪器与试剂
ECO IC型离子色谱仪:瑞士Metrohm公司,配抑制型电导检测器;Milli-Q Advantage A10型超纯水系统,法国默克密理博公司;0.22 µm水系针式微孔滤膜过滤器,比克曼生物公司。
氯化钠、甲酸钠为优级纯,天津光复科技发展有限公司。
碳酸钠、碳酸氢和氢氧化钾均为分析纯,天津光复科技发展有限公司。
以氢气为稀释气的氯化氢标气和甲酸标气,大连大特气体有限公司。
1.2 仪器工作条件
METROSEP A SUPP 5 -150型阴离子色谱柱(25 cm×4 mm);Metrosep RP2 Guard/3.5通用型保护柱(5 cm×4 mm);柱温 35 ℃;流动相为 3.2 mmol·L-1Na2CO3+1.0 mmol·L-1NaHCO3的 淋 洗 液 ; 进 样体积 100 µL;流量为 0.7 mL·min-1;洗脱方式为等度洗脱。
1.3 标准溶液配制
分别准确称取 0.165 g和 0.152 g(精确至0.1mg)于105 ℃条件下烘干2 h的氯化钠和甲酸钠,溶解于水中,定容至1 000 mL容量瓶,摇匀,得到浓度为 0.1 g·L-1的氯离子标准贮备液 A和0.1 g·L-1的甲酸离子标准贮备液B。
1.4 试验方法
将50 L氢气以0.5 L·min-1的流速通过50 mL去离子水,氢气中的氯化氢和甲酸被水吸收,定容过的吸收液经过0.22 µm水系针式微孔滤膜过滤器过滤后经离子色谱进行定量测定,再根据通过去离子水吸收的气体总体积,换算出气体中的氯化氢和甲酸含量。
2 结果与讨论
2.1 吸收条件优化
2.1.1 吸收装置
采用如图1所示的气体吸收装置用水溶液对氢气中的氯化氢和甲酸进行吸收。应用质量流量计对吸收氢气体积进行精确计量,提高分析准确度。
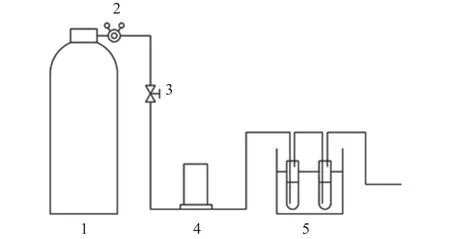
图1 气体吸收装置示意图
2.1.2 吸收瓶串联数量优化
为了防止单一吸收瓶吸收不够完全,将4个吸收瓶分别装入同体积纯水,以串联的方式分别对5.11 µmol·mol-1的氯化氢和 1.60 µmol·mol-1的甲酸进行吸收试验,考察4个串联吸收瓶各自的吸收回收率,吸收回收率以测试结果与标气浓度之比计算而得,结果见图2。
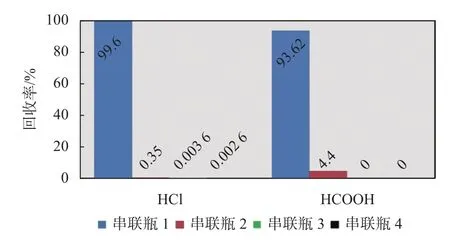
图2 串联瓶吸附回收率
由图 2 可知,对于 5.11 µmol·mol-1的氯化氢,第一个吸收瓶的吸收回收率已达到99%以上,而对于1.60 µmol·mol-1的甲酸,第一个吸收瓶的吸收回收率未达到95%。合计前2个吸收瓶的吸收回收率,结果均已达到99.9%以上。为保证吸收完全,采用2个吸收瓶串联的方式进行吸收实验。
2.1.3 正交实验
吸收过程中影响吸收回收率的因素主要有气体流速、吸收液体积和吸收时间,设计正交试验,对参数进行优化,确定吸收的最佳条件。考虑到实际氢气产品中的杂质含量量级,分别选取5.11 µmol·mol-1的氯化氢和1.60 µmol·mol-1的甲酸进行正交试验,其结果分别见表1和表2。
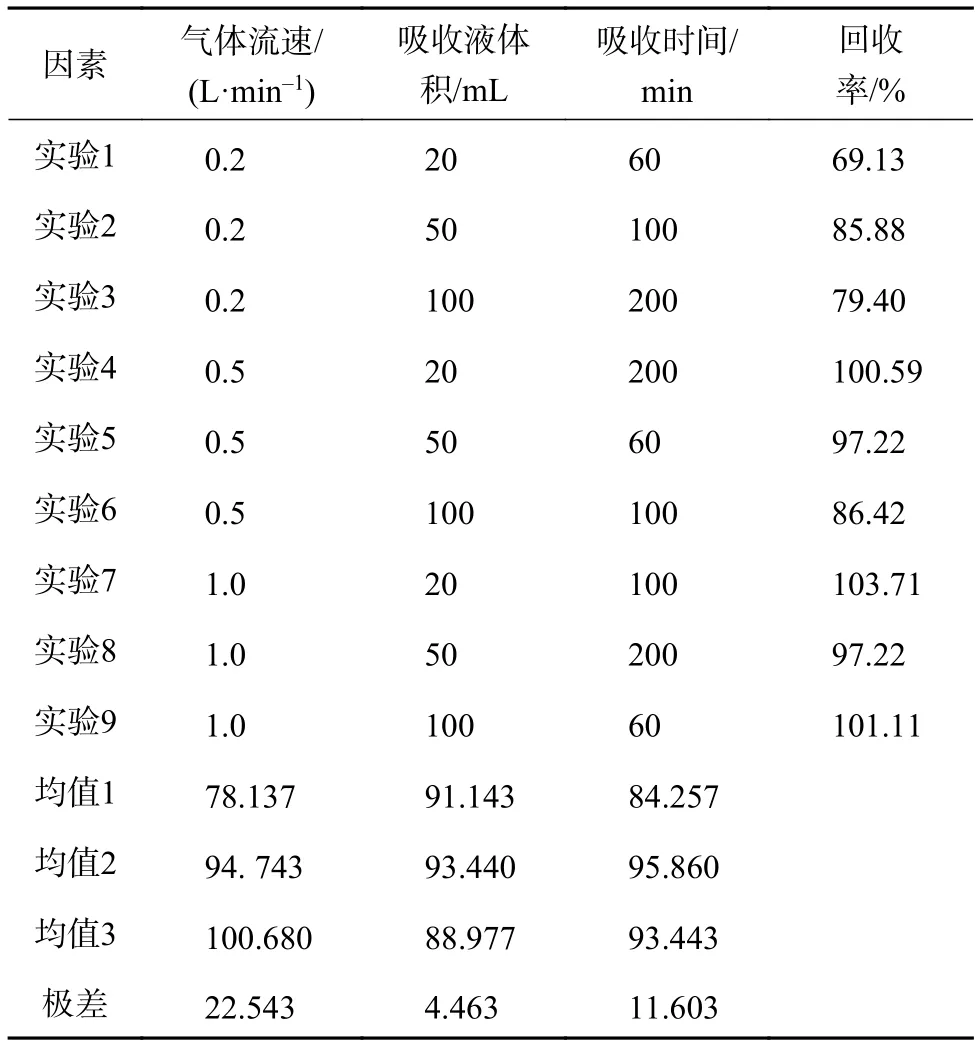
表1 5.11 µmol·mol-1 HCl正交试验结果
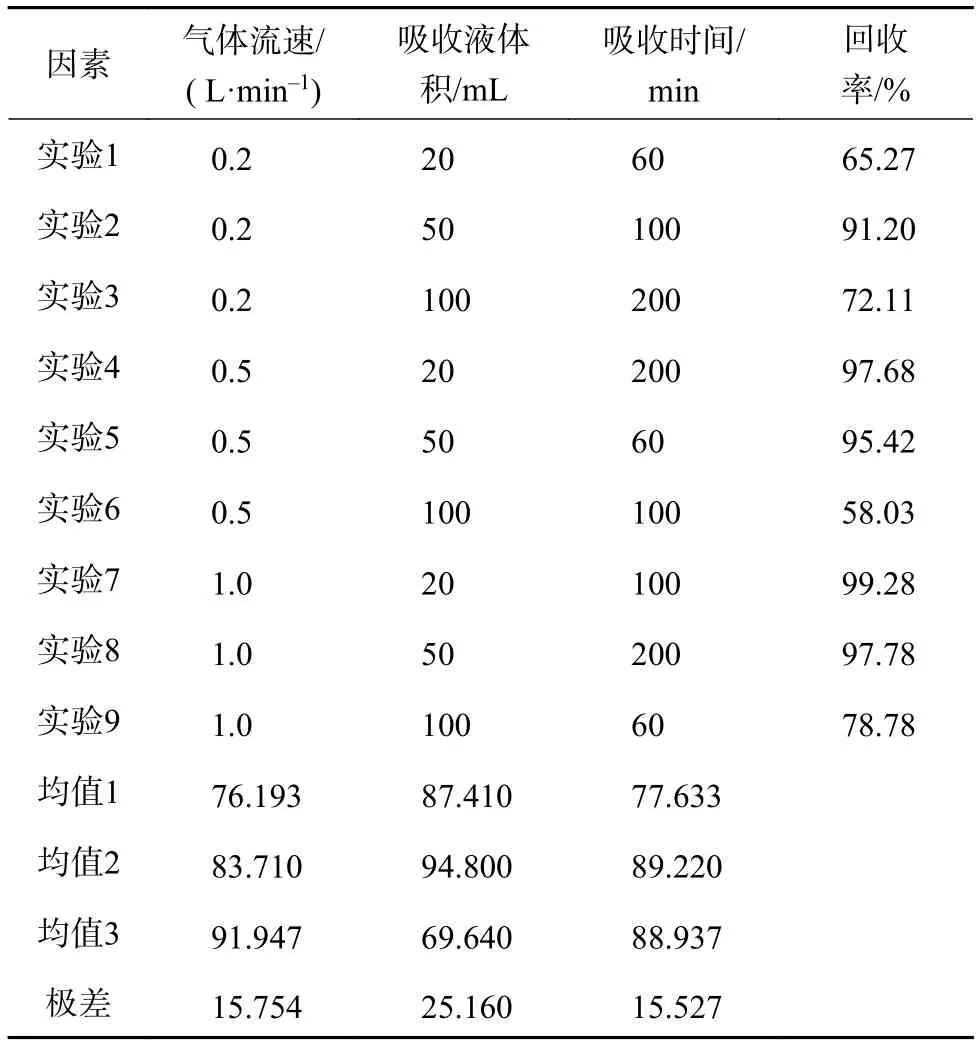
表2 1.60 µmol·mol-1 HCOOH 正交试验结果
由表1和表2可知,气体流速过慢,会使吸收不完全,吸收回收率大幅降低,这可能是因为适当的气流速度对吸收溶液起到搅拌作用,加快了吸收反应;同样地,吸收液体积过多也会导致吸收回收率降低,这是因为气体中的氯化氢和甲酸含量非常低,过多的溶液对其起到大倍数稀释作用,使其定量准确度降低。对于5.11 µmol·mol-1的氯化氢,吸收条件对吸收回收率的影响大小排序为气体流速>吸收时间>吸收液体积,对于 1.60 µmol·mol-1的甲酸,吸收条件对吸附回收率的影响排序则为吸收液体积>气体流速>吸收时间,且二组实验的最优吸收条件均为吸收液体积50 mL,气体流速1.0 L·min-1,吸收时间100 min(以下称条件1)。
考虑到方法测试用气量大,实际样品采样、运输的特殊要求,且实际样品中待测物质浓度较低,将气体流速降低至0.5 L·min-1(以下称条件2)。进一步考察两个吸收条件下的吸收回收率,结果见表3。
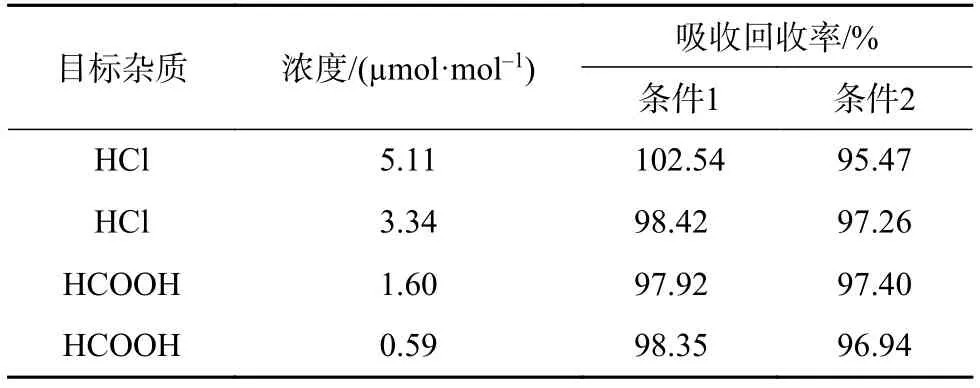
表3 不同吸收条件吸收回收率结果
由表3可以看出,将气体流速由1.0 L·min-1调整为 0.5 L·min-1后,除 5.1 µmol·mol-1的氯化氢吸收回收率下降较大,其余浓度的氯化氢和甲酸吸收回收率未发生明显下降,且各组试验的吸收回收率均在95%~100%之间,故最终确定试验吸收条件为吸收液体积50 mL,气体流速0.5 L·min-1,吸收时间100 min。
2.2 色谱行为
按试验方法对吸收用空白水进行分析,见图3,在仪器工作条件下,典型色谱图见图3。
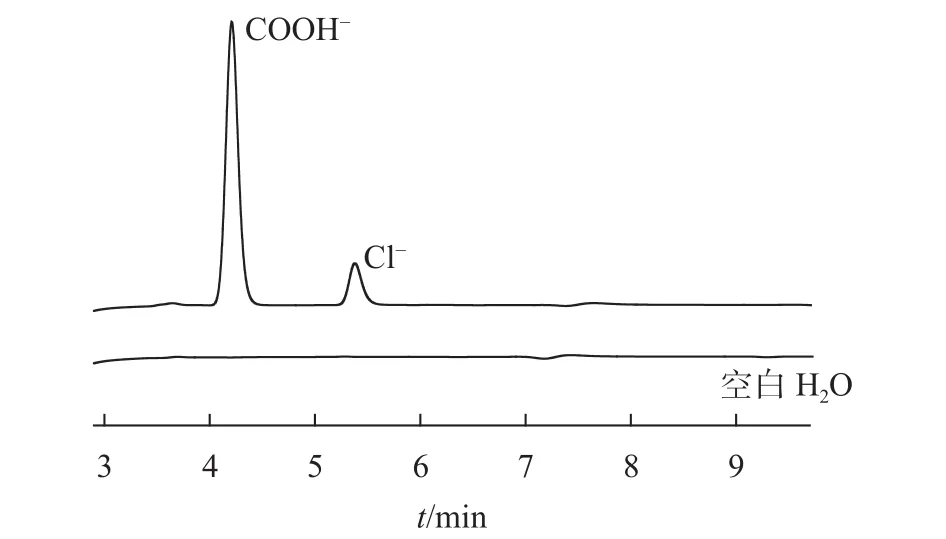
图3 典型色谱图
由图3可见,氯离子和甲酸离子可以实现良好分离,且吸收用空白水中不存在待测组分。
2.3 标准曲线和检出限
移取氯离子标准贮备液A和甲酸离子标准贮备液B用水逐级稀释得到高含量和低含量两种梯度级别的标准溶液。高含量和低含量的氯离子标准溶液浓度分别为 1.00,2.50,5.00,7.50,10.00 mg·L-1和 2.00,3.00,5.00,10.00,15.00 µg·L-1。高含量和低含量的甲酸离子标准溶液浓度分别为0.50,1.00,2.00,5.00,10.0 mg·L-1和 5.00,10.00,20.00,50.00,75.00 µg·L-1。
应用仪器工作条件对上述标准溶液进行测定,并以氯离子或甲酸根离子的质量浓度为横坐标,对应的峰面积为纵坐标绘制标准曲线,结果见表4。
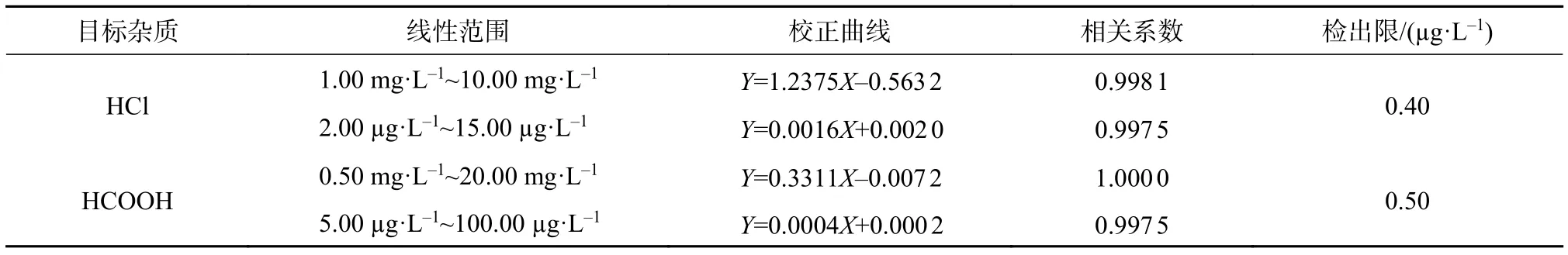
表4 线性参数和检出限
由表4可知,高含量和低含量的氯化氢及甲酸的相关系数均大于0.995。按3倍信噪比计算方法的检出限(3S/N),结果见表4。在标况下,当吸收液体积为50 mL,采气50 L时,通过公式1的换算,氯化氢的检出限为0.27 nmol·mol-1,甲酸的检出限为0.27 nmol·mol-1,该灵敏度可以满足实际氢气产品的测定需要。
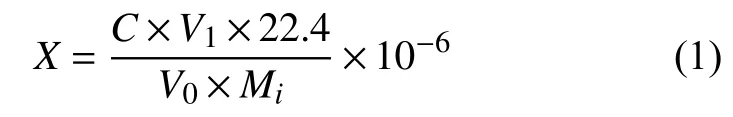
式中:X——氢气中氯化物或甲酸的体积分数;
C——吸收液中氯离子或甲酸根离子浓度,mg·L-1;
V1——吸收液的体积,mL;
V0——标准状态下,待测氢气的采样体积,L;
Mi——氯离子以35.5计,甲酸根离子以45计。
目前应用最广泛的氢气制取技术包括氯碱工业副产氢、电解水制氢、化工原料制氢,如:甲醇裂解,石化资源制氢,如煤制氢等[11-13]。氯碱工业副产氢中会含有一定的卤化物,高含量的标准曲线适用于原料气的测试,而低含量的标准曲线则适用于提纯后产品氢气的分析,用以验证提纯效果。高、低两条标准曲线可以避免由标准曲线跨越数量级造成的线性拟合失真。
2.4 精密度和回收试验
按试验方法对不同浓度的氯化氢和甲酸进行加标回收试验,计算各物质的回收率,同时,每个样品平行测定7次,计算测定结果的相对标准偏差(RSD),结果见表5。
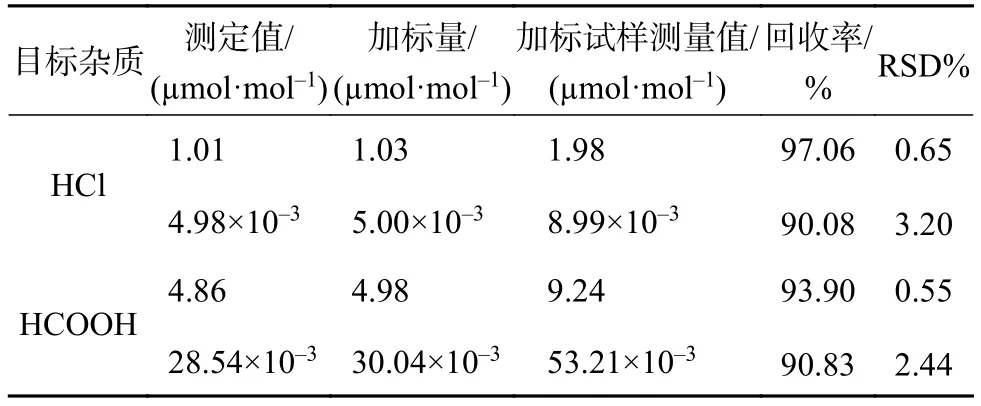
表5 精密度和回收试验结果(n=7)
由表5可知,高含量物质的回收率和RSD均优于低含量物质,且回收率均大于90%,RSD为0.55%~3.20%,表明该方法有较好的精密度。
2.5 方法比对
取3个标气样品,分别采用所建方法与标准方法进行测定,即氯化氢采用GB/T 37244—2018[3]附录A中规定的条件进行吸收并采用离子色谱法进行测定,甲酸采用ASTM D7653-18[4]中的红外光谱法进行测试,测试结果见表6。
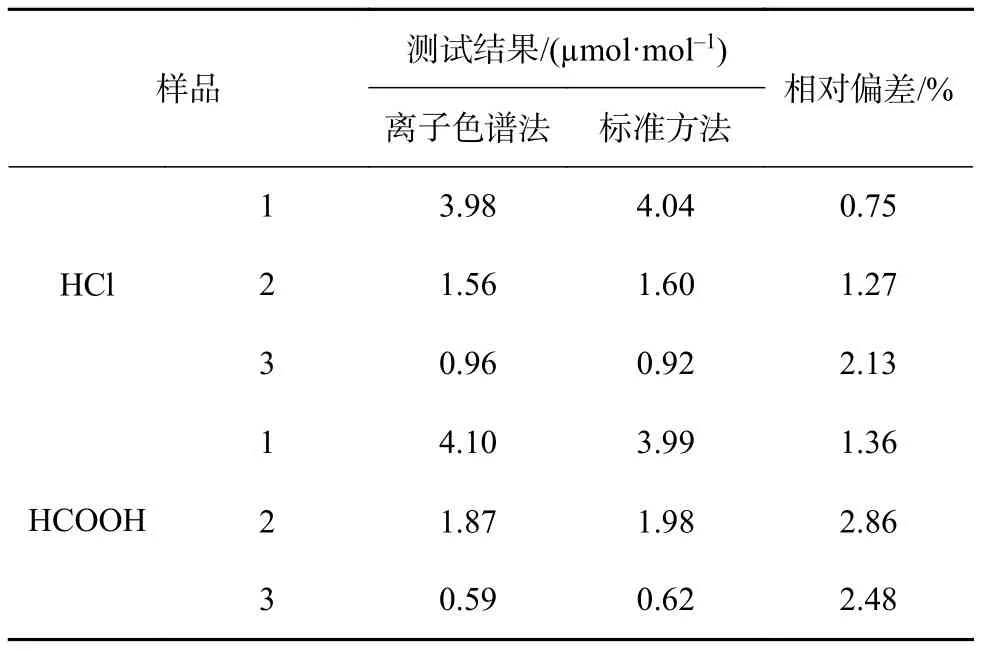
表6 不同测试方法结果1)
由表6 可知,对于HCl,两种方法测定结果的相对偏差为0.75%~2.13%,对于HCOOH,两种方法测定结果的相对偏差为1.36%~2.86%,均在误差允许范围内。相比标准方法,所建离子色谱法可同时测定氢气中氯化氢和甲酸含量,且测试结果准确,方法可行。
2.6 实际样品分析
按试验方法对30个不同来源的氢气样品进行测定,其中,煤制氢气检测到含有 1.71 µmol·mol-1的氯化氢,氯碱工业副产氢提纯后产品检测到9.40 nmol·mol-1的氯化氢,其余均不含有氯化氢和甲酸。
3 结束语
本工作通过正交实验优化了吸附条件,减少了气体用量,建立了离子色谱法同时测定燃料电池车用燃料氢气中氯化氢和甲酸含量的分析方法。该方法检出限远低于GB/T 37244—2018《质子交换膜燃料电池汽车用燃料氢气》中对总卤化物和甲酸的规定限值,并可以满足实际样品检测需求。
