过渡金属硫族化物纳米片的制备与生物应用
2022-11-10周雪蒙焦静静
周雪蒙,焦静静
(上海师范大学化学与材料科学学院,上海 200234)
0 引言
癌症是日益威胁人类生命健康的严重疾病之一.根据世界卫生组织报告,世界上有六分之一的死亡是由癌症引发的[1-2].尽管癌症的传统治疗方式,如化疗与放疗,在临床上已被长期应用与推广,但这类治疗方式会对人体造成很大的伤害,且有较高的肿瘤复发率[3-4].随着纳米技术的发展,功能性纳米材料的出现和应用使突破癌症治疗障碍成为可能.近几十年来,不同维度的纳米材料在各个领域得到了广泛的制备与应用,尤其是在生物成像、疾病治疗和药物传递等生物医学领域有着较好的应用前景[5-6].
过渡金属碳氮化物、氮化物与碳化物(MXenes)、氧化石墨烯(GO)、黑鳞(BP)、六方氮化硼(h-BN)、过渡金属硫族化物(TMDCs)[7]、金属有机框架(MOFs)和共价有机框架(COFs)等二维材料,由于其超薄的平面纳米结构和独特的物理化学性质,在新型肿瘤诊断与治疗试剂中受到了广泛的关注.TMDCs是一类类石墨烯材料,其广义的化学式为MX2,其中M代表元素周期表中ⅣB-Ⅷ族的过渡金属原子,如钼(Mo)、钨(W)、钛(Ti)等;X则代表硫原子或硒原子,其中金属原子形成的六边形层状结构夹在了两层硫原子之间,如图1所示[8].典型的TMDCs有二硫化钼(MoS2)、二硫化钨(WS2)、二硫化钛(TiS2)和二硒化钼(MoSe2)等.目前,水热/溶剂热合成方法、化学气相沉积法、液相剥离法和机械剥离法等合成方法已被用于设计和制备各类二维纳米材料.与其他二维纳米材料相比,TMDCs有较低毒性和良好的生物相容性,在肿瘤治疗和成像方面有着潜在的应用价值.TMDCs具有超高的比表面积和大量的活性作用位点,使材料表面易于被修饰且易为药物分子或生物分子提供负载的锚定位点[9].同时,TMDCs具有高近红外吸收特性,可作为光敏剂(PS)或光热剂载体进行肿瘤的光动力治疗(PDT)或光热治疗(PTT).其中,PTT相比传统的肿瘤治疗方式,具有侵袭性小、副作用低和靶向能力强等优点,是目前治疗肿瘤的有效方法之一.此外,通过负载具有不同功能的纳米颗粒或药物小分子,PTT还可以与其他治疗方式相结合,如PDT、化学动力学疗法(CDT)和化疗等,来提高材料整体的治疗效果[8].
近年来,人们对GO和MXenes等二维纳米材料的合成方法、改性策略以及它们在各个领域的应用都进行了综述.本研究主要针对TMDCs纳米片,总结了目前常用的合成方法与各种方法之间的优缺点,以及纳米材料的常用改性方法和它们在肿瘤诊疗领域的应用.
1 TMDCs纳米材料的合成与修饰
1.1 TMDCs纳米材料的合成
目前常用的TMDCs合成方法有机械剥离法、液相剥离法、化学剥离法和化学气相沉积法等.其中,剥离法均为自上而下的合成方法.简单来说,就是通过物理或者化学的方法将原本块状的材料层层剥离为单层或者少层的材料.这类剥离方法随着技术的发展,可以得到层数可控且质量稳定的层状材料,但大部分剥离法的条件相对复杂.而化学气相沉积法是一类自下而上的合成方法,通过化学方法直接合成得到单层或少层的纳米片,在合成的过程中,还可以直接掺杂金属等.
1.1.1 机械剥离法
微机械剥离是一种简单的用来剥离块状材料生产二维纳米薄片的方法.其中一种方法为透明胶带法,其最大的优点就是不需要使用昂贵而复杂的设备.TMDCs块状材料被放置在2个胶带之间,形成一个由胶带-MX2-胶带制成的夹层,通过将两端胶带分开,原本的块状材料分裂,在两边胶带上得到较薄且表面积相同的材料.重复上述操作,直到材料肉眼几乎看不见为止,然后将材料从胶带上转移至二氧化硅/硅(SiO2/Si)衬底上[10].这种剥离方法虽然简便,但不能保证获得厚度稳定且层数可控的纳米片.
而另一种机械剥离方法为纳米力学剥离法,可以有效避免以上弊端,该方法能剥离出具有精确层数且质量更好的二维纳米薄片.这种剥离方法通常在高分辨率透射电子显微镜(HRTEM)的检测下,使用非常锋利的钨探针对块状材料进行剥离[11].
1.1.2 液相剥离法
液相剥离法(LPE)是制备二维TMDCs纳米片的另一种广泛应用的方法.具体操作为:将大块的材料分散至合适的溶剂中,然后利用超声的方式,将大块材料剥离成纳米片.YI等[12]采用液相剥离法,将二硫化钨(WS2)粉末剥离成单层WS2.简单来说,将WS2粉末与N-甲基吡咯烷酮(NMP)混合后,溶液超声4 h,油浴搅拌,随后随机抽取了300张扫描电子显微镜(SEM)图对材料粒径进行分析统计,该纳米片的平均粒径为150 nm,与动态光散射(DLS)测得的粒径大小基本一致,说明该方法可以获得尺寸均一的纳米片.
1.1.3 化学剥离法
化学剥离法通过将简单原子、聚合物、有机金属化合物等客体物质插入TMDCs层中,来降低材料间的范德华力,从而将材料剥离出来.例如LIU等[13]在正己烷中加入正丁基锂(n-Bu-Li)和二硫化钼(MoS2),在氮气(N2)中搅拌混合液,使锂离子(Li+)完全穿插,之后通过离心收集产物,在超声中处理即可得到剥落的MoS2纳米片.通过原子力显微镜(AFM)测得纳米片平均厚度为1 nm,表明这些纳米片大部分是单层的.一般来说,用Li+剥离块状材料会使用有机锂化合物作为Li+前驱体.CHNG等[14]深入探究了各类有机锂化合物对TMDCs材料剥离的效果,选用了n-Bu-Li、叔丁基锂(t-Bu-Li)和甲基锂(Me-Li)作为插层剂来剥离MoS2.经过毒性评估显示:用n-Bu-Li和t-Bu-Li插层剂剥离的纳米片的细胞毒性要明显高于Me-Li剥离的纳米片,且Me-Li剥离的MoS2毒性特征与块状MoS2基本相似,如图2(a)所示.其他实验数据证实:n-Bu-Li和t-Bu-Li插层剂对MoS2的剥离效率要高于Me-Li,因此导致剥离后MoS2层数减少,且比表面积增加.将细胞毒性结果与层数表征数据结合,证实了MoS2纳米片剥落效率与材料细胞毒性之间有很强的关联性,可以通过选择不同的插层剂来改变材料的毒性与层数.
与上述使用Li+插入剥离方法相比,铵根(NH4+)或硫酸分子(H2SO4)插层剂剥离法对空气和水均不敏感,因此可以被放大生产纳米片.例如YONG等[15]将WS2粉末分散在浓硫酸中,在90℃搅拌下充分插层,通过离心收集产品,如图2(b)所示.接着将穿插H2SO4的WS2分散到去离子水,通过搅拌、超声,得到单层/少层的WS2纳米片.通过AFM分析,WS2纳米片的平均厚度约为1.6 nm,与Li+剥离得到的纳米片厚度很相近,如图2(c)和图2(d)所示.
1.1.4 化学气相沉积法
化学气相沉积法是一种典型的自下而上制备纳米片方法.通常将金属前驱体,如氯化钨(WCl6)、氯化钛(TiCl4)等与硫(S)、硒(Se)前驱体在混合溶剂中溶解,然后在高温下生长成TMDCs纳米片.该方法可以制备出横向尺寸可调、厚度可控的单层或多层纳米片.CHENG等[16]在WS2纳米片中掺杂了不同类型的金属,如铁离子(Fe3+)、钴离子(Co3+)、镍离子(Ni2+)、锰离子(Mn2+)、钆离子(Gd3+).将WCl6或其他金属前驱体与硫磺(S)溶解在油胺(OM)和1-十八烯(ODE)的混合溶剂中,在N2下高温反应.通过调节反应中添加的金属离子的物质的量,可以改变最终纳米片中金属离子掺杂率.最终产物TEM表明,掺杂了不同金属离子的WS2均显示出片状的形态,且元素图谱显示纳米片中W,S和掺杂的金属离子分布均匀.因此,这种自下而上的化学气相沉积法可以用于合成各类掺杂金属离子的纳米片.
1.2 TMDCs纳米材料的修饰
虽然通过化学剥离法合成的TMDCs纳米片具有一定的水稳定性,但电子筛选效应会使材料在盐溶液中聚集,尤其是在磷酸盐缓冲溶液中.因此,在将材料用于生物应用之前,改性是必要的.通常使用含有二硫醚基团的硫辛酸共轭聚乙二醇(LA-PEG)或巯基化透明质酸(HA-SH)对纳米片进行功能化改性.LA-PEG或HA-SH上的硫代分子可以固定在TMDCs纳米片表面的缺陷位点.LIU等[17]将HA-SH加入到MoS2纳米片水溶液中.在超声与搅拌作用下,得到透明质酸(HA)修饰的纳米片MOS2-SS-HA.通过傅里叶变换红外吸收光谱(FT-IR)等表征,证实HA-SH成功接枝到纳米片表面,如图3所示.
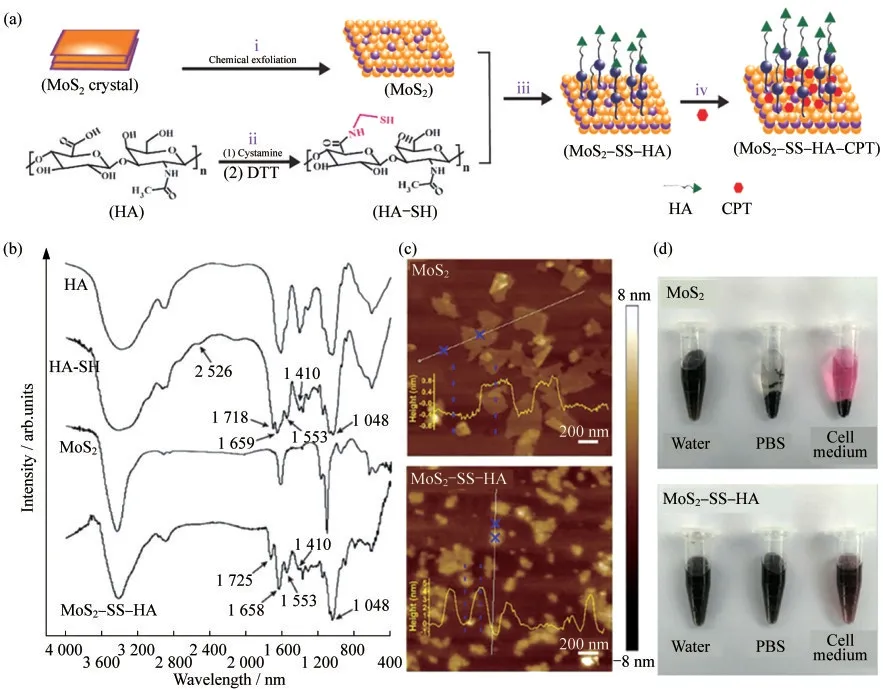
图3 MoS2-SS-HA纳米片的合成与表征.(a)MoS2-SS-HA合成示意图;(b)MoS2在HA修饰前后的FT-IR光谱图;(c)MoS2和MoS2-SS-HA的AFM图;(d)MoS2和MoS2-SS-HA悬浮液在水、磷酸盐缓冲溶液(PBS)、细胞介质中一周后的稳定性
2 TMDCs用于肿瘤治疗与成像
2.1 PTT
PTT作为一种新型的肿瘤治疗模式,与传统的化疗和放疗相比,PTT具有较低的毒副作用.同时,PTT使用的近红外光具有较强的组织穿透能力,可以刺激材料在动物体内对光信号做出较好反应.二维TMDCs作为石墨烯类似物,因其较大比表面积,成为了一类很好的近红外光纳米材料,例如WS2,TiS2和MoS2等已被证明具有良好光热性能.QIAN等[18]通过自下而上的溶液法合成了TiS2纳米片.经过聚乙二醇(PEG)修饰后的TiS2纳米片,表现出良好的生物相容性,且无毒副作用.对携带4T1肿瘤小鼠尾静脉注射TiS2-PEG,24 h后用808 nm近红外激光照射小鼠肿瘤5 min,发现该治疗组肿瘤处温度迅速上升至65℃,与只注射生理盐水的对照组有明显差别,如图4(a)~4(c)所示.同时,治疗后的小鼠存活超过60 d,且肿瘤完全消融,说明TiS2-PEG具有很好的肿瘤治疗效果.由于二维材料较大的比表面积,可以通过负载其他纳米颗粒来增加材料功能和提高材料在肿瘤方面的治疗效果.XIE等[19]合成的磁性MoS2,通过自组装制备壳聚糖/羧甲基纤维素功能化MoS2纳米复合材料(mMoS2-CS/CMC),接着在材料上负载阿霉素(DOX).当药物释放时,复合材料表现出明显pH依赖释放行为.此外,mMoS2-CS/CMC具有良好的光热效应,如图4(d)所示.XU等[20]原位合成了负载金(Au)纳米颗粒的MoS2纳米片.Au纳米颗粒的加入,使MoS2纳米片在808 nm近红外周围吸收明显增强,且负载了Au的MoS2纳米片表现出更高的光热转化效率.
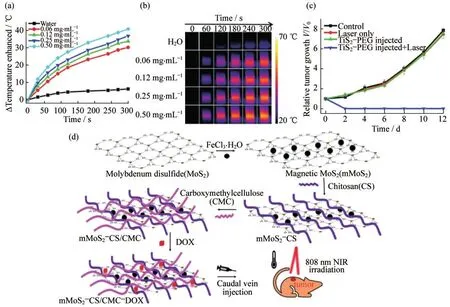
图4 TMDCs的肿瘤治疗应用.不同质量浓度TiS2-PEG溶液在808 nm激光照射下的(a)光热曲线和(b)红外热图像;(c)不同组别小鼠4T1肿瘤在不同材料处理后的生长情况;(d)mMoS2-CS/CMC的合成与DOX负载示意图
2.2 PDT
不同于PTT,PDT是一类依赖PS、氧气(O2)与特定波长激光来治疗肿瘤的疗法.PS在特定波长激发下,将肿瘤微环境中的O2转化为有毒的活性氧(ROS),从而杀死肿瘤细胞.相比PTT需要高功率密度激光照射,PDT重点在于肿瘤细胞对PS的有效吸收.但PDT对O2的浓度要求比较苛刻,在缺氧的肿瘤微环境条件下,PS对肿瘤的疗效有限.因此,将PTT与PDT相结合,可以更好地协同治疗肿瘤.
GENG等[21]合成了碳/二硫化钨(C/WS2)异质结来增强骨肉瘤的PTT效果.通过微波辅助水热法合成WS2纳米片,然后通过静电驱动组装的方式在带负电的纳米片两侧结合C,形成C/WS2异质结.该异质结材料可以在低功率密度下完全消融骨肉瘤.WANG等[22]设计了一种新型PDT/PTT/化疗联合疗法纳米片.通过阳离子交换得到了三明治结构的纳米材料BiSe3/MoSe2/NiSe3.该异质结构有1.17 eV的狭窄带隙和更强的近红外吸收能力.
2.3 成 像
随着诊疗在单一纳米粒子中的整合,PTT可以在各种成像指导下进行,如正电子发射断层扫描成像(PET)、X射线计算机断层扫描成像(CT)和光声成像(PAI)等.这些成像方式可用于治疗前病变组织的定位、治疗过程中的监测以及治疗后的疗效评估,从而大幅度提高治疗效率.其中,PAI与PTT都是利用光能进行成像与治疗,因此TMDCs作为优异的光热剂,也是PA造影剂.不仅如此,大部分TMDCs中的过渡金属为高原子数元素,可以作为CT造影剂使用.
MIAO等[23]组合成的二硫化铼(ReS2)纳米片具有很强的近红外吸收能力和高的光热转换效率(79.2%),可用于PAI与PTT.ReS2具有较强的X射线衰减,还可以用作CT造影剂.LIU等[24]制备的MoS2-Au(MA)表现出更强的近红外吸收能力和光稳定性.修饰后的MA-PEG显示出较强的X射线衰减和光热转换能力,可以用于CT和PAI造影剂,如图5所示.此外该纳米片还可通过放射治疗和PTT联合治疗肿瘤.FU等[25]合成得到了负载氧化铁纳米粒子的TiS2纳米片(TSIO).该复合材料在NIR-Ⅱ窗口具有很强的吸收能力,并具有较好的磁性.在施加磁场时,TSIO纳米平台在肿瘤处显示出较强的积累,同时可以通过PA和MR双重成像来实时监测PTT治疗过程,为改善肿瘤内部免疫抑制提供有效途径.

图5 (a)双模态PA和CT成像引导下用于PTT的ReS2纳米片的剥离过程;(b),(c)分别为ReS2纳米片水溶液体外PA和CT成像;(d),(e)分别为小鼠在注射MA-PEG前后的体内CT和PA成像;(f),(g)分别为基于d和e中成像数据的小鼠CT和PA强度量化
3 总结
文章主要总结了一部分TMDCs合成与修饰方法,讨论了4种常用合成方法的优缺点,以及TMDCs纳米片在肿瘤诊疗中的应用.作为一类类石墨烯的材料,TMDCs具有较高的近红外吸收能力.它可以将接收到的光能最终以超声波的形式释放出来,作为PAI造影剂.此外这类材料通常以二维纳米片的形式存在,纳米片提供了更多的活性位点,有助于负载各种不同功能的纳米颗粒、药物小分子或生物大分子,可以赋予材料更多的治疗方式.此外,TMDCs中的过渡金属通常为高原子数的金属,因此可以为肿瘤治疗提供以PTT为基础的协同治疗和双模式成像引导下的治疗,极大提高肿瘤治疗效率.因此,TMDCs材料将来有望应用在更广泛的生物学领域,激发出更多的生物应用潜能.
