一种新型微创腰椎融合工具治疗腰椎峡部裂的临床应用
2022-11-10付拴虎覃海飚钟远鸣覃浩然韦家鼎伍亮陈勇喜宋泉生卢大汉谷金许伟
付拴虎 覃海飚 钟远鸣 覃浩然 韦家鼎 伍亮 陈勇喜 宋泉生 卢大汉 谷金 许伟
1广西中医药大学第一附属医院脊柱外科(南宁 530000);2广西中医药大学(南宁 530023)
腰椎峡部裂是指相邻腰椎上下关节突区域之间的单侧或双侧骨质缺损或不连续,最常见的原因是遗传易感个体正在发育的未成熟骨骼受到重复性创伤引起,早期一般无临床症状[1]。随着腰椎的继续退变,约有10%的个体出现临床症状:反复发作的轴性腰痛、臀部及大腿后部疼痛,继而引起腰椎滑脱的发生,可出现下肢相应皮节区的疼痛、麻木症状[2]。治疗的目标是缓解疼痛症状及恢复稳定性,保守治疗的主要原则体现在限制活动以控制疼痛[3],然而对于系统保守治疗超过半年症状未缓解的患者,建议通过手术方式以达到骨性融合,重建脊柱稳定性[4]。现相关文献[4-7]报道针对青少年的手术方式,如椎弓根螺钉U 形棒内固定、内镜下峡部植骨联合经皮钉内固定、开放下峡部植骨联合椎弓根螺钉内固定等多种方式,均可取得临床效果。然而对于腰椎峡部裂合并腰椎退行性疾病,椎间植骨融合术式能更好地体现治疗效果的优势,因其具有融合率高、有效重建腰椎稳定性被广泛应用于临床[8-10]。在现有腰椎椎间融合技术的基础上,本团队通过不断创新研发出一套器械,可以通过对安全三角及椎间盘的直接撑开、直接椎间盘切除、直接终板植骨床处理、直接融合器植入,达到脊柱融合手术所提倡的解除脊髓和神经压迫,重建脊柱稳定性目的。本研究拟进一步探讨此套器械在临床上的安全性和可行性。
1 资料与方法
1.1 一般资料采用随机对照研究,将2021年1~8月在广西中医药大学第一附属医院脊柱外科住院诊断为腰椎峡部裂的20 例患者,根据随机数字表法分组。其中A 组10 例患者,男4 例,女6 例,年龄26~75 岁,平均(50.90 ± 5.90)岁,病变节段:1 例L3/4、9 例L4/5;B组10例患者,男5例,女5例,年龄38~72 岁,平均(51.90 ± 8.95)岁,病变节段:2 例L3/4、8 例L4/5。纳入的所有患者由第二作者实施手术操作,同时该项研究经过广西中医药大学第一附属伦理委员会审查审批同意,所有患者均获得知情同意。
两组患者术前在年龄、性别、体质指数(BMI)、手术节段等指标方面对比,均提示差异无统计学意义(P>0.05),见表1。
表1 患者基本资料对比Tab.1 Comparison of basic data between groups±s
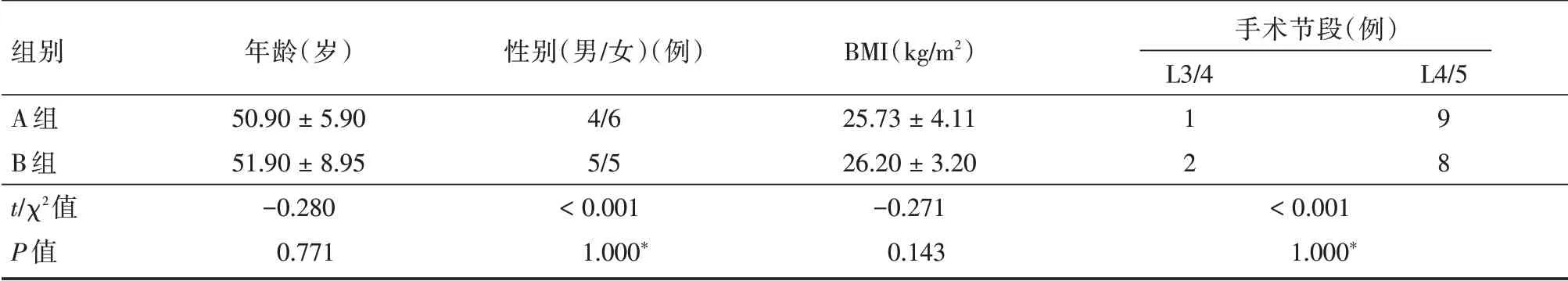
表1 患者基本资料对比Tab.1 Comparison of basic data between groups±s
注:*Fisher 确切概率法
组别A 组B 组t/χ2值P 值年龄(岁)50.90±5.90 51.90±8.95-0.280 0.771性别(男/女)(例)4/6 5/5<0.001 1.000*BMI(kg/m2)25.73±4.11 26.20±3.20-0.271 0.143手术节段(例)L3/4 L4/5 1 2 9 8<0.001 1.000*
1.2 纳入与排除标准纳入标准:(1)诊断为腰椎峡部裂或伴有轻度腰椎退变、Ⅰ度腰椎滑脱、腰椎不稳患者;(2)病变节段均为单节段(L3/4 或L4/5);(3)腰痛或腰痛伴一侧肢体症状;(4)系统保守治疗大于6 个月的无效患者。
排除标准:(1)有严重心肺脑病变的患者;(2)病变节段累计≥2;(3)病变节段为单节段的L1/2 或L2/3或L5/S1的患者;(4)有腰椎手术病史的患者。
1.3 手术方法A 组手术方法:(1)术前准备:患者采用全身麻醉,取屈髋屈膝俯卧位于手术床上。借助定位网在C 臂机透视下标记并画出病变节段上位椎体的下终板及下位椎体的上终板,两条线之间为椎间隙,于椎间隙中间画一条起于棘突、平行于终版、向患侧的延长线,长约5~9 cm(简称a 线);同时标出棘突连线、患侧椎体外侧连线及需要置钉的椎弓根体表定位点。常规消毒、铺巾。(2)导丝定位:在C 臂透视下用经皮穿刺针置入相应椎弓根,透视见位置满意后留置导丝并退出穿刺针。在a 线上于棘突连线旁开5~9 cm选取进针点,与病变间隙下位椎体的上关节突下缘的连线构成穿刺线,对穿刺线要满足两个条件:一是要保证其在椎间隙内的前提下越过棘突间连线,二是不能进入椎管以内,进针点的选取有个体差异(可根据患者术前腰椎CT 及术中C 臂来定,第二个条件术中C 臂可以判断)。当穿刺针置入位置理想后留置导丝,退出穿刺针。(3)置入撑开器及工作套管:在导丝处做一横行或纵行的2 cm切口,将自主研发的撑开器(直径分别6、8、10、12、14 mm)沿导丝方向进入椎间盘内逐级撑开椎间隙,依据术前测量的椎间隙高度撑开至合适高度。置入相应的工作套管。其深度以超过椎体后缘20%为宜。(4)椎间盘处理:通过工作套管,直接用自主研发的绞刀、特殊刮匙对椎间盘进行切除,直至暴露骨性终板结构,此步骤可在内镜辅助下验证是否处理彻底。(5)椎间隙植骨及椎间融合器置入:将同种异体骨通过工作套管置入椎间隙前缘并夯实,将可调节高度的钛合金融合器,通过融合器置入器置入椎间隙内,透视见融合器位于离椎体后缘约1/4 处为宜,透视下逐步调节椎间隙高度(可调节高度范围为9~14 mm),直至椎间隙高度恢复与上下相邻椎间隙高度相近为止。(6)经皮椎弓根螺钉置入:通过术前标记出的患侧上下椎体的椎弓根体表标识,置入穿刺针,透视见穿刺位置合适后置入导丝并退出穿刺针,在患侧及健侧的四处导丝处各做一长约2 cm 纵行切口,通过经皮钉工作套管逐级扩开周围软组织直至椎弓根处,沿导丝进行丝攻并退出,并沿导丝方向置入经皮椎弓根螺钉,将连接棒经切口位置在肌肉内置于上下椎体内的椎弓根螺钉钉尾内,透视下见椎弓根螺钉及连接棒位置满意后,加压拧紧螺帽并折断钉尾片。再次透视后见融合器、椎弓根螺钉、连接棒位置合适后缝合伤口。
B 组手术方法:行后路腰椎间融合术(PLIF),按目前公认的方法进行[11]。

图1 手术操作流程图Fig.1 Flow chart of surgical operation

图2 部分配套工具Fig.2 Partial supporting tools
1.4 术后处理两组患者术后均行抗生素预防感染及对症支持治疗。A 组术口无需留置引流管,术后第一天鼓励患者戴腰围保护下地活动;B 组术口留置引流管3~5 d,如引流量24 h小于50 mL时,可予拔除,拔除引流管后鼓励患者戴腰围下地活动。
1.5 观察指标记录两组患者的年龄、性别、体质量指数、手术节段、手术时间、术中出血量、下床时间、伤口长度、术中X 线透视次数、术后并发症、VAS 评分、JOA 评分、ODI 评分等情况,并对以上指标进行统计学分析。视觉模拟评分法(visual analogue scal,VAS):分数为0~10 分,分数越高代表疼痛程度越明显;日本骨科协会评估治疗分数(Japanese Orthopaedic Association,JOA):分数为0~29 分,分数越低代表功能障碍越明显;Oswestry功能障碍指数问卷表(Oswestry disability index,ODI):分数为0~100%,分数越高代表功能障碍越明显。
1.6 统计学方法通过SPSS 20.0 进行相关数据分析处理,计数资料采用频数表示,采用χ2检验或Fisher 确切概率法分析;计量资料采用均数±标准差表示,采用t检验或方差检验,组间比较采用单因素方差分析,P<0.05为差异有统计学意义。
2 结果
2.1 两组术中指标比较A 组与B 组在手术时间、术中出血量、伤口长度方面对比,差异有统计学意义(P<0.001)。两组在术中X 线透视次数相比,差异有统计学意义(P<0.001)。见表2。
表2 A 组和B 组患者术中相关指标对比Tab.2 Comparison of intraoperative related indexes between A group and B group±s
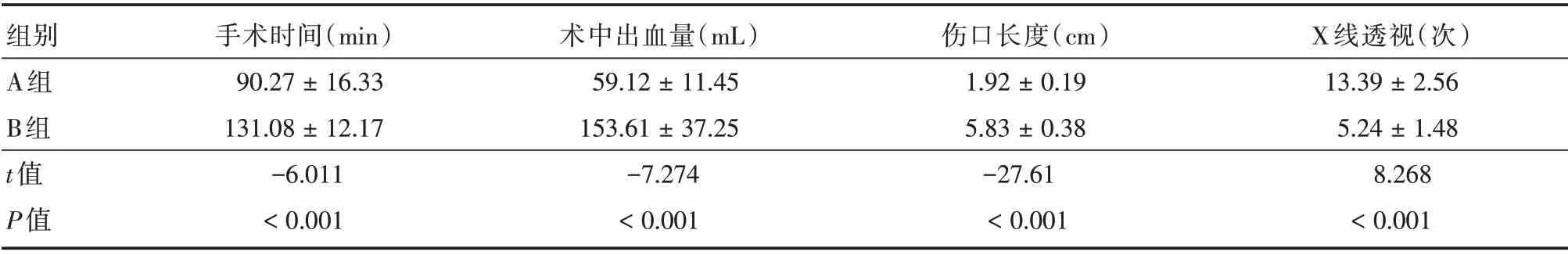
表2 A 组和B 组患者术中相关指标对比Tab.2 Comparison of intraoperative related indexes between A group and B group±s
组别A组B组t值P值手术时间(min)90.27 ± 16.33 131.08 ± 12.17-6.011<0.001术中出血量(mL)59.12 ± 11.45 153.61 ± 37.25-7.274<0.001伤口长度(cm)1.92 ± 0.19 5.83 ± 0.38-27.61<0.001 X 线透视(次)13.39 ± 2.56 5.24 ± 1.48 8.268<0.001
2.2 两组术前及术后疗效指标比较两组患者术前腰腿痛VAS 评分、腰椎JOA 评分、ODI 评分方面对比,均提示差异无统计学意义(P>0.05);A 组和B 组在术后第1 天、第7 天伤口疼痛VAS 评分,术后第1 天、第14 天、术后1 个月腰椎JOA 评分、ODI 评分等方面对比,均提示差异有统计学意义(P<0.05);A 组和B 组在术后第14 天伤口疼痛VAS 评分对比,提示差异无统计学意义(P>0.05)。见表3。
表3 A 组和B 组患者术后相关指标对比Tab.3 Comparison of postoperative related indicators between A group and B group±s,分
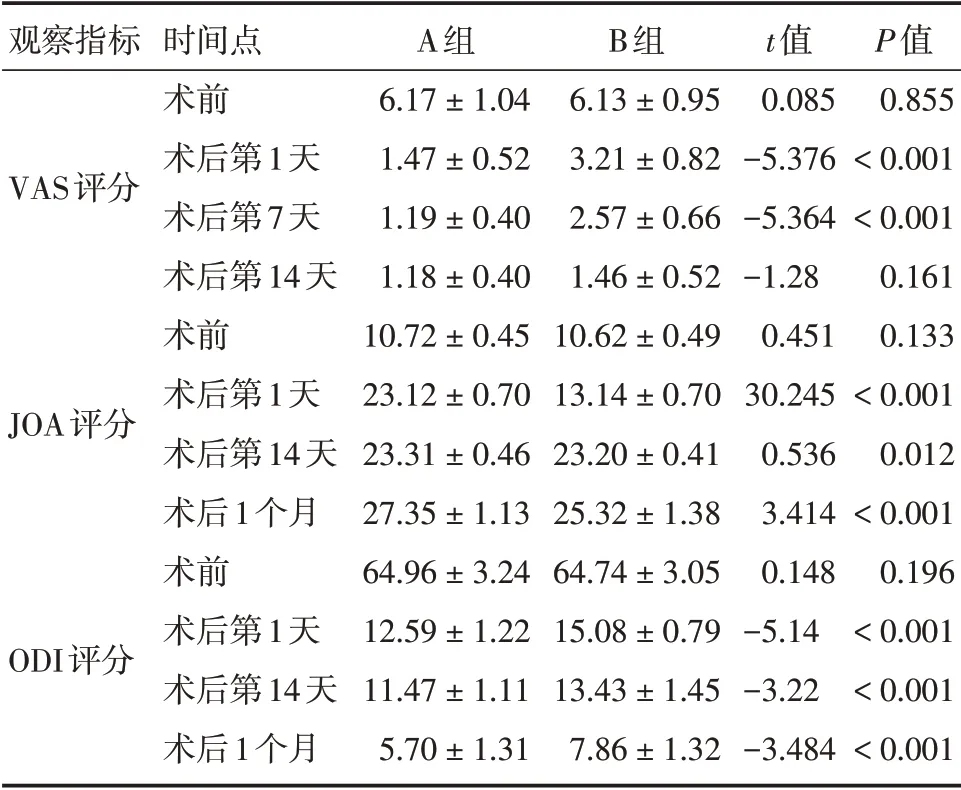
表3 A 组和B 组患者术后相关指标对比Tab.3 Comparison of postoperative related indicators between A group and B group±s,分
观察指标VAS评分JOA评分ODI评分时间点术前术后第1天术后第7天术后第14天术前术后第1天术后第14天术后1个月术前术后第1天术后第14天术后1个月A组6.17±1.04 1.47±0.52 1.19±0.40 1.18±0.40 10.72±0.45 23.12±0.70 23.31±0.46 27.35±1.13 64.96±3.24 12.59±1.22 11.47±1.11 5.70±1.31 B组6.13±0.95 3.21±0.82 2.57±0.66 1.46±0.52 10.62±0.49 13.14±0.70 23.20±0.41 25.32±1.38 64.74±3.05 15.08±0.79 13.43±1.45 7.86±1.32 t值0.085-5.376-5.364-1.28 0.451 30.245 0.536 3.414 0.148-5.14-3.22-3.484 P值0.855<0.001<0.001 0.161 0.133<0.001 0.012<0.001 0.196<0.001<0.001<0.001
2.3 术后并发症围手术期观察过程中,A 组术后第7 天有1 例患者出现伤口脂肪液化,予多次换药及拆线撑开伤口彻底引流后正常愈合;B 组发现1 例患者术后第4 天引流液量大并呈清亮色,考虑脑脊液漏可能,嘱患者绝对卧床并呈头低脚高位,动态观察引流量情况,逐日夹闭引流管,14 d 拔除。
2.4 典型病例患者欧某某,女,34 岁,因反复腰痛1年入院。见图3。
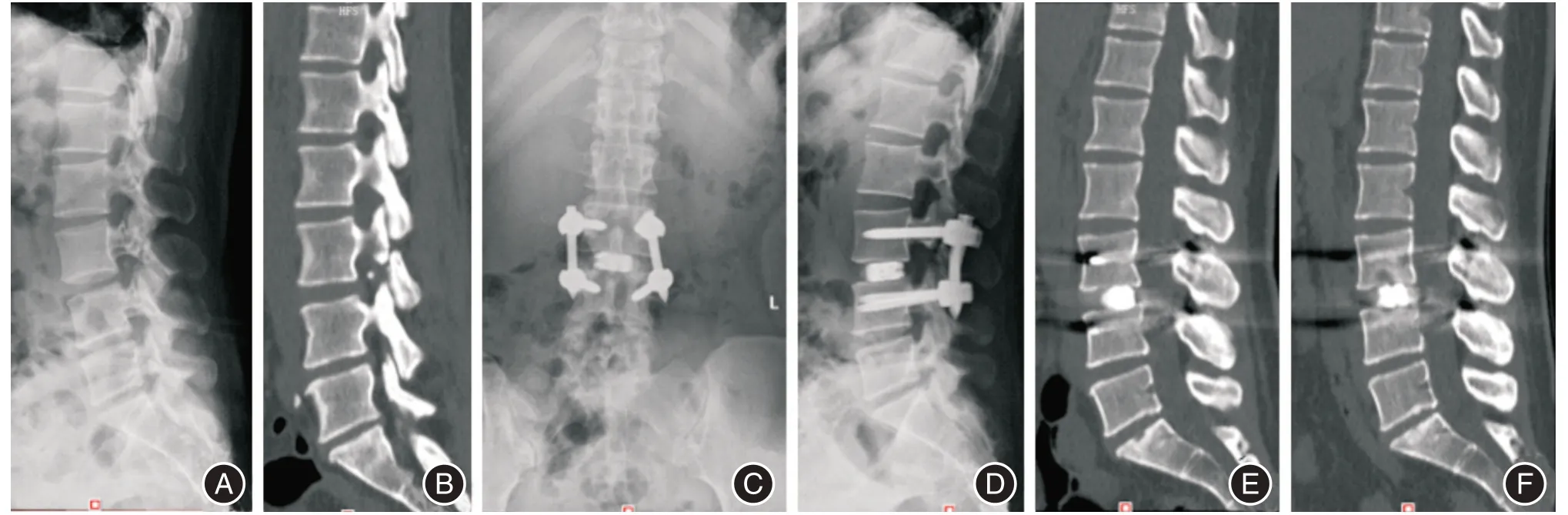
图3 L3 峡部裂影像示例Fig.3 The image example of lumbar 3 spondylolysis
3 讨论
目前临床上报道的腰椎间融合术有PLIF、经椎间孔腰椎椎间融合术(transforaminal interbody fusion,TLIF)、直接外侧椎间融合术(direct lateral lumbar interbody fusion,DLIF)、极外侧椎间融合术(extreme lateral lumbar interbody Fusion,XLIF)、前路腰椎间融合术(anterior lumbar interbody fusion,ALIF)、斜外侧腰椎间融合术(oblique lumbar interbody fusion,OLIF)等[12-13],随着内镜技术的不断发展,衍生出较多微创术式,同样临床效果满意,比如经皮内镜后路腰椎间融合术[14](percutaneous endoscopic posterior lumbar interbody fusion,Endo-PLIF)、镜下经椎间孔入路腰椎椎间融合术[15](percutaneous endoscopic transforaminal lumbar interbody fusion,Endo-TLIF)、单侧双通道内镜下经椎间孔腰椎间融合术[16](unilateral biportal endoscopic transforaminal lumbar interbody fusion,UBE-TLIF)等。
传统的腰椎椎间融合技术,已被临床上广泛证实效果的可靠性及安全性,然而多种手术方式存在对解剖结构破环多致脊柱稳定性丢失,同时存在创伤性大,恢复周期长,临床上多数患者对手术产生恐惧心理,导致依从性不佳。因此随着内窥镜技术的迅速发展,微创技术不断涌现,因其具有对身体入侵性小、安全性高、临床效果显著,患者接受程度较高。尽管目前临床上通过创新不断涌现的镜下辅助微创术式存在相当大的差异,但相似的原理和技术对所有类型都是通用的,同时治疗目标也是一致的,体现在:手术伤口的最小化、围手术期的疼痛轻微化、术中操作简便化、恢复社会的迅速化及临床效果的最大化[17]。针对现有微创技术理念的基础上,本团队拟在探索出一种适用于临床的腰椎椎间融合技术。
本研究的核心理念体现在:通过自主研发的特殊撑开器及相应的配套工具,在有效保护同位神经的前提下,对Kambin 安全三角及椎间隙进行直接撑开、直接去除椎间盘、直接植骨处理及直接置入椎间融合器的一系列技术。通过恢复椎间隙高度,从而达到增加椎间孔面积,改善冠状平衡,以及置入融合器达到减压神经的目的,起到改善症状的作用[18]。实际操作过程中需要注意以下几点:(1)术前需要计算出穿刺针的进针方向和角度,术中透视时穿刺针针尖在侧位片上到达椎体后缘,在正位片上不超过上下椎体椎弓根内侧缘连线,同时需要平行上下终板;(2)如果患者病变节段椎间隙较窄,需要更换自主研发的半球形椎间隙撑开器,应用匹配的舌状工作套管通过环锯对下位椎体的上关节突进行部分去除,直到能放入椎间隙工作套管;(3)如需要进行椎管减压,植入融合器后可将椎间隙工作套管退至椎间隙后缘,借助内镜行关节突、椎弓根上壁部分切除,切除黄韧带暴露神经行走根(采用的方法同椎间孔镜YESS 技术[19])。
本项研究表明,与传统入路下的B 组相比,术中出血量较少、伤口较小,对局部正常解剖结构破坏小,同时患者术后下地时间较早、住院时间短、恢复快等。在早期临床疗效评价方面,术后1 个月时A 组和B 组在腰椎JOA 评分、ODI 评分方面对比,差异有统计学意义(P<0.05),提示A 组技术在功能恢复上具有一定优势。本手术采用的是经椎间孔入路,由于解剖结构Kambin 安全三角的特殊性,如何局部置管固定和通过此处安全置入融合器,是经椎间孔入路所有术者需要思考的问题。LÜ 等[20]的研究表明,通过Endo-TLIF 治疗Ⅰ度腰椎滑脱,可以最大限度保留正常的肌肉韧带,改善术后镇痛率,功能恢复更快等优势,同时长期随访后发现可以取得满意骨性融合效果。MORGENSTERN 等[21]的一项研究报道中指出,Endo-TLIF 操作过程中感觉迟钝率高于常规的内镜系统,考虑为可能由于Endo-TLIF 的工作套管直径更大,出现置管时局部把持力不够及放入融合器时的震动有关。同时由于传统的PEEK 融合器偏大,受工作套管的影响,一般选择偏小的融合器置入,可能出现融合器移位及椎间不融合现象[22]。本团队在解决上述问题时,首先用可撑开器直接对椎间隙逐级撑开,之后放入匹配的工作套管,在套管固定牢固后置入可撑开融合器,可撑开融合器具有灵活调节、抗压易植入、耐磨防移位等优势,适合于内镜下操作[23]。因此基于如何更好的扩大Kambin 安全三角、增加器械操作时的稳定性、更安全的置入融合器,是本团队设计该套器械的出发点,与多数学者[24]的理念相似。
本研究存在一定局限性,纳入研究的患者多以腰椎峡部裂为主或伴有轻度腰椎退变、Ⅰ度腰椎滑脱、腰椎不稳等,病变节段为L3/4 或L4/5,由于此两处椎间隙及Kambin 安全三角较大,利于初试者操作,安全性更高。针对L5/S1 节段,此套器械存在不足,有待进一步研发。目前此套器械的适应症范围较小,后期是否可以广泛适用于治疗腰椎退行性疾病,还待于进一步研究证实。
综上所述,本团队研发的新型腰椎椎间融合工具,在对应的适应症范围内进行治疗,早期可以达到满意临床疗效。由于本研究所纳入的病例较少,病种单一症状程度轻,恢复期是否发生严重并发症,还需要进一步大样本、多中心随机对照研究、长期随访进一步明确。
