犬ELF4基因原核表达及其卵黄抗体的制备
2022-11-09喻娇曹馨唐青海侯鑫军高翠翠韩涛涛黎露刘会敬唐斯萍
喻娇,曹馨,唐青海,侯鑫军,高翠翠,韩涛涛,黎露,刘会敬,唐斯萍
(衡阳师范学院生命科学与环境学院/南岳山区生物资源保护与利用湖南省重点实验室/动物微生物新型检测技术及生物制剂衡阳市重点实验室,湖南衡阳 421008)
0 引言
【研究意义】ELF4(E74-like factor 4)是ETS(E26 transformation specific)家族中的重要成员之一,最早是从人类巨核细胞系中克隆获得,与人类ELF-1基因在结构上存在一些相似之处,因此早期被命名为骨髓elf-1(E74-like factor 1)样因子(Myeloid elf-1-like factor,MEF)(You et al.,2013;Szabo and Rajnavolgyi,2014),被认为是X染色体上一个潜在的肿瘤抑制子(Seki et al.,2002)。ELF4参与细胞多种生理或病理的过程,如肿瘤发生、DNA损伤修复反应、调控细胞周期和成骨分化(Baek and Baek,2013;Kosti et al.,2020;Sze et al.,2021;Du et al.,2021)。因此,克隆犬ELF4基因(cELF4)并制备抗cELF4蛋白的卵黄抗体,可为该蛋白生物学功能研究提供基础材料。【前人研究进展】近年来,研究发现,ELF4在免疫应答方面发挥着重要功能,其能与血小板因子4(Platlet factor 4,PF4)和猪源干扰素刺激基因(Porcine interferon-stimulating gene)的启动子相结合启动转录,ELF4能在上皮细胞中上调溶菌酶基因启动子的活性和人类β防御素2基因的转录水平,且能在造血细胞中激活白细胞介素-8(IL-8)(Kai et al.,1999;Lu et al.,2004;Suico et al.,2017)。2013年You等首次发现ELF4是一种Ⅰ型IFNs转录因子,并通过直接调节Ⅰ型IFNs反应来抑制病毒的复制。ELF4参与Ⅰ型干扰素(IFNs)的产生,IFNs是宿主建立抗病毒状态阻止病毒在宿主细胞内复制的关键转录因子。此外,ELF4在机体抗病毒的细胞免疫反应中也起着重要作用,可调控CD8+T细胞的发育、增殖和归巢等(Yamada et al.,2009)。ELF4基因缺失导致NK细胞或细胞毒性T细胞(CTL)发育及其穿孔素基因的表达障碍(Lacorazza et al.,2002)。ELF4是近年来新发现的一个在肿瘤发生、发展及肿瘤免疫中至关重要的癌基因(Sashida et al.,2009),且作为抑癌或者促癌的研究均有报道。研究发现,ELF4基因在神经胶质母细胞瘤中异常高表达,可通过直接激活机体细胞内Sox2基因的表达从而赋予其干细胞特性,促使神经胶质母细胞瘤的形成(Bazzoli et al.,2012)。也有研究发现,ELF4可能通过调节Wnt/β-catenin通路,进而实现对胃癌细胞增殖和侵袭的正向调节作用(刘伟等,2021)。此外,ELF4基因高表达可促进人胰岛素瘤细胞增殖,同时增强人胰岛素瘤细胞抗凋亡能力,其作用机理是通过激活Akt通路而促进胰岛素瘤细胞增殖和抗凋亡(卫国红等,2021)。然而,在急性髓性白血病中ELF4则是作为抑癌基因起作用(Okabayashi et al.,2013)。【本研究切入点】ELF4基因的功能具有多样性,在抗感染和肿瘤的发生发展中发挥重要作用,但目前国内外尚无有关犬ELF4基因克隆、表达及其功能的研究报道。【拟解决的关键问题】克隆犬转录因子ELF4基因(cELF4),并通过原核表达制备免疫原,免疫蛋鸡制备抗犬ELF4特异性卵黄抗体(IgY)并鉴定其免疫活性,为进一步研究犬ELF4蛋白功能提供基础材料。
1 材料与方法
1.1 试验材料
1.1.1 细胞、质粒、菌株及试验动物感受态细胞DH5α、BL21(DE3)、Transtta(DE3)和Top 10购自天根生化科技(北京)有限公司;原核表达载体pET-28a、pEGFP-C1购自Novagen公司;120日龄左右的产蛋鸡购自衡阳某养鸡场。
1.1.2 主要试剂RNAiso试剂、PrimeScript II First Strand cDNA Synthesis Kit、GXL polymerase高保真酶、内切酶及XfectTM转染试剂均购自宝生物工程(北京)有限公司;His-Tag Mouse mAb、EGFP-Tag Mouse mAb、HRP-Goat-Anti-Mouse IgG购自武汉三鹰生物技术有限公司;HRP-Goat-Anti-Chicken IgG购自Invitrogen公司;疫苗佐剂ISA 15AVG、ISA 71VG和ISA 201VG佐剂购自SEPPIC公司;增强型HRPDAB显色试剂盒购自天根生化科技(北京)有限公司;Bradford蛋白浓度测定试剂盒购自上海碧云天生物技术有限公司,Hoechst 33342购自Abbkine Scientific公司。
1.2 试验方法
1.2.1cELF4基因克隆及序列分析采用RNAiso试剂提取中华田园犬血液中总RNA,取20.0μL总RNA样 品,采 用PrimeScript II First Strand cDNA Synthesis Kit合成cDNA第一链。根据人ELF4基因序列(GenBank No.NM_001421)设计cELF4基因克隆引物cELF4-F1/cELF4 R1992(表1),并以2.0μL cDNA为模版进行PCR扩增。PCR产物经纯化后连接至pMD19-T,然后转化DH5α感受态细胞进行抗性筛选,重组质粒进行酶切鉴定和序列测定。利用DNAStar 7.0 MegAlign和MEGA 5.0对犬ELF4、人ELF4(Homo sapiens,NM_001421)、猪ELF4(Sus scrofa,KU097322)、牛ELF4(Bos taurus,NM_0011 92029)、小鼠ELF4(Mus musculus,NM_019680)及褐家鼠ELF4(Rattus norvegicus,NM_001191735)的核苷酸序列和氨基酸序列进行对比分析。
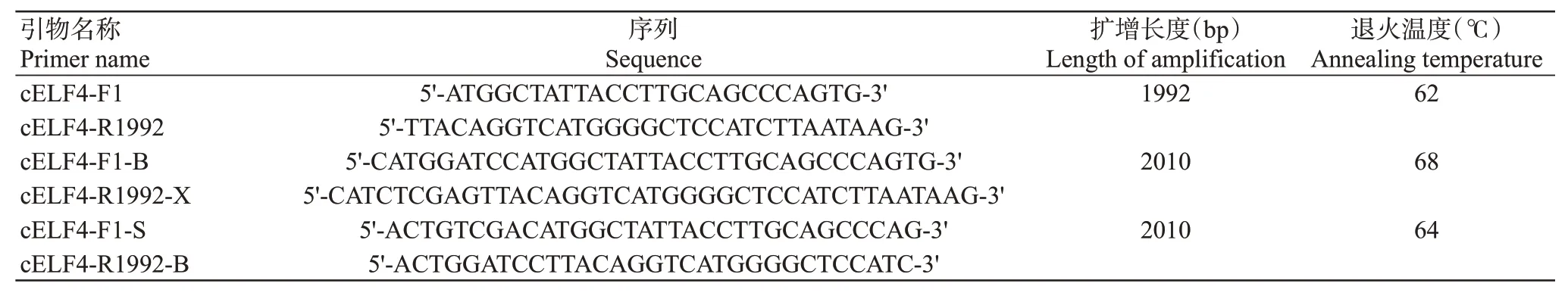
表1 引物序列及其反应条件Table 1 Primer sequences and their reaction conditions
1.2.2 重组原核表达载体构建与鉴定以pMD19TcELF4载体为模板,参照GXL polymerase高保真酶说明书,利用表达引物cELF4-F1-B/cELF4 R1992-X扩增cELF4基因。PCR产物经BamH I和XhoI双酶切后与pET-28a载体连接后,分别转化大肠杆菌BL21(DE3)和Rosetta(DE3)感受态细胞,采用双酶切和测序鉴定阳性克隆。
1.2.3 重组cELF4蛋白(rcELF4)的诱导表达及鉴定将双酶切和测序结果正确的阳性菌株接种新鲜LB培养基,活化后扩大培养4 h,加入终浓度为1 mmol/L IPTG(王瑾等,2017),置于37℃、220 r/min的摇床诱导目的蛋白表达,设不加诱导剂重组菌株对照和含空载体菌株诱导对照。10000 r/min离心2 min收集菌体,超声破碎,10000 r/min离心10 min、收集上清和沉淀。蛋白样品经SDS-PAGE电泳后,转印到PVDF膜上,用2%脱脂奶粉-PBS于37℃封闭1 h,PBST漂洗3次后与His-Tag Mouse mAb单克隆抗体(1∶3000稀释)孵育1 h,PBST洗3次,与Gaot-Anti-Mouse IgG(1∶6000稀释)孵育1 h,PBST洗涤后,用DAB显色试剂盒显色。
1.2.4 rcELF4蛋白特异性卵黄抗体(IgY)的制备将重组蛋白表达菌株Rosetta(DE3)-pET28a-cELF4加入到新鲜LB培养基中,于37℃、160 r/min的摇床过夜,再进行二次活化,10000 r/min离心2 min收集浓缩菌体,10000 r/min离心10 min三次超声破碎,取第1次超声上清、第2次超声上清、第3次超声溶解蛋白样品进行SDS-PAGE和Western blotting分析,将表达得到的蛋白分别与佐剂ISA 15VG、ISA 71VG、ISA 201VG按照3∶17、3∶7、1∶1的比例进行乳化,具体乳化参数参照说明书进行,制备好的免疫原于4℃保存备用。取20周龄左右的产蛋鸡,分为ISA 15VG组、ISA 71VG组、ISA 201VG组和空白组,每组6只,分两次免疫,间隔21 d,免疫剂量为1 mL/羽。首次免疫后第21、38和51 d进行翼下静脉采血,将采集到的血液于37℃静置2 h,4℃过夜,5000 r/min离心分离血清,同时设不免疫鸡作为阴性对照。收集首次免疫后第7、14、21、28、35、42和49 d的鸡蛋,用聚乙二醇法提取卵黄抗体。
1.2.5 rcELF4蛋白特异性IgY抗体Western blotting效价检测以rcELF4蛋白为抗原,采用Western blotting检测血清及卵黄抗体滴度。血清稀释方法:将血清按初始浓度1∶200稀释,然后在此基础上进行2倍比稀释到1∶64000,反应结果为阳性的最大稀释度即为血清抗体滴度。卵黄抗体稀释方法:将卵黄抗体按初始浓度1∶200稀释,然后在此基础上进行2倍比稀释直到1∶256000,反应结果为阳性的最大稀释度即为卵黄抗体滴度。
1.2.6 卵黄中总IgY含量测定使用Bradford蛋白浓度测定试剂盒测定提取的rcELF4蛋白IgY浓度。通过梯度稀释配制0、0.125、0.250、0.500、0.750、1.000和1.500 mg/mL蛋白标准,取5μL不同浓度蛋白标准加入96孔板的蛋白标准孔内,取5μL IgY样品到96孔板的样品孔中,各孔加入250μL G250染色液,用酶标仪测定吸光度值(A595nm),以标准蛋白质浓度为横坐标、A595nm为纵坐标,绘制蛋白质标准曲线并计算样品中的蛋白浓度。
1.2.7 重组真核表达载体构建及转染以pMD19TcELF4载体为模板,参照GXL polymerase高保真酶说明书,利用表达引物cELF4-F1-S和cELF4-R1992-B扩增cELF4基因。PCR产物经S和BamH I双酶切后与pEGFP-C1连接,分别转化大肠杆菌Top 10感受态细胞,采用双酶切和测序鉴定阳性克隆。将生长状态良好的Hela细胞接种于96孔细胞培养板内,置于37℃、5% CO2培养箱培养24 h;形成单层细胞后,采用Xfect™转染试剂将pEGFP-cELF4转染细胞,同时设置空载体pEGFP-C1和不转染空白细胞对照。转染40 h后弃培养基,0.85%的生理盐水洗涤1次,加入Hoechst 33342染液,室温孵育3~5 min,弃染液,用0.85%的生理盐水洗涤3次,荧光倒置显微镜下观察荧光。
1.2.8 cELF4特异性IgY与重组真核表达蛋白EGFPcELF4反应性检测将pEGFP-cELF4转染Hela细胞,方法同1.2.7。转染48 h后弃培养基,PBS洗涤2次,加入4%多聚甲醛室温固定30 min,加2%的BSA-PBS后37℃封闭1 h,分成两组,其中一组使用本研究制备的cELF4特异性IgY作为一抗,另一组采用EGFP鼠单克隆抗体作为一抗,37℃孵育1 h,两组的二抗分别为HRP标记的羊抗鸡抗体和HRP标记的羊抗鼠抗体,37℃孵育1 h,加入AEC底物,室温显色15 min,加入蒸馏水终止反应,显微镜下观察结果。
2 结果与分析
2.1 cELF4基因的克隆
经RT-PCR扩增得到1条分子量大小约2000 bp的条带,与预期结果相符(图1泳道1)。提取重组菌的质粒进行EcoR I和HindⅢ双酶切鉴定,结果(图1)显示,酶切产物分别得到片段约2000 bp的目的条带和2500 bp的载体片段,表明目的基因已成功克隆到pMD-19T载体中。
2.2 cELF4基因的序列分析结果
序列分析结果显示,cELF4基因的开放阅读框(ORF)全长为1992 bp,编码663个氨基酸残基,蛋白分子量大小约70.7 kD。通过与GenBank染色体序列数据库基因组序列(GenBank No.NC_006621.4)进行比对分析,结果显示,cELF4基因位于猪X号染色体,由8个外显子组成,覆盖位置103071073~103080846 bp,5′端非编码区至3′端非编码区合计9774 bp(图2)。将cELF4基因序列递交到GenBank数据库,获得登录号为MZ198105。
目前,GenBank中已有人、牛、野猪、小鼠和褐家鼠5种动物的ELF4基因被测序,其他动物的ELF4基因mRNA序列均为预测序列。将犬ELF4基因编码的氨基酸序列与被测序的5种动物ELF4蛋白氨基酸序列进行对比分析,结果显示,该序列与人、野猪、牛、小鼠和褐家鼠的ELF4氨基酸序列在第198~304位氨基酸之间均高度保守,其他区段均存在不同程度的差异(图3)。此外,同源比对结果显示,将cELF4基因与狐、人、牛、野猪、小鼠和褐家鼠ELF4基因的核苷酸相似性分别为99.3%、89.4%、88.5%、89.8%、81.5%和82.0%,其编码蛋白与狐、人、牛、野猪、小鼠和褐家鼠ELF4蛋白的氨基酸相似性依次为99.7%、89.6%、89.0%、91.8%、78.8%和78.4%。利用MEGA 5.0中的最大相似法对53个物种的ELF4基因进行系统进化分析,结果显示,cELF4基因与狐、大熊猫、欧洲雪貂、北美水獭等动物ELF4基因的亲缘关系较近,而与人和猴等灵长类动物及啮齿类鼠ELF4基因的亲缘关系相对较远(图4)。
2.3 重组表达菌株鉴定结果
pET28a-cELF4分别转化大肠杆菌BL21(DE3)和Rosetta(DE3)感受态细胞后,经扩大培养后分别提取阳性克隆的质粒,用XhoI和BamH I双酶切后,酶切产物用1.2%琼脂糖凝胶电泳检测,结果发现,从重组表达菌株BL21(DE3)-pET28a-cELF4和Rosetta(DE3)-pET28a-cELF4中提取的质粒酶切产物中均含有约1992 bp的目的条带和5369 bp的载体片段,表明重组表达菌株BL21(DE3)-pET28a-cELF4和Rosetta(DE3)-pET28a-cELF4构建成功。
2.4 重组蛋白rcELF4诱导表达及鉴定结果
重组表达菌株BL21(DE3)-pET28a-cELF4用1 mmol/L的IPTG诱导后未观察到目的条带(图6-A);Rosetta(DE3)-pET28a-cELF4用1 mmol/L的IPTG诱导后沉淀在100 kD附近出现目的条带,且上清和包涵体中均有目的蛋白表达(图6-B)。
2.5 重组蛋白rcELF4纯化及检测结果
将得到的rcELF4蛋白采用超声法进行3次纯化,对第1次超声、第2次超声上清和第3次超声溶解蛋白进行SDS-PAGE检测,结果发现在100 kD附近出现清晰条带,纯化效果较好。对重组菌株大量表达的目的蛋白进行Western blotting检测,结果发现第3次超声溶解蛋白在100 kD处出现目的条带(图7)。
2.6 rcELF4卵黄抗体制备及检测结果
收集免疫后第7、14、21、28、35、42和49 d的鸡蛋,用聚乙二醇法提取卵黄抗体,并进行SDS-PAGA凝胶电泳检测,结果发现重链(70 kD)和轻链(25 kD)条带明显,提取的卵黄抗体分子完整性好、纯度较高(图8)。
2.7 rcELF4蛋白血清抗体免疫活性鉴定
对首免后第0、21、38和51 d的鸡进行翅静脉采血,将分离到的血清进行Western blotting滴度测定,结果如图9所示。rcELF4蛋白可刺激鸡产生相应抗体,ISA 15AVG组血清抗体滴度在首免后第21、38和51 d分别为1600、64000和8000倍;ISA 71VG组血清抗体滴度在首免后第21、38和51 d分别为12800、64000和8000倍;ISA 201VG组血清抗体滴度在首免后第21、38和51 d分别为25600、128000和64000倍。
2.8 rcELF4蛋白卵黄抗体滴度检测
提取首免后第7、14、21、28、35、42和49 d的鸡蛋卵黄中的抗体进行Western blotting滴度测定。由图10可知,rcELF4蛋白可刺激鸡产生相应抗体,ISA 15AVG组卵黄抗体滴度在首免后第14、21、28、35、42和49 d分别为1600、1600、1600、16000、8000和8000倍;ISA 71VG组卵黄抗体滴度在首免后第14、21、28、35、42和49 d分别为25600、6400、3200、32000、32000和16000倍;ISA 201VG鸡卵黄抗体滴度在首免后第14、21、28、35、42和49 d分别为51200、6400、25600、256000、256000和16000倍。
2.9 卵黄中总IgY含量测定结果
采用Bradford法,以标准蛋白质浓度为横坐标,以吸光度值A为纵坐标制得标准曲线(图11)。将提取成功的首免后第7、14、21、28、35、42和49 d的卵黄抗体进行IgY含量测定,结果如图12所示。ISA 15AVG组鸡所产鸡蛋卵黄中抗体含量在首免后第7、14、21、28、35、42和49 d分别为3.99、3.88、3.84、3.88、3.50、3.80和3.57 mg/10 mL卵黄液;ISA 71VG组鸡所产鸡蛋卵黄中抗体含量在首免后第7、14、21、28、35、42和49 d分别为4.02、3.92、3.92、3.75、3.87、1.70、3.14 mg/10 mL卵黄液;ISA 201VG组鸡所产鸡蛋卵黄中抗体含量在首免后第7、14、21、28、35、42和49 d分别为3.93、4.09、3.43、3.54、3.08、2.45、3.73 mg/10 mL卵黄液。
2.10 cELF4基因真核表达载体的构建结果
以pMD19T-cELF4载体为模板、cELF4-F1-S和cELF4-R1992-B为引物,PCR扩增获得一条分子量大小约1992 bp的条带,与预期结果相符。将目的片段连接至pEGFP-C1,并转化大肠杆菌Top 10感受态细胞。提取阳性克隆菌Top-pEGFP-cELF4的重组质粒用SalI和BamHⅠ进行双酶切鉴定,结果发现酶切产物分别得到片段为1992 bp的目的条带和4700 bp的载体片段,表明目的基因已连接至pEGFP-C1载体,成功构建真核表达载体pEGFP-cELF4(图13)。
2.11 EGFP-cELF4融合蛋白荧光观察及其与cELF4特异性IgY反应性检测结果
结合绿色荧光和Hoechst 33342染色可看出,转染pEGFP-cELF4细胞的绿色荧光主要呈现较规则的圆形或椭圆形,而转染pEGFP-C1细胞的绿色荧光在细胞质和细胞核中均匀分布,空白对照中则无绿色荧光,说明EGFP-cELF4融合蛋白细胞绿色荧光定位在细胞核中(图14-A)。
EGFP单克隆抗体孵育组:Hela-pEGFP-cELF4呈细胞核特异性着色、Hela-pEGFP-C1细胞质和细胞核均有着色,Hela细胞无反应。cELF4特异性IgY孵育组:Hela-pEGFP-cELF4、Hela-pEGFP-C1、Hela细胞均呈细胞核特异性着色,且Hela-pEGFP-cELF4细胞着色细胞数量最多,Hela-pEGFP-C1和Hela着色细胞数量相对较少。说明EGFP单克隆抗体和cELF4特异性IgY均可与EGFP-cELF4融合蛋白发生特异性反应;cELF4特异性IgY可与对照细胞Hela-pEGFP-C1和Hela细胞发生反应,且与Hela-pEGFP-cELF4一样呈细胞核特异性着色(图14-B)。
3 讨论
ELF4基因在抗感染和肿瘤的发生发展中发挥重要调控作用。目前GenBank数据库中正式测定的ELF4基因序列仅有5种动物(人、牛、野猪、小鼠和褐家鼠),软件预测的有47种动物。但目前尚无有关犬ELF4基因克隆、表达及其功能的研究报道。本研究克隆了犬ELF4基因(cELF4),并制备了其特异性的抗体,研究发现,cELF4基因与狐ELF4的核苷酸相似性最高(99.3%),氨基酸相似性最高(99.7%),其次是与野猪ELF4(GenBank No.KU097322)的核苷酸相似性较高(89.8%),氨基酸相似性较高(91.8%)。将系统进化分析结果与动物分类学相结合分析发现,犬与狐处于同一分支上,均属于犬科,二者的ELF4基因亲缘关系最近,虽然从动物分类学角度同科的物种亲缘关系较近,其ELF4基因也应处于同一分支,但也有例外,如海豹、南象海豹和港海豹属于豹科,北美水獭属于鼬科,四者的ELF4基因处于同一分支;此外,鼠科动物(鼠和褐家鼠)的ELF4与cELF4的亲缘关系相对较远。
本研究将cELF4基因与pET28a载体连接,分别转化BL21(DE3)和Rosetta(DE3)表达菌株,经IPTG诱导表达发现,BL21(DE3)表达菌株未表达rcELF4蛋白,而Rosetta(DE3)表达菌株能表达rcELF4蛋白,其原因是Rosetta(DE3)菌株能提供稀有密码子,而BL21(DE3)不能提供稀有密码子;经SDS-PAGE和Western blotting检测发现,在Rosetta(DE3)表达菌株表达的rcELF4蛋白分子量约100 kD。本研究将cELF4基因插入pET-28a载体的BamHⅠ和XhoⅠ之间,cELF4基因上游从NcoⅠ到BamHⅠ之间有His与T7标签基因、其编码蛋白的分子量大小约为3.5 kD,与cELF4形成融合蛋白,而软件预测的cELF4分子量约为70.7 kD,两者之和(约74.2 kD)远小于表达的rcELF4蛋白分子量,推测由于rcELF4蛋白在表达菌中被修饰所致(李晓蓉等,2015)。
本研究结果显示,不同类型的免疫佐剂会对rcELF4蛋白抗原的免疫原性产生不同的影响,三组佐剂疫苗的鸡血清抗体滴度均在首免后38 d达到最高值,以ISA 201VG组效价最优;三组佐剂免疫鸡的卵黄抗体均在首免后第14 d特异性抗体转阳,在首免后35 d三组佐剂免疫鸡的卵黄抗体滴度均达最高峰,首免后38 d三组蛋鸡血清的效价也达到最高,且比首免后第35 d和42 d的卵黄抗体效价要高,ISA 201VG组除外,因为血清首免后第38 d为128000倍呈阳性,因此最高效价大于128000倍,可得出血清中的抗体效价与卵黄抗体的效价呈正相关,且血清抗体效价要高于卵黄抗体效价,与杭柏林等(2020)的研究结果一致。此外,三组鸡蛋卵黄含量均在总体上表现出先减少后增加的趋势,随着时间的推移,IgY含量逐渐减少,二次免疫后IgY含量增加。张小莺和陈琛(2011)研究表明,特异性血清抗体转移到卵黄大约需要3~6 d,因此卵黄抗体峰值出现的时间相对血清抗体峰值出现的时间要晚。刘铭(2020)研究发现,水稀释-硫酸铵二次沉淀法提取IgY含量为3.837 mg/mL卵黄液、辛酸法提取IgY含量为3.422 mg/mL卵黄液、氯仿法提取IgY含量为4.512 mg/mL卵黄液;路桂霞(2020)研究发现,水稀释-硫酸铵二次沉淀法提取IgY含量为1.05 mg/mL卵黄液。本研究使用聚乙二醇法提取的IgY含量最高,为4.09 mg/10 mL卵黄液,与向冬梅等(2020)研究发现聚乙二醇法提取的IgY纯度最高、杂质最少的结论相符。上述研究所制备的IgY含量均有所差异,一方面跟提取方法不同有关,另一方面与个体差异和品种差异也有一定关系(路桂霞,2020)。
本研究通过不同佐剂试验组比较发现,比ISA 15AVG佐剂相比,ISA 201VG佐剂和ISA 71VG佐剂激发的抗体水平更高。ISA 201VG是一种新型矿物水包油包水的佐剂,具有良好的耐受性,可快速诱导短期免疫反应并激发细胞免疫反应;ISA 71VG是一种新型矿物油包水佐剂,可诱导长期体液免疫反应,并能较好地激发细胞免疫反应。与标准佐剂相比,新型矿物油佐剂更能引发类似的IgG1反应,不仅增强IgG2a反应,还可增强鸡艾美尔球虫抑制蛋白亚单位疫苗的体液和细胞免疫应答反应(Jang et al.,2011),诱导肉鸡对H5N1亚型禽流感灭活疫苗的细胞免疫应答、提高HI抗体水平(王彦妮等,2011)。卵黄抗体具有高特异性、高亲和力(Lee et al.,2017)、化学性质稳定、生产制备过程简单、经济产量高等优点,可替代哺乳动物的IgG抗体,被广泛应用于畜禽细菌性肠道疾病防治病、急性呼吸道感染、免疫分析检测和食品行业的保鲜(王刚和吕殿红,2002;Zhang et al.,2015;张璐等,2017;Constantin et al.,2020;Kota et al.,2020;贺维朝等,2021)。本研究所优化的佐剂配伍免疫后的IgY产量高,为后续应用降低了成本。
本研究通过荧光观察和免疫染色确定cELF4定位在细胞核中,与Suico等(2004)报道的人ELF4细胞核定位结果一致。此外,通过免疫染色发现,cELF4特异性IgY不仅与融合蛋白EGFP-cELF4反应良好,且与Hela细胞也呈特异性的细胞核染色反应,一个视野中仅为部分Hela细胞细胞核着色,部分细胞无着色。这可能是由于cELF4与人ELF4氨基酸序列相似性较高(89.6%),且存在保守区,故而产生交叉反应。至于其中仅部分细胞细胞核着色、部分不着色,可能与每个Hela细胞中ELF4表达量的大小有关。那么,cELF4特异性IgY是否还与其他物种的ELF4存在交叉反应,且交叉反应的强度是否有差异,交叉反应的具体抗原表位是否相同,这些问题是后续深入研究的方向。
4 结论
cELF4基因与狐的ELF4基因亲缘关系最近,rcELF4蛋白在大肠杆菌中成功表达且存在翻译后修饰现象。不同类型的免疫佐剂对rcELF4蛋白的免疫原性产生不同影响,所制备rcELF4抗体免疫活性良好、且与人ELF4蛋白存在交叉反应。
