Janus激酶靶点药物国内外研发总览
2022-11-05王素云王立峰
王素云,王立峰
〔华诺通(北京)医药科技有限公司,北京 100070〕
Janus激酶(Janus kinase,JAK)是一类非受体型酪氨酸蛋白激酶家族,包括JAK1,JAK2,TYK2和JAK3。JAK1,JAK2和TYK2广泛存在于多种组织和细胞,能被多种细胞因子激活;而JAK3仅存在于骨髓和淋巴系统中,只在白细胞中表达。JAK的底物为信号转导及转录激活因子(signal transduction and activator of transcription,STAT)。JAK通过催化与之相连的STAT使其酪氨酸磷酸化而激活细胞。STAT是一类存在于胞浆、激活后转入细胞核内结合DNA的蛋白家族。细胞因子与相应的受体结合后引起膜通道开放,使与受体偶联的JAK相互接近并活化。JAK被激活后,催化受体上的酪氨酸残基发生磷酸化修饰,活化的STAT以二聚体形式进入细胞核内与DNA结合,调控基因转录及表达,该信号转导途径被称为JAK/STAT信号通路[1]。JAK/STAT信号通路对调控免疫系统、促进细胞生长、抗凋亡及促进细胞周期等发挥重要作用,同时与肿瘤的发生发展也有密切关系,对造血细胞的生长发育也有重要的调控作用[2]。因此,开发适合的JAK抑制剂抑制JAK激活进而阻断JAK/STAT信号通路,可用于血液系统疾病、肿瘤、类风湿性关节炎和银屑病等治疗。本文主要从JAK抑制剂药理作用,全球已批准上市、申请上市和正处于临床研究阶段的JAK靶点药物及其临床应用的潜在风险等方面介绍JAK靶点药物研发概况,并跟进追踪了当前国内JAK靶点药物基础及临床研究进展。
1 JAK抑制剂药理作用
不同的细胞因子激活不同的JAK亚型,因此针对不同JAK的选择性抑制剂可能具有不同的潜在用途和不良反应。基于它们的选择性和作用靶点不同,将JAK小分子抑制剂分为3类,即非选择性JAK抑制剂、选择性JAK抑制剂及JAK和其他激酶共同抑制剂[3]。
1.1 非选择性JAK抑制剂
非选择性JAK抑制剂指的是一类同时作用于多个JAK的小分子化合物,这类化合物能阻断多条JAK相关信号通路,对多种自身免疫性疾病有效。2011年最先获得美国食品药品监督管理局(Food and Drug Administration,FDA)批准的芦可替尼(ruxolitinib)是一种非选择性JAK抑制剂,2017年3月在中国上市。芦可替尼既可用来抑制JAK1,也可用来抑制JAK2,因此其既可用于治疗炎症性疾病,也可用于治疗由于JAK2功能异常而引发的骨髓纤维化、真性红细胞増多症和银屑病等。2012年美国FDA批准上市的托法替布(tofacitinib)也是典型的非选择性JAK抑制剂的代表药物,2017年3月在中国上市,批准用于与甲氨蝶呤(methotrexate)或其他非生物改善病情抗风湿药物联用治疗对甲氨蝶呤反应不足或对其无法耐受的中度至重度活动性类风湿性关节炎成年患者,其作用时优先抑制与JAK3或JAK1相关细胞因子受体的信号转导,对JAK2有较弱的抑制作用,但对TYK2无效[4]。巴瑞替尼(baricitinib)也是一种非选择性JAK抑制剂,强效抑制JAK1和JAK2,但对TYK2和JAK3的抑制作用较弱[5]。
1.2 选择性JAK抑制剂
由于非选择性JAK抑制剂出现较多不良反应,因此针对某一特定JAK靶点的药物,则可在控制疾病发展的同时显著减少不良反应事件的发生。因此,此类小分子抑制剂是当前JAK抑制剂研发的热点之一[6]。
1.2.1 选择性JAK1抑制剂
JAK1与白细胞介素6和干扰素γ等炎症因子的激活密切相关,因此认为选择性JAK1抑制剂对治疗类风湿性关节炎和银屑病等自身免疫性疾病具有潜在的治疗效果。索西替尼(solcitinib)是通过高通量筛选得到的代表性选择性JAK1抑制剂,其首先被开发应用于治疗斑块型银屑病,并取得了较好的临床疗效,而后对其用于治疗成人系统性红斑狼疮也进行了Ⅱ期临床试验研究,但在该项研究中发生了10例严重不良反应事件,该临床试验被提前终止[7]。由于JAK1和JAK2与细胞因子的ATP结合方式各不相同,因此通过结构预测开发出选择性JAK1抑制剂乌帕替尼(upadacitinib)。该产品对类风湿性关节炎的治疗效果较好,重复给药无明显累积。在健康受试者每天服用2次数日后,头痛是最常见的不良事件,所有因治疗引起的不良事件的严重程度均为轻度或中度[8]。国内企业恒瑞制药申报的硫酸伊伐马替尼(ivarmacitinib sulfate,SHR-0302)也是JAK1抑制剂。
1.2.2 选择性JAK2抑制剂
JAK1主要针对于炎症靶点,而JAK2适宜作为治疗自身免疫性疾病的靶点。JAK2可单独介导红细胞生成素等细胞因子,与血液细胞增殖和分化密切相关。JAK2突变体JAK2V617F与真性红细胞增多症、原发性血小板增多症和骨髓纤维化密切相关。因此,JAK2抑制剂有可能应用于此类血液疾病的治疗,同时因可能具有抑制血细胞生成的作用,多数选择性JAK2抑制剂的不良反应相对较大。临床试验结果表明,JAK2抑制剂潜在的不良反应与剂量因素有关,因此其疗效窗口很小。目前进展最快的选择性JAK2抑制剂是进入到Ⅱ期临床阶段的加多替尼(gandotinib)、BMS-911543和依吉替尼(ilginatinib)。
1.2.3 选择性JAK3抑制剂
JAK3仅存在于骨髓和淋巴系统,在NK细胞和胸腺细胞中高表达,且在T细胞、B细胞和髓样细胞中可被诱导表达。因此,选择性靶向JAK3可能具有较小的不良反应,可用于预防移植排斥和治疗多种自身免疫性疾病如类风湿性关节炎、强直性脊柱炎、银屑病、关节炎和克罗恩病等,并且可降低由于抑制JAK1和JAK2而引发的不良反应[9]。地舍诺替尼(decernotinib)是通过筛选针对免疫细胞中关键信号激酶JAK3的化合物库得到的一种新型选择性JAK3抑制剂,Ⅱ期临床研究用于联合甲氨蝶呤治疗对甲氨蝶呤单用无效的类风湿性关节炎患者,服药后患者病情最快可在1周内得到改善,但存在高脂血症、肌酐升高、转氨酶升高、嗜中性白细胞减少症和淋巴细胞减少症等不良反应[10],因此目前临床无更新的进展。PF-06651600是美国辉瑞(Pfizer)公司开发的选择性JAK3抑制剂,目前正在进行治疗克罗恩病、类风湿性关节炎和溃疡性结肠炎的Ⅱ期临床试验研究[11]。
1.3 JAK和其他激酶共同抑制剂
还有一部分在研药物,在抑制JAK的同时对其他激酶也具有抑制作用。如色度拉替尼(cerdulatinib)是一种JAK和SYK共同抑制剂,在Ⅱ期临床试验中显示出对外周T细胞淋巴瘤(peripheral T-cell lymphoma,PTCL)和皮肤T细胞淋巴瘤(cutaneous T-cell lymphoma,CTCL)良好的疗效和耐受性,在PTCL和CTCL部分亚型甚至可观察到完全而持久的缓解[12],该结果也为SYK和JAK共同抑制剂提供了有力支持。SB-1578是作用于JAK2、集落刺激因子1受体和FMS样酪氨酸激酶3(FMS-like tyrosine kinase 3)的共同抑制剂,2010年被欧洲委员会授予用于治疗骨髓纤维化的孤儿药资格[13],但近几年未见进一步的临床进展报告。
2 全球已批准上市、申请上市和正处于临床研究阶段的JAK靶点药物
目前JAK靶点药物,全球共批准上市10个,申请上市1个,临床Ⅲ期8个,临床Ⅱ期20个,临床Ⅰ期23个(表1)。上市的10个药物分别是诺华治疗血液病的芦可替尼(Jakavi)、辉瑞治疗类风湿性关节炎的托法替布(Xeljanz)和治疗特应性皮炎的阿布昔替尼(abroxitinib,Cibinqo)、Incyte Corp的巴瑞替尼(Olumiant)、Concert和中国台湾杏国新药治疗骨髓纤维化的帕瑞替尼(pacritinib,Vonjo)、比利时Galapagos Nv的非戈替尼(filgotinib,Jyseleca)、日本烟草的地戈昔替尼(delgocitinib,Corectim)、艾伯维的乌帕替尼(Rinvoq)、赛诺菲的菲卓替尼(fedratinib,Inrebic)和安斯泰来的吡西替尼(peficitinib,Smyraf)。正在申请上市的是百时美施贵宝的氘可来昔替尼(deucravacitinib,BMS-986165),用于治疗皮肤红斑狼疮、盘状红斑狼疮、溃疡性结肠炎、克罗恩病和狼疮性肾炎。
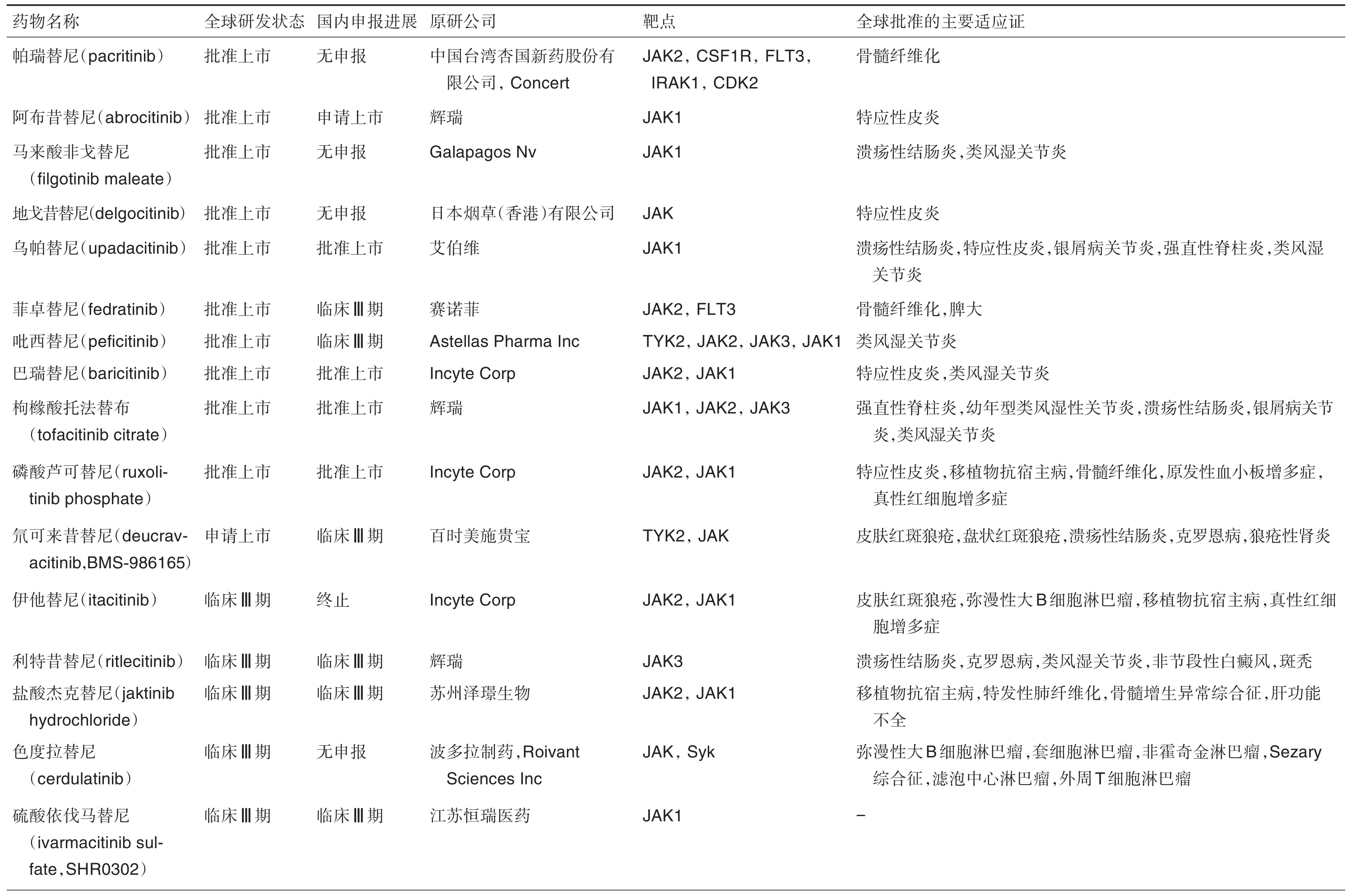
表1 全球已批准上市、申请上市及正处于临床Ⅲ期、Ⅱ期和Ⅰ期研究的Janus激酶(JAK)靶点药物汇总(截止2022年4月1日)

续表1
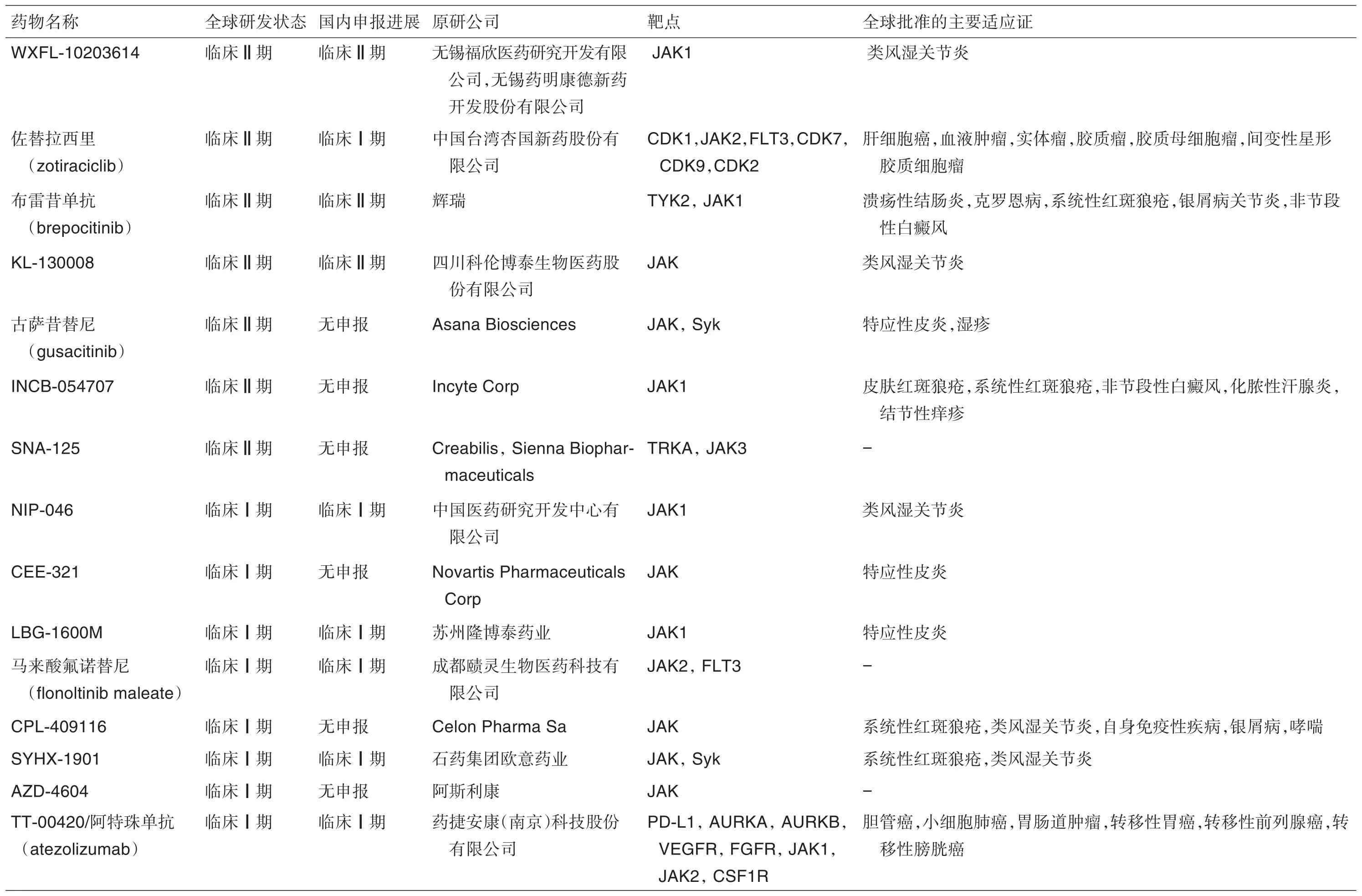
续表1
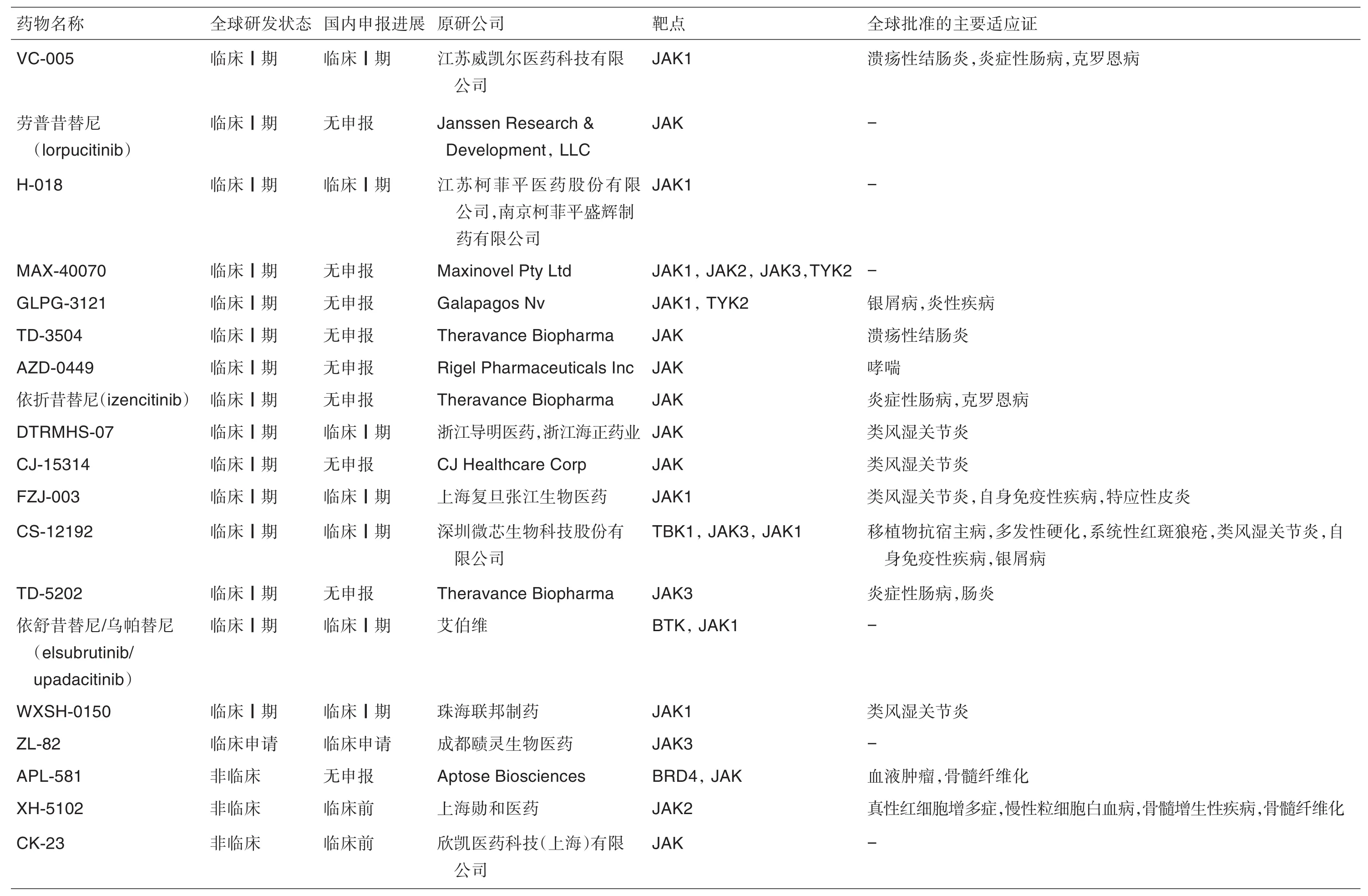
续表1

续表1

续表1
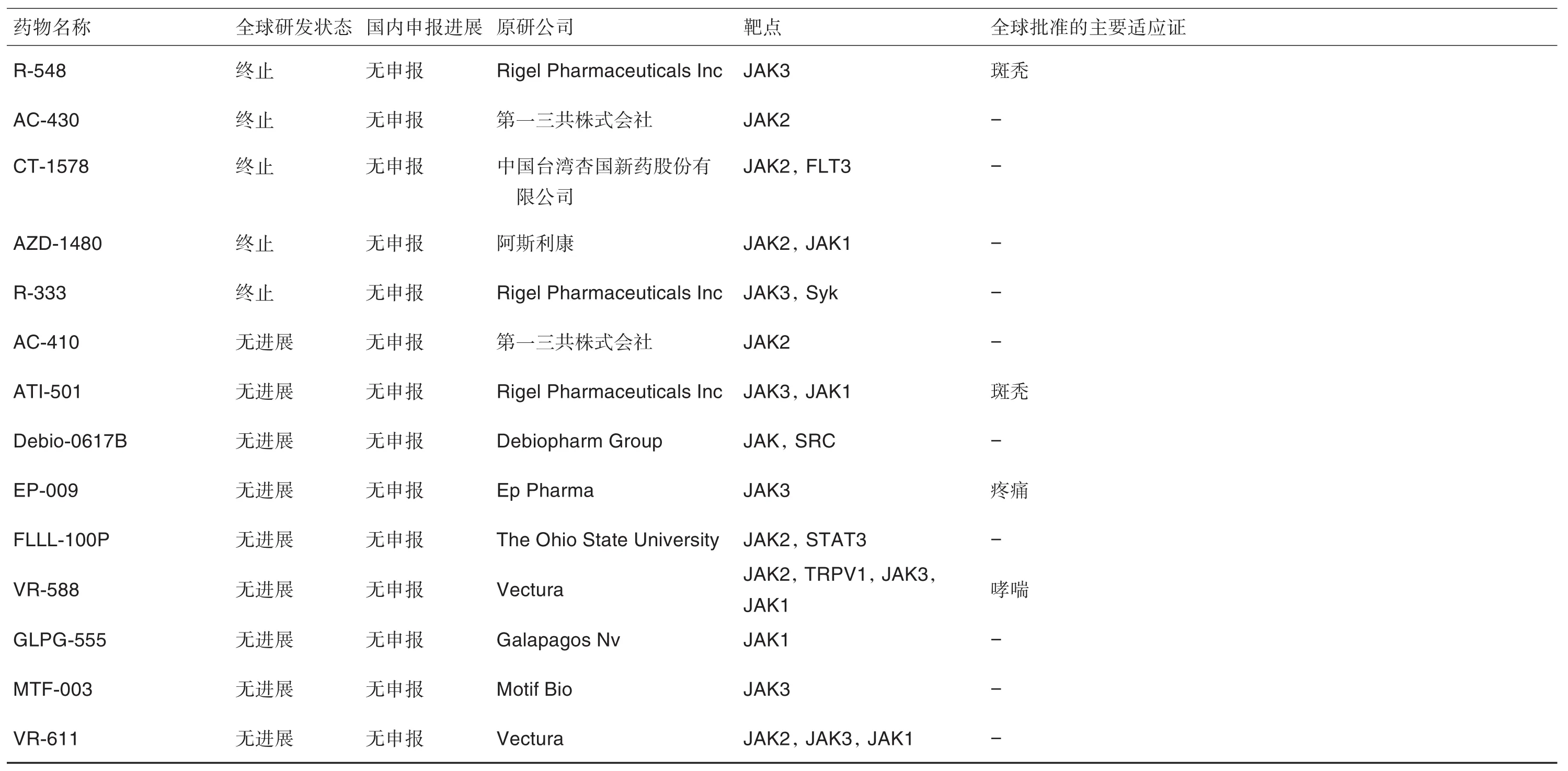
续表1
3 国内JAK靶点药物临床安全性研究
目前,国内进展到临床Ⅲ期以上的JAK靶点药物见表2,其中已上市的有5个:阿布昔替尼、乌帕替尼、巴瑞替尼、枸橼酸托法替布和磷酸芦可替尼。氢溴酸吡西替尼、氘可来昔替尼和硫酸伊伐马替尼也完成了部分适应证的临床研究,未来几年将陆续提交上市申请。
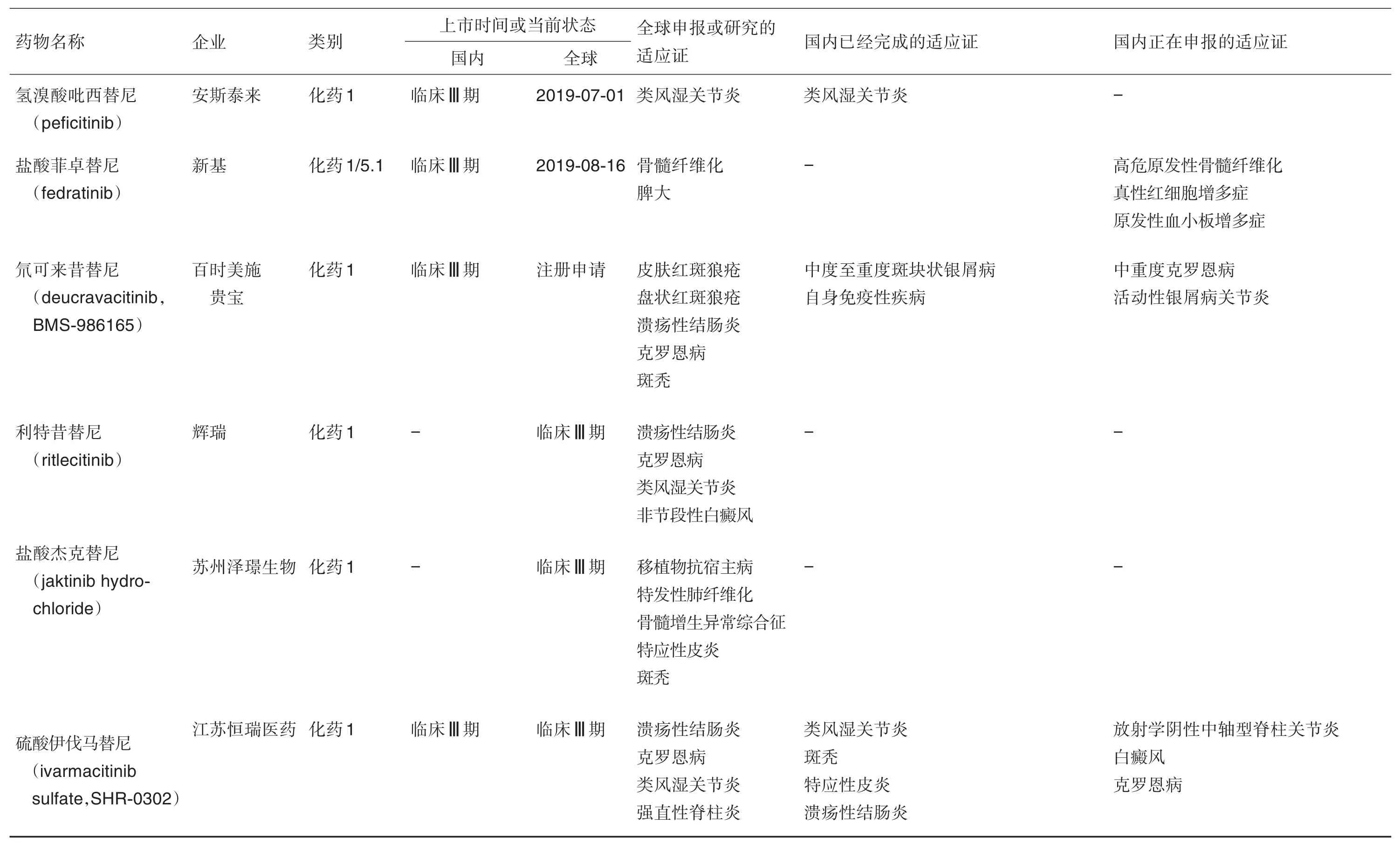
续表2
由于阿布昔替尼和乌帕替尼在我国上市时间较短,尚未见其临床安全性的相关报道。巴瑞替尼国内有少量的临床报道,刘擘等[14]观察了24例巴瑞替尼治疗中重度特应性皮炎患者的疗效和安全性,仅出现3例轻微胃部不适和1例眼部瘙痒。张梨等[15]通过对美国FDA 15 480 927份不良事件报告的系统研究,挖掘药物不良反应(adverse drug reactions,ADR)信号1162个,数量排名前3位的分别为感染和侵袭性疾病(invasive disease),呼吸系统、胸及纵隔疾病和良性、恶性及性质不明的疾病;ADR报告数量排名前3位的首选语(preferred terms)分别为肺检塞、带状疱疹和深静脉血栓形成;信号强度(signal intensity)排名前3位的分别为弥漫性大B细胞淋巴瘤Ⅳ期、带状疱疹脑膜炎和结核性胸膜炎。其中女性多发于男性;年龄≥45岁者最多,占76.40%;认为使用巴瑞替尼时除需关注常见ADR外,还应重视药品说明书中未涉及的新的ADR信号。用药期间需密切关注呼吸道和皮肤等部位的严重感染及栓塞等,以便及时采取相应防范措施,避免发生严重ADR。秦元等[16]通过国内外临床数据进行荟萃(Meta)分析,纳入6个符合标准的共3546例患者数据。结果表明,巴瑞替尼与安慰剂比较可增加感染和带状疱疹的不良反应发生率,且巴瑞替尼剂量增加并未显著提高疗效。
托法替布和芦可替尼由于上市时间较长,安全性研究相关报道较多。罗洁等[17]对2年内使用芦可替尼治疗骨髓纤维化超过12个月的60例患者进行跟踪研究,发现血液系统不良反应主要为贫血(68.09%)和血小板减少(40.3%),非血液系统不良反应主要是感染(23.33%)。李淼[18]通过回顾性研究发现,随访33例使用芦可替尼治疗骨髓纤维化的患者,其中31例出现1次及以上的不良事件,最常见的血液系统不良反应是贫血和血小板减少,非血液系统不良反应主要有脱发、头晕、腹胀、带状疱疹、水肿、血糖升高、牙龈出血、恶心、肺炎和失眠。患者对不良反应可耐受,很少因不良事件而停药。吴晶[19]通过检索国内外各大数据库(包括中国知网和Pubmed等)建库以来至2020年1月的数据并进行Meta分析,纳入的8项研究中含2139例参与者和1440项事件。在安全性方面,贫血发生率〔相对危险度(relative risk,RR)=1.60,95% 置信区间(confidence interval,CI)(1.24,2.05),P=0.0003〕和血小板数减少发生率〔RR=1.61,95%CI(1.17,221),P=0.003〕较安慰剂相比有所升高。中性粒细胞减少发生率〔RR=1.82,95%CI(0.83,3.98),P=0.13〕、消化道反应〔RR=6.31,95%CI(0.96,41.52),P=0.06〕、感染〔RR=1.48,95%CI(0.95,2.28),P=0.08〕及其他常见不良反应发生率,包括疲劳乏力、腹痛、呼吸困难、发热、心脏毒性和周围神经病等,与安慰剂比较无统计学差异。在第二肿瘤发生率方面,芦可替尼不良反应发生率〔RR=3.12,95%CI(1.87,5.20),P<0.0001〕高于安慰剂。高乐女等[20]采用托法替布联合甲氨蝶呤治疗对传统改善病情抗风湿药物或联合生物制剂治疗效果均不佳的中重度类风湿性关节炎患者21例,所有患者在接受托法替布治疗前后均未发生过敏反应,血常规、肝肾功能无异常变化,亦无其他严重不良反应,认为托法替布联合甲氨蝶呤治疗类风湿性关节炎安全性较高。张爱玲等[21]对托法替布临床数据库进行Meta分析,纳入8项随机对照研究,共3308例银屑病患者。数据结果分析显示,与安慰剂相比,托法替布组的体内胆固水平升高和带状疱疹发生率增加,其他不良反应,如严重感染、机会性感染、恶性肿瘤和胃穿孔等发生率无统计学差异。
刘洁等[22]收集美国FDA不良反应报告系统数据库中关于JAK靶点类药物相关的血栓栓塞事件并进行统计分析,结果4种JAK抑制剂均检测出血栓栓塞事件,芦可替尼、托法替布、巴瑞替尼和乌帕替尼发生血栓栓塞事件的总数分别为484,1886,157和174例;在年龄构成上,芦可替尼、托法替布和巴瑞替尼发生血栓栓塞事件的年龄多分布于65~85岁,乌帕替尼多分布于18~64岁;在性别构成上,女性均高于男性。
相较而言,国内对这几个新型JAK抑制剂的临床疗效较为认可,促进了此类药物在临床上的广泛快速应用。但同时,国内对此类药物严重不良反应的报道较为少见,多数是对美国FDA不良反应数据跟进研究。因此,未来需要加强对此类药物严重不良反应的跟踪以确保用药安全,同时及时公布临床监测数据并提高临床安全性认知。
4 JAK抑制剂临床应用的潜在风险
目前海外已上市的10个产品,预计2024年全球销售额将接近200亿美元,国内市场预计也将在2024年超过100亿元。目前已经出现年销售额超过10亿美元的重磅产品芦可替尼、托法替布和乌帕替尼,其中乌帕替尼2019年刚刚上市,2021年的销售额即高达16.51亿美元,预计2025年其销售额将超过75亿美元[23]。
由于JAK抑制剂在临床上取得了良好的治疗效果,此类药物与甲氨喋呤单用或联用已成为一些疾病如类风湿性关节炎的一二线临床治疗方案[24]。但与此同时,JAK抑制剂的毒理学问题日益突出。由于许多信号转导途径均通过JAK活化完成,JAK缺失可导致严重的免疫缺陷综合征,而JAK过度激活则会引起肿瘤发生,这也是开发JAK靶点新药面临的最主要风险。美国FDA在其药品安全通讯中发布专题警示,要求对于治疗某些慢性炎症的JAK抑制剂引起严重心脏相关事件、癌症、血栓和死亡风险增加发出警告,批准的用途也仅限于某些特定患者群体。同时美国FDA要求对托法替布、巴瑞替尼和乌帕替尼说明书进行修订,增加黑框警告(美国FDA最重要的警告),以纳入包括严重心脏相关事件、癌症、血栓和死亡风险的安全性信息。对医务人员的建议包括在开始或继续治疗前,需要综合考虑对个体患者的获益和风险。此外,为确保该3种药物对接受治疗的患者的获益大于风险,美国FDA将所有批准的临床使用限制为对一种或多种肿瘤坏死因子抑制剂反应不充分或不能耐受的特定患者。美国FDA同时要求生产企业修订药品说明书的处方信息,要求修订多个相关的用药指南,提醒临床等专业人士和患者关注相应的信息变化,注意不良反应风险[25]。
其他JAK抑制剂尚未进行类似的大型安全性临床试验研究,因此该类药物的风险尚未得到评估。然而,由于它们与托法替布具有相同的作用机制,美国FDA认为该类药物可能具有与托法替布安全性试验类似的风险。
事实上,虽然JAK靶点药物巨大的市场潜力促进了该类新药的研发,但潜在的安全风险也会影响新药上市。葛兰素史克开发的索西替尼在Ⅱ期临床试验中由于严重的不良事件(肝酶升高、药疹伴嗜酸粒细胞增多和系统症状)及其与他汀类药物的相互作用而提前终止。Vertex公司的地舍诺替尼由于Ⅱ和Ⅲ期临床试验中出现中性粒细胞减少而终止研究。非戈替尼虽然在欧盟和日本获批,但美国FDA以安全隐患为由,拒绝批准其上市。
5 展望
虽然JAK抑制剂的临床应用具有潜在风险,但JAK仍然是国内外众多企业关注的热门靶点,特别是JAK高选择性抑制剂,因为其有助于降低不良反应而将成为后续“best in class”研发的重点。JAK靶点新药的不断上市及其优异的市场表现和巨大的市场潜力,也会带动我国该靶点药物研发快速跟进,且该类药物在斑秃、白癜风和瘢痕等领域拓宽了JAK靶点类药物的适应边界,新的剂型和给药方式也会受到关注。但与此同时,该类药物的不良反应在临床大量使用后可能会表现得更加突出,需要在临床中加大关注并加强上报力度。
