胸外科术后30 d内非计划二次手术的临床特点
2022-11-03张家齐陈野野刘洪生李单青
张家齐,刘 磊,赵 珂,郭 超,黄 诚,陈野野,刘洪生,李单青
中国医学科学院 北京协和医学院 北京协和医院胸外科,北京 100730
非计划二次手术是指同一患者同一次住院期间因手术并发症、医疗差错失误、检验检查结果误差等原因造成的2次或2次以上手术[1-2]。有研究表明,10%患者在住院期间会出现与手术或药物等相关的不良事件发生,其中大部分是可以预防的[3]。围手术期的安全管理已被世界卫生组织列入患者安全目标[4]。2015版美国医师质量报告系统将术后30 d内非计划二次手术作为普通外科7种衡量指标之一[5]。近年来,胸外科的术后快速康复发展迅速,患者有效的快速恢复是医疗安全的主要目标,但目前对不安全手术事件的报道较少,对非计划二次手术的分析更少。本研究旨在分析北京协和医院胸外科术后30 d内非计划二次手术的临床特点,以供临床参考。
资料和方法
资料来源检索2016年5月至2021年5月北京协和医院胸外科收治的患者,包括急诊及门诊途径入院患者,纳入其中术后30 d内非计划二次手术患者。本研究通过北京协和医院伦理委员会审批(伦理审查编号:S-K1796)。
方法通过电子病例系统收集所有患者的临床资料,包括性别、年龄、美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级、入院时间、入院诊断、手术时间、手术名称、出院时间、出院诊断、治疗经过、出院结局转归、住院费用等。
统计学处理采用SPSS 23.0统计软件,符合正态分布的计量资料以均数±标准差表示,组间比较采用t检验;非正态分布的计量资料以M(Q1,Q3)表示,组间比较采用秩和检验;计数资料以频数(百分比)表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
结 果
一般情况共10 543例患者入院接受胸外科手术治疗,79例患者于术后30 d内接受非计划二次手术,发生率为0.75%,中位年龄为60.05(49.43,64.67)岁,其中男性患者54例,占68.35%;除4例(5.06%)患者经急诊入院,其余均由门诊收入院。2016年5月至2017年5月发生非计划二次手术的例数最多,占27.85%。43例(54.43%)患者合并全身性基础疾病。ASA Ⅰ、Ⅱ、Ⅲ级患者分别占43.04%、45.57%、11.39%。22例(27.85%)为食管/贲门疾病,16例(20.25%)为良性疾病。64例(81.01%)首次手术为微创手术,59例(74.68%)非计划二次手术为微创手术。22例(27.85%)患者接受输血治疗,26例(32.91%)患者接受重症监护治疗。所有非计划二次手术患者中位住院天数19(12,37)d,中位住院费用109 929.11(80 549.46,173 491.87)元。
根据是否为食管/贲门疾病进行分组,患者性别(χ2=7.171,P=0.007)、年龄(χ2=426.000,P=0.028)、首次手术方式(χ2=9.526,P=0.002)、住院费用(χ2=333.000,P=0.001)、住院天数(χ2=253.500,P<0.001)以及重症监护治疗(χ2=13.037,P<0.001)在食管/贲门组和非食管/贲门组之间差异有统计学意义;合并基础疾病(χ2=0.267,P=0.605)、ASA分级(χ2=0.305,P=0.858)以及输血治疗(χ2=0.239,P=0.625)在食管/贲门组和非食管/贲门组之间差异无统计学意义(表1)。
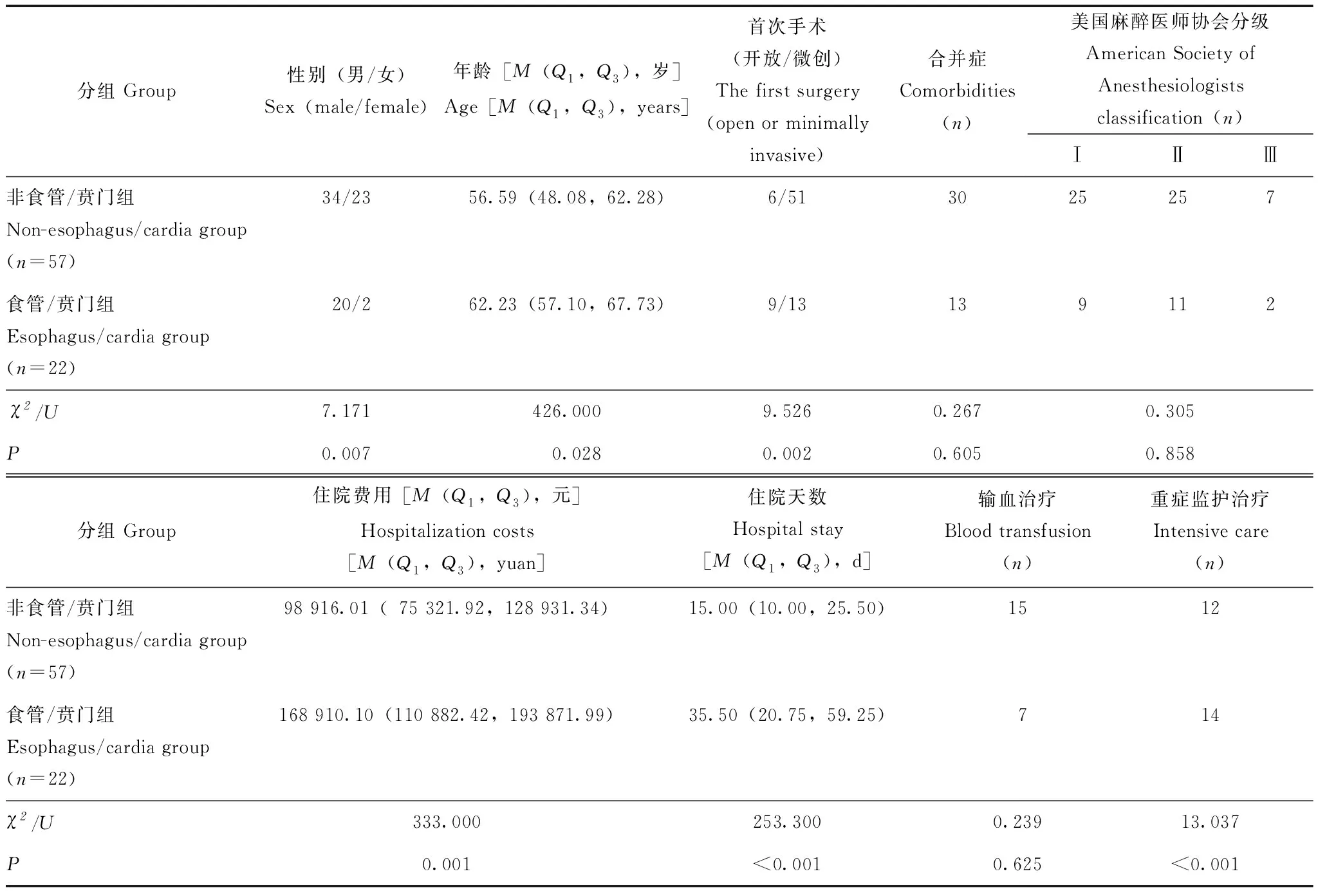
表1 食管/贲门组和非食管/贲门组患者的基线特点Table 1 Characteristics of patients between esophagus/cardia and non-esophagus/cardia groups
非计划二次手术因素所有非计划二次手术原因包括:出血(21.52%)、乳糜胸(17.72%)、肺漏气(16.46%)、肺不张(13.92%)、消化道瘘(11.39%)、切口愈合不良(6.33%)、病变遗漏(2.53%)、引流管脱落(2.53%)、人工血管堵塞(1.27%)、肠梗阻(1.27%)、膈疝(1.27%)以及非手术相关因素(术中冰冻病理与术后石蜡病理结果不一致)(3.80%)。其中,非食管/贲门组患者非计划二次手术原因为出血(22.81%)、肺漏气(22.81%)、肺不张(19.30%)、乳糜胸(17.54%)、病变遗漏(3.52%)、引流管脱落(1.75%)、膈疝(1.75%)、消化道瘘(1.75%)、人工血管堵塞(1.75%)、切口愈合不良(1.75%)、非手术相关因素(5.26%);食管/贲门组患者非计划二次手术原因为消化道瘘(36.36%)、切口感染愈合不良(18.18%)、出血(18.18%)、乳糜胸(18.18%)、引流管脱落(4.55%)及肠梗阻(4.55%)。
转归所有非计划二次手术患者中,4例死亡,包括1例重症肺炎,1例口腔颌面部感染继发纵隔感染、脓胸、感染性休克,1例食管癌行三切口手术术后吻合口瘘、食管气管瘘继发感染性休克,1例术后持续肺漏气突发心源性死亡可能;17例好转,二次手术后存在持续肺漏气、淋巴漏或慢性感染,病情迁延、稳定;58例痊愈。与非食管/贲门组比较,食管/贲门组患者非计划二次手术结局转归更差,差异有统计学意义(χ2=6.823,P=0.033)(图1)。
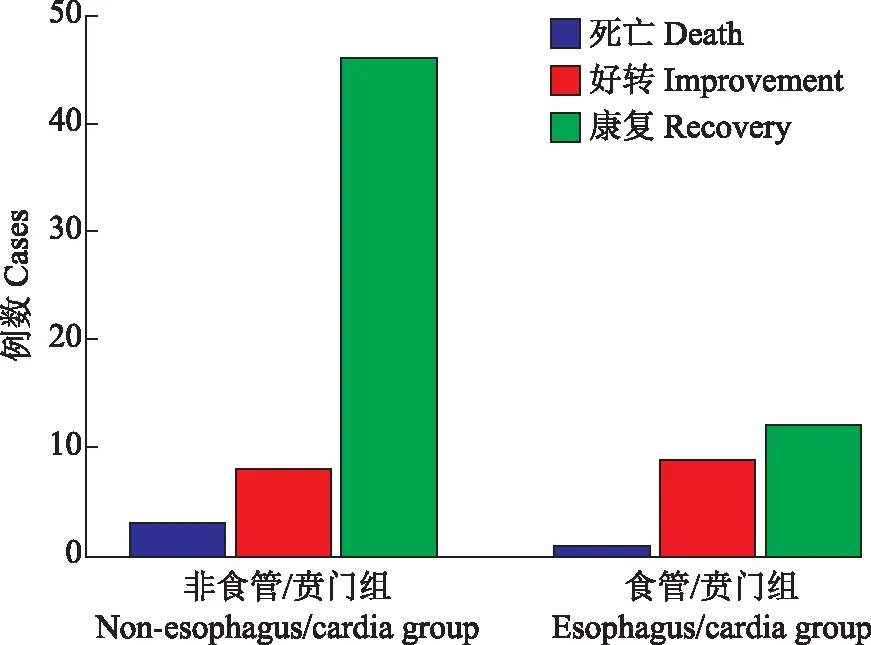
图1 食管/贲门组和非食管/贲门组患者临床结局比较Fig 1 Comparison of clinical outcomes between non-esophagus/cardia group and esophagus/cardia group
讨 论
有研究表明,胸外科术后常见的严重并发症主要包括肺部感染、胸腔感染、食管吻合口瘘、肺不张及肺栓塞等,这些并发症也是围手术期患者死亡的主要因素[6]。本研究着重分析胸外科术后30 d内非计划二次手术患者的临床特点,结果显示术后出血、乳糜胸、肺漏气、肺不张及消化道瘘是胸外科非计划二次手术的主要原因,其中,非食管/贲门组患者非计划二次手术原因主要为出血、肺漏气、肺不张及乳糜胸;食管/贲门组患者非计划二次手术原因主要为消化道瘘、切口感染愈合不良、出血及乳糜胸,与既往研究报道结果一致[7]。Petrella等[8]总结2016年1月至2020年12月单中心胸部肿瘤手术患者非计划二次手术的影响因素,结果发现首次手术以全肺切除术为主,非计划二次手术发生率为1.76%,主要原因为血胸(54.9%)、支气管瘘(26.8%)、脓胸(4.2%)、长时间肺漏气(4.2%)等。与之不同的是,本中心总手术量更大,非计划二次手术发生率较低,出血导致非计划二次手术的比例仅占21.52%。此外,本中心2016年5月至2017年5月发生非计划二次手术的例数最多(27.85%),之后较为稳定,可能与手术技术的改进相关。相比于非食管/贲门患者,食管/贲门患者住院费用、住院天数以及接受重症监护治疗的比例显著升高,这可能与食管/贲门手术难度大、并发症风险高以及消化道瘘恢复时间长等因素相关。
手术过程中的风险控制至关重要,其能降低非计划二次手术的发生率,节约医疗成本,提高患者安全系数以及生活质量。在快速康复时代,临床患者的管理更需精细化、个体化,积极做好术前评估、术中操作、术后监测,降低各种并发症的发生,提高手术安全性。本研究结合单中心实践经验及国内外文献资料,总结非计划二次手术的主要原因及处理措施。
手术部位的出血,尤其是切口内出血,是非计划二次手术的主要原因。胸腔镜肺手术出血管理国际专家共识[9]建议,胸壁切口应始终沿肋骨上缘,逐层仔细止血;在插入伤口保护装置之前,应仔细检查切口的任何出血点并进行适当的处理;此外,手术完成后应重新检查切口部位是否止血彻底。对于术区的出血,手术操作过程中,应该确保血管离断的确切性;术毕冲洗胸腔时,应仔细观察有无活动性出血,必要时再次处理各血管残端;术后对于出血的及时发现至关重要,结合胸腔引流液性状、血常规化验及胸部影像学检查可以辅助诊断术后出血。对于较大量的活动性出血可能需要手术积极干预,及时清除胸腔内积血,减少继发性脓胸的发生;少量渗血一般可自限,保守治疗下动态监测即可。
研究显示胸腔镜肺癌根治术后乳糜胸的总体发生率为0.3%[10]。胸外科术后的乳糜胸与术中清扫淋巴结过程中淋巴管的损伤相关。术中能量器械的使用对淋巴管损伤的影响尚缺乏充足的证据,有研究认为术中使用Hem-o-lock夹闭淋巴管残端可以减少右侧肺癌患者术后的胸腔引流量[11]。目前在临床实践中一般多先采取保守治疗,若引流量持续较多,应适当积极进行手术干预[10,12]。较小的淋巴管损伤时,部分患者可通过术后严格低脂饮食或者禁食禁水后好转痊愈,高渗葡萄糖胸膜固定治疗亦有一定的疗效,而且相对无创[13];较大的淋巴管损伤时,术后乳糜胸积液量较多,胸腔镜下胸导管结扎术是比较常见且有效的一种治疗方式,此外,一项Meta分析结果显示奥曲肽辅助治疗对于中到大量乳糜胸具有一定的治疗获益[14]。
胸外科术后肺漏气是一种常见的并发症,持续肺漏气可能会影响肺复张,增加术后胸腔内感染、脓胸的风险。胸腔内广泛粘连、严重肺气肿是肺部术后漏气的主要危险因素。对于术中发现肺漏气的患者,使用聚乙醇酸网片和密封剂治疗是安全的,可以有效减少肺漏气的持续时间、胸腔引流和住院时间[15-16]。术后使用数字化胸腔引流系统持续低压吸引可有效缩短术后肺漏气的时间[17]。有观点认为新鲜冰冻血浆胸腔内治疗也是术后肺漏气的一种有效治疗方法[18]。
胸外科术后的肺不张比较常见,其原因主要包括医源性支气管狭窄、肺淤血以及患者术后主动排痰不畅等。术中应该警惕残余支气管的扭转、成角导致的狭窄,应充分保证残肺的动静脉血液供应,避免肺组织过度淤血,影响肺通气。胸外科术后术区疼痛常影响患者的主动排痰,术后积极镇痛以及正确的咳嗽训练可以帮助患者主动排痰,减少术后痰液阻塞所致的肺不张。结合本中心的临床经验建议术前进行积极有效的宣教及呼吸功能训练,能够有效改善术后咳嗽相关的恐惧心理和并发症,有助于患者术后肺部恢复。
消化道瘘是消化道手术常见且极具危险性的一种并发症。研究显示食管癌术后吻合口或食管胃闭合口瘘的发生率为4.6%[19]。消化道瘘的发生常影响患者术后营养供应及后续辅助治疗,甚至导致肺部感染、脓胸、切口愈合不良等一系列并发症,预后较差。体重指数、吸烟、长期饮酒、糖尿病等全身性疾病、食管上段肿瘤、颈部吻合、管状胃以及术后严重的肺部感染是术后消化道瘘的危险因素[20-22],而新辅助放化疗对消化道瘘的影响并不明确。直接影响消化道瘘的主要原因是吻合口张力过大、血运欠佳,因此手术操作过程中保证吻合口足够的血运、避免其张力过大是降低吻合口瘘的关键因素。有学者通过改良Ivor Lewis技术,简化手术步骤,避免不必要的切除,保护缺血组织,进而降低术后吻合口瘘的发生[23]。除此之外,术后积极、有效的营养支持,预防其他并发症的发生亦至关重要。对于消化道瘘的早期识别会影响其干预措施及预后,本中心经验认为,术中吲哚菁绿荧光显影可辅助判断吻合口附近的血运情况,术后上消化道造影联合造影后的胸部CT对于较小的消化道瘘的诊断较为敏感。此外,切口愈合不良常继发于感染性并发症,且多为开放手术,微创手术少见。本研究中所有切口愈合不良患者均为开胸手术,包括1例开胸肺切除,4例开胸食管/贲门手术。
本研究存在一定的局限性:(1)回顾性研究存在临床数据缺失,导致一部分病例未纳入本研究中;(2)本中心胸外科疾病谱广、手术种类多,非计划二次手术发生率偏低,且非计划二次手术的指征无法统一,故单中心的临床经验存在一定的偏倚;(3)本研究侧重于回顾性临床数据分析结果的描述,无法解决如何有效预测胸外科术后非计划二次手术发生的临床问题,尚需更多大样本病例的对照试验进一步验证。
综上,本研究结果表明,胸外科非计划二次手术患者住院时间长,住院费用高。出血、乳糜胸、肺漏气、肺不张及消化道瘘是非计划二次手术的主要原因。做好术前充分评估,有效提高手术操作技巧以及加强术后精细化管理,是减少非计划二次手术的关键。
