环介导等温扩增技术快速检测粪便样本艰难拟梭菌的 临床应用
2022-10-31王诗淇李荷楠刘井波王占伟王知任迟大利
王诗淇, 李荷楠, 刘井波, 王占伟, 王知任, 迟大利, 王 辉
[1. 北京大学人民医院检验科,北京 100044;2. 复星诊断科技(上海)有限公司参考检测中心,上海 200444]
艰难拟梭菌是一种有芽孢、无荚膜、有鞭毛的革兰阳性专性厌氧杆菌,广泛存在于土壤、人类和其他动物的肠道中。随着高毒力和多重耐药艰难拟梭菌的出现,医院感染暴发的风险增加。快速检出艰难拟梭菌,将其从医院环境中根除,同时隔离有症状的艰难拟梭菌感染患者是阻止艰难拟梭菌芽孢扩散、有效预防医院感染的重要措施。目前,环介导等温扩增技术(loop-mediated isothermal amplification,LAMP)因操作方便、反应时间短、无需额外购买特殊设备等优势,已被应用于多种病原体感染的检测中[1-3]。 本研究拟比较LAMP法与细菌培养法、艰难拟梭菌毒素法快速检测粪便样本中艰难拟梭菌的 差异。
1 材料和方法
1.1 样本来源
收集2021年6—8月北京大学人民医院住院患者临床送检剩余粪便样本132例,其中54例血液科患者样本。本研究经北京大学人民医院伦理委员会审批通过(2019PHB063)。
1.2 方法
1.2.1 艰难拟梭菌毒素检测 取200 μL液体粪便样本或200 mg固体粪便样本,加入1 000 μL样本稀释液(pH值7.2的Tris缓冲液、50%小牛血清、去污剂、防腐剂),用涡旋振荡器彻底混匀,13 680×g离心5 min,分离上清液。取300 μL上清液,采用Mini VIDAS全自动荧光酶标免疫分析仪(法国生物梅里埃公司)及配套艰难拟梭菌毒素A/B检测试剂盒(酶联免疫荧光法)检测。剩余样本用于LAMP检测。
1.2.2 艰难拟梭菌核酸提取 取蛋白酶K(北京索莱宝公司)20 μL,内参反应液[复兴诊断科技(上海)有限公司] 5 μL,再加入300 μL制备好的粪便样本稀释上清液,采用TANBead E13200核酸提取仪(台湾圆点奈米技术开发有限公司)提取艰难拟梭菌核酸。严格按照仪器和试剂说明书要求进行操作。
1.2.3 细菌培养及鉴定 (1)艰难拟梭菌培养。将粪便样本分别接种于环丝氨酸头孢西丁果糖琼脂(cycloserine-cefoxitin-fructose agar,CCFA)平板(英国OXOID公司)和血平板(美国ThermoFisher Scientific公司),放入厌氧产气袋(法国生物梅里埃公司),置于5% CO2培养箱中,35 ℃培养48 h,采用Autoflex speed质谱仪(德国布鲁克公司)鉴定可疑菌落。(2) 沙门菌和志贺菌培养。 将粪便样本分别接种于SS平板、麦康凯平板(美国ThermoFisher Scientific公司),置于5% CO2培养箱中,35 ℃环境下培养24~48 h后观察菌落;分离、纯化可疑菌落后,采用VITEK 2 Compact自动鉴定药敏仪(法国生物梅里埃公司)进行菌种鉴定;同时进行多价血清凝集试验(沙门菌属和志贺菌属诊断血清购自宁波天润公司)。
1.2.4 L A M P法的建立 通过L A M P引物设计软件Primer Explorer(http://primerexplorer.jp/e/)设计引物,包括外引物F3(5'-GTGGGGAGCAAACAGGATT-3')、B3(5'-TCTTCGCGTTGCTTCGAATT-3'),内引物FIP(5'-CGTTAGCTGCGGCACCGAAGAGTCCACGCTGTAAACGATG-3')、BIP(5'-CCTGGGAAGTACGCTCGCAAACATGCTCCGCTACTTGTG-3'),环引物LF(5'-GGTAACCCCCGACACCTAGTAC-3')、LB(5'-CTCAAAGGAATTGACGGGGAC-3')。LAMP反应体系为25 μL,包括14 μL艰难拟梭菌反应液[复兴诊断科技(上海)有限公司]、 1 μL Bst DNA聚合酶[复兴诊断科技(上海)有限公司]、10 μL核酸提取液,反应温度为 63 ℃[4];反应时间为30 min。以无菌0.9%NaCl溶液为阴性对照,以循环阈值(cycle threshold,Ct)≤10.0为阳性。
1.2.5 LAMP法性能评价 (1)特异性评价。 将粪便样本分别接种于血平板、SS平板和麦康凯平板,5% CO2培养箱中35 ℃培养24~48 h后观察菌落,采用VITEK 2 Compac自动化鉴定药敏仪和Autoflex speed质谱仪进行菌种鉴定,鉴定结果用于评价LAMP法的特异性。(2)灵敏度评价。①核酸提取。取3 mL经高压处理后的无菌0.9%NaCl溶液,将艰难拟梭菌标准菌株(ATCC 9689,购自美国典型培养物保藏中心)制备成0.5麦氏浊度单位菌悬液,浓度相当于 108CFU/mL;取1 mL菌悬液,加入Eppendorf管中, 13 680×g离心5 min,弃上清液,加入300 μL无菌纯水,充分混匀,用核酸提取试剂盒提取艰难拟梭菌标准菌株(ATCC 9689)核酸,具体操作步骤与粪便样本艰难拟梭菌核酸提取相同。②稀释。先在5个Eppendorf管中分别加入90 μL无菌纯水,然后在第1个Eppendorf管中加入10 μL 0.5麦氏浊度菌液,充分混匀后取10 μL加入第2个Eppendorf管,用同样的方法稀释到第5管,稀释后的5个Eppendorf管中的细菌浓度分别为107、106、105、104和103CFU/mL,用于LAMP法灵敏度评价。每个浓度进行8个平行测试。
2 结果
2.1 132份粪便样本LAMP检测结果
132份粪便样本均进行了LAMP检测。132份粪便样本中,有110份进行了艰难拟梭菌毒素测定,其中10份(9.09%)艰难拟梭菌毒素检测为阳性,8份(7.27%)为弱阳性;有99份粪便样本进行了艰难拟梭菌培养,其中11份(11.11%)阳性;有113份粪便样本进行了肠道致病菌沙门菌和志贺氏菌培养,仅1份样本检出肠炎沙门菌。54份血液科患者的粪便样本一般细菌培养结果显示,有43份样本培养出至少1种细菌,6份样本培养出真菌,3份样本同时培养出细菌和真菌,2份样本无细菌生长。
2.2 LAMP法特异性评价结果
对未培养出艰难拟梭菌、培养出其他种类细菌或真菌的37份粪便样本进行LAMP检测,结果显示,有20份样本分离出1种细菌,8份样本分离出2种细菌,6份样本分离出1种真菌,3份样本同时分离出1种细菌和1种真菌;37份样本共检出48株菌,LAMP的Ct值均>10.0。见表1。

表1 LAMP法特异性评价试验结果
2.3 LAMP法灵敏度评价结果
以5个稀释度的艰难拟梭菌标准菌株(ATCC 9689)为模板,进行LAMP法灵敏度试验,8次重复试验结果显示,随着核酸浓度的降低,扩增曲线的时间逐渐延长,当浓度降到 104CFU/mL时,平均Ct值为12.5,最终确定LAMP法灵敏度为105CFU/mL。
2.4 LAMP法与细菌培养法、艰难拟梭菌毒素法检测结果的比较
132份粪便样本中,LAMP 法检测阳性18例,阴性114例,阳性检出率为13.64%。LAMP法阳性检出率高于培养法(11.11%)(χ2=18.74,P<0.05)和艰难拟梭菌毒素法(9.09%)(χ2=35.94,P<0.05)。艰难拟梭菌阳性样本中,LAMP法与细菌培养法的一致率为63.64%;与艰难拟梭菌毒素法的一致率为60%。艰难拟梭菌毒法素弱阳性样本中,LAMP法与艰难拟梭菌毒素法的一致率为50%。见表2、表3。
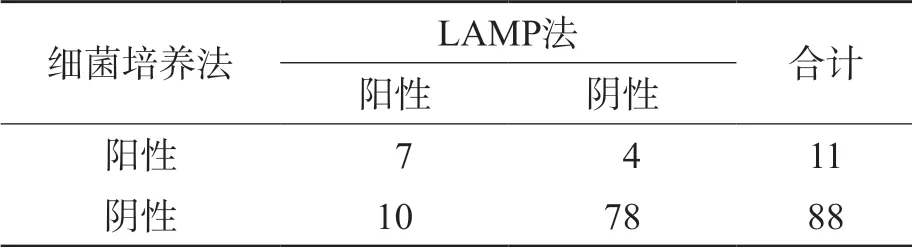
表2 LAMP法与细菌培养法的比较 例

表3 LAMP法与艰难拟梭菌毒素法的比较 例
2.5 LAMP法检测艰难拟梭菌的效能
以细菌培养法为金标准,ROC曲线分析结果显示,LAMP法判断艰难拟梭菌阳性的曲线下面积(95%可信区间)为0.737(0.596~0.878),最佳临界值(Ct值)为10.0。见图1。
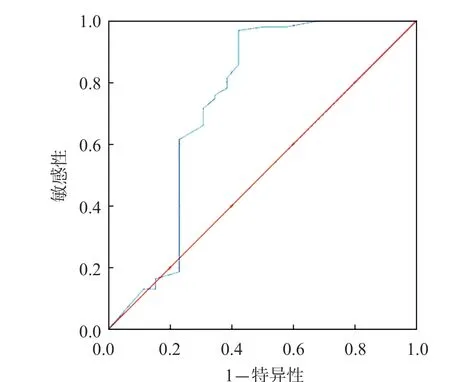
图1 LAMP法检测艰难拟梭菌的ROC曲线
3 讨论
本研究结果显示,LAMP法检测艰难拟梭菌的阳性率(13.64%)高于细菌培养法(11.11%),提示采用LAMP法检测粪便样本可提高病原体的检出率。LAMP法根据不同菌种的高度保守区多个位点设计引物,灵敏度较高[5]。LAMP法检测原理与细菌培养法不同,LAMP法通过扩增来检测病原菌靶基因,如果病原体的基因数达到检测限度,无论病原体是否为活体,结果都是阳性;而培养法要求病原菌必须是活菌,只有优势菌群才能被培养出 来[6]。另外,消化道样本具有复杂性,艰难拟梭菌对培养条件的要求高,也是导致培养分离率低的原因之一。有研究结果显示,10份培养法阴性LAMP法阳性样本中,艰难拟梭菌毒素法阳性有5份、弱阳性有2份,提示细菌培养可能会漏检艰难拟梭菌,如果样本未能及时接种,培养结果可能会出现假阴性[7];另外,如患者入院前使用了抗菌药物,也会导致细菌培养阴 性[8]。有研究发现,在核酸提取过程中,可能会受到细胞壁和芽孢的影响,艰难拟梭菌属于革兰阳性专性厌氧芽孢杆菌,革兰阳性菌细胞壁较厚,含15~50层肽聚糖;此外,芽孢对热力、干燥、辐射、化学消毒剂等因素均有强大的抵抗力,艰难拟梭菌核酸的提取可能会受到以上因素的影响,提取效率有所减低[9]。如果样本中病原体核酸浓度低,达不到最低检测限,也会导致LAMP法检测结果和培养法结果不同。虽然分子技术被认为是临床诊断艰难拟梭菌感染敏感的方法之一,但在使用这种方法时,似乎不可避免地会漏掉一些培养阳性的病例。有研究发现,2 308份样本中,有50份培养法阳性,而聚合酶链反应结果为阴性,原因可能是样本中艰难拟梭菌的核酸水平低于聚合酶链反应的检测下限所致,提示检测限可能影响分子生物学方法检测艰难拟梭菌的结果[10]。目前,临床检测艰难拟梭菌主要依靠细菌培养法和毒素免疫学检测,这些方法耗时长、成本高,对检测人员的要求高,而LAMP法可快速筛查出粪便样本中的艰难拟梭菌。
本研究也存在一定的局限性,即LAMP法不能检测病原菌的毒性,不能区分携带者和感染者。只有携带了含有艰难拟梭菌肠毒素TcdA和/ 或细胞毒素TcdB的艰难拟梭菌才能引起感 染[11]。但有研究发现,无症状携带者是艰难拟梭菌在社区和医院环境中的重要感染源[12-13],因非产毒株可在人体内定植,所以单纯检测病原体的方法与毒素检测方法相结合,才能更好地评估艰难拟梭菌状态。另外,本研究纳入的艰难拟梭菌阳性样本较少,后续将收集不同等级医院更多数量的阳性样本,进一步对LAMP法检测艰难拟梭菌的性能进行评价。
综上所述,艰难拟梭菌的3种检测方法(厌氧培养、毒素法、LAMP)比较,LAMP法特异性强,反应时间短,10 min即可判读结果,且操作简单,无需特殊设备,成本低,适合现场快速检测,可用于医疗资源相对匮乏的基层机构,也可应用于医院感染控制和艰难拟梭菌的早期筛查[14]。采用LAMP法快速检测粪便中的艰难拟梭菌,可有效监测艰难拟梭菌感染,在重症患者和血液病患者感染预警中有一定的价值。
致谢:感谢河北燕达医院对第一作者王诗淇的支持。
