Na2 EDTA容量法测定高镉次氧化锌烟尘中酸溶锌含量
2022-10-27杨晓婷
杨晓婷
(湖南有色环保研究院有限公司,湖南 长沙 410100)
次氧化锌烟尘中仍然含有铅、锌、镉、铁等金属。通常采用的湿法处理次氧化锌烟尘法,是现阶段较为成熟且相对环境友好的处理办法。但目前对于高镉次氧化锌烟尘中酸溶性锌含量的测定未有充分研究。大多数情况下,是浸出酸溶锌后,参考锌精矿化学分析方法[1],对样品中酸溶锌的含量进行测定,但是国标中对于高镉的样品未曾提出参考方案。因此,为准确测定出该类样品中的酸溶锌含量同时也避免采用原子吸收测镉含量,再减镉,计算出锌含量。本文讨论了通过加入适量碘化钾[2],以此来测定高镉次氧化锌烟尘中酸溶锌的含量。
1 试 验
1.1 仪器与试剂
1.1.1 主要试验设备与仪器
电子天平(北京赛多利斯制,精确至0.000 1 g);电热鼓风干燥箱(北京中兴伟业制,101-2AB);水浴恒温振荡器(上海博讯制,SHZ-B);原子吸收分光光度计(普析,TAS-990)。
1.1.2 主要试验试剂
1.盐酸(ρ=1.19 g/mL)。
2.硝酸(ρ=1.42 g/mL)。
3.硫酸(ρ=1.85 g/mL)。
4.氯化铵:AR。
5.氨水:(1+1)。
6.乙酸:AR。
7.乙酸钠:AR。
8.抗坏血酸:AR。
9.过氧化氢:AR。
10.氟化钾:50 g/L。
11.硫代硫酸钠:AR。
12.硫酸铁:330 g/L。
13.甲基橙指示剂:0.5 g/L。
14.二甲酚橙指示剂:5 g/L。
15.过硫酸胺:200 g/L,现配现用。
16.乙酸-乙酸钠缓冲溶液:pH=5.5。配制:120 g乙酸钠溶于水中,加入10 mL乙酸,用水稀释至1 000 mL,摇匀。
17.洗涤液:20 g氯化铵溶于1 000 mL水中,加入2~3 mL氨水混匀。
18.锌标准溶液:1 mg/mL、10 mg/mL。
19.镉标准溶液:10 mg/mL。
20.Na2EDTA标准溶液:0.02 mol/L。配制:称取乙二胺四乙酸二钠18.6 g,以水加热溶解,过滤,转移至1 000 mL容量瓶中,定容,摇匀,静置3 d后标定。
标定:移取10.00 mL含锌10 mg/mL的锌标准溶液于300 mL烧杯中,加入氯化铵3 g,加入1滴甲基橙溶液,用硫酸(1+1)和氨水(1+1)调节pH,到溶液中红色恰好消失,随后加入1滴二甲酚橙溶液,20 mL(HAc-NaAc)缓冲溶液,用Na2EDTA标准溶液滴定,溶液由紫红色变为亮黄色为终点。随同标定作空白试验。
按式(1)计算Na2EDTA标准滴定溶液的浓度:

式中:c为Na2EDTA标准滴定溶液的浓度,mol/mL;m1为移取锌标准溶液中锌质量,g;65.38为锌的摩尔质量,g/mol;V1为标定时消耗Na2EDTA标准滴定溶液的体积,mL;V0为标定时滴定空白试验溶液所消耗Na2EDTA标准滴定溶液的体积,mL。
平行标定3份,结果保留4位有效数字,其极差值不大于8×10-8mol/mL时,取其平均值。否则重新标定。
1.2 试验原料
试验所采用的材料是高镉次氧化锌烟尘,该烟尘中铅、镉、锌含量较高,分别为10.17%、6.39%、54.82%;铁、铋、锑含量为4.65%、0.75%、0.49%。稀硫酸酸溶,过滤可使铅、钡等共存元素分离,故后文中不再涉及铅、钡等元素的干扰。
1.3 试验研究方法
在恒温水浴锅中进行可溶锌浸出试验,水温设置到试验温度90℃[3]。称0.200 0 g样品于300 mL烧杯中,加入50 mL提前升温至90℃的硫酸浓度(80 g/L)。浸出时间为30 min。取下冷却至室温,采用慢速定量滤纸过滤。用硫酸(1+9)洗涤烧杯和沉淀各5次,再用超纯水洗涤烧杯和沉淀各1次。
在滤液中加入3~5 g氯化铵,5 mL过硫酸铵,用氨水中和至沉淀完全,再过量10 mL,加热微沸1~2 min,趁热用快速定性滤纸过滤,用热的洗涤液洗涤烧杯和沉淀各两次,滤液保留。
沉淀用热盐酸溶于原烧杯中,用热水洗净滤纸,加入5 mL过硫酸氨(200 g/L)溶液,用氨水中和至沉淀完全,再过量10 mL,加热微沸1~2 min,取下,经原滤纸过滤保留液的烧杯中,再用热的洗涤液洗涤烧杯和沉淀各3~4次[4]。
将滤液煮沸并浓缩至体积约为100 mL,彻底破坏过剩的过硫酸铵,取下冷却,加入8 mL盐酸酸化,溶液加0.1 g抗坏血酸,5 mL氟化铵,5 mL硫脲,摇匀加入两滴对硝基苯酚,用氨水调制黄色出现,用硫酸调pH,至黄色刚好消失滴加二甲酚橙指示剂,加入10~20 g碘化钾,加入20 mL乙酸-乙酸钠缓冲溶液。用Na2EDTA标准溶液滴定,滴定至紫红色变为亮黄色,为终点。并随同试样做空白试验。
2 浸出试验结果及讨论
2.1 浸出条件的选取
2.1.1 浸出液浓度影响
首先选取不同浓度的硫酸(6%、8%、10%)在90℃条件下浸出60 min,过滤后测得浸出液中锌和镉的含量。试验结果见表1,在硫酸浓度为8%时,浸出基本达到平衡,而镉的浸出持续升高。为降低硫酸浓度过高对后续分析结果的影响,接下来的研究均采用8%的硫酸作为浸出液。(下文中w(Zn)/%、w(Cd)/%均只浸出液中的锌、镉含量)。
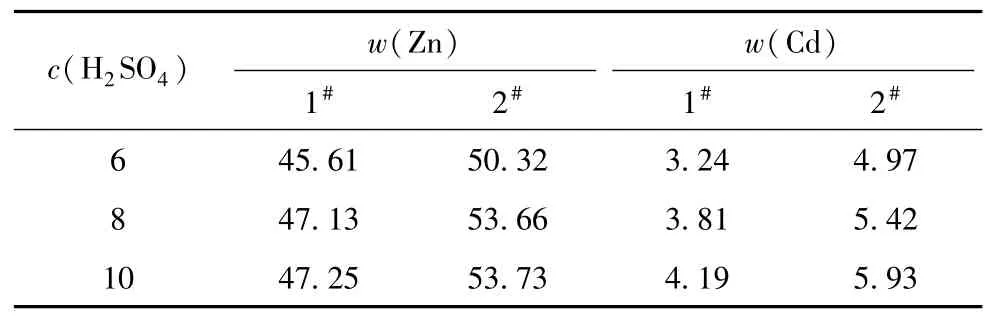
表1 硫酸浓度影响 %
2.1.2 浸出温度的影响
选取8%的硫酸继续在70℃、80℃、90℃条件下进行60 min的浸出试验。过滤后测得浸出液中锌和镉的含量。参照表2中条件下的试验结果显示,锌的浸出率随温度升高而明显提高,在80~90℃之间,基本达到平衡。但镉的浸出率,在80~90℃之间,出现下降的现象。试验结果见表2。镉浸出率降低,对于测定浸出液中锌含量形成有利条件,便于接下来锌含量的准确测定。
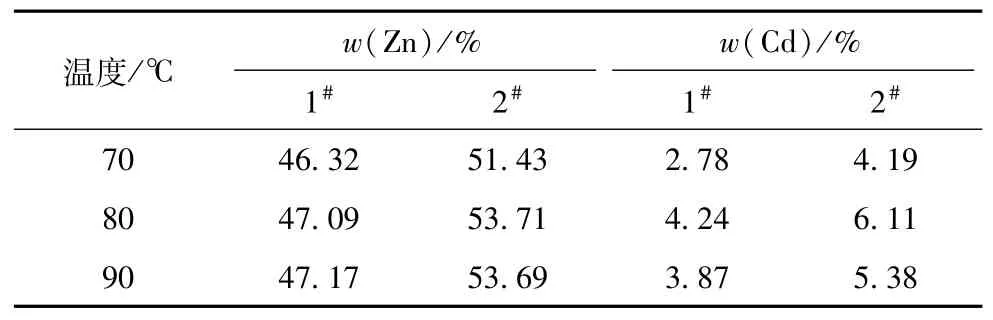
表2 浸出温度的影响
2.1.3 浸出时间的影响
通过表1和表2得出适合锌浸出的硫酸浓度为8%,浸出温度为90℃,因此,选择在8%的硫酸,温度为90℃条件下分别浸出15、30、60 min。试验结果见表3。在浸出30 min后,锌浸出率达到平衡。
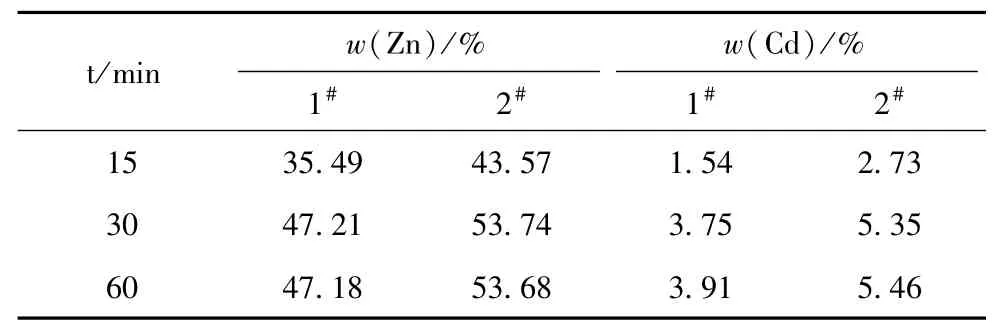
表3 浸出时间的影响
2.1.4 小结
对于该类次氧化锌烟尘可溶锌的最佳浸出条件是在硫酸浓度为8%,水浴温度为90℃条件下浸出30 min,即可最大程度实现对该类样品中锌的浸出。
2.2 浸出液中镉的影响及消除
在乙酸-乙酸钠缓冲溶液中,镉与过量的碘化钾在指示剂二甲酚橙的条件下,促进生成稳定的离子络合物,同时消除镉对锌滴定的影响,称取100 mg的金属锌,取最大量镉共存元素标准,按下表的步骤进行试验,测定结果见表4。
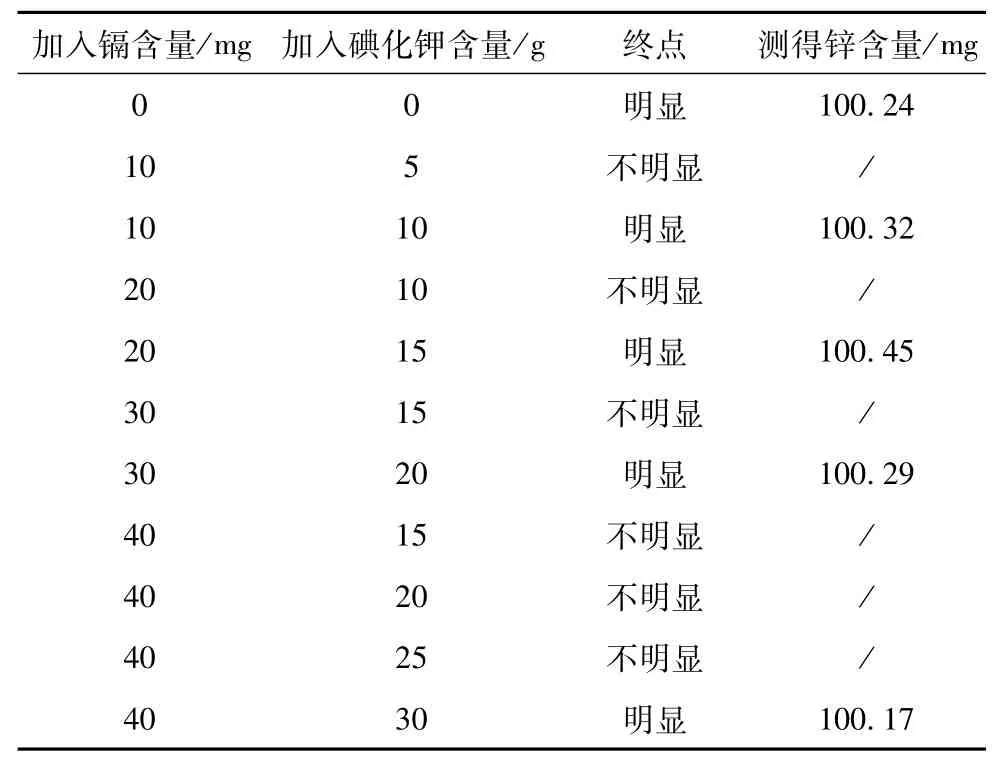
表4 碘化钾掩蔽镉测定锌
在高镉次氧化锌烟尘中,锌的滴定分析时,根据试样中的镉含量,加入适量的碘化钾,掩蔽镉元素对锌滴定的影响,滴定终点明显。表4的结果显示,镉含量越高所需加入的碘化钾也就越多,碘化钾的加入量与对镉的掩蔽之间没有明显的比例关系,当镉含量偏高时,可以逐步加入碘化钾,使其能达到较好的掩蔽效果,在观察溶液中紫黑色完全转化为紫红色时,则是碘化钾加入量最合适,也是掩蔽效果最佳时,继续滴定,终点明显。测得锌量与加入锌量结果在误差允许范围内。
2.3 加标试验
按照前文所述方法对样品1#、2#进行加标回收试验,结果见表5。表5结果显示,样品的加标回收率在100.4%~101.3%之间,稳定性较高,方法可行性良好。
2.4 重复性及再现性
为验证该方法的可行性,选取2个高镉次氧化锌烟尘按照本文中方法测定酸溶锌含量,结果见表6。
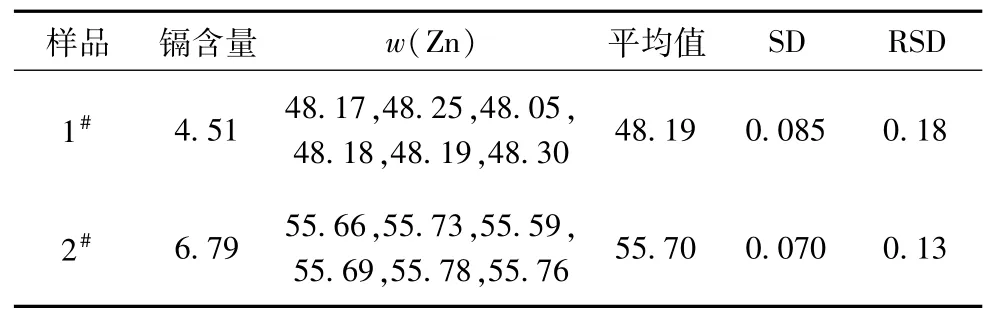
表6 重复性及再现性试验 %
由表6重复性及再现性试验可知,标准偏差小于1%,结果精密度较高,该方法可以应用于高镉次氧化锌烟尘中酸溶锌的测定。
3 结 论
该方法利用8%的硫酸溶液在90℃的恒温水浴锅中浸出酸溶锌,再通过加入适量碘化钾掩蔽溶液中与锌一同浸出的镉,达到测定样品中酸溶锌的目的。研究显示,该方法对于这类高镉次氧化锌烟尘中酸溶锌的测定,结果可靠。
