以弥漫性肺泡出血为首发症状的幼年特发性关节炎1例报告并文献复习
2022-10-27肖景玉林发全
肖景玉 林发全
1 广西医科大学,广西南宁市 530021; 2 广西医科大学第一附属医院检验科
幼年特发性关节炎(Juvenile idiopathic arthritis, JIA)是儿童时期常见的风湿性疾病,可导致关节损伤、慢性疼痛和畸形,部分患儿还可伴发热、皮疹、肝脾肿大、心包炎和肺部病变等关节外表现[1]。本文回顾性分析1例以弥漫性肺泡出血(Diffuse alveolar hemorrhage, DAH)为首发症状的JIA患儿的临床症状和诊治经过,并结合相关文献进行复习,探讨该疾病的临床特征和诊治原则,为儿童DAH提供诊治思路。
1 病例资料
1.1 一般资料 患儿男,5岁,2019年8月因“活动耐力下降2年,口唇紫绀2个月,发热1个月余”收入我院。患儿2年前无诱因出现活动耐力下降,快步或上楼时出现气促、乏力、面色苍白,无胸痛、喘息。2个月前开始出现口唇、手指、足趾紫绀,1个月前症状加重,伴发热、咳嗽、咳痰,热峰39℃,曾于当地医院诊断为“重症肺炎、Ⅰ型呼吸衰竭”,经抗感染、吸氧等治疗后症状好转,但仍有间断发热,血氧偏低。既往史:2015—2017年间有反复贫血史(Hb最低60g/L),骨髓细胞形态学检查提示骨髓增生明显活跃(增生性贫血骨髓象),G-6-PD正常,地中海贫血基因分析未见异常,Coombs试验阴性;予输注红细胞、补充铁剂后血红蛋白维持在正常水平。否认哮喘发作史。父母体健,无类似家族病史。
1.2 体格检查 体温36.6℃,脉搏116次/min,呼吸34次/min,身高100cm,体质量13kg。神志清楚,口唇紫绀,吸凹征(+),双肺呼吸音粗,未闻及干湿性啰音,心律齐,心脏各瓣膜区无杂音,腹软,肝、脾肋下未触及,手指、足趾紫绀,见杵状指(趾),双下肢无水肿。
1.3 辅助检查 入院查血常规:WBC 11.50×109/L,RBC 4.67×1012/L,Hb 133.00g/L,PLT 482×109/L;ESR 66mm/h;血气分析:动脉血氧分压(PaO2)46.0mmHg(1mmHg=0.133kPa),二氧化碳分压(PaCO2)29.8mmHg,碳酸氢根(HCO3-)浓度19.2mmol/L;肺炎支原体(MP)抗体(IgM)定量1∶320;RF 17.31IU/ml(参考范围0.00~12.5IU/ml);抗CCP抗体68.60U/ml(参考范围0.00~5U/ml);抗核抗体弱阳性,其余抗dsDNA抗体、抗中性粒细胞胞浆抗体(ANCA)、抗肾小球基底膜(GBM)抗体、抗磷脂抗体等均为阴性;肝肾功能、凝血功能正常;全外显子基因检测无异常。心脏B超示心脏形态结构及血流无异常。胸部CT示两肺透亮度减低,两肺叶呈弥漫磨玻璃影(见图1a)。肺功能提示轻—中度阻塞性病变,呼出气一氧化氮在正常范围。支气管镜检查:气管、隆突未见异常,肺泡灌洗液呈血红色。肺泡灌洗液检查:见大量含铁血黄素巨噬细胞,细菌涂片和培养、巨细胞病毒检测、EB病毒检测、G实验、GM实验、特殊染色(Ag、PAS、抗酸染色)未见异常。肺组织病理提示肺泡腔内见大量含铁血黄素巨噬细胞,肺泡间隔轻度纤维增生,伴淋巴细胞及浆细胞浸润。
1.4 诊治经过 入院予甲强龙冲击、阿奇霉素抗感染、改善氧合等治疗,患儿气促症状改善,经皮血氧饱和度维持在92%~95%,出院后以口服泼尼松[0.7mg/(kg·d)×14kg]维持治疗。2019年10月复查胸部CT,肺部病变较前增多(见图1b),考虑病情控制不佳,予激素联合免疫抑制剂(羟氯喹片)治疗,并逐渐减少口服激素剂量。2019年11月—2020年3月间,患儿3次返院治疗,住院期间以甲强龙脉冲治疗后气促、口唇紫绀情况明显改善。出院后患儿病情易反复,其胸部CT提示两肺病变逐渐增多(见图1c、d)。自2019年上半年来,患儿间断出现阵发性双膝关节疼痛,2019年11月住院期间复查RF 32.2IU/ml,抗CCP抗体183.10U/ml,膝关节MRI检查提示双膝关节积液。结合患儿以往多次查RF、抗CCP抗体结果,诊断为JIA合并DAH,予加用甲氨蝶呤治疗。2020年3月再次复查RF 57.0IU/ml,抗CCP抗体141.90 U/ml,膝关节积液消失,自行停用甲氨蝶呤。2020年4月患儿因气促加重,伴咳嗽、咳少量血丝痰,进入他院治疗;期间患儿出现肺部严重感染,最终于入院第16日因出现急性肺泡大出血和呼吸衰竭,经抢救无效死亡。
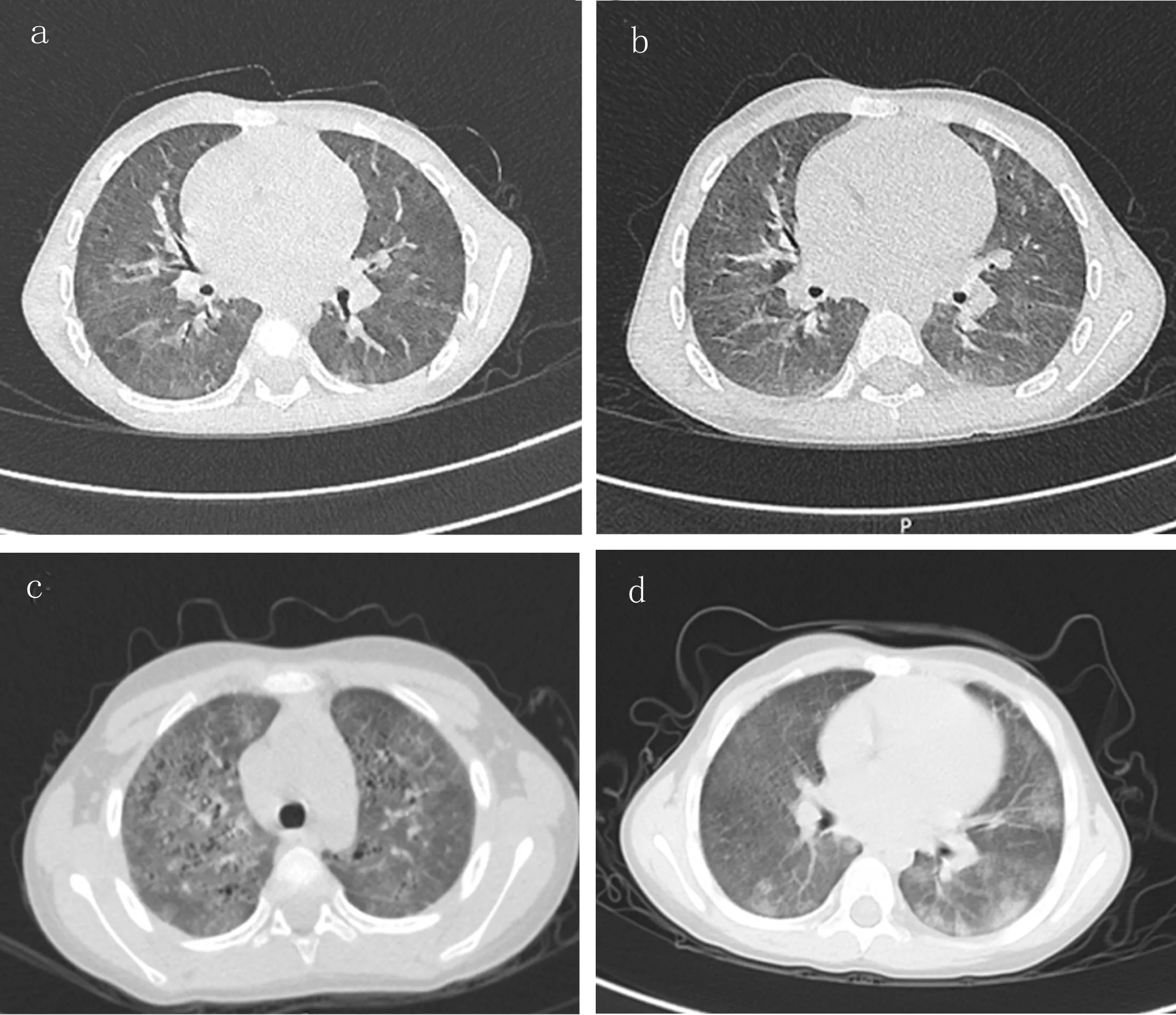
图1 以弥漫性肺泡出血为首发症状的幼年特发性关节炎患儿胸部CT表现
2 讨论
JIA是一组原因不明且具有高度异质性的慢性风湿性疾病,除了外周关节炎外,还可伴眼、心血管和肺等全身器官的损害。合并肺胸膜受累时,以胸腔积液/胸膜炎、间质性肺炎发生率最高[2]。DAH是一种多病因导致肺泡—毛细血管基底膜受损,从而引起肺泡内广泛出血的临床综合征。作为一种罕见的肺部并发症,DAH在成人类风湿性关节炎(RA)中已有案例报道[3],而JIA并发DAH的情况较为罕见。
查阅文献,在中国全文期刊数据库和万方数据库以“幼年特发性关节炎”和“弥漫性肺泡出血”为关键词,在Pubmed数据库、Web of science数据库和Springer link数据库以“juvenile idiopathic arthritis”AND“diffuse alveolar hemorrhage”为关键词,自建库至2021年10月1日进行检索,筛选出相关案例报道共2篇。Watanabe等[4]2012年报道了1例男性患者,幼年时被诊断为JIA,在33岁时发生了继发于肺毛细血管炎的肺泡出血的案例;Gubichuk等[5]2020年报道了1例JIA合并机化性肺炎(Organizing Pneumonia,OP)的8岁女孩,经支气管镜检查后,诊断为并发DAH的病例。
DAH病因复杂,尽早查明病因对患者的治疗和预后具有重要意义。临床上,儿童肺泡出血常见的病因包括特发性肺含铁血黄素沉着症、免疫相关性疾病、凝血功能障碍、感染等[6-7]。本例患儿入院后查血常规、肝功能、凝血功能及心脏超声均无异常;自身抗体除RF、抗CCP抗体阳性,其余抗dsDNA抗体、ANCA、抗GBM抗体等均为阴性,且患儿无血尿、蛋白尿等表现,排除系统性红斑狼疮、ANCA相关性血管炎、肺出血—肾炎综合征等疾病;肺部感染(如巨细胞病毒、腺病毒、侵袭性曲霉菌病、支原体、军团菌腺病毒等)也可引起DAH[8],本病例患儿多次行肺泡灌洗液病原学检查,结果均为阴性,排除了肺部感染继发的肺泡出血。直至2019年11月患儿出现膝关节疼痛,膝关节MRI提示关节积液,结合多次查RF和抗CCP抗体的结果变化,诊断为JIA合并DAH。
DAH症状不一,主要以咯血、贫血、呼吸困难、低氧血症和肺部弥漫性浸润为临床特征。咯血是最有意义的症状,约1/2的患儿表现出咯血[6]。长期慢性肺泡出血时,患儿还可表现为缺铁性贫血。部分患儿可能无明显咯血,仅表现为贫血、咳嗽和运动不耐受[9],易与贫血性疾病混淆。胸部X线或高分辨CT可呈弥漫性玻璃影、斑片影等;长期肺泡内出血还可导致肺间质纤维化,CT有局部肺泡间隔增厚、网格状、蜂窝状等改变,多提示不良预后。本例患儿自2015年开始反复出现原因不明的贫血,并逐渐出现活动后气促等症状,肺组织病理提示肺间隔纤维增生,符合长期肺泡出血的表现。诊断DAH主要依靠支气管镜检查,肺泡灌洗连续回收血性液体、肺泡灌洗液中发现≥20%含铁血黄素巨噬细胞有助于确诊;对于病因不明病例可行肺组织活检进一步诊断[6,10]。
DAH急性期病情重,死亡率达23.2%[7],一经确诊必须立即采取治疗措施。目前,DAH以经验性治疗为主,针对自身免疫性疾病引起的DAH,治疗方法包括使用不同剂量的糖皮质激素、免疫抑制剂(如环磷酰胺、硫唑嘌呤、甲氨蝶呤、羟氯喹)、血浆置换、静脉注射免疫球蛋白(IVIG)等;当严重的DAH导致呼吸衰竭时,还需机械通气以改善氧合[7,9-10]。Watanabe报道的案例中,患者经IVIG、甲基泼尼松龙及环磷酰胺脉冲治疗后,肺泡出血得到了良好地控制[4];Gubichuk报道的患儿经激素脉冲治疗、IVIG、利妥昔单抗治疗后病情也得到改善[5]。本文患儿经激素脉冲治疗后病情一度缓解,但肺部病变仍不断进展,可能与激素依赖及病程迁延有关。另外,长期使用激素治疗的患儿有继发感染的风险,临床医师需密切关注患儿病情变化,并及时调整用药方案。
综上所述,JIA在病情发展中可伴发肺部损害,DAH作为其罕见的肺部并发症,一旦进行性发展,病情往往较重,急性期死亡率高,早期诊治是提高患儿生存率和改善预后的关键。
