新型2-烷氧基取代苯甲酸香叶酯类蚜虫报警信息素类似物的设计、合成及生物活性
2022-10-25秦耀果杨朝凯张以涵周雨蓓潘世香杨新玲
秦耀果, 杨朝凯, 张以涵, 周雨蓓, 潘世香,刘 彦, 石 卓, 杨新玲*,
(1. 中国农业大学 理学院 农药创新研究中心,北京 100193;2. 中国农业大学 植物保护学院 昆虫学系,北京 100193)
蚜虫是一种广泛分布的农林害虫,具有一年多世代、繁殖迅速、种类众多以及易产生抗药性等特点,对农作物的危害十分严重[1-3]。作为刺吸式口器害虫,蚜虫主要通过直接刺吸韧皮部汁液、分泌蜜露诱发烟煤病和传播植物病毒3 种方式为害农作物。目前蚜虫的防治主要依靠传统杀虫剂,但随着蚜虫抗药性的产生,杀虫剂的用量持续增加,不仅造成环境污染,而且部分杀虫剂对人畜、天敌、蜜蜂等非靶标生物也存在一定毒性,从而引起全世界的高度关注[4-6],这严重限制了传统杀虫剂在蚜虫防治上的应用。因此,开发环境友好的新型蚜虫控制剂刻不容缓。以生态友好为前提,利用蚜虫自身分泌的具有行为调控功能的信息素已经成为蚜虫防治的重要策略[7]。
蚜虫在受到外界干扰时会从腹管分泌出油状液滴,这种液滴含有蚜虫报警信息素,其主要成分为(E)-β-farnesene (图式1),简称EβF[8-9]。EβF能对同种其他个体产生报警反应,使蚜虫逃离现场,停止侵害作物[10]。此外,EβF 还具有调控有翅蚜比例、高剂量毒杀、杀虫剂增效作用[11-14],以及吸引天敌等多重生物活性[15]。由于EβF 分子结构中存在不稳定的共轭双键,使其易挥发、易氧化,极大地限制了其在蚜虫防治中的实际应用。因此,研究人员对EβF 的结构进行了修饰和改造[16-26],以期发现活性与稳定性兼备的 EβF 类似物。

图式1 (E)-β-farnesene 的结构Scheme 1 The structure of (E)-β-farnesene
本课题组在EβF 的结构改造和生物活性研究方面做了多年工作。前期通过引入吡唑环、吡啶环、噻唑环、三嗪环、水杨酸结构等基团,获得大量EβF 类似物,部分类似物不仅对蚜虫具有较好的驱避活性, 而且稳定性比EβF 有很大提高[2,22-26],尤其是引入水杨酸结构的EβF 类似物,还表现出强烈的与靶标气味结合蛋白OBPs 结合的活性。例如,水杨酸酯类EβF 类似物3e(2-羟基-3-甲氧基苯甲酸香叶酯),不仅对桃蚜和豌豆蚜Acyrthosiphon pisum显示出较高的驱避活性,而且有很好的稳定性,可与豌豆蚜气味结合蛋白ApisOBP3、ApisOBP7及ApisOBP9 强烈结合,尤其是与ApisOBP9 的结合最为明显[25]。有文献报道,含烷氧基的化合物具有杀虫、杀菌等生物活性[27-28],为发现结构新颖、对蚜虫有效的新型EβF 类似物,本研究以3e为先导,用不同取代的烷氧基替换3e中邻位的羟基,设计合成了一系列含烷氧基的EβF 类似物(图式2 和图式3),并测试了目标化合物对蚜虫的驱避活性及其与靶标ApisOBP9 蛋白的结合活性,最后利用分子对接技术研究了代表性化合物6i与ApisOBP9 的结合模式,以其为进一步设计蚜虫行为控制剂提供理论基础。

图式2 目标化合物的设计策略Scheme 2 Design strategy of the target compounds
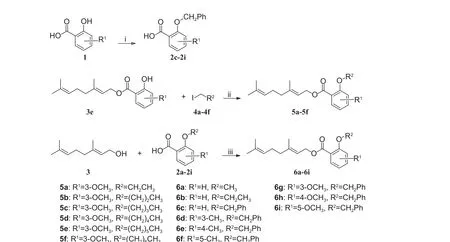
图式3 目标化合物的合成路线Scheme 3 Synthetic routes of the target compounds
1 实验部分
1.1 仪器与供试材料
Bruker DPX 300 或 Ascend 500 MHz 核磁共振仪 (以 DMSO-d6或CDCl3为溶剂,TMS 为内标)(德国Bruker 公司);FTICR-MS 7.0 质谱仪 (美国瓦里安公司);PerkinElmer Spectrum 100 傅立叶变换红外光谱仪 (美国PerkinElmer 公司); X-5 型数字显示显微熔点测试仪 (北京富凯仪器有限公司);T 型行为嗅觉仪 (即双向T 型嗅觉仪,由玻璃制成,横臂长20 cm,内径1.5 cm,横臂中心处与一竖直管相通,竖直管起释放蚜虫及出气口作用,横臂内置滤纸片,方便蚜虫爬行。北京广达恒益科技有限公司);F-380 型荧光分光光度计 (天津港东科技股份有限公司)。柱层析硅胶 (200~300 目,筛孔径75~48 μm) 和薄层层析硅胶板,青岛海洋化工厂;先导化合物3e (本课题组自制[25]);对照药剂95% EβF (美国Sigma-Aldrich 公司);中间体2-甲氧基苯甲酸 (2a) 和2-乙氧基苯甲酸 (2b) (北京偶合科技有限公司);其余试剂均为市售化学纯或分析纯,除特别注明外,所用溶剂未经无水处理。豌豆蚜Acyrthosiphon pisum由中国农业科学院植物保护研究所提供。
1.2 化合物的合成
1.2.1 2-苄氧基取代苯甲酸 (2c~2i) 的合成 中间体2-甲氧基苯甲酸 (2a) 和2-乙氧基苯甲酸 (2b) 为购买所得。中间体2-苄氧基取代苯甲酸 (2c~2i) 参考文献方法[29]合成。在200 mL 三口瓶中,加入取代水杨酸 (1,100.0 mmol)、相转移催化剂四丁基溴化铵 (TBAB) 3.2 g (10.0 mmol)、50 mL 二氯甲烷和50 mL 水,冰浴下滴加溴化苄 (300.0 mmol),在常温下反应5 h。用二氯甲烷萃取,无水硫酸钠干燥,减压浓缩,硅胶柱层析分离 (V(石油醚) :V(乙酸乙酯) = 10: 1) 除去多余的溴化苄。将分离后的产物投入100 mL 三口瓶中,加入氢氧化钠12.0 g (300.0 mmol)和50 mL 乙醇,回流4 h。减压脱溶,用水溶解所得白色固体,滴加6 mol/L 的盐酸溶液至pH = 4.0。过滤,滤饼用乙醇润洗,干燥得中间体2c~2i。
1.2.2 目标化合物5a~5f 的合成 参考文献方法[30]进行。0 ℃下,向50 mL 三口瓶中加入先导化合物3e (6.6 mmol)、叔丁醇钾(t-BuOK,9.9 mmol)和20 mL 无水四氢呋喃 (THF),将中间体4 (33.0 mmol) 用10 mLN,N-二甲基甲酰胺 (DMF) 溶解后滴加至上述反应液后反应0.5 h,随后在常温下反应4 h。反应液用1 mol/L 的盐酸调节pH 至中性,用饱和氯化钠萃取,无水硫酸钠干燥,过滤,减压脱溶,硅胶柱层析 (V(石油醚) :V(乙酸乙酯) = 80 : 1) 分离纯化,得到目标化合物5a~5f。
1.2.3 目标化合物6a~6i 的合成 参考文献方法[25-26]进行。在100 mL 三口瓶中,加入香叶醇(10.0 mmol)、2-烷氧基取代苯甲酸(10.0 mmol)、二环己基碳二亚胺 (DCC) 2.3 g (11.0 mmol) 和40 mL无水THF,0 ℃下将4-二甲氨基吡啶 (DMAP) 0.1 g(1.0 mmol)用10 mL 无水THF 溶解后滴加至上述反应液反应0.5 h,然后常温下反应8 h。用二氯甲烷萃取,无水硫酸钠干燥,过滤,减压脱溶,硅胶柱层析 (V(石油醚) :V(乙酸乙酯) = 100 : 1) 分离纯化,得到目标化合物6a~6i。
1.3 蚜虫驱避活性测试
采用 T 型行为嗅觉仪测定目标化合物对豌豆蚜A.pisum的驱避活性,测定方法及剂量参照文献方法[22]进行。由释放口释放 20 头豌豆蚜无翅成蚜, 每臂经抽气泵通入经活性炭及蒸馏水的持续气流。嗅觉仪的两臂分别放置 5 μg 样品 (气味源) 和等体积的溶剂,记录导入样品 15 min 时蚜虫在各臂的数目[31]。按 (1) 式计算驱避率RP。

其中RP为驱避率(repellent proportion),C为对照组虫数,T为处理组虫数。
利用SPSS 软件 (IBM 公司) 对化合物的驱避率进行单因素方差分析,并在α= 0.05 的水平上使用Tukey B 检验进行显著性差异分析。
1.4 ApisOBP 蛋白结合实验
参照文献方法[25-26],利用大肠杆菌原核表达系统表达出靶标蛋白ApisOBP9,并经过离子交换层析对重组蛋白纯化。蛋白竞争结合实验所用容器为1 cm 宽的石英杯,缝宽为10 nm。设定激发光波长为337 nm,扫描的发射光波长范围为390~500 nm。向荧光比色皿中加入1 mL 浓度为50 mmol/L 的Tri-HCl 缓冲液(pH=8.0),使ApisOBP9的终浓度为2 μmol/L,选择N-苯基-1-萘胺 (1-NPN) 为荧光探针,陆续向比色皿中加入溶于甲醇的1 mmol/L 荧光探针1-NPN,使加入的1-NPN浓度从2 μmol/L 递增到20 μmol/L,每加入一次1-NPN 就记录该浓度下的最大荧光强度值,利用Scatchard 方程计算ApisOBP9 和1-NPN 的结合常数。用荧光竞争的方法测试化合物与蛋白ApisOBP9的结合能力:在荧光比色皿中加入1 mL 50 mmol/L的Tri-HCl 缓冲液(pH=8.0),然后加入ApisOBP9和荧光探针1-NPN,终浓度均为2 μmol/L,记录最大荧光强度值。随后将溶于甲醇的1 mmol/L 化合物逐次加入到荧光比色皿中,使加入的化合物浓度从2 μmol/L 递增到20 μmol/L,记录各梯度浓度下的最大荧光强度值。每次试验重复3 次。根据IC50值(ApisOBP/1-NPN 复合物的荧光强度值下降一半时配体的浓度),按 (2) 式计算目标物和ApisOBP9 的解离常数(Kd)。

其中[1-NPN] 为未结合的1-NPN 的浓度,K1-NPN为ApisOBP/1-NPN 复合物的结合常数。
1.5 化合物与ApisOBP9 的分子对接研究
由于ApisOBP9 的氨基酸与PDB 蛋白数据库中的蛋白晶体模板序列同源性都低于30%,为了获得更好的模型,使用一种快速准确的蛋白质结构预测算法 (名称为trRosetta,https://yanglab.nankai.edu.cn/trRosetta)[32]对ApisOBP 9 的结构进行建模,最终的3D 模型在在线结构分析和验证服务器上使用多种方法进行评估(http://services.mbi.ucla.edu/SAVES/)。采用Sybyl 7.3 软件包中的Surflex Dock 算法进行配体和ApisOBP9 之间的分子对接研究,使用AMBER MMFF94 力场和电荷对化合物进行构建和优化,选择代表性化合物的低能构象作为初始对接构象。配体分子保留30 个对接构象,保留得分最低的构象以进一步探究配体与蛋白质的相互作用。
2 结果与分析
2.1 化合物合成
中间体2-苄氧基取代苯甲酸 (2c~2i) 由取代-水杨酸与溴化苄发生亲核取代反应的产物经皂化反应得到。目标化合物5a~5f 由先导化合物3e 与碘代烷发生烷基化反应制得,3e 的合成参考文献方法[25],由香叶醇与3-甲氧基水杨酸经亲核取代反应得到。目标化合物6a~6i 则以香叶醇 (3) 为起始原料,与相应的2-烷氧基苯甲酸 (2a~2i) 发生亲核取代反应制得。目标化合物的结构表征数据如下。
2-乙基-3-甲氧基苯甲酸香叶酯 (5a):无色液体, 产率73.3%.1H NMR (500 MHz, DMSO-d6),δ: 7.22 (dd,J= 7.4,2.4 Hz, 1H, ArH), 7.16~7.10 (m, 2H, ArH), 5.41 (td,J= 7.1,1.0 Hz, 1H, C=CH), 5.13~4.96 (m, 1H, C=CH), 4.75 (d,J=7.1 Hz, 2H, O=COCH2), 3.98 (q,J=7.0 Hz, 2H, ArOCH2),3.81 (d,J=7.4 Hz, 3H, ArOCH3), 2.13~1.99 (m, 4H,CCH2CH2), 1.72 (s, 3H, CH3), 1.62 (s, 3H, CH3), 1.56 (s, 3H,CH3), 1.26 (t,J= 7.0 Hz, 3H, CH3). IR (KBr),ν/cm-1: 2 974, 2 931,1 726, 1 581, 1 475, 1 383, 1 309, 1 261, 1 147, 1057. HRMS(ESI):C20H28O4[M + Na]+,测量值355.188 6, 计算值355.188 0。
2-丙基-3-甲氧基苯甲酸香叶酯 (5b):无色液体, 产率68.5%.1H NMR (500 MHz, DMSO-d6),δ: 7.21 (dd,J= 7.5,2.1 Hz, 1H, ArH), 7.16~7.09 (m, 2H, ArH), 5.40 (t,J= 6.9 Hz,1H, C=CH), 5.07 (t,J= 6.6 Hz, 1H, C=CH), 4.75 (d,J= 7.1 Hz, 2H, O=COCH2), 3.88 (t,J= 6.7 Hz, 2H, ArOCH2), 3.81(s, 3H, ArOCH3), 2.05 (dt,J= 21.0, 6.7 Hz, 4H, CCH2CH2),1.71 (s, 3H, CH3), 1.68 (dd,J= 14.2, 7.1 Hz, 2H, CH2), 1.62(s, 3H, CH3), 1.56 (s, 3H, CH3), 0.94 (t,J= 7.4 Hz, 3H, CH3).IR (KBr),ν/cm-1: 2 964, 2 933, 2 881, 1 726, 1 670, 1 581, 1 473, 1 382,1 309, 1 261, 1 147, 1058. HRMS(ESI):C21H30O4[M +Na]+,测量值369.203 2, 计算值369.203 6。
2-正丁基-3-甲氧基苯甲酸香叶酯 (5c):无色液体, 产率60.4%.1H NMR (500 MHz, DMSO-d6),δ: 7.21 (dd,J=7.6, 2.2 Hz, 1H, ArH), 7.16~7.08 (m, 2H, ArH), 5.40 (td,J=7.1, 1.0 Hz, 1H, C=CH), 5.14~5.00 (m, 1H, C=CH), 4.74 (d,J= 7.1 Hz, 2H, O=COCH2), 3.92 (t,J= 6.6 Hz, 2H, ArOCH2),3.80 (d,J= 4.1 Hz, 3H, ArOCH3), 2.05 (tt,J= 13.7, 7.0 Hz,4H, CCH2CH2), 1.71 (s, 3H, CH3), 1.67~1.60 (m, 5H, CH2,CH3), 1.55 (s, 3H, CH3), 1.45~1.36 (m, 2H, CH2), 0.91 (t,J=7.4 Hz, 3H, CH3). IR (KBr),ν/cm-1: 2 959, 2 933, 1 726, 1 581, 1 477,1 381, 1 310, 1 262, 1 147, 1058. HRMS(ESI):C22H32O4[M +Na]+,测量值383.218 4, 计算值383.219 3。
2-正戊基-3-甲氧基苯甲酸香叶酯 (5d):无色液体, 产率57.7%.1H NMR (500 MHz, DMSO-d6),δ: 7.21 (dd,J=7.5, 2.0 Hz, 1H, ArH), 7.15~7.08 (m, 2H, ArH), 5.40 (t,J= 7.0 Hz, 1H, C=CH), 5.07 (t,J= 6.6 Hz, 1H, C=CH), 4.74 (d,J=7.1 Hz, 2H, O=COCH2), 3.91 (t,J= 6.6 Hz, 2H, ArOCH2),3.81 (s, 3H, ArOCH3), 2.12~1.98 (m, 4H, CCH2CH2), 1.71 (s,3H, CH3), 1.69~1.64 (m, 2H, CH2, CH2), 1.62 (s, 3H, CH3),1.55 (s, 3H, CH3), 1.41~1.26 (m, 4H, CH2, CH2), 0.88 (t,J=7.0 Hz, 3H, CH3). IR (KBr),ν/cm-1: 2 933, 1 727, 1 581, 1 474, 1 381,1 310, 1 262, 1 232, 1 147, 1057. HRMS(ESI):C23H34O4[M +H]+,测量值375.252 5, 计算值375.253 0。
2-正己基-3-甲氧基苯甲酸香叶酯 (5e):浅黄色液体, 产率53.2%.1H NMR (500 MHz, DMSO-d6),δ: 7.30 (dd,J=7.4, 1.8 Hz, 1H, ArH), 7.08~6.99 (m, 2H, ArH, ArH), 5.46 (t,J= 6.9 Hz, 1H, C=CH), 5.09 (t,J= 6.6 Hz, 1H, C=CH), 4.82 (d,J= 7.1 Hz, 2H, O=COCH2), 4.00 (t,J= 6.9 Hz, 2H, ArOCH2),3.85 (s, 3H, ArOCH3), 2.16~2.03 (m, 4H, CCH2CH2), 1.79(dd,J= 14.6, 7.3 Hz, 2H, CH2), 1.75 (s, 3H, CH3), 1.68 (s, 3H,CH3), 1.60 (s, 3H, CH3), 1.49~1.39 (m, 2H, CH2), 1.33 (dd,J=8.7, 5.4 Hz, 4H, CH2, CH2), 0.90 (t,J= 6.7 Hz, 3H, CH3). IR(KBr),ν/cm-1: 2 930, 2 858, 1 727, 1 581, 1 474, 1 381, 1 310, 1 261,1 147, 1058. HRMS(ESI):C24H36O4[M + Na]+,测量值411.250 1,计算值411.250 6。
2-正庚基-3-甲氧基苯甲酸香叶酯 (5f):浅黄色液体, 产率42.4%.1H NMR (500 MHz, DMSO-d6),δ: 7.21 (dd,J=6.9, 2.9 Hz, 1H, ArH), 7.16~7.08 (m, 2H, ArH), 5.39 (dd,J=7.1, 6.1 Hz, 1H, C=CH), 5.07 (dd,J= 9.5, 3.9 Hz, 1H, C=CH),4.74 (d,J= 7.1 Hz, 2H, O=COCH2), 3.90 (t,J= 6.6 Hz, 2H,ArOCH2), 3.81 (s, 3H, ArOCH3), 2.12~2.00 (m, 4H,CCH2CH2), 1.71 (s, 3H, CH3), 1.68~1.61 (m, 5H, CH3, CH2),1.56 (s, 3H, CH3), 1.39~1.24 (m, 8H, CH2, CH2, CH2, CH2),0.86 (t,J= 6.9 Hz, 3H, CH3). IR (KBr),ν/cm-1: 2 927, 2 856, 1 727,1 581, 1 474, 1 381, 1 310, 1 261, 1 146, 1058. HRMS(ESI):C25H38O4[M + H]+,测量值403.284 3, 计算值403.284 3。
2-甲氧基苯甲酸香叶酯 (6a):浅黄色液体, 产率67.0%.1H NMR (300 MHz, CDCl3),δ: 7.77~7.80 (m, 1H, ArH),7.42~7.48 (m, 1H, ArH), 6.94~6.99 (m, 2H, ArH), 5.44~5.49(m, 1H, =CH), 5.08~5.12 (m, 1H, =CH), 4.82 (d, 2H,J= 7.06 Hz, CH2), 3.90 (s, 3H, ArOCH3), 2.05~2.13 (m, 4H, CH2CH2),1.76 (s, 3H, CH3), 1.68 (s, 3H, CH3), 1.60 (s, 3H, CH3). IR(KBr),ν/cm-1: 2 966, 2 923, 2 855, 1 377, 1 601, 1 583, 1 491, 1 463,1 727, 1250. HRMS(ESI):C18H25O3[M + H]+,测量值289.179 86,计算值289.179 82。
2-乙氧基苯甲酸香叶酯 (6b):浅黄色液体, 产率78.0%.1H NMR (300 MHz, CDCl3),δ: 7.75~7.78 (m, 1H, ArH),7.39~7.44 (m, 1H, ArH), 6.93~6.97 (m, 2H, ArH), 5.45~5.50(m, 1H, =CH), 5.08~5.10 (m, 1H, =CH), 4.82 (d, 2H,J= 7.02 Hz, CH2), 4.11 (q, 2H, ArOCH2CH3), 2.03~2.17(m, 4H,CH2CH2), 1.76 (s, 3H, CH3), 1.6 8(s, 3H, CH3), 1.60 (s, 3H,CH3), 1.45 (t, 3H,J= 6.18 Hz, ArOCH2CH3). IR (KBr),ν/cm-1:2 980, 2 926, 1 384, 1 601, 1 582, 1 492, 1 453, 1 728, 1248.HRMS(ESI):C19H26O3Na [M + Na]+,测量值325.177 40,计算值325.177 42。
2-苄基-3-甲基苯甲酸香叶酯 (6d):黄色液体, 产率41.7%.1H NMR (300 MHz, CDCl3),δ: 7.66~7.69 (m, 1H,ArH), 7.47~7.50 (m, 2H, ArH), 7.33~7.41 (m, 4H, ArH), 7.07(t, 1H,J= 15.31 Hz, ArH), 5.39~5.44 (m, 1H, =CH),5.07~5.09 (m, 1H, =CH), 4.96 (s, 2H, CH2), 4.81 (d, 2H,J=7.12 Hz, CH2), 2.31 (s, 3H, ArCH3), 2.02~2.09 (m, 4H,CH2CH2), 1.70 (s, 3H, CH3), 1.64 (s, 3H, CH3), 1.59 (s, 3H,CH3). IR (KBr),ν/cm-1: 2 966, 2 923, 1 376, 1 593, 1 497, 1 454, 3 030,1 724, 1286. HRMS(ESI):C25H31O3[M + H]+,测量值379.226 32,计算值379.226 77。
2-苄基-4-甲基苯甲酸香叶酯 (6e):黄色液体, 产率70.1%.1H NMR (300 MHz, CDCl3),δ: 7.75 (d, 1H,J= 7.77 Hz, ArH), 7.24~7.52 (m, 5H, ArH), 6.78~6.82 (m, 2H, ArH),5.41~5.47 (m, 1H, =CH), 5.15 (s, 2H, CH2), 5.07~5.11 (m, 1H,=CH), 4.82 (d, 2H,J= 7.02 Hz, CH2), 2.35 (s, 3H, ArCH3),2.02~2.11 (m, 4H, CH2CH2), 1.73 (s, 3H, CH3), 1.67 (s, 3H,CH3), 1.59 (s, 3H, CH3). IR (KBr),ν/cm-1: 2 966, 2 924, 2 856,1 384, 1 623, 1 579, 1 504, 1 452, 1 672, 1250. HRMS(ESI):C25H31O3[M + H]+,测量值379.226 41, 计算值379.226 77。
2-苄基-5-甲基苯甲酸香叶酯 (6f):黄色液体, 产率44.4%.1H NMR (300 MHz, CDCl3),δ: 7.62 (d, 1H, J = 2.19 Hz, ArH), 7.46~7.49 (m, 2H, ArH), 7.17~7.38 (m, 4H, ArH),6.88 (d, 1H,J= 8.46 Hz, ArH), 5.43~5.48 (m, 1H, =CH), 5.11(s, 2H, CH2), 5.08~5.09 (m, 1H, =CH), 4.83 (d, 2H,J= 7.05 Hz, CH2), 2.28 (s, 3H, ArCH3), 2.05~2.13 (m, 4H, CH2CH2),1.73 (s, 3H, CH3), 1.69 (s, 3H, CH3), 1.59 (s, 3H, CH3). IR(KBr),ν/cm-1: 2 924, 1 381, 1 614, 1 583, 1 502, 1 454, 1 724,1249. HRMS(ESI):C25H31O3[M + H]+,测量值379.226 81,计算值379.226 77。
2-苄基-3-甲氧基苯甲酸香叶酯 (6g):黄色液体, 产率68.4%.1H NMR (300 MHz, CDCl3),δ: 7.52 (d, 2H,J= 7.03 Hz, ArH), 7.27~7.38 (m, 4H, ArH), 7.02~7.11 (m, 2H, ArH),5.37~5.42 (m, 1H, =CH), 5.08 (s, 2H, CH2), 5.04~5.05 (m, 1H,=CH), 4.78 (d, 2H,J= 7.05 Hz, CH2), 3.85 (s, 3H, ArOCH3),2.00~2.09 (m, 4H, CH2CH2), 1.74 (s, 3H, CH3), 1.66 (s, 3H,CH3), 1.58 (s, 3H, CH3). IR (KBr),ν/cm-1: 2 967, 2 929, 1 376, 1 581,1 497, 1 475, 1 725, 1264. HRMS(ESI):C25H31O4[M + H]+,测量值395.221 28, 计算值395.221 69。
2-苄基-4-甲氧基苯甲酸香叶酯 (6h):黄色液体, 产率40.8%.1H NMR (300 MHz, CDCl3),δ: 7.88 (d, 1H,J= 8.46 Hz, ArH), 7.51 (d, 2H,J= 7.40 Hz, CH2), 7.25~7.39 (m, 3H,ArH), 6.48~6.51 (m, 2H, ArH), 5.39~5.44 (m, 1H, =CH), 5.14(s, 2H, CH2), 5.07~5.09 (m, 1H, =CH), 4.81 (d, 2H,J= 6.98 Hz, CH2), 3.79 (s, 3H, ArOCH3), 2.02~2.11 (m, 4H, CH2CH2),1.70 (s, 3H, CH3), 1.67 (s, 3H, CH3), 1.59 (s, 3H, CH3). IR(KBr),ν/cm-1: 2 925, 2 855, 1 381, 1 608, 1 577, 1 504, 1 442, 1 719,1249. HRMS(ESI):C25H29O4[M-H]-,测量值393.206 39,计算值393.206 04。
2-苄基-5-甲氧基苯甲酸香叶酯 (6i):黄色液体, 产率76.6%.1H NMR (300 MHz, CDCl3),δ: 7.47 (d, 2H,J= 7.08 Hz, ArH), 7.24~7.38 (m, 4H, ArH), 6.91~6.99 (m, 2H, ArH),5.42~5.47 (m, 1H, =CH), 5.09 (s, 2H, CH2), 5.06~5.07 (m, 1H,=CH), 4.83 (d, 2H,J= 7.05 Hz, CH2), 3.77 (s, 3H, ArOCH3),2.02~2.11 (m, 4H, CH2CH2), 1.73 (s, 3H, CH3), 1.67 (s, 3H,CH3), 1.59 (s, 3H, CH3). IR (KBr),ν/cm-1: 2 967, 2 928, 1 380, 1 584,1 500, 1 454, 1 726, 1284. HRMS(ESI):C25H31O4[M + H]+,测量值395.220 25, 计算值395.221 69。
2.2 驱避活性
以豌豆蚜为对象,首先测试了无翅成蚜对溶剂正己烷的行为反应,结果显示蚜虫不偏向行为嗅觉仪的任何一端 (x2= 0.12,df= 1,P= 0.729);然后测试了目标化合物的驱避活性。结果(表1)表明:在5 μg 剂量下,所有目标化合物对豌豆蚜均有驱避活性,部分活性较明显,例如化合物 6c、6e、6f、6h 和6i 的驱避率达到 50%以上;化合物5c~5f 的活性较低,驱避率仅为20%左右。当苯环上的酚羟基被烷氧基或苄氧基取代后,化合物的驱避活性都不及先导化合物3e 和对照药剂EβF,其中6i 的活性最高,驱避率达到60.9%,与先导3e 的活性没有显著性差异。因此,在水杨酸2 位引入含醚基团对EβF 类似物的驱避活性不利。以6i 为先导化合物,在水杨酸的2 位仍保持羟基结构或引入酯基[25-26]等与靶标位点有较好结合的基团,设计合成其他结构的类似物,有进一步研究的价值。
在进行地表施工作业时,地表浅层土通常是施工的重要目标。但是地表浅层土会受温度、土体、气候等多方面因素的干扰,因此其水分场与温度场都会不断改变,而且相互影响。土壤的温度在发生改变时,土体内部的水分也会相应变化,这一变化进而会导致其自身导热系数与比热的改变,最终引起土壤温度场与传热能力的变化。在温度降低的时候,土壤会迅速凝固并释放热能,此时水分也会相应发生移动,那么土体的温度场就会产生变化。[2]

表1 目标化合物的豌豆蚜驱避活性Table 1 The aphid repellent activity against A. pisum
初步构效关系分析表明,R1与R2取代基均对化合物驱避活性有影响。当R1为3-甲氧基时,不论R2为苄基或烷基,化合物的驱避活性均不明显,尤其是R2为C4~C7直链烷基时的驱避活性仅为20%左右 (5c~5f);当R1为氢时,R2为苄基比烷基对活性有利 (6c > 6a 和6b),且R2为乙基比甲基对活性有利 (6b > 6a)。当R2为甲基或乙基时,不论R1为氢或3-甲氧基,化合物的驱避活性均不理想。由此可见,R2为苄基较烷基对驱避活性更有利。当R2为苄基时,R1基团为4 位取代或5 位取代对活性更有利,如6e 和6f > 6d,6h 和6i > 6g。
2.3 蛋白结合活性
蚜虫OBP9 几乎只在触角中表达,在不同蚜虫种类之间具有良好的保守性[33],在豌豆蚜、桃蚜、麦长管蚜中均有报道[25,33-35],是识别气味小分子的关键靶标蛋白。本课题组前期研究发现,ApisOBP9可与EβF 及其大多数类似物强烈结合,其结合能力甚至高于已报道的潜在靶标ApisOBP3 和ApisOBP7[25-26]。D'Onofrio 等研究发现,豌豆蚜ApisOBP9 还与长链的、尤其是与16 个碳原子的醇类和醛类挥发物有好的结合[33]。麦长管蚜的SaveOBP9 与大多数小麦挥发物具有广谱且较高的结合能力[34]。桃蚜的MperOBP9 则与EβF 及部分植物挥发物具有较高的结合活性[35]。
参考文献方法[25],表达纯化出模式蚜虫豌豆蚜的气味结合蛋白ApisOBP9,并研究其与目标化合物的结合特性。结果 (图1,图2) 表明:与驱避活性所得结果相似,苯环上的酚羟基被烷氧基或苄氧基取代后的目标物仍与ApisOBP9 表现出结合活性。部分化合物的蛋白结合活性较好,例如化合物 6b、6c、6e 和6i,其中6i 的蛋白结合活性最高,但不及先导3e;而R2为脂肪链的化合物5a~5f 与ApisOBP9 的结合活性较低。

图1 目标化合物与ApisOBP9 的荧光竞争结合曲线Fig. 1 Fluorescence competitive binding curves of the target compounds to ApisOBP9

图2 目标化合物与ApisOBP9 的结合活性Fig. 2 Binding activity of the target compounds with ApisOBP9 from A. pisum
初步构效关系分析表明,取代基R1与R2的种类均对蛋白结合活性有影响。总体上,R2为苄基比烷基对活性有利,尤其是当R2为C2-C7直链烷基时,化合物 (5a~5f) 的蛋白结合活性较低,结合常数 (解离常数的倒数:1/Kd) 仅为0.62 μmol/L及以下。当R2为苄基时, R1基团为4 位取代或5 位取代对活性更有利,如6e 和6f > 6d,6h 和6i > 6g。对比分析目标化合物的蚜虫驱避活性和蛋白结合活性,发现二者表现出一致性的趋势。例如,目标化合物6i 具有最高的蛋白结合活性,也具有最好的驱避活性,而R2为直链烷基的化合物 (5a~5f) 则表现出较弱的蛋白结合活性,它们的驱避活性也相对较低。
2.4 分子对接结果分析
选择代表性化合物6i,研究其与蛋白ApisOBP9的结合模式。分子对接结果显示,6i 与3e 在蛋白结合口袋中的方向一致,但也有所不同:3e 的芳香环区域靠近Leu130 一侧,EβF 链靠近Pro69 一侧[26],而6i 的双芳香环区域靠近Arg126 一侧,EβF 链靠近Cys97 一侧 (图3);此外,6i 的EβF链与氨基酸残基Pro69、Pro71、Phe74、Tyr94、Cys97、Phe112、Ala116 和Val127 形成疏水相互作用,而3e 的EβF 链则主要与Met53、Met62、Pro69、Pro71、Phe74、Val93、Lys96、Ala113 和Ala116 等氨基酸残基形成重要的疏水作用。这表明6i 在与ApisOBP9 的结合作用上,可能与3e 分子有类似的作用机理。但对比3e 与6i的结合构象图发现,3e 分子是舒展的线形分子,6i 分子则因为在2 位引入了新的大位阻基团苄基,导致配体分子扭曲折叠起来。因此推测6i 在2-OH 位点引入苄基后,导致分子的空间位阻过大,与ApisOBP9的结合口袋不匹配,这可能是导致该化合物与ApisOBP9 结合活性降低的原因。此外,新引入化合物6i 的苄基基团可以与Phe117 形成“T-π”相互作用,同时又与Arg126 形成了“Cation-π”相互作用,增强了其与蛋白的结合活性。因此引入的苄基芳香环可能发挥了重要的极性相互作用。这也可能是含苄基类化合物结合活性高于脂肪链化合物的原因之一 (6i > 5a~5f)。
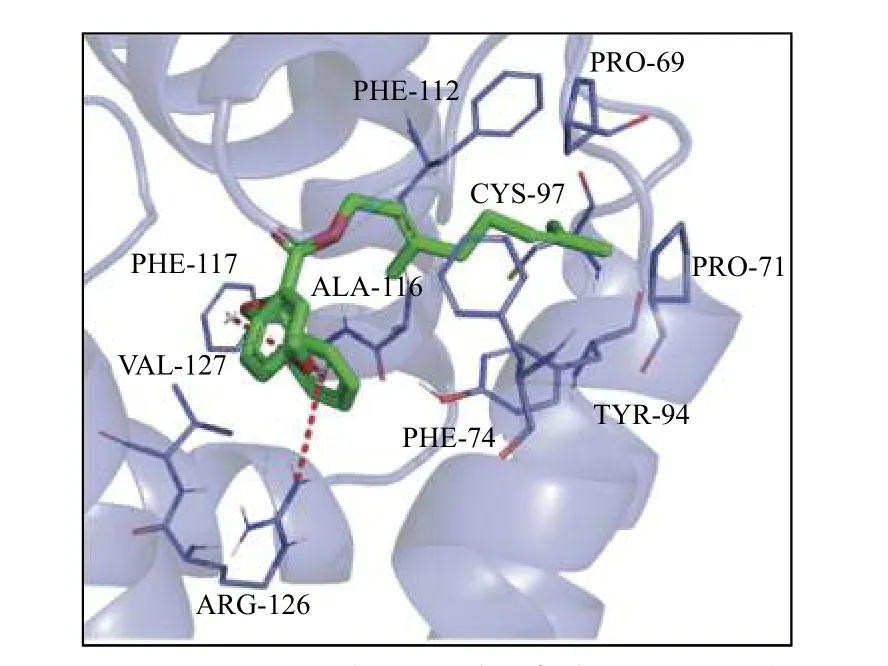
图3 目标化合物6i 与豌豆蚜气味结合蛋白ApisOBP9 的结合模式Fig. 3 Binding mode of the compound 6i with ApisOBP9
3 结论
本研究以前期发现的水杨酸酯类EβF 类似物3e 为先导,以蚜虫气味结合蛋白为靶标,通过活性亚结构拼接设计并合成了一系列新型2-烷氧基取代苯甲酸香叶酯类EβF 类似物,其结构均经过1H NMR、IR 和HRMS 确证。活性测定结果表明,目标化合物对豌豆蚜无翅成蚜都有驱避活性,但均不及先导化合物3e,其中6i 的驱避活性最高,在5 μg 剂量下达到60.9%,与先导3e 的活性没有显著性差异。靶标蛋白结合实验证明,部分目标化合物与气味结合蛋白ApisOBP9 具有较好的结合活性,尤其是化合物6i 与ApisOBP9 的结合活性最优。进一步分子对接结果表明, 6i 与ApisOBP9 具有较好的疏水作用力,可以很好地结合到靶标气味结合蛋白的活性位点,其结合模式和先导相似。本研究结果表明,在先导化合物3e 的水杨酸2 位羟基结构上引入直链烷氧基或苄氧基后,化合物的蚜虫驱避活性和靶标蛋白结合活性均有不同程度的降低。因此,在水杨酸2 位引入含醚基团对EβF 类似物的驱避活性不利,建议水杨酸2 位仍保持羟基结构或引入酯基等与靶标位点结合较好的基团。该研究结果为后续化合物的进一步设计和结构优化提供了重要参考价值。
谨以此文庆贺中国农业大学农药学学科成立70 周年。
Dedicated to the 70th Anniversary of Pesticide Science in China Agricultural University.
作者简介:

秦耀果,女,讲师。2011 年6 月在贵州大学植物保护专业获农学学士学位。2011.9—2017.6 在中国农业大学农药学专业硕博连读,并获博士学位,期间(2014.10—2015.09)由国家留学基金委资助在英国Rothamsted Research 进行博士联合培养,毕业后在中国农业科学院植物保护研究所从事博士后研究工作。2020 年入职中国农业大学,研究方向为蚜虫及其天敌感知气味分子的作用机制。主持国家自然科学基金青年基金 1 项,主持博士后基金面上基金 1 项。

杨朝凯,男,博士研究生。2016年6 月在山西农业大学植物保护专业获农学学士学位。2016 年9 月至今在中国农业大学理学院农药学专业硕博连读,期间 (2019年5 月至8 月) 在学校研究生国际化培养提升项目资助下赴美国加州大学戴维斯分校进行合作研究,主要从事基于植物挥发性物质的新型蚜虫行为控制剂的设计、合成和生物活性研究。

杨新玲,教授,博士生导师,绿色农药分子设计与发现团队负责人。1995年于北京农业大学农药学专业获得理学博士学位。1995 年至今在中国农业大学从事教学科研工作,研究领域为新农药分子设计与合成、化学生物学,主要研究方向包括靶标导向的新型昆虫生长调节剂的创制、以昆虫源或植物源活性物质为模型的新型害虫行为控制剂研究等,先后主持或参加国家自然科学基金、国家科技支撑计划、973 计划、农业部公益行业项目、国家重点研发计划等课题10 余项。曾获IUPAC 农药化学 ‘农药科学特殊贡献奖’,现任北京农药学会副理事长兼秘书长,中国农药工业协会知识产权专业委员会副主任委员,中国化工学会农药专业委员会委员,中国化学会农业化学专业委员会委员,中国生化制药工业协会多肽分会专家委员会委员等。担任Pest Management Science等期刊编委,现任《农药学学报》常务编委。
