喹唑啉酮肟醚衍生物的设计、合成、杀菌活性及其与琥珀酸脱氢酶受体的结合模式
2022-10-25王金玲
王金玲, 李 忠
(华东理工大学 药学院,上海市化学生物学 (芳香杂环) 重点实验室,上海 200237)
喹唑啉酮骨架在多种天然生物碱中广泛存在[1],该类结构因其广泛的生物活性[2]而成为农药创制领域常用的活性骨架之一,喹唑啉酮生物碱及其衍生物在农药领域表现出广泛的药理学特性,例如抗真菌[3-4]、杀虫[5]、除草[6]和抗烟草花叶病毒(TMV)等活性[7-8],是一个值得深入研究的优异药效团。
含肟醚结构的衍生物具有多种生物活性,例如在杀菌剂吡菌苯威和四唑吡氨酯,杀虫、杀螨剂唑螨酯以及除草剂噻草酮中均含有肟醚片段(图式1)[9]。有研究表明,肟醚可以成为开发新型琥珀酸脱氢酶抑制剂 (succinate dehydrogenase inhibitor,SDHI) 类杀菌剂的新的连接桥[10]。

图式1 含有肟醚结构的代表性农药[9]Scheme 1 Representative pesticides containing oxime ether structures[9]
近几年,SDHI 类杀菌剂[11]因高速增长的销量量而备受关注。SDHI 类杀菌剂作用于病原菌线粒体呼吸电子传递链上的复合体 Ⅱ [即琥珀酸脱氢酶 (succinate dehydrogenase,SDH) ][12]。尽管SDHI 类杀菌剂在控制植物病害方面发挥着重要作用,但由于其结构相似,导致交叉抗性发展迅速,同时其对卵菌活性较差,因此,迫切需要寻找具有全新结构的新型SDHI 类杀菌剂。
为探索具有全新结构的SDHI 类杀菌剂先导,本研究依据中间体衍生化策略,对本课题组前期研究所得的新型2-(硝基甲基)喹唑啉-4(3H)-酮骨架进行了结构衍生:通过硝基选择性还原的方法实现该新型喹唑啉酮骨架和肟醚键两个活性片段的拼接 (图式2),设计并合成了25 个未见报道的新型喹唑啉酮肟醚衍生物(A1~A25),合成路线见图式3。以氟吡菌酰胺作为对照,对目标化合物开展理化性质预测、杀菌活性测试以及与SDH 受体结合模式研究,以期发现高杀菌活性先导化合物。

图式2 目标化合物的分子设计示意图Scheme 2 Design strategy of the target compounds

图式3 目标化合物的合成路线Scheme 3 Synthetic route of target compounds
1 实验部分
1.1 仪器与试剂
Bruker AM-400/600 核磁共振仪 (内标:TMS,氘代试剂:DMSO-d6或CDCl3);电子轰击 (EI)-高分辨飞行时间质谱仪 (GCT Premier);Büchi Melting Point B-540 熔点仪等。所有试剂均为分析纯或化学纯,均购自商业供应商,除特别注明外,未经进一步处理。纯度≥98%的氟吡菌酰胺(fluopyram) 固体原药,购自上海源叶生物科技有限公司。
1.2 化合物合成
1.2.1 中间体2 的合成 参考文献方法[13]合成:使用气相色谱仪(GC)监测反应结束后,分液,减压蒸馏,得黄绿色液体产物,收率95%。原料与产物均为液态,沸点较低,采用气相色谱归一法定量。气相色谱-质谱联用(GC-MS),m/z: 141(M+,57), 125(10), 111(15), 95(100), 83(49), 60(71)。其中141~83 的峰均有9 : 6 : 1 的同位素峰存在,说明结构中含有两个氯,产物保留时间在9 min 左右,归一化纯度为95.725%。
1.2.2 中间体5 的合成 参考文献方法[14-15]合成。采用薄层层析(TLC) [V(正庚烷) :V(乙酸乙酯) =2 : 1] 监测反应至结束,第1 步反应结束后,用饱和碳酸氢钠水溶液淬灭反应,抽滤,上层固体用乙醚洗涤3 次后置于红外烘箱中干燥,粗产物不经分离直接用于下一步反应。第2 步反应结束后,加水淬灭反应,水相用乙酸乙酯萃取 (20 mL ×3),无水硫酸钠干燥有机相,减压浓缩除去溶剂。粗产物经硅胶柱层析[V(正庚烷) :V(乙酸乙酯) = 3 : 1] 分离提纯,得白色固体产物 (R=3-CH3),收率为90%。1H NMR (400 MHz, DMSOd6),δ: 7.34 (dd,J= 7.8 Hz, 0.8 Hz, 1H), 7.14 (d,J=6.9 Hz, 1H), 6.88~6.84 (m, 2H), 6.42 (t,J= 7.6 Hz,1H), 6.38 (s, 2H), 7.67 (s, 1H), 2.06 (s, 3H).13C NMR(101 MHz, DMSO-d6),δ: 171.93, 148.26, 135.67,127.31, 123.10, 114.67, 113.24, 18.21.
1.2.3 中间体6 的合成 参考文献方法[16]合成。室温下,向50 mL 茄形瓶中加入2-氨基苯甲酰胺 (5 mmol)和20 mL 水,取1,1-二氯-2-硝基乙烯(10 mmol) 加入上述混合液中,70 ℃下反应2 h。采用TLC [V(正庚烷) :V(乙酸乙酯) = 1 : 2] 监测反应至结束。抽滤,用石油醚洗涤,产物无需柱层析分离,直接投入下一步。
1.2.4 中间体7 的合成 称取2.05 g 中间体6(10 mmol) 于100 mL 圆底烧瓶中,加入30 mL 四氢呋喃,搅拌溶解,冰浴条件下分批次加入11.29 g 氯化亚锡 (50 mmol),升至室温反应约12 h,采用TLC [V(正庚烷):V(乙酸乙酯) = 20 : 1] 监测反应至结束。向反应体系中加入30 mL 二氯甲烷和30 mL 水,少量多次加入碳酸氢钠固体,直至反应液不再冒出气泡。在抽滤漏斗中垫上硅藻土进行抽滤,并用二氯甲烷洗涤滤饼,滤液用二氯甲烷萃取 (30 mL × 3),饱和氯化钠溶液洗涤,无水硫酸钠干燥,减压浓缩后得粗产物,经硅胶柱层析 [V(正庚烷) :V(乙酸乙酯) = 30 : 1] 分离提纯,得白色固体产物,收率85%。1H NMR (400 MHz,DMSO-d6,δ: 12.47 (s, 1H), 10.17 (s, 1H), 7.85 (dd,J= 7.8, 1.1 Hz, 1H), 7.78 (d,J= 7.5 Hz, 1H), 7.73(dd,J= 7.3, 1.3 Hz, 1H), 7.70 (s, 1H), 7.43~7.36 (m,1H).13C NMR (101 MHz, DMSO-d6),δ: 161.30,143.67, 139.96, 134.37, 133.59, 126.47, 125.75,117.13, 107.82.
1.2.5 目标化合物A1~A25 的合成 参考文献方法[17]合成并稍作修改。室温条件下,将0.38 g (E)-4-氧代-3,4-二氢喹唑啉-2-甲醛肟7 (2 mmol) 和卤化物8 (3 mmol) 溶解在20 mL 四氢呋喃中,加入0.28 g 碳酸钾 (2 mmol),升温至65 ℃,搅拌过夜。采用TLC [V(正庚烷) :V(乙酸乙酯) = 3 : 1]监测反应至结束后,用饱和氯化铵水溶液调节pH 至中性,水相用乙酸乙酯萃取 (20 mL × 3),合并有机相,用饱和氯化钠溶液洗涤3 次,无水硫酸钠干燥,减压浓缩,粗产物经硅胶柱层析 [V(正庚烷) :V(乙酸乙酯) = 3 : 1] 分离提纯,得到目标化合物。
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛邻丙基肟 (A1):白色固体,收率 69%,m.p. 97.2~97.3 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.40 (s, 1H), 7.86 (dd,J= 7.8, 1.1 Hz,1H), 7.80 (s, 1H), 7.72 (td,J= 7.4, 1.4 Hz, 1H), 7.66 (d,J=8.1 Hz, 1H), 7.41 (td,J= 7.7, 1.1 Hz, 1H), 4.19 (t,J= 6.7 Hz,2H), 1.75~1.67 (m, 2H), 0.93 (t,J= 7.4 Hz, 3H).13C NMR(101 MHz, DMSO-d6),δ: 160.39, 143.59, 139.72, 134.39,133.67, 126.80, 126.21, 117.13, 108.34, 76.96, 22.27, 10.53.HRMS (EI) 计算值 C12H13N3O2[M]+: 231.100 8, 实测值 231.100 9.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-乙基肟 (A2): 白色固体,收率为75%,m.p. 96.5~96.7 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.42 (s, 1H), 7.86 (d,J= 7.7 Hz, 1H),7.79 (s, 1H), 7.73 (t,J= 7.8 Hz, 1H), 7.65 (d,J= 8.1, 1H),7.41 (t,J= 7.5 Hz, 1H), 4.28 (q,J= 7.0 Hz, 2H), 1.29 (t,J=7.0 Hz, 3H).13C NMR (101 MHz, DMSO-d6),δ: 160.39,143.60, 139.72, 134.40, 133.68, 126.80, 126.23, 117.14,108.36, 71.17, 14.84. HRMS (EI) 计算值 C11H11N3O2+217.085 1,实测值 217.085 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-异戊基肟 (A3):白色固体,收率为85%,m.p. 97.0~97.9 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.41 (s, 1H), 7.86 (dd,J= 7.8, 1.2 Hz,1H), 7.80 (s, 1H), 7.73 (td,J= 7.8, 1.4 Hz, 1H), 7.69 (d,J=7.2 Hz, 1H), 7.41 (td,J= 7.6, 1.3 Hz, 1H), 4.27 (t,J= 6.8 Hz,2H), 1.75~1.65 (m, 1H), 1.62~1.57 (m, 2H), 0.92 (d,J= 6.6 Hz, 6H).13C NMR (101 MHz, DMSO-d6),δ: 160.34, 143.53,139.73, 134.36, 133.65, 126.71, 126.04, 117.12, 108.17, 74.10,37.63, 24.92, 22.89, 22.89. HRMS (EI) 计算值 C14H17N3O2+259.132 1, 实测值 259.132 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-环丙基甲基肟(A4):白色固体,收率为78%,m.p. 103.4~103.8 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.39 (s, 1H), 7.86 (dd,J=7.8, 1.3 Hz, 1H), 7.81 (s, 1H), 7.73 (td,J= 7.8, 1.5 Hz, 1H),7.67 (d,J= 7.3 Hz, 1H), 7.41 (td,J= 7.6, 1.3 Hz, 1H), 4.06 (d,J= 7.3 Hz, 2H), 1.26-1.21 (m, 1H), 0.59~0.52 (m, 2H),0.37~0.31 (m, 2H).13C NMR (101 MHz, DMSO-d6),δ:160.42, 143.45, 139.72, 134.40, 133.67, 126.77, 126.14,117.12, 108.25, 80.13, 10.46, 3.51, 3.51. HRMS (EI) 计算值C13H13N3O2+243.100 8, 实测值 243.101 2.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(2-氟乙基) 肟(A5):白色固体,收率为86%,m.p. 127.3~127.6 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.51 (s, 1H), 7.90 (s, 1H),7.87 (d,J =7.7 Hz, 1H), 7.77~7.71 (m, 1H), 7.65 (d,J =8.0 Hz, 1H), 7.42 (t,J =7.4 Hz, 1H), 4.74 (dt,J =47.8, 3.8 Hz,2H), 4.48 (dt,J =30.2, 3.8 Hz, 2H).13C NMR (101 MHz,DMSO-d6),δ: 160.16, 144.60, 139.61, 134.42, 133.73, 126.92,126.34, 117.12, 108.48, 81.17 (d,1JCF= 166.1 Hz), 74.78 (d,2JCF=18.6 Hz).19F NMR (376 MHz, DMSO-d6),δ: -162.10 (s,1F). HRMS (EI) 计算值 C11H10FN3O2+235.075 7, 实测值 235.076 0.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(3-氟丙基) 肟(A6):白色固体,收率为88%,m.p. 127.9~128.1 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.46 (s, 1H), 7.87 (dd,J=7.8, 1.4 Hz, 1H), 7.83 (s, 1H), 7.74 (td,J= 7.4, 1.5 Hz, 1H),7.65 (d,J= 7.8 Hz, 1H), 7.42 (td,J= 7.6, 1.1 Hz, 1H), 4.57(dt,J= 47.2, 5.9 Hz, 2H), 4.33 (t,J= 6.4 Hz, 2H), 2.10 (m,2H).13C NMR (101 MHz, DMSO-d6),δ: 160.27, 144.15,139.66, 134.41, 133.71, 126.87, 126.30, 117.13, 108.43, 81.22 (d,1JCF= 161.7 Hz), 71.52 (d,3JCF= 5.4 Hz), 30.03 (d,2JCF= 19.5 Hz).19F NMR (565 MHz, DMSO-d6),δ: -220.16 (s, 1F).HRMS (EI) 计算值 C12H12FN3O2+249.091 4, 实测值249.0912.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4,4,4-三氟丁基)肟 (A7):白色固体,收率为88%,m.p. 95.2~95.6 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.47 (s, 1H), 7.86 (dd,J=7.8, 1.3 Hz, 1H), 7.78 (s, 1H), 7.73 (td,J= 7.9, 1.5 Hz, 1H),7.64 (d,J= 7.8 Hz, 1H), 7.42 (td,J= 7.7, 1.0 Hz, 1H),3.94~3.85 (m, 2H), 2.18~2.07 (m, 1H), 2.05~1.83 (m, 3H).13C NMR (101 MHz, DMSO-d6),δ: 160.35, 144.87, 139.67,134.39, 133.69, 126.89 (q,1JCF= 163.09 Hz), 126.38, 117.14,108.52, 107.97, 68.20(q,4JCF= 2.3 Hz), 30.88(q,2JCF= 23.1 Hz), 23.61 (q,3JCF= 6.7 Hz).19F NMR (565 MHz, DMSOd6).δ: -62.85 ~ -63.15 (m, 3F). HRMS (EI) 计算值C13H12F3N3O2+299.088 2, 实测值 299.088 0.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4-甲基苄基)肟(A8):白色固体,收率为85%,m.p. 102.2~102.5 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.43 (s, 1H), 7.86 (d,J= 6.5 Hz, 2H), 7.76~7.70 (m, 1H), 7.68 (d,J= 7.7 Hz,1H),7.44~7.38 (m, 1H), 7.34 (d,J= 7.9 Hz, 2H), 7.21 (d,J=7.9 Hz, 2H), 5.24 (s, 2H), 2.31 (s, 3H).13C NMR (101 MHz,DMSO-d6),δ: 160.20, 144.18, 139.67, 138.11, 134.40, 133.90,133.70, 129.51, 129.21, 127.6, 127.0, 126.79, 126.10, 117.11,108.17, 77.22, 21.28. HRMS (EI) 计算值 C17H15N3O2+293.116 4,实测值 293.1163.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4-甲氧基苄基)肟 (A9):白色固体,收率为89%,m.p. 104.7~105.0 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.41 (s, 1H), 7.90~7.81(m, 2H), 7.76-7.64 (m, 2H), 7.48~7.30 (m, 3H), 6.94 (d,J=8.0 Hz, 2H), 5.20 (s, 2H), 3.76 (s, 3H).13C NMR (101 MHz,DMSO-d6),δ:160.23, 159.84, 144.04, 139.68, 134.41, 133.70,130.99, 130.99, 128.77, 126.78, 126.10, 117.12, 114.32,114.32, 108.16, 77.10, 55.58. HRMS (EI) 计算值C17H15N3O3+309.111 3, 实测值 309.111 5.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-(2-甲基苄基)肟(A10):白色固体,收率为85%,m.p. 103.2~103.4 ℃。1H NMR (400 MHz, DMSO-d6),δ:10.46 (s, 1H), 7.88 (s, 1H),7.86 (dd,J= 7.8, 1.3 Hz, 1H), 7.72 (dd,J= 7.3, 1.5 Hz, 1H),7.69~7.64 (m, 1H), 7.44~7.35 (m, 2H), 7.31~7.18 (m, 3H),5.32 (s, 2H), 2.35 (s, 3H).13C NMR (101 MHz, DMSO-d6),δ:160.20, 144.25, 139.67, 137.44, 134.81, 134.40, 133.71,130.64, 130.03, 129.02, 126.81, 126.35, 126.15, 117.11,108.22, 75.80, 19.11. HRMS (EI) 计算值 C17H15N3O2+293.116 4,实测值 293.116 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-(3-甲基苄基)肟(A11):白色固体,收率为84%,m.p. 103.9~104.2 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.46 (s, 1 H), 7.87 (s, 1H),7.86~7.84 (m, 1H), 7.76~7.70 (m, 1H), 7.67 (d,J= 8.3 Hz,1H), 7.41 (dd,J= 7.3, 1.5 Hz, 1H), 7.26 (m, 3H), 7.17 (d,J=7.3 Hz, 1H), 5.25 (s, 2H), 2.33 (s, 3H).13C NMR (101 MHz,DMSO-d6),δ:160.20, 144.27, 139.65, 138.15, 136.84, 134.42,133.71, 129.62, 129.38, 128.88, 126.84, 126.16, 126.15,117.12, 108.23, 77.35, 21.42. HRMS (EI) 计算值C17H15N3O2+293.116 4, 实测值 293.116 8.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-(4-氟苄基) 肟(A12):白色固体,收率为78%,m.p. 109.9~110.2 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.47 (s, 1H), 7.87 (s, 1H),7.86~7.85 (m, 1H), 7.77~7.71 (m, 1H), 7.67 (d,J= 7.6 Hz,1H), 7.52 (dd,J= 8.5, 5.7 Hz, 2H), 7.42 (dd,J= 7.7, 1.1 Hz,1H), 7.23 (m, 2H), 5.28 (s, 2H).13C NMR (101 MHz, DMSOd6),δ: 162.56 (d,1JCF= 244.3 Hz), 160.15, 144.43, 139.63,134.41, 133.71, 133.26 (d,3JCF= 3.0 Hz), 131.42 (d,3JCF= 8.2 Hz), 131.37, 126.84, 126.51 (d,2JCF= 68.4 Hz), 117.11,115.80 (d,2JCF= 21.5 Hz), 115.68, 108.23, 76.44.19F NMR(376 MHz, DMSO-d6),δ: -113.76 (s, 1F).. HRMS (EI) 计算值C16H12FN3O2+297.091 4, 实测值 297.091 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-(2-氟苄基) 肟(A13):白色固体,收率为85%,m.p. 106.7~106.9 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.46 (s, 1H), 7.90~7.84 (m,2H), 7.77-7.70 (m, 1H), 7.66 (d,J= 7.8 Hz, 1H), 7.55 (t,J=7.5 Hz, 1H), 7.49~7.38 (m, 2H), 7.30~7.22 (m, 2H), 5.35 (s,2H).13C NMR (101 MHz, DMSO-d6),δ: 161.08 (d,1JCF=246.5), 144.65, 139.61, 134.09, 133.73, 132.01 (d,3JCF= 4.2 Hz), 131.36 (d,3JCF= 8.5 Hz), 126.54 (d,2JCF= 68.4 Hz),126.19, 125.05, 123.75, 117.10, 116.02, 115.93(d,2JCF= 21.1 Hz), 108.24, 71.14.19F NMR (376 MHz, DMSO-d6),δ:-118.13 (s, 1F). HRMS(EI) 计算值 C16H12FN3O2+297.091 4,实测值 297.091 3.
(E)-4-氧代-3,4-二氢喹唑啉-2-氨基甲醛-O-(3,4-二氟苄基)肟 (A14):白色固体,收率为70%,m.p. 104.9~105.1 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.47 (s, 1H), 7.90 (s, 1H),7.87 (dd,J= 7.7, 1.5 Hz, 1H), 7.77~7.71 (m, 1H), 7.67 (dd,J=8.2, 1.2 Hz, 1H), 7.54~7.51 (m, 1H), 7.50~7.40 (m, 2H),7.36~7.29 (m, 1H), 5.28 (s, 2H).13C NMR (101 MHz, DMSOd6),δ: 160.08, 149.85 (d,1JCF= 264.4 Hz), 149.73 (d,1JCF=245.4 Hz), 144.79, 139.59, 134.86 (dd,2JCF= 9.1, 1.0 Hz),134.41, 133.70, 126.88, 126.21, 125.98 (dd,2JCF= 10.1, 3.0 Hz), 118.14 (d,3JCF= 4.0 Hz), 117.96 (d,3JCF= 4.2 Hz),117.09, 108.29, 75.73.19F NMR (565 MHz, DMSO-d6),δ:-1 3 9.0 3 ~ -1 3 9.9 1 (m, 2 F). H R M S (E I) 计算值C16H11F2N3O2+315.081 9, 实测值 315.081 4.
(E)-4-氧代-3,4-二氢喹唑啉-2-氨基醛-O-(4-(三氟甲基)苄基)肟 (A15):白色固体,收率为85%,m.p.100.9~101.2 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.51 (s, 1H),7.95 (s, 1H), 7.87 (dd,J= 7.8, 1.2 Hz, 1H), 7.78 (d,J= 8.1 Hz,2H), 7.76~7.71 (m, 1H), 7.66 (dd,J= 8.1, 3.0 Hz, 3H), 7.42(td,J= 7.7, 1.1 Hz, 1H), 5.40 (s, 2H).13C NMR (101 MHz,DMSO-d6),δ: 160.02, 144.96, 142.03, 139.58, 134.42, 133.80,133.73, 129.31, 128.94, 126.89, 126.22, 125.90, 125.86(q,3JCF= 3.7 Hz), 125.79, 117.10, 108.27, 76.09.19F NMR (565 MHz,DMSO-d6),δ: -60.98 (s, 3F). HRMS (EI) 计算值C17H12F3N3O2+347.088 2, 实测值 347.088 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-氨基甲醛-O-(4-氯苄基)肟 (A16):白色固体,收率为87%,m.p. 122.1~122.3 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.47 (s, 1H), 7.89 (s, 1H),7.87 (dd,J= 7.8, 1.3 Hz, 1H), 7.73 (td,J= 7.4, 1.5 Hz, 1H),7.67 (d,J= 7.4, 1H), 7.47 (m, 4H), 7.41 (td,J= 7.6, 1.2 Hz,1H), 5.29 (s, 2H).13C NMR (101 MHz, DMSO-d6),δ: 160.09,144.62, 139.62, 136.09, 134.41, 133.72, 133.39,130.89,130.89, 128.97, 128.97, 126.85, 126.18, 117.11,108.23, 76.26. HRMS (EI) 计算值 C16H12ClN3O2+313.061 8,实测值 313.062 1.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(3-氯苄基) 肟(A17):白色固体,收率为87%,m.p. 98.9~99.1 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.48 (s, 1H), 7.91 (s, 1H),7.86 (dd,J= 7.8, 1.3 Hz, 1H), 7.73 (td,J= 7.9, 1.5 Hz, 1H),7.66 (d,J= 7.7 Hz, 1H), 7.51 (s, 1H), 7.45~7.38 (m, 4H), 5.30(s, 2H).13C NMR (101 MHz, DMSO-d6),δ: 160.07, 144.8,139.65, 139.61, 134.41, 133.72, 133.59, 130.91, 128.62,128.57, 127.48, 126.89, 126.24, 117.10, 108.31, 76.17. HRMS(EI) 计算值 C16H12ClN3O2+313.061 8, 实测值 313.062 0.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4-溴苄基) 肟(A18):白色固体,收率为86%,m.p. 132.6~132.8 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.45 (s, 1 H), 8.00-7.81 (m,2H), 7.79~7.55 (m, 4 H), 7.42 (s, 3H), 5.26 (s, 2H).13C NMR(101 MHz, DMSO-d6),δ:160.08, 144.65, 139.61, 136.52,134.41, 133.72, 131.90, 131.90, 131.19, 131.18, 126.86,126.19, 121.98, 117.11, 108.24, 76.29. HRMS (EI) 计算值C16H12BrN3O2+357.011 3, 实测值 357.011 7.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4-异丙基苄基)肟 (A19):白色固体,收率为86%,m.p. 98.4~98.5 ℃。1H NMR (400 MHz, DMSO-d6),δ:10.44 (s, 1H), 7.86 (d,J=7.5 Hz, 2H), 7.75~7.66 (m, 2H), 7.43~7.35 (m, 3H), 7.27 (d,J= 7.9 Hz, 2H), 5.24 (s, 2H), 2.94~2.86 (m, 1H), 1.20 (d,J=6.9 Hz, 6H).13C NMR (101 MHz, DMSO-d6),δ: 160.20,154.89, 149.06, 144.20, 139.67, 134.40, 134.34, 133.70,131.79, 129.25, 126.87, 126.80, 126.13, 117.12, 108.19, 77.22,33.70, 24.32, 24.32. HRMS (EI) 计算值r C19H19N3O2+321.147 7,实测值 321.147 1.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(4-(叔丁基)苄基)肟 (A20):白色固体,收率为86%,m.p. 79.8~80.2 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.45 (s, 1H), 7.45 (dd,J=7.7, 1.5 Hz, 1H), 7.34 (d,J= 8.3 Hz, 2H), 7.28 (d,J= 8.3 Hz,2H), 6.81~6.78 (m, 2H), 6.63 (d,J= 4.4 Hz, 1H), 6.61 (d,J=3.4 Hz, 1H), 4.39 (s, 2H), 1.25 (s, 9H).13C NMR (101 MHz,DMSO-d6),δ: 160.20, 154.89, 149.06, 144.20, 139.67, 134.40,134.34, 133.70, 131.79, 129.25, 126.87, 126.80, 126.13,117.12, 108.19, 77.22, 33.70, 24.32, 24.32, 24.32. HRMS (EI)计算值 C20H21N3O2+335.163 4, 实测值 335.163 2.
(E)-4-氧代-3,4-二氢喹唑啉-2-甲醛-O-(2,6-二甲基苄基)肟 (A21):白色固体,收率为88%,m.p. 158.9~159.0 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.45 (s, 1H), 7.86 (dd,J=7.8, 1.1 Hz, 1H), 7.82 (s, 1H), 7.76~7.71 (m, 1H), 7.67 (d,J=7.6 Hz, 1H), 7.41 (td,J= 7.7, 1.1 Hz, 1H), 7.20~7.13 (m, 1H),7.07 (d,J= 7.5 Hz, 2H), 5.36 (s, 2 H), 2.39 (s, 6H).13C NMR(101 MHz, DMSO-d6),δ: 160.23, 144.04, 139.72, 139.68,138.69, 138.64, 134.42, 133.72, 132.59, 129.16, 128.53,126.81, 126.11, 117.11, 108.16, 71.91, 19.90, 19.90. HRMS(EI) 计算值 C18H17N3O2+307.132 1, 实测值 307.132 0.
(E)-4-氧代-3,4-二氢喹唑啉-2-氨基醛-O-(2,6-二氯苄基)肟 (A22):白色固体,收率为86%,m.p. 148.8~148.9 ℃。
1H NMR (400 MHz, DMSO-d6),δ: 10.43 (s, 1H), 7.90 (s, 1H),7.86 (d,J= 7.7 Hz, 1H), 7.73 (d,J= 3.4 Hz, 1H), 7.55 (d,J=7.4 Hz, 2H), 7.49~7.45 (m, 1H), 7.44~7.38 (m, 2H), 5.54 (s,2H).13C NMR (101 MHz, DMSO-d6),δ: 159.96, 144.78,139.61, 136.81, 135.91, 134.39, 133.71, 132.24, 131.29,129.25, 128.97, 126.74, 125.88, 117.05, 107.88, 71.87. HRMS(EI) 计算值 C16H11Cl2N3O2+347.022 8, 实测值 347.022 6.
(E)-4-氧代-3,4-二氢喹唑啉-2-氨基醛-O-(2,6-二氟苄基)肟 (A23):白色固体,收率为80%,m.p. 105.6~105.8℃。1H NMR (400 MHz, DMSO-d6),δ: 10.46 (s, 1H), 7.87 (s,1H), 7.85 (d,J= 1.3 Hz, 1H), 7.72 (dd,J= 8.7, 1,1 Hz, 1H),7.69~7.66 (m, 1H), 7.55~7.52 (m, 1H),7.41 (t,J= 7.0 Hz, 1H),7.20~7.16 (m, 2H), 5.35 (s, 2H).13C NMR (101 MHz, DMSOd6),δ: 162.07 (d,1JCF= 238.2 Hz), 159.92 (d,1JCF= 237.4 Hz),154.00, 144.88, 140.67, 139.58, 134.36, 133.75, 132.34,126.84, 126.05, 125.66, 117.11 (d,2JCF= 12.5 Hz), 112.35 (d,3JCF= 5.5 Hz), 107.96(d,2JCF= 24.2 Hz), 64.83.19F NMR (376 MHz, DMSO-d6),δ: -114.48 (s, 1F), -114.58 (s, 1F). HRMS(EI) 计算值 C16H11F2N3O2+315.081 9, 实测值 315.0823.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-萘-2-基甲基肟(A24):白色固体,收率为86%,m.p. 126.2~126.5 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.49 (s, 1H), 8.01~7.90 (m,5H), 7.86 (d,J= 7.6 Hz, 1H), 7.73 (t,J= 8.3 Hz, 1H), 7.67 (d,J= 7.9 Hz, 1H), 7.59 (d,J= 8.6 Hz, 1H), 7.57~7.53 (m, 2H),7.41 (t,J= 7.3 Hz, 1H), 5.46 (s, 2H).13C NMR (101 MHz,DMSO-d6),δ: 160.17, 144.49, 139.65, 134.61, 134.42, 133.72,133.23, 133.18, 130.88, 129.63, 128.60, 128.38, 128.09,127.91, 126.85, 126.83, 126.16, 117.12, 108.20, 77.37. HRMS(EI) 计算值 C20H15N3O2+329.116 4, 实测值 329.116 5.
(E)-4-氧代-3,4-二氢喹唑啉-2-碳醛-O-((6-氯吡啶-3-基)甲基)肟 (A25):白色固体,收率为70%,m.p. 107.6~108.2 ℃。1H NMR (400 MHz, DMSO-d6),δ: 10.48 (s, 1H),8.33 (d,J= 2.1 Hz, 1H), 7.61 (dd,J= 8.1, 2.1 Hz, 1H), 7.32(d,J= 8.5 Hz, 1H), 7.86 (dd,J= 7.9, 1.2 Hz, 1H), 7.76 (d,J=7.3 Hz, 1H), 7.75 (dd,J= 7.3, 1.2 Hz, 1H), 7.71 (s, 1H),7.42~7.35 (m, 1H), 5.35 (s, 2H).13C NMR (101 MHz, DMSOd6),δ: 161.30 ,157.84, 150.71, 148.74, 143.67, 139.96, 138.82,134.37, 132.47, 133.59, 126.47, 125.75, 117.13, 107.82, 73.39.HRMS (EI) 计算值 C15H11ClN4O2+314.057 1, 实测值 314.057 2.
1.3 生物活性测试
1.3.1 试材及药剂配制 二叶期的小麦 (品种为扬麦15)、一叶一心期的黄瓜 (品种为新泰密刺) 和两叶一心期的水稻 (品种为太湖糯)。
小麦赤霉病菌Fusarium graminearum、黄瓜白粉病菌Erysiphe cichoracearum以及水稻纹枯病菌Rhizoctonia solani等试材,均引进自上海晓明检测技术服务有限公司。
将待测样品先用少量N,N-二甲基甲酰胺 (DMF)溶解,再用含有0.1%的吐温-80 水溶液稀释,配制成500 mg/L 的药液。以氟吡菌酰胺作阳性对照药剂,质量浓度为100 mg/L。
1.3.2 室内抑菌活性测定 生物活性初筛和复筛均采用盆栽活体试验法[18]。采用孢子悬浮液喷雾接种法[19]测定药剂对黄瓜白粉病菌的杀菌活性;采用盆栽苗接菌丝块法[20]测定药剂对小麦赤霉病菌和水稻纹枯病菌的杀菌活性,每处理重复3 次。接种后的作物置于人工气候室中培养,对以上病害分别培养7~8 d 后调查防效。病害分级参照《农药田间药效试验准则》,根据参考文献由病情指数计算防治效果[21]。
1.4 理化性质预测及分子对接
用网络服务器ALOGPS 2.1 (http://www.vcclab.org/lab/alogps/start.html) 对目标化合物的logP和logS进行预测,用软件ACD/Labs 预测化合物的pKa、MOE 预测化合物的极性表面积(TPSA)。以与RsSDH 具有高度同源性的猪心脏琥珀酸脱氢酶的复合晶体结构 (PDB ID:1ZOY)作为受体蛋白结构,采用Glide 方法进行分子对接,活性口袋设置为以泛醌结合位点的三维坐标为中心周围20 Å(2 nm)的区域,使用PyMOL 软件对分子对接结果进行分析和展示。
2 结果与分析
2.1 目标化合物合成
2.1.1 关键中间体7 的合成 以中间体6 为起始原料,将硝基选择性还原成肟基,得到中间体7。7 需要大量累积以便做后续的底物扩充。为保证中间体7 的产率,对还原条件进行了优化 (表1),最终筛选出最佳反应条件为:以路易斯酸氯化亚锡作催化剂、四氢呋喃作溶剂,在氩气保护及室温条件下反应24 h,最终以85%的高收率获得化合物7。

表1 关键中间体7 的合成条件筛选Table 1 Screening of synthetic conditions for key intermediate 7
2.1.2 目标化合物的合成 中间体7 在碱性条件下与各种取代氯 (溴) 苄发生亲核进攻,脱去一分子氯化氢得到目标化合物。在反应过程中,温度过高、时间过长以及氯 (溴) 苄的量太多等因素均会导致双取代副产物的产生,因此要严格控制反应的投料比、反应时间和温度,才能保证产物的收率。
2.2 活体杀菌活性
测试结果表明:在500 mg/L 下,部分目标化合物对小麦赤霉病菌表现出一定的防治效果,其中化合物A19 和A25 的防效分别为43.74%和42.46%(表2);对于黄瓜白粉病菌,除化合物A2 的防效为36.36%外,其余目标化合物均未表现出杀菌活性;同时所有目标化合物对水稻纹枯病菌也无活性。
2.3 理化性质及结合模式研究
化合物理化性质预测结果 (表2) 表明,目标化合物logP值在0.95~4.00 之间,处于合理的范围[22],但杀菌剂的最佳logP范围应为3.00~4.00,而本研究中大部分目标化合物的logP值小于3.00,表明其渗透能力较差;除A20 外,目标化合物的logS值均比氟吡菌酰胺的大,说明溶解度较好;而pKa以及极性表面积 (TPSA) 均与氟吡菌酰胺的差异较大,这些因素可能导致目标化合物难以通过细胞膜到达靶标,从而导致活性降低。
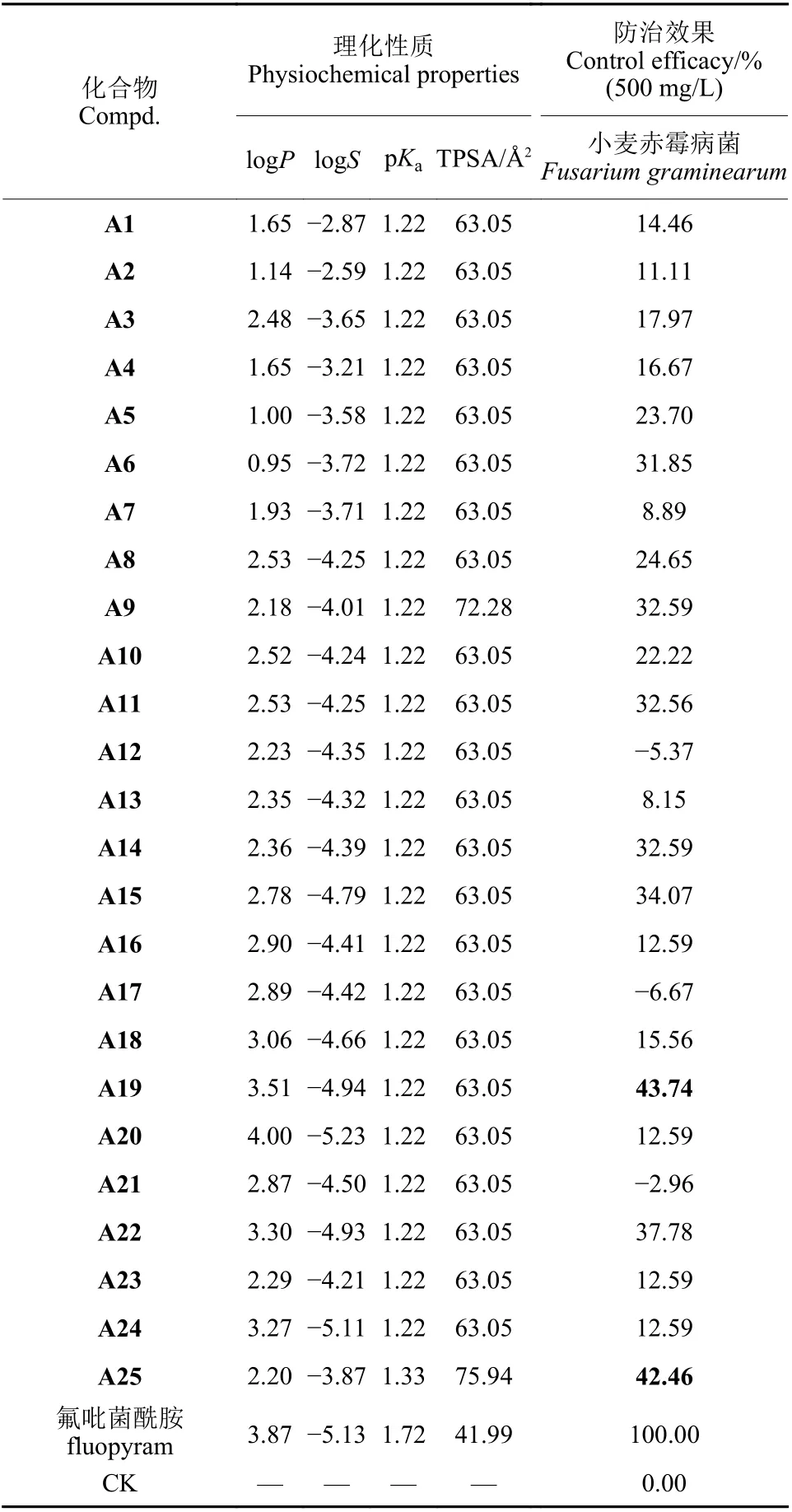
表2 目标化合物的理化性质以及活体杀菌活性Table 2 The physiochemical properties and in vivo antifungal activities of target compounds
通过分子对接,将活性最高的目标化合物A19和氟吡菌酰胺对接到 SDH (受体) 的活性位点,对接结果如图1 所示:化合物A19与氟吡菌酰胺均能结合在SDH 受体的活性口袋中。比较其结合模式可以发现,A19的喹唑啉酮环上的氧原子与氨基酸残基Tyr91 形成了氢键相互作用,距离为3.1 Å (1 Å=0.1 nm),喹唑啉酮环上的氧原子与氨基酸残基Trp173 也形成了氢键作用,距离为3.0 Å。而氟吡菌酰胺的羰基氧原子分别与氨基酸残基Tyr91 和 Trp173 形成了距离为2.9 和3.0 Å的氢键相互作用。此外,氟吡菌酰胺的吡啶环还与残基Tyr91 有π-π 堆积相互作用。氟吡菌酰胺形成的氢键相互作用力比A19略强,而且与靶标周围氨基酸形成的相互作用力更多,这可能是A19活性低于氟吡菌酰胺的原因之一,氨基的缺失可能是化合物A19比氟吡菌酰胺活性低的关键因素;另外,由于A19在结合口袋中的构象与氟吡菌酰胺的构象差异较大,整个分子未完全进入到结合活性口袋中,这也可能是导致活性降低的原因之一。

图1 氟吡菌酰胺(淡红色)及A19 (绿色)与SDH受体的结合模式Fig. 1 Binding mode of fluopyram (light red) and A19 (green) with SDH receptor
3 结论
本研究以氟吡菌酰胺为药剂对照,采用中间体衍生化法,根据活性亚结构拼接的原理将硝基甲基喹唑啉酮和肟醚键等多种药效团进行组合,设计合成了25 个未见报道的喹唑啉酮肟醚类化合物,并初步测定了其对小麦赤霉病菌、黄瓜白粉病菌以及水稻纹枯病菌的活体杀菌活性。结果表明,尽管目标化合物A19和A25在温室盆栽条件下对小麦赤霉病菌表现出一定的防治效果,但对小麦赤霉病菌的防效远低于氟吡菌酰胺。化合物活性较差的原因可能是由于其理化性质及结合模式与氟吡菌酰胺存在差异。
谨以此文庆贺中国农业大学农药学学科成立70 周年。
Dedicated to the 70th Anniversary of Pesticide Science in China Agricultural University.

作者简介:王金玲,女,硕士研究生。2019年7 月于河南农业大学制药工程专业获工学学士学位。2019 年9 月保送华东理工大学药学院攻读农药学专业硕士学位,主要从事绿色新农药的创制研究。

李忠,男,教授,博士生导师,国家级高层次人才。1996 年获华东理工大学精细化工专业博士学位,1999 年至2001 年日本筑波国立工业研究院物质工学研究所从事AIST 和ITIT 博士后研究。现任华东理工大学药物化工研究所所长,上海市化学生物学重点实验室主任。 主要聚焦绿色农药创制研究,开展顺硝烯新烟碱杀虫剂创制、关键中间体有合成技术研究及绿色工程工艺优化等方面的研究。主持国家重点研发计划项目、国家“863”课题、国家“973”子课题等数十项国家及省部级重要科研项目。现任《农药学学报》编委。
