一维核磁共振氢谱法在肺炎链球菌多糖结合疫苗检定中的应用
2022-10-25张凡曹方陈亚茹蒋苏王博雅陈高风杨艳喻峥嵘
张凡,曹方,陈亚茹,蒋苏,王博雅,陈高风,杨艳,喻峥嵘
艾美探索者生命科学研发有限公司,上海 201109
肺炎链球菌性疾病(pneumococcal disease,PD)是全球严重的公共卫生问题之一。肺炎链球菌是引起获得性肺炎(community-acquiredpneumonia,CAP)的重要病原菌之一,也是引起儿童肺炎、脑膜炎、菌血症、急性中耳炎和鼻窦炎等严重疾病的主要病原菌。随着抗生素的广泛使用,抗生素耐药菌株不断增加,广泛使用肺炎链球菌多糖结合疫苗可通过影响抗生素耐药肺炎链球菌的产生机制,从而减少出现耐药菌株。肺炎链球菌疫苗是预防肺炎链球菌感染的最有效手段,目前应用最为广泛的是23价肺炎链球菌多糖疫苗和7、10、13价肺炎链球菌多糖结合疫苗[1]。多糖结合疫苗是在多糖抗原上结合了载体蛋白,从而提高了多糖抗原的免疫原性,解决了多糖疫苗不能有效应用于幼儿或儿童的问题[2]。
肺炎链球菌多糖疫苗和多糖蛋白结合疫苗的质量有赖于荚膜多糖的纯度、抗原活性和稳定性等因素,一维核磁共振氢谱(one dimensional nuclear magnetic resonance hydrogen spectrum,1H-NMR)能够直观分析肺炎链球菌多糖的化学结构、取代基类型及其位置和数目,目前已应用于肺炎链球菌多糖疫苗的检定[3-4],而多糖结合疫苗的在降解、活化、衍生及结合过程中的多糖结构变化尚无有效的检测方法[5],因此,本研究将1H-NMR应用于肺炎链球菌多糖结合疫苗的检定,以期对上述指标进行质量控制。
1 材料与方法
1.1 菌株及载体蛋白9V、14、6A、11A型肺炎链球菌及破伤风类毒素(tetanus toxoid,TT)载体蛋白均由艾美探索者生命科学研发有限公司提供。
1.2 主要试剂及仪器 肺炎链球菌多糖标准品购自美国ATCC;氯化钠购自国药集团化学试剂有限公司;1-氰基-4-二甲氨基吡啶四氟硼酸酯(1-cyano-4-dimethylaminopyridinium tetrafluoroborate,CDAP)、溴化氰(cyanogenbromide,CNBr)、己二酰肼(adipicdihydrazide,ADH)及1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐[1-(3-dimethylaminopropyl)-3-ethylcarbodiimide hydrochloride,EDAC]均购自美国Sigma-Aldrich(Shanghai)Trading Co.,Ltd.公司;重水(D2O)购自美国Cambridge Isotope Laboratories,Inc公司;Sepharose 4FF层析介质购自格莱赛生命科学(上海)有限公司;VnmrS DD2 700MHz核磁共振仪购自美国Agilent公司。
1.3 多糖结合原液的制备 分别将9V、14、6A、11A型肺炎链球菌复苏后,在肺炎链球菌发酵培养基中发酵培养,杀菌,去除培养基成分,纯化,经无水乙醇、丙酮、乙醚洗涤后,真空抽干获得精糖[6]。各型肺炎链球菌精糖经0.2 mol/L氯化钠溶液溶解后,经超声降解,获得降解多糖;加入活化剂CDAP或CNBr得到活化多糖;再加入ADH进行衍生,经超滤得到多糖衍生物;多糖衍生物与TT载体蛋白按1∶(0.8±0.5)比例在EDAC的作用下结合,反应液通过Sepharose 4FF层析柱经0.85%的NaCl溶液洗脱,收集V0附近的吸收峰,纯化,除菌过滤获得各型肺炎链球菌多糖结合原液[2-8]。
1.41H-NMR样品的制备 取1.3项制备的肺炎链球菌精糖,用纯化水溶解至5 mg/mL,取450 μL,加入50 μL D2O,混匀,即为肺炎链球菌多糖1H-NMR样品;分别取1.3项制备的降解多糖溶液、活化多糖溶液、多糖衍生物溶液及多糖结合原液450 μL,加入50 μL D2O,混匀,即为肺炎链球菌降解多糖、活化多糖、多糖衍生物及多糖结合原液1H-NMR样品。
1.51H-NMR检测数据采集及处理 采用VnmrS DD2 700MHz核磁共振仪进行检测。探头类型:5 mm xyz PFG HCN probe,样品处理温度:300 K(约27℃),中心频率:699.812 MHz,图谱宽度:14 ppm,采样时间:3 s,累加次数:32,弛豫时间(d1):10 s,处理软件:vnmrJ&Mnova。用10% D2O锁场,以半重水(HDO)峰对样品化学位移进行校正。
1.6 样品1H-NMR结构鉴定 将获得的1H-NMR图谱用MestRenova软件进行分析归属,将肺炎链球菌多糖与标准品的图谱进行比较,确定结构是否一致。将肺炎链球菌多糖、降解多糖、活化多糖、多糖衍生物和多糖结合原液的图谱进行比较,确定肺炎链球菌多糖在降解、活化、衍生及结合过程中的结构变化。
2 结果
2.1 9V型肺炎链球菌的1H-NMR结构9V型肺炎链球菌降解多糖、活化多糖、多糖衍生物与肺炎球链菌多糖标准品指纹区结构一致,多糖结合原液多糖指纹区信号不清晰。HDO化学位移为4.6 ppm,5.38、5.30、5.06、4.82 ppm分别为α-Glc H1、α-Gal H1、α-GlcA H1、β-ManNAc H1的信号;2.12、2.05 ppm分别为OAc、NAc的信号;3.13 ppm为杂质C多糖的磷脂酰胆碱甲基信号。活化多糖1.96 ppm为残留溶剂乙腈(CH3CN)的甲基信号。9V型肺炎链球菌多糖在衍生过程中引入了ADH,2.20、1.51 ppm为ADH亚甲基信号。见图1。
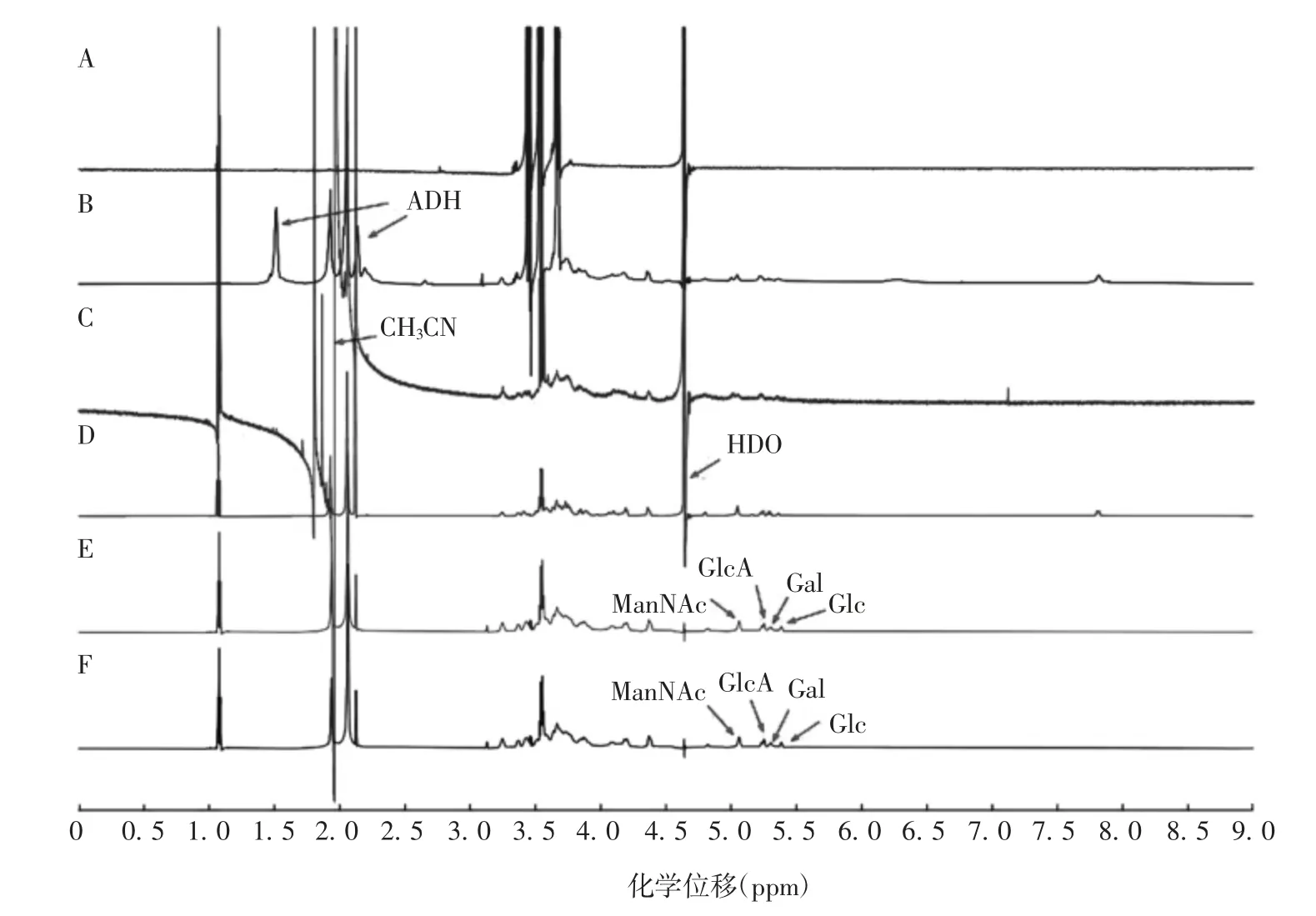
图1 9V型肺炎球菌多糖结合原液(A)、多糖衍生物(B)、活化多糖(C)、降解多糖(D)、精制多糖(E)、标准品(F)的1H-NMR图谱Fig.1 1H-NMR spectra of bulk of polysaccharide conjugate(A),polysaccharide derivative(B),activated polysaccharide(C),degraded polysaccharide(D),purified polysaccharide(E)and standard polysaccharide(F)of type 9V pneumococcus
2.2 14型肺炎链球菌的1H-NMR结构14型肺炎球菌降解多糖、活化多糖、多糖衍生物与肺炎链球链菌多糖标准品指纹区结构一致,多糖结合原液多糖指纹区信号不清晰。HDO化学位移为4.6 ppm,4.45、4.34 ppm分别为β-Gal H1和侧链β-Gal H1信号;1.93 ppm为NAc信号;3.13 ppm为杂质C多糖的磷脂酰胆碱甲基信号。活化多糖1.96 ppm为残留溶剂CH3CN的甲基信号。14型肺炎链球菌多糖在衍生过程中引入了ADH,2.14、1.51 ppm为ADH亚甲基信号。见图2。
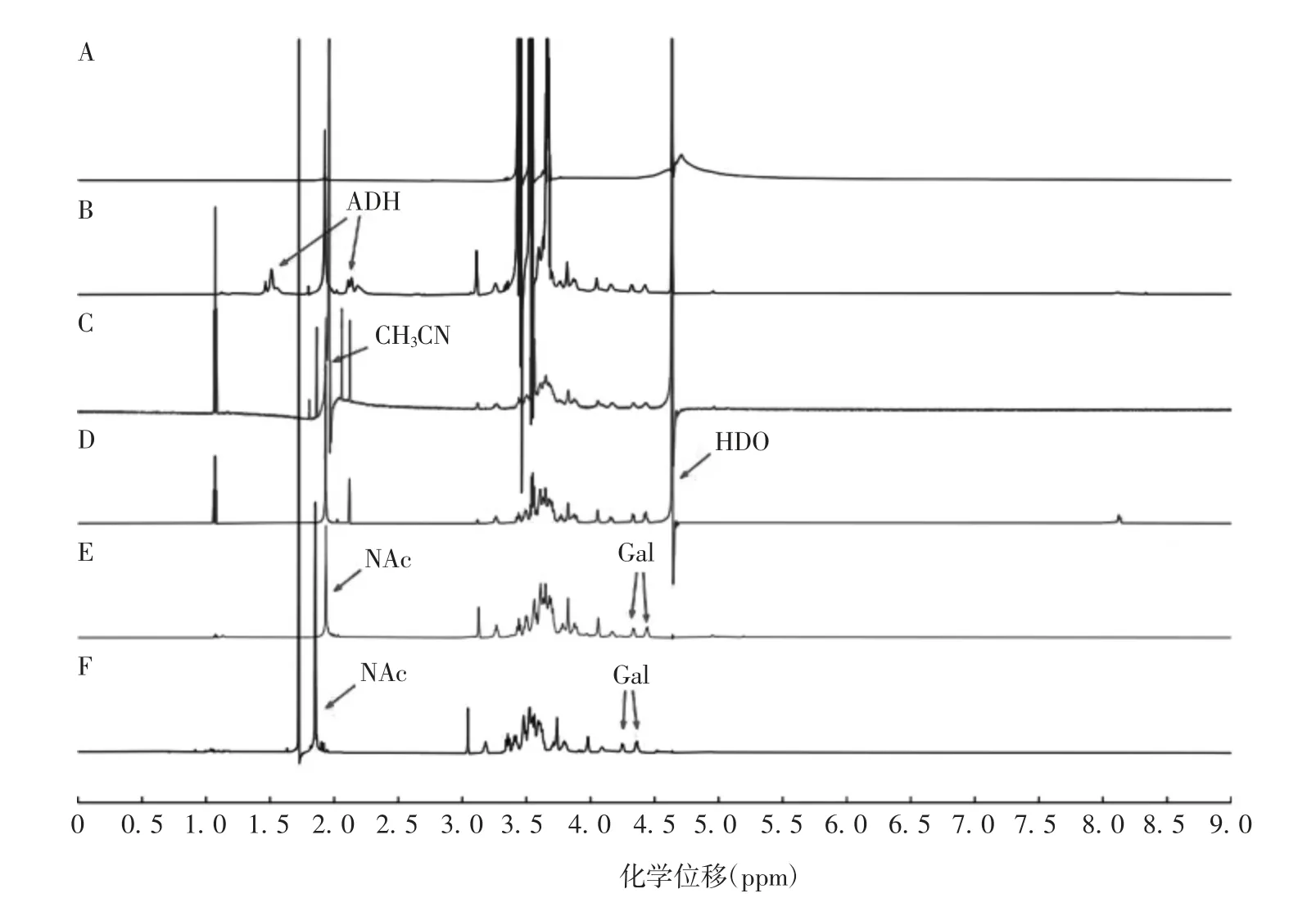
图2 14型肺炎球菌多糖结合原液(A)、多糖衍生物(B)、活化多糖(C)、降解多糖(D)、精制多糖(E)、标准品(F)的1H-NMR图谱Fig.2 1H-NMR spectra of bulk of polysaccharide conjugate(A),polysaccharide derivative(B),activated polysaccharide(C),degraded polysaccharide(D),purified polysaccharide(E)and standard polysaccharide(F)of type 14 pneumococcus
2.3 6A型肺炎链球菌的1H-NMR结构6A型肺炎链球菌降解多糖、活化多糖、多糖衍生物及多糖结合原液指纹区结构与6A型肺炎链球菌多糖标准品指纹区结构一致。HDO化学位移为4.6 ppm,5.51、5.02、4.93 ppm分别为α-Gal H1、α-Glc H1、α-Rha H1信号。活化多糖7.91、6.78 ppm为4-二甲氨基吡啶(4-dimethylaminopyridine,DMAP)吡啶环质子信号,证明CDAP的降解产物DMAP引入了6A型肺炎链球菌多糖;1.97 ppm为活化多糖中残留溶剂CH3CN的甲基信号。多糖衍生物引入了ADH,2.10、1.50 ppm为ADH亚甲基信号。见图3。

图3 6A型肺炎球菌多糖结合原液(A)、多糖衍生物(B)、活化多糖(C)、降解多糖(D)、精制多糖(E)、标准品(F)的1H-NMR图谱Fig.3 1H-NMR spectra of bulk of polysaccharide conjugate(A),polysaccharide derivative(B),activated polysaccharide(C),degraded polysaccharide(D),purified polysaccharide(E)and standard polysaccharide(F)of type 6A pneumococcus
2.4 11A型肺炎链球菌的1H-NMR结构11A型肺炎链球菌降解多糖、活化多糖、多糖衍生物指纹区结构与11A型肺炎球菌多糖标准品指纹区结构一致,多糖结合原液多糖指纹区信号不清晰。HDO化学位移为4.6 ppm,5.15、5.04ppm分别为α-GalH1、α-GlcH1信号,2.15ppm为OAc信号。活化多糖7.91、6.78 ppm为DMAP吡啶环质子信号,证明CDAP的降解产物DMAP引入了11A型肺炎链球菌多糖;1.97 ppm为活化多糖中残留溶剂CH3CN的甲基信号。多糖衍生物引入了ADH,2.10、1.50 ppm为ADH亚甲基信号。见图4。

图4 11A型肺炎球菌多糖结合原液(A)、多糖衍生物(B)、活化多糖(C)、降解多糖(D)、精制多糖(E)、标准品(F)的1H-NMR图谱Fig.4 1H-NMR spectra of bulk of polysaccharide conjugate(A),polysaccharide derivative(B),activated polysaccharide(C),degraded polysaccharide(D),purified polysaccharide(E)and standard polysaccharide(F)of type 11A pneumococcus
3 讨论
端基质子区(5.80~4.40 ppm)信号含丰富的多糖结构信息(如重复单位单糖的个数、糖苷键的构型和糖苷键的位置等),与其他信号区比较,端基质子区信号的分辨率最高,因此一般选择端基质子区作为肺炎球菌荚膜多糖血清型别鉴定的“指纹”鉴定区[3]。
多糖超声降解是一个非随机性过程,该过程中最大分子中心附近优先发生链的剪切作用,超声降解不改变重复单元的化学结构,不会引起多糖空间构像的变化,能够有效保持多糖的生物学活性[9],因此降解多糖和多糖的指纹区结构保持一致。活化多糖样品中残留溶剂使活化多糖峰受杂质干扰,另外由于活化多糖不稳定也会影响检测。目前多糖活化一般用CNBr或CDAP作为活化剂[10-12],其中CNBr活化多糖上的羟基后会生成氰酸酯,氰酸酯不稳定会水解为氨基甲酸酯,若多糖邻位存在顺式羟基,氰酸酯会发生重排,生成更稳定的亚胺碳酸酯,氰酸酯和亚胺碳酸酯为活化多糖的活性基团[13]。9V型活化多糖7.12 ppm可能为亚胺碳酸酯信号,而14型活化多糖在该区域无信号,可能是由于亚胺碳酸酯与D2O迅速发生了氢原子交换。另外,氰酸酯不含氢原子,可结合13C-NMR和15N-NMR图谱对CNBr活化的多糖结构进行表征。CDAP在碱性条件下会水解成DMAP,使活化多糖中引入DMAP环质子峰,证明CDAP活化的多糖结构可能为吡啶异脲结构[14-15]。6A和11A型肺炎链球菌多糖衍生物中仍有较小DMAP环质子信号,表明活化多糖在衍生过程中会释放出DMAP,而6A型多糖结合原液中未检测出DMAP环质子信号,与文献中提到的吡啶异脲结构中的DMAP在结合过程中才会完全释放出来的结论一致[14-15]。
多糖结合物中TT载体蛋白无重复结构,无法进行对其进行表征,TT蛋白质子峰混杂在3.5~4.5 ppm区域,结合物分子结构翻滚较慢,蛋白质较高较宽的峰可能会掩蔽多糖信号峰,使多糖信号峰减弱[16-17],但6A型肺炎链球菌多糖结合原液多糖指纹区结构仍有较好的分辨率,且与各型肺炎链球菌多糖标准品一致,表明6A型肺炎链球菌多糖结合原液在结合过程中多糖结构完整性未受到显著影响,采用1H-NMR对其他型别肺炎球菌多糖结合原液的结构鉴定有待进一步研究[18-19]。
9V、14、6A和11A型肺炎链球菌精制多糖、降解多糖、活化多糖、多糖衍生物1H-NMR对比结果表明,肺炎链球菌多糖在降解、活化、衍生过程中结构完整性未受到显著影响[20-23],因此,1H-NMR作为一种灵敏度高且快速的检测方法,可用于肺炎链球菌多糖、降解多糖、活化多糖及多糖衍生物的结构完整性及基团分析,以便更有效地对疫苗进行质量控制,且能指导活化、衍生及结合工艺的优化[5,24-25]。另外,还可结合13C-NMR和15N-NMR图谱对活化多糖活性基团进行分析,但对肺炎球菌多糖结合原液的结构鉴定需进一步研究。
