发酵桑葚汁的新型菌种筛选及润肠通便功能研究
2022-10-24岳停停田洪涛王志刚
张 澜,李 晨,3,张 波,岳停停,田洪涛,,3*,王志刚
(1 河北农业大学食品科技学院 河北保定 071000 2 国家北方山区农业工程技术研究中心 河北保定 071000 3 河北省益生功能性乳制品技术创新中心 河北保定 071000)
桑果又称桑葚(Mulberry),被誉为“民间圣果”“21世纪最佳保健果品”,被原卫生部认证为首批“药食两用”农产品,其营养丰富,富含花青素、多酚等保健功能性成分,具有增强免疫力,抗氧化,促进营养物质代谢及润肠通便等功能[1-2],然而,由于桑葚属于果肉柔软多汁且缺乏坚硬保护性外皮的浆果,不耐贮藏和运输,极易发生霉变腐烂,制约了桑产业的发展。大力发展桑葚加工产业,乃大势所趋[3-4]。目前桑葚加工产业不尽如人意,存在的主要问题是: 桑葚加工产品大多为简单初级低端产品,附加值低、市场竞争力差、经济效益不佳。利用现代生物工程技术面向大健康产业进行桑葚精深加工及其高端产品研发,提高产品的营养保健功能性与附加值以及市场竞争力势在必行。
随着益生菌及其促进人体健康功能性研究的深入,益生菌发酵食品产业在国民经济中占有越来越重要的地位。目前,新型益生菌主要应用于发酵乳制品,而新型益生菌发酵果蔬汁制品仍处于起步阶段,现已有研究报道[5-6],一般采用混菌发酵,很少采用纯种发酵。总体来看,在新型益生菌发酵果蔬汁产业缺乏专用菌种或菌株,发酵桑葚汁的专用菌种或菌株更是空白。筛选适宜发酵桑葚汁的新型特定益生菌是关键。
参照与发酵果蔬汁相关的国家与行业食品质量安全标准,对筛选的新型益生菌发酵桑葚汁的感官、理化与营养成分等指标进行质量分析与评价,对于制定新型益生菌发酵桑葚汁产品的质量与安全标准,实现产业化,具有重要意义。通便功能是《益生菌类保健食品申报与审评规定》(试行)中产品功能性评价的重要指标之一。目前,关于发酵果蔬制品的通便功能研究已见报道,如张想等[7]研究了发酵刺梨果渣对便秘小鼠的润肠通便作用;蒋欣容[8]研究了单一及混合乳酸菌发酵果蔬制品对小鼠的润肠通便作用;Lee 等[9]研究发现乳酸菌发酵的桑叶提取物对便秘大鼠有通便作用。而新型益生菌发酵桑葚汁产品的通便功能尚待探究。
本文以黑珍珠桑葚为原料,以从自然发酵葡萄汁中自行分离、选育并鉴定的12 株新型益生乳酸菌为试验菌株,通过初筛和复筛获得适宜发酵桑葚汁的益生乳酸菌株。分析用其发酵的桑葚汁的品质和润肠通便功能。
1 材料与方法
1.1 试验材料
1.1.1 试验菌株及试验动物 试验菌株: 植物乳杆菌(Lactobacillus plantarum)P9、P17、P29、PJ-L-1、PJ-L-2、PJ-L-4、R1-4、R1-7,短乳杆菌(Lactobacillus breris)R1-3、R1-6、R1-8、R1-12,均从发酵食品中分离选育并鉴定,-80 ℃冰箱保存于河北农业大学食品科技学院发酵工程研究室。
试验动物:SPF 级ICR 雄性小鼠60 只 (体重20 g±1 g),购自济南鑫百诺生物科技有限公司,用于发酵产品润肠通便功能研究。
1.1.2 原料与试剂 桑葚,由河北省石家庄市衡水锦地农业开发公司提供的黑珍珠品种,用于桑葚基质的制备;盐酸洛哌丁胺,西安杨森制药有限公司,用于通便试验;麻仁丸,湖北诺得胜制药有限公司,用于通便试验,作阳性对照;阿拉伯树胶、活性碳粉,天津市天力化学有限公司,用于通便试验中墨汁的制备;一氧化氮(NO)试剂盒、乙酰胆碱酯酶(AchE)活性检测试剂盒,索莱宝科技有限公司,用于通便试验中小鼠血清中神经递质水平的检测;脱脂乳粉、蔗糖,市售,用于桑葚基质的制备。
1.1.3 培养基与溶液
1) 初步的桑葚汁培养基:将桑葚与纯净水按体积比1∶3 打浆,取100 mL 加入已灭菌的玻璃罐中,85 ℃杀菌20 min,冷却至室温备用,用于发酵桑葚汁备选菌株的初筛。
2) 优化的桑葚汁发酵培养基:将桑葚与纯净水按体积比1∶3 打浆,取100 mL 加入已灭菌的玻璃罐中,加入800 mg/kg 复合酶(400 mg/kg 纤维素酶、200 mg/kg 果胶酶、200 mg/kg 脂肪酶)55 ℃酶解120 min,随后加入6%蔗糖、3%脱脂乳粉、0.25%黄原胶,充分混合后,85 ℃杀菌20 min,冷却至室温备用,用于发酵桑葚汁备选菌株的复筛。
3) 盐酸洛哌丁胺:无菌生理盐水配置药物质量浓度6 mg/mL 的盐酸洛哌丁胺混悬液,现用现配,用于通便试验。
4) 墨汁:称取阿拉伯树胶50 g,加水煮沸至溶液透明,再加入活性碳粉末25 g,煮沸3 次,冷却后定容到500 mL,4 ℃保存,用前摇匀,用于通便试验。
5)麻仁丸:无菌生理盐水配置药物质量浓度60 mg/mL 的麻仁丸混悬液,现用现配,用于通便试验。
1.1.4 主要仪器设备 FLC-3 超净台,哈尔滨市东联公司;YXQ-SG46-280S 高压灭菌锅,上海博迅实业有限公司;SPX-150B-Z 型生化培养箱,上海博迅实业有限公司;FA1004A 电子天平,上海精天电子仪器有限公司;电子恒温水浴锅,北京市光明医疗仪器厂;TGL16M 型离心机,长沙市易达科贸公司;752N 型紫外分光光度计,上海精密科学仪器有限公司;美的榨汁机MJ-W BL2521H,芜湖美的生活电器制造有限公司。
1.2 试验方法
1.2.1 工艺流程与技术路线 原料处理(挑选无腐烂、新鲜的桑葚,清洗去梗)→打浆(料水比1∶3打浆,所得桑葚汁定义为桑葚原汁)→酶解(添加400 mg/kg 纤维素酶、200 mg/kg 果胶酶、200 mg/kg脂肪酶,55 ℃,120 min)→调配(蔗糖6%、脱脂乳粉3%、黄原胶0.25%)→装罐→杀菌 (85 ℃,20 min)→接种(3%)→发酵(37 ℃、24 h)→4 ℃冷藏24 h→成品→产品质量分析与评价→润肠通便功能研究
1.2.2 菌株活化 将1.1.1 节备选的12 株菌冻干菌粉分别经液体MRS 培养基[10]37 ℃活化2~3次,使各菌株在24 h 内达到对数末期与稳定初期并使活菌数均达到109CFU/mL 以上,备用。
1.2.3 发酵桑葚汁菌株的筛选
1.2.3.1 发酵桑葚汁备选菌株的初筛 将12 株活化好的乳酸菌分别以3%(体积分数) 接种在初步的桑葚汁培养基(即料水比1∶3 打浆的桑葚原汁)中,37 ℃恒温培养与发酵24 h,分别取样测定总酸(g/kg)与活菌数(CFU/mL)。
1.2.3.2 发酵桑葚汁初筛菌株的复筛 将活化好的初筛乳酸菌分别以3%(体积分数) 接种在优化的桑葚汁发酵培养基中,37 ℃恒温培养与发酵24 h,分别进行感官分析与评价。
1.2.4 发酵桑葚汁产品的质量分析与评价 将复筛获得的最适乳酸菌株根据1.2.1 节工艺流程制备发酵产品,在以下5 个方面对发酵产品进行质量分析与评价。
1.2.4.1 感官指标分析与评价 由15 名经过专业培训的老师和同学组成感官指标评定小组,从色泽(10 分)、香气(20 分)、组织状态(30 分)、口感(40 分)4 个方面对发酵桑葚汁产品进行评分,取平均值记录评分结果。
1.2.4.2 理化与主要功能性成分及益生菌活菌数指标分析与评价 pH 值由PHS-3C 酸度计直接测定;可溶性固形物由手持糖度仪测定;总酸含量按照国标GB/T 12456-2008 测定;总糖含量按照国标GB/T 5009.7 测定;蛋白质含量按照国标GB/T 5009.5;花青素含量采用pH 示差法测定[11];总酚含量采用Foiln-酚法测定[12];采用梯度稀释平板计数法进行益生菌活菌计数。
1.2.4.3 抗氧化指标分析与评价 参照蒋增良等[13]的方法测定DPPH 自由基、ABTS 自由基、羟基自由基、超氧阴离子自由基清除率。
1.2.4.4 安全卫生指标分析与评价 大肠菌群按照GB 4789.3-2016 检测;金黄色葡萄球菌按照GB 4789.10-2016 检测;沙门氏菌按照GB 4789.4-2016 检测;霉菌、酵母菌按照GB 4789.15-2016检测。
1.2.4.5 贮藏稳定性与保质期指标分析与评价发酵产品4 ℃冷藏30 d,每5 d 测定1 次活菌数、pH 值、总酸、总酚、花青素,并结合《感官分析 食品货架期评估(测评和确定)GB/T 38493-2020》[14]标准分析感官及组织状态的变化确定发酵产品的冷藏期。
1.2.5 发酵桑葚汁产品润肠通便功能的研究 将复筛获得的最适乳酸菌株根据1.2.1 节工艺流程制备发酵产品,根据《保健食品检验与评价技术规范》[15]进行润肠通便功能的研究。
1.2.5.1 小鼠分组饲养与造模 将适应喂养1 周的ICR 小鼠随机分组,每组10 只,设置为空白对照组(生理盐水)、模型对照组(蒸馏水并造模)、阳性对照组(麻仁丸5 g/kg bw)、低剂量组(2.5 g/kg bw)、中剂量组(5 g/kg bw)、高剂量组(10 g/kg bw)。早上9 点,空白组按0.1 mL/10g bw 灌胃生理盐水,其余小组同量同法灌胃盐酸洛哌丁胺悬液,连续7 d,造便秘模型,通过试验证实造模成功、小鼠生长状态良好。取造模成功的小鼠,早上9:00 持续同量同法灌胃盐酸洛哌丁胺悬液;下午3:00,阳性对照组灌胃麻仁丸混悬液,低、中、高剂量组的小鼠灌胃乳酸菌发酵桑葚汁,空白组和模型组按0.1 mL/10g bw 灌胃蒸馏水,连续14 d,期间各组小鼠自由饮水与进食,并记录体重(g)。
1.2.5.2 发酵桑葚汁对便秘模型小鼠排便功能影响试验 连续灌胃14 d 相应受试物后,禁食不禁水16 h,模型组、阳性组及低、中、高剂量样品组灌胃盐酸洛哌丁胺(0.1 mL/10g bw),空白对照组同量同法灌胃生理盐水。0.5 h 后,阳性组和低、中、高剂量组灌胃含相应受试物的墨汁,空白、模型组灌胃墨汁,正常进食饮水。从给予墨汁开始,记录每只小鼠首次排黑便的时间和6 h 内排黑便粒数及质量,烘干测定粪便含水量,公式如下。
粪便含水率 (%)=(粪便鲜重-粪便干重)/粪便鲜重×100
1.2.5.3 发酵桑葚汁对便秘模型小鼠小肠运动功能影响试验 小鼠灌胃步骤参照1.2.5.2 节,0.5 h后脱颈处死并解剖,剪取上自幽门、下至回盲部的肠管,将肠管轻轻平铺呈直线,测量小肠总长度与墨汁推进长度。按以下公式计算墨汁推进率。
墨汁推进率(%)=墨汁推进长度(cm)/小肠总长度(cm)×100
1.2.5.4 发酵桑葚汁干预下便秘模型小鼠结肠组织病理切片及HE 染色观察分析 连续灌胃14 d相应受试物后,禁食不禁水16 h,脱颈处死并解剖,剪取1~2 cm 结肠置于4%多聚甲醛中,固定48 h,委托武汉市皮诺飞生物科技有限公司进行各组小鼠的小肠组织病理切片及HE 染色。
1.2.5.5 发酵桑葚汁对便秘模型小鼠血清中神经递质水平的影响 连续灌胃14 d 相应受试物后,禁食不禁水16 h,眼球取血,静置2 h 后,离心取血清,对小鼠血清中一氧化氮(NO)、乙酰胆碱酯酶(AchE)进行测定。
1.3 数据处理
试验数据(重复次数n=3)采用SPSS 软件,首先进行方差分析即F 检验(或t 检验)处理间差异显著性(F=MSA/MSe),然后在方差分析处理间差异显著性基础上,用最小极差法进行多重比较。
2 结果与分析
2.1 发酵桑葚汁的菌种筛选
2.1.1 发酵桑葚汁备选菌株的初筛 根据1.2.3.1节试验方法进行发酵桑葚汁备选菌株的初筛,结果见表1、表2。
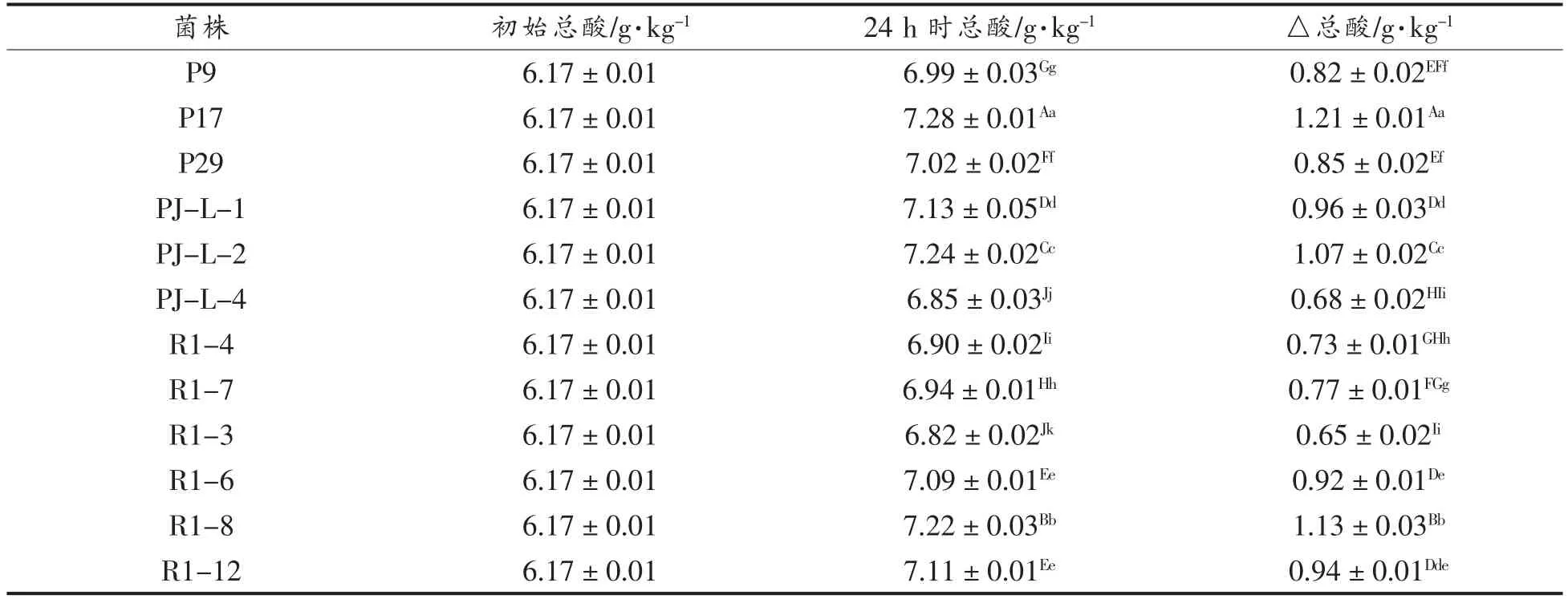
表1 12 株乳酸菌在初步的桑葚汁培养基中发酵24 h 的总酸变化Table 1 Changes of total acid of 12 strains of lactic acid bacteria in the preliminary mulberry juice medium for 24 h fermentation
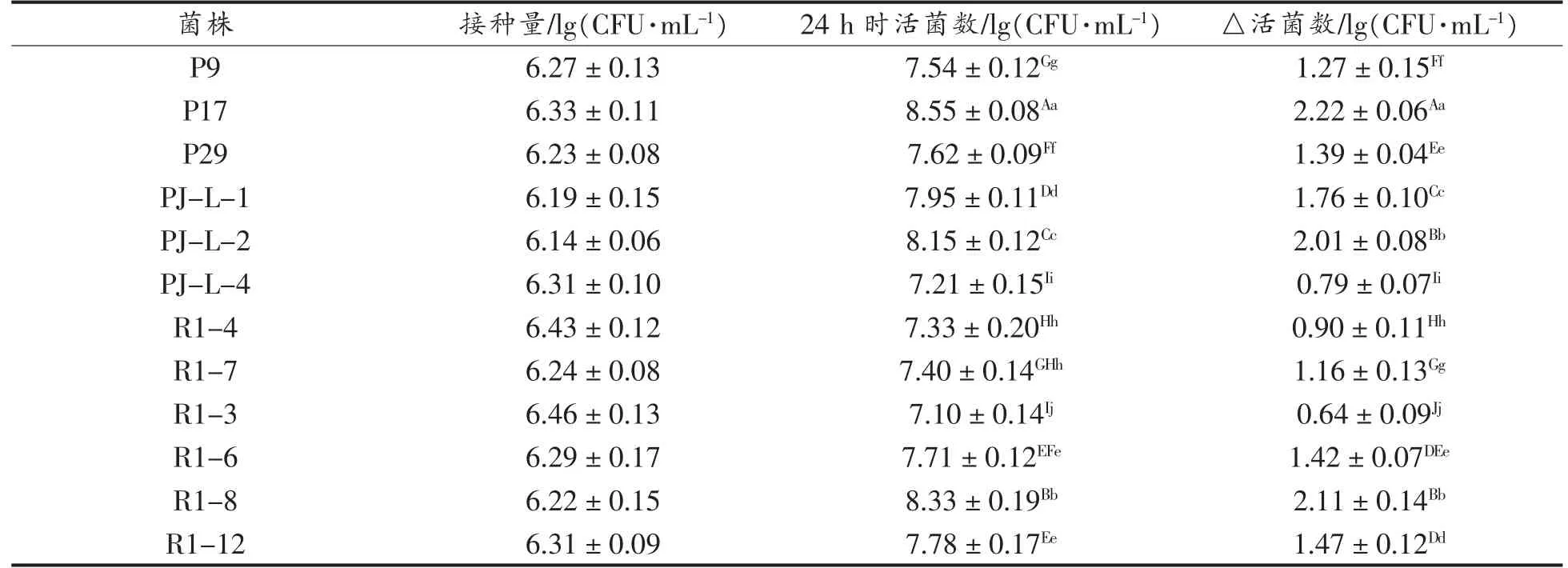
表2 12 株乳酸菌在初步的桑葚汁培养基中发酵24 h 的活菌数变化Table 2 Changes in the number of viable bacteria of 12 strains of lactic acid bacteria in the preliminary mulberry juice medium for 24 hours of fermentation
由表1可见:12 株备选乳酸菌分别在初步的桑葚汁培养基中发酵后总酸含量相对于发酵前均有提高,但菌株之间发酵产酸后的总酸含量存在极显著差异(P<0.01)。其中,植物乳杆菌P17 在初步的桑葚汁培养基中发酵产酸活力最强,总酸含量达到(7.28±0.01)g/kg;而植物乳杆菌PJ-L-2 与短乳杆菌R1-8 在初步的桑葚汁培养基中发酵产酸活力次之;其它乳酸菌株在初步的桑葚汁培养基中发酵产酸的△总酸变化幅度均没有超过1.00 g/kg。
乳酸菌的产酸能力是衡量发酵性能的重要指标,上述结果表明:多数新型益生乳酸菌在初步的桑葚汁培养基中均具有发酵产酸活力,但发酵产酸活力较弱。
由表2看出:12 株备选乳酸菌均能在初步的桑葚汁培养基中发酵生长,但菌株之间发酵生长后的活菌数存在极显著差异(P<0.01)。其中,植物乳杆菌P17、植物乳杆菌PJ-L-2 和短乳杆菌R1-8 此3 株乳酸菌在初步的桑葚汁培养基中发酵生长力显著高于其它乳酸菌株,发酵生长后的活菌数均达到1×108CFU/mL 以上,与发酵前初始活菌数相比,均提高了2 个lg 数量级以上;而其它乳酸菌株在初步的桑葚汁培养基中发酵生长力相对较弱,发酵生长后的活菌数均在1×107CFU/mL 至1×108CFU/mL 之间,与发酵前初始活菌数相比,提高幅度均在1~2 个lg 数量级之间或1 个lg 数量级以下。
乳酸菌的发酵生长力即发酵后的活菌数是衡量乳酸菌发酵产品益生功能性极其重要的指标,上述结果表明: 多数新型益生乳酸菌在初步的桑葚汁培养基中均具有发酵生长力,但发酵生长力较弱。综合分析12 株备选乳酸菌在初步的桑葚汁培养基中发酵生长力即发酵后活菌数及发酵产酸活力,确定植物乳杆菌P17、植物乳杆菌PJ-L-2和短乳杆菌R1-8 作为初筛菌株进行下一步复筛。
2.1.2 发酵桑葚汁初筛菌株的复筛 根据1.2.3.2节试验方法,进行初筛3 菌株在优化的桑葚汁培养基中发酵产品的感官评价即复筛,结果见图1。
由图1显示: 植物乳杆菌P17 发酵的产品感官评分较高,与植物乳杆菌PJ-L-2、短乳杆菌R1-8 发酵产品相比,差异极显著(P<0.01),植物乳杆菌P17 发酵的产品色泽明亮,组织状态均一稳定,口感柔和,酸甜适中,香气浓郁;而植物乳杆菌PJ-L-2 发酵的产品组织状态不稳定,口感不协调;短乳杆菌R1-8 发酵的产品口感寡淡,发酵香气不足。因此确定:植物乳杆菌P17 作为发酵桑葚汁产品的复筛益生菌株。

图1 初筛3 株乳酸菌在优化的桑葚培养基中发酵24 h 后产品的感官评分Fig.1 The sensory score of the product after initial screening of 3 strains of lactic acid bacteria in the optimized mulberry medium for 24 h fermentation
2.2 发酵桑葚汁产品的质量分析与评价
2.2.1 感官指标分析与评价 根据1.2.4.1 节试验方法进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品感官指标分析与评价,结果见图2。
由图2可知: 植物乳杆菌P17 纯种发酵桑葚汁产品感官评分综合分值为(92.00±1.34)分,深紫色泽,有光泽,组织状态均匀稳定,口感柔和,酸甜适中,香气浓郁。

图2 植物乳杆菌P17 纯种发酵桑葚汁产品感官评分图Fig.2 Sensory score chart of Lactobacillus plantarum P17 pure fermented mulberry juice product
2.2.2 理化与主要功能性成分及益生菌活菌数指标分析与评价 根据1.2.4.2 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品理化与功能性成分指标分析与评价,结果见表3。
由表3可知: 在发酵后产品的理化与主要营养指标中,总糖含量降至16.13 g/kg,pH 值降为3.94,总酸含量升至7.48 g/kg,蛋白质含量降为23.65 μg/mL,可溶性固形物含量升至11.11 Brix%,说明: 植物乳杆菌P17 利用了优化后桑葚汁发酵培养基中的可发酵性糖类物质而产生酸类物质,使总糖含量降低、pH 值下降、总酸含量上升;同时,P17 菌株可能会利用培养基中可发酵性糖、可发酵性肽等物质产生可溶性的低聚糖、小肽和氨基酸,使蛋白质含量降低、可溶性固形物含量上升。在发酵后产品的主要功能性指标中,总酚含量升至199.59 μg/mL,花青素含量为29.12 mg/L,说明:P17 菌株在发酵桑葚汁后,产生了较多的多酚物质;而花青素在发酵过程中有所损失。在发酵后产品的益生菌活菌数指标中,植物乳杆菌P17 益生菌活菌数达到8.70×108CFU/mL,说明利用植物乳杆菌P17 菌株纯种发酵优化后桑葚汁是可行的。

表3 植物乳杆菌P17 发酵桑葚汁产品理化指标和主要功能性成分及益生菌活菌数指标检测结果Table 3 Test results of physical and chemical indexes and main functional components of mulberry juice fermented by Lactobacillus plantarum P17 and the number of probiotics
上述结果表明: 虽然植物乳杆菌P17 发酵优化后桑葚培养基后某些生物活性成分(总糖、蛋白质、花青素)有所降低,但发酵产品仍具有较高的生物活性与营养功能性。同时提示:由于可溶性固形物含量提高、花青素含量降低,应进一步检测发酵产品中低聚糖、活性小肽、氨基酸与维生素的含量;在工艺中应进一步采取降低花青素损失的措施。
2.2.3 抗氧化指标分析与评价 抗氧化指标也是衡量发酵果蔬汁的重要功能指标[16],根据1.2.4.3节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品抗氧化指标检测,结果见表4。

表4 植物乳杆菌P17 发酵桑葚汁产品抗氧化指标检测结果Table 4 Test results of antioxidant indexes of fermented mulberry juice products by Lactobacillus plantarum P17
由表4可见,与未发酵桑葚汁相比,发酵产品的4 项体外抗氧化指标均显著提高 (P<0.01),其中,DPPH 自由基清除率提高了14.92%达到85.12%,羟自由基清除率提高了12.20%达到36.41%,ABTS 自由基清除率提高了11%达到80.35%,超氧阴离子自由基清除率提高了11.95%达到56.59%,表明经益生乳酸菌植物乳杆菌P17 纯种发酵后的桑葚汁产品具有较高的抗氧化活性。
2.2.4 安全卫生指标分析与评价 根据1.2.4.4节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品安全卫生指标检测,结果见表5。

表5 植物乳杆菌P17 发酵桑葚汁产品安全卫生指标检测结果Table 5 Test results of safety and sanitation indexes of mulberry juice fermented by Lactobacillus plantarum P17
由表5看出: 在发酵产品的安全卫生指标检测中,未检出沙门氏菌、大肠杆菌菌群、金黄色葡萄球菌以及霉菌和酵母菌等致病菌和条件致病菌,符合国家卫生部颁布的《食品安全国家标准饮料》GB 7101-2015。
2.2.5 贮藏稳定性与保质期指标分析与评价 根据1.2.4.5 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品贮藏稳定性与保质期指标试验,结果见图3。

图3 植物乳杆菌P17 发酵桑葚汁产品4 ℃贮藏30 d 内活菌数、pH 值、总酸、总酚、花青素的变化Fig.3 Changes in the number of viable bacteria,pH,total acid,total phenols,and anthocyanins of mulberry juice fermented by Lactobacillus plantarum P17 stored at 4 ℃for 30 days
图3显示: 发酵产品在4 ℃冷藏30 d 内,活菌数、pH 值、总酚、花青素呈整体下降趋势,总酸呈上升趋势,说明:P17 菌株在发酵产品中可能仍在进行缓慢的代谢活动,但由于酸和冷的胁迫,活菌数逐渐下降,同时使pH 值、总酚、花青素逐渐下降,总酸上升。结合《感官分析 食品货架期评估(测评和确定)》GB/T 38493-2020 标准[14],发酵产品4 ℃冷藏第30 天,活菌数为8.9×107CFU/mL,pH 值下降至3.48,总酸含量上升至8.86 g/kg,总酚含量下降为156.25 μg/mL,花青素含量下降为27.15 mg/L,发酵桑葚汁出现轻微分层现象,口感略酸,感官品质降低。发酵产品4 ℃冷藏第25 天,活菌数为9.5×107CFU/mL,pH 值为3.53,总酸为8.47 g/kg,总酚为162.95 μg/mL,花青素的含量为27.44 mg/L,仍保持着较高的生物活性,且发酵桑葚汁组织状态均匀稳定,口感良好。因此确定:植物乳杆菌P17 纯种发酵桑葚汁产品的4 ℃冷藏期为25 d。
2.3 发酵桑葚汁产品润肠通便功能的研究
2.3.1 发酵桑葚汁对便秘模型小鼠排便功能的影响 根据1.2.5.2 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品对便秘模型小鼠排便功能影响试验,结果见表6。
由表6可见,模型组与空白组相比,小鼠的首粒排黑便时间,6 h 内排黑便粒数与质量及粪便含水率均有极显著性差异(P<0.01),说明:小鼠便秘模型造模可行。阳性组与发酵桑葚汁剂量组均在不同程度上缩短了首粒排黑便时间,增加了6 h内排便粒数及质量,其中阳性组、高剂量组与空白组最接近,且与模型组存在极显著差异(P<0.01)。由粪便含水率可知:随着发酵桑葚汁剂量的升高,小鼠粪便的含水率明显提高,中、高剂量组、阳性组均与空白对照组无显著差异(P>0.05)。表明:发酵桑葚汁产品对便秘模型小鼠排便功能具有明显的促进作用。
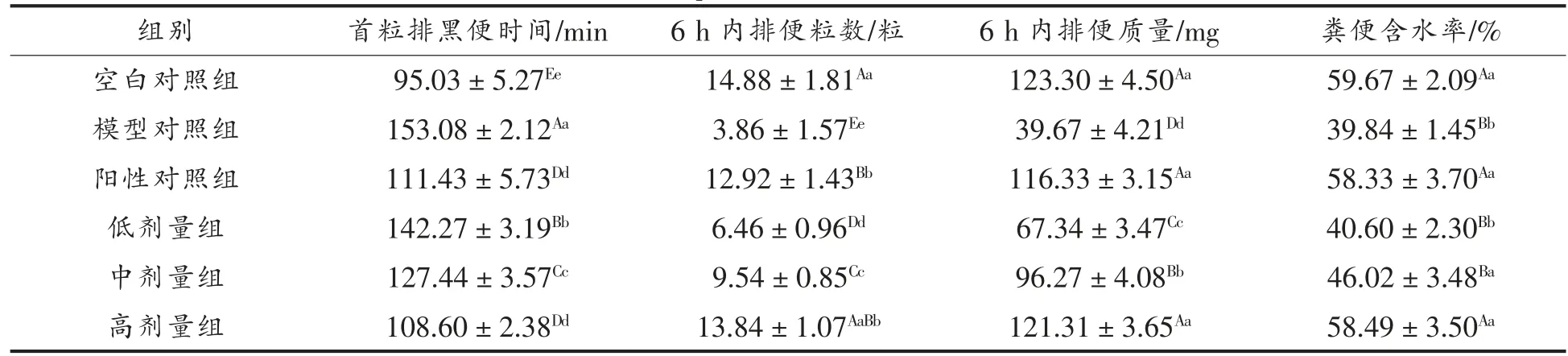
表6 植物乳杆菌P17 发酵桑葚汁产品对便秘模型小鼠排便功能的影响Table 6 Effect of mulberry juice fermented by Lactobacillus plantarum P17 on defecation function in constipation model mice
2.3.2 发酵桑葚汁对便秘模型小鼠小肠运动功能的影响 根据1.2.5.3 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品对便秘模型小鼠的小肠运动功能影响试验,结果见表7。

表7 植物乳杆菌P17 发酵桑葚汁产品对便秘模型小鼠小肠墨汁推进率的影响Table 7 Effect of mulberry juice product fermented by Lactobacillus plantarum P17 on intestinal ink advancement rate of constipation model mice
由表7看出: 空白组小鼠的小肠墨汁推进率与模型对照组有极显著差异(P<0.01),说明小鼠便秘模型造模可行。阳性组、中、高剂量组的墨汁推进率与空白对照组无显著差异(P>0.05),表明:发酵桑葚汁产品能够显著促进便秘模型小鼠的肠道运动并缩短粪便在小肠内的停留时间。
2.3.3 发酵桑葚汁干预下便秘模型小鼠结肠组织病理切片及HE 染色观察分析 根据1.2.5.4 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品干预下便秘模型小鼠结肠组织病理切片及HE 染色观察,结果见图4。
图4显示: 空白组小鼠结肠切面结构清晰完整,绒毛排列整齐;而模型组小鼠结肠切面绒毛萎缩粘连,黏膜层可见少量炎性细胞浸润,说明:盐酸咯哌丁胺在诱导便秘模型时,造成了绒毛损伤。与模型组相比,发酵桑葚汁灌胃干预的剂量组,小鼠结肠绒毛损伤程度明显低于模型对照组。通过比较低、中、高剂量组与阳性对照组小鼠结肠组织切片可以看出,阳性对照组与中、高剂量组小鼠结肠黏膜腺体排列整齐,绒毛损伤程度较轻,只在中剂量组小鼠结肠的固有层存在少许炎性细胞浸润,其它未见明显异常。表明提高发酵桑葚汁的干预剂量对便秘模型小鼠的结肠病变具有明显的改善和保护作用。

图4 各组不同处理的小鼠结肠组织病理切片及HE 染色照片(H&E×200)Fig.4 Pathological sections and HE staining micrographs of mouse colon tissues of different treatments in each group (H&E×200)
2.3.4 发酵桑葚汁对便秘模型小鼠血清中神经递质水平的影响 根据1.2.5.5 节试验方法,进行复筛菌株植物乳杆菌P17 纯种发酵桑葚汁产品对便秘模型小鼠血清中神经递质水平的影响试验,结果见表8。
由表8可知: 模型组小鼠血清中一氧化氮(NO)含量与空白组存在极显著差异(P<0.01),说明小鼠便秘模型造模可行。阳性组与高剂量组NO含量显著降低,表明发酵桑葚汁能有效地减少了小鼠血清中NO 的生成,增强了小鼠肠道的蠕动能力。各受试物组与模型组相比,小鼠血清中乙酰胆碱酯酶(AchE)活力均有所提高,其中高剂量组与阳性组的小鼠血清中AchE 活力之间无显著差异(P>0.05),且最接近空白组小鼠血清中AchE 活力,表明发酵桑葚汁可促进AchE 的释放并改善小鼠便秘状况。

表8 植物乳杆菌P17 发酵桑葚汁产品对便秘模型小鼠血清中神经递质水平的影响Table 8 Effect of mulberry juice fermented by Lactobacillus plantarum P17 on serum neurotransmitter levels in constipation model mice
3 讨论
如今桑产业被公认为是兼顾社会、经济、生态三大效益的新一代健康黄金农业,桑葚被誉为“民间圣果”、“二十一世纪最佳保健果品”并被卫生部认证为首批“药食两用”农产品,但桑葚不耐贮藏,极易腐烂,造成经济损失;在目前桑葚加工产业中,简单初级低端产品多,精深加工高端产品少,附加值低、市场竞争力差、经济效益不佳,因而制约了桑产业的发展。随着益生菌研究的深入及其促进人体健康功能性的揭示,益生菌发酵食品产业在国民经济中占有越来越重要的地位,当今以植物乳杆菌、干酪乳杆菌、鼠李糖乳杆菌、短乳杆菌、发酵乳杆菌、罗伊氏乳杆菌等为代表的第二代新型益生菌较以双歧杆菌、嗜酸乳杆菌为代表的第一代益生菌显示出更加优良的特性和巨大的应用价值,而受到全球的高度重视。但目前第二代新型益生菌主要应用于发酵乳制品行业;在发酵果蔬制品行业的研究与应用,处于起步阶段,主要是缺乏专用菌种或菌株;而对于发酵桑葚汁制品的专用菌种或菌株,更是处于空白状态。因此,利用现代生物工程技术面向大健康产业进行桑葚精深加工,研发融合桑葚与益生菌二者功能特性于一身,集感官风味和多种营养保健功能于一体的第二代新型益生菌发酵桑葚汁产品,提高产品的功能性与附加值及市场竞争力,满足人民日益增长的对营养健康食品的需求乃大势所趋,势在必行。
筛选适宜发酵桑葚汁制品的特定新型益生菌,是研发新型益生菌发酵桑葚汁制品的关键环节和首要任务。根据目前已有的其它发酵果蔬汁的研究报道: 大多采用益生菌株与传统酸奶菌株(保加利亚乳杆菌和嗜热链球菌)混种发酵[17-18];有些采用益生菌混合发酵[19-20]。传统酸奶菌株虽然对人体有益,但属于人体肠道“过路菌”,不具有定殖于人体肠道的益生特性,如果采用益生菌与传统酸奶菌株混种发酵,那么发酵产品中益生菌的益生功能的发挥则会大打折扣;而益生菌混合发酵需要解决菌种或菌株之间相互协同或抑制彼此益生功能的发挥、接种顺序与发酵调控等问题。本研究以黑珍珠桑葚为原料,以从发酵食品中自行分离并鉴定出的12 株新型益生乳酸菌为试验菌株,通过初筛和复筛,获得了1 株适宜发酵桑葚汁的新型益生菌株即植物乳杆菌P17,该菌株在初步的桑葚汁培养基中发酵的产酸活力与生长能力以及在优化后的桑葚汁培养基中发酵后的感官风味均显著优于其它益生乳酸菌株;该菌株在初步的桑葚汁培养基中发酵后的活菌数达到8.55×108CFU/mL,在优化后的桑葚汁培养基中发酵后的感官风味良好;对P17 菌株的前期研究表明:该菌株不仅具有诸多的益生功能,而且属于安全的(GRAS,Generally Regard As Saft) 食品级微生物,这为下一步研发新型益生菌植物乳杆菌P17纯种发酵桑葚汁功能性产品及其工艺,奠定了基础。今后尚有待进一步研究植物乳杆菌P17 在发酵桑葚汁过程中的风味物质与有益代谢产物形成机制,在发酵贮藏销售食用以及进入人体胃肠道过程中受各种环境胁迫的耐受性与产品质量和功能的关系及其调控机制,发酵产品的功能及其功能机制以及高效发酵剂制备的原理与技术等。
目前,已出台了与益生菌发酵食品或发酵果蔬汁及果蔬汁相关的国家与行业食品质量安全标准,包括《中华人民共和国轻工行业标准 果蔬发酵汁》QB/T 5356-2018、《中华人民共和国农业行业标准 绿色食品 果蔬汁饮料》NY/T 434-2016、《中华人民共和国轻工行业标准 植物酵素》QB/T 5323-2018、《中国生物发酵产业协会团体标准食用植物酵素》T/CBFIA 08003-2017、《食品安全国家标准饮料》GB 7101-2015 与《食品安全国家标准 发酵乳》GB 19302-2010。但桑葚作为典型的营养保健果品,其益生菌发酵产品的相关质量安全标准,尚未出台。本研究参照相关国家与行业食品质量安全标准,对复筛新型益生菌植物乳杆菌P17 纯种发酵桑葚汁产品感官、理化与营养成分、活菌数与功能性成分、抗氧化性、安全卫生、贮藏稳定性与保质期等指标进行了质量分析与评价,结果表明:发酵产品呈深紫色,有光泽,组织状态均匀稳定,具有浓郁的果香与发酵香气,口感柔和,酸甜适口;理化与营养成分符合相关国家与行业标准,益生菌活菌含量达到8.7×108CFU/mL 且富含多酚物质(199.59 g/kg ± 0.12 g/kg)与花青素(29.12 mg/L±0.06 mg/L);具有较强的抗氧化能力;无致病菌和条件致病菌检出;4 ℃保质期为25 d,益生菌活菌数仍在9.5×107CFU/mL,下降不足1个lg 数量级。这对于进一步制定新型益生菌发酵桑葚汁产品的质量与安全标准,实现新型益生菌发酵桑葚汁产品的产业化提供了科学依据。但考虑到发酵产品中可溶性固形物含量提高与花青素含量的降低,今后有待进一步检测发酵产品中低聚糖、活性小肽、氨基酸与维生素的含量,并在工艺中进一步采取降低花青素损失的措施。
通便功能是《益生菌类保健食品申报与审评规定》(试行)中功能性评价的重要指标之一,目前与益生菌发酵食品或发酵果蔬汁及果蔬汁相关的通便功能的研究已有报道[7-9]。而益生菌发酵桑葚汁产品通便功能的研究未见报道,有必要进一步探明。本文研究了复筛新型益生菌植物乳杆菌P17 纯种发酵桑葚汁产品对试验小鼠的润肠通便功能,进行了便秘模型小鼠结肠组织病理切片及HE 染色观察,检测了便秘模型小鼠血清中神经递质水平,动物试验结果表明:发酵产品促进了便秘模型小鼠肠道运动与内容物排放,缩短了排便时间,提高了粪便的含水率及质量,减轻了由便秘引起的结肠绒毛损伤,缓解了由便秘引起的结肠病变,有利于小鼠血清中乙酰胆碱酯酶(AchE)的释放并改善了小鼠的便秘状况。本研究结果对于研发新型益生菌发酵桑葚汁功能性产品具有重要意义。
综上所述,本研究筛选获得了1 株适宜发酵桑葚汁的新型益生菌即植物乳杆菌P17,其发酵产酸活力、生长力与活菌数、感官风味良好;根据相关国家与行业食品质量安全标准,对植物乳杆菌P17 纯种发酵桑葚汁产品进行了质量分析与评价,发酵产品呈深紫色、有光泽、组织状态均匀稳定、具有浓郁的果香与发酵香气、口感柔和、酸甜适口,理化与营养成分符合相关国家与行业标准,益生菌活菌含量达到8.7×108CFU/mL 且富含多酚物质(199.59 g/kg±0.12 g/kg)与花青素(29.12 mg/L±0.06 mg/L),具有较强的抗氧化能力,无致病菌和条件致病菌检出,4 ℃保质期为25 d,益生菌活菌数仍在9.5×107CFU/mL,下降不足1 个lg 数量级;植物乳杆菌P17 纯种发酵桑葚汁产品缩短了便秘模型小鼠排便时间,促进了肠道运动与内容物排放,减轻了由便秘引起的结肠绒毛损伤,缓解了由便秘引起的结肠病变,有利于小鼠血清中乙酰胆碱酯酶(AchE)的释放并改善了小鼠的便秘状况。本研究为进一步研发及工业化生产新型益生菌发酵桑葚汁功能性产品提供了理论依据和技术支撑,进而提高了桑葚加工产品的营养保健功能和附加产值,开辟了桑葚精深加工产品的新途径,也为新型益生菌发酵其它果蔬功能性产品提供了借鉴指导。
