纳武利尤单抗联合常规化疗对老年中晚期非小细胞肺癌T细胞、NK细胞的影响及安全性
2022-10-21南通市通州区人民医院肿瘤科江苏南通226300
张 莉 (南通市通州区人民医院肿瘤科,江苏 南通 226300)
非小细胞肺癌(NSCLC)多发于老年人群,隐匿性强,早期缺乏特异性表现,75%左右的患者确诊时已处于Ⅲ~Ⅳ期,手术疗效差,术后复发率达25%~50%[1]。药物化疗是治疗中晚期NSCLC重要手段,但实践证实化疗会引发一系列不良反应,影响老年患者化疗完成率,且远期效果欠佳[2]。随着肿瘤研究不断深入,发现程序性死亡受体-1(PD-1)与程序性死亡受体配体-1(PD-L1)结合引发的免疫逃避作用是治疗肿瘤有效靶点,为NSCLCD治疗提供新思路[3]。纳武利尤单抗属PD-1抑制剂,近年来作为自身免疫抗癌新型药物逐渐在临床得到应用。本研究选取96例老年中晚期NSCLC患者为研究对象,探讨纳武利尤单抗联合常规化疗的疗效。
1 资料与方法
1.1一般资料:选取2019年7月~2021年7月在我院接受治疗的96例老年中晚期NSCLC患者为研究对象,按随机抽签法分为单一组和联合组各48例。单一组男女比例为19:29;年龄60~74岁,平均(66.46±3.13)岁;TNM分期:12例Ⅲa期,20例Ⅲb期,16例Ⅳ期;病理类型:30例腺癌,12例鳞癌,6例腺鳞癌;体重指数(BMI)18.57~27.38 kg/m2,平均(22.41±1.82)kg/m2。联合组男女比例为17∶31;年龄60~75岁,平均(67.55±3.62)岁;TNM分期:9例Ⅲa期,21例Ⅲb期,18例Ⅳ期;病理类型:33例腺癌,10例鳞癌,5例腺鳞癌;BMI18.21~27.09 kg/m2,平均(22.88±2.03)kg/m2。两组一般资料(病理类型、年龄、男女比例、TNM分期、BMI)比较,差异无统计学意义(P>0.05),有可比性。本研究由本院医学伦理委员会审核通过。
1.2纳入和排除标准:纳入标准:①均对本研究知情、同意;②符合《非小细胞肺癌分子病理检测临床实践指南(2021版)》[4]中NSCLC诊断标准,经病理组织活检证实;③TNM分期为Ⅲa~Ⅳ期;④卡氏评分≥60分;⑤对化疗耐受;⑥首次接受治疗;⑦病历资料完整。排除标准:①预期寿命<6个月;②伴有免疫系统疾病、心脑血管疾病、血液系统疾病、代谢系统疾病、传染性疾病、肝肾功能不全;③癌细胞向远处转移或合并其他部位良恶性肿瘤;④伴有精神疾病;⑤过敏体质;⑥年龄<60岁;⑦依从性差,不配合治疗。
1.3方法:①单一组:予以常规化疗,静脉滴注培美曲塞(国药一心制药有限公司,国药准字:H20080169,规格:0.5 g),500 mg/m2,每3 w 1次,3 w为1个周期,治疗4个周期。②联合组:在单一组基础上静脉滴注纳武利尤单抗(Bristol-Myers Squibb Holdings,批准文号:S20180015,规格:10 ml∶0.1 g/瓶),3 mg/kg,滴注时间为1 h,每2 w 1次,2 w为1个周期,治疗4个周期。
1.4观察指标
1.4.1治疗总有效率:治疗4个周期后评估效果,评估标准为:病灶完全消失,并维持4 w及以上为完全缓解;病灶直径总和减少>30%,并维持4 w及以上为部分缓解;病灶直径总和增加>20%或有新病灶出现为疾病进展;处于疾病进展与部分缓解之间的为疾病稳定[5]。(完全缓解+部分缓解)/总例数×100%=总有效率。
1.4.2免疫功能、肿瘤标志物水平:比较两组治疗前与治疗4个周期后免疫功能[T细胞(CD3+、CD4+、CD8+)、NK细胞]、肿瘤标志物[癌胚抗原(CEA)、糖类抗原125(CA125)、细胞角蛋白19片段(CY211)]水平,抽取患者5 ml晨起空腹静脉血,离心(3 000 r/min,10 min,15 cm)分离血清,使用流式细胞仪[艾森生物(杭州)有限公司,NovoCyte D1041]以间接免疫荧光法测定CD3+、CD4+、CD8+、NK细胞水平,使用全自动生化分析仪(希森美康公司,JCA-BM6010/C)以化学发光法测定CEA、CA125、CY211水平。
1.4.3沉默信息调节因子1(SIRT1)阳性率、微小核糖核酸-21(miR-21)表达量:比较两组治疗前与治疗4个周期后SIRT1阳性率、miR-21表达量,取患者肿瘤组织保存于液氮中,取适量组织制作成组织匀浆,以实时荧光定量PCR法测定miR-21表达量,对剩余组织进行免疫组化,借助高倍镜观察,选10个视野,共1 000个细胞,SIRT1阳性率即为染为棕黄色颗粒细胞占1 000个细胞的比例。
1.4.4不良反应:不良反应包括骨髓抑制、恶心呕吐、肝肾功能受损、血小板减少、白细胞减少、贫血等。

2 结果
2.1两组患者治疗总有效率比较:联合组治疗总有效率54.17%,高于单一组的31.25%,差异均有统计学意义(P<0.05)。见表1。
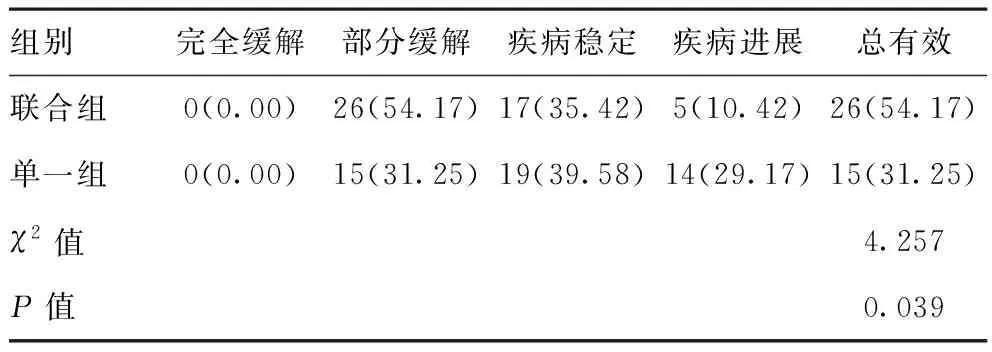
表1 两组患者治疗总有效率比较[n(%),n=48]
2.2两组患者治疗前后免疫功能:两组治疗前CD3+、CD4+、CD8+、NK细胞水平比较,差异无统计学意义(P>0.05);治疗4个周期后,联合组CD3+、CD4+、NK细胞水平均比治疗前升高,CD8+水平比治疗前下降;单一组CD3+、CD4+、NK细胞水平均比治疗前下降,CD8+水平比治疗前升高;联合组CD3+、CD4+、NK细胞水平较单一组高,CD8+水平较单一组低,差异均有统计学意义(P<0.05)。见表2。
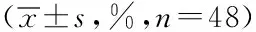
表2 两组患者治疗前后免疫功能比较
2.3两组患者治疗前后肿瘤标志物水平比较:两组治疗前CEA、CA125、CY211水平比较,差异无统计学意义(P>0.05);两组治疗4个周期后CEA、CA125、CY211水平均比治疗前下降,且联合组低于单一组,差异有统计学意义(P<0.05)。见表3。

表3 两组患者治疗前后肿瘤标志物水平比较
2.4两组患者治疗前后SIRT1阳性率、miR-21表达量比较,两组治疗前SIRT1阳性率、miR-21表达量比较,差异无统计学意义(P>0.05);治疗4个周期后两组SIRT1阳性率、miR-21表达量均比治疗前下降,且联合组低于单一组,差异有统计学意义(P<0.05)。见表4。

表4 两组患者治疗前、后SIRT1阳性率、miR-21表达量比较
2.5两组患者不良反应比较:两组骨髓抑制、恶心呕吐、肝肾功能受损、血小板减少、白细胞减少、贫血等发生率比较差异均无统计学意义(P>0.05)。见表5。

表5 两组患者不良反应比较[n(%),n=48]
3 讨论
培美曲塞是一种多靶点化疗药物,可阻碍DNA原料合成,抑制癌细胞生长,从而促进癌细胞凋亡,发挥抗癌作用[6]。但化疗会带来一定不良反应,影响机体各项功能,降低免疫力,部分患者会因难以耐受化疗不良反应中断治疗。纳武利尤单抗作为细胞免疫疗法常用药物,通过增强机体免疫功能,达到治疗肿瘤目的,安全有效[7]。吕厚宽等[8]学者指出,对于NSCLC患者采用化疗药物与纳武利尤单抗联合治疗,疗效明显高于单一使用化疗药物。本研究发现,联合组总有效率较单一组高(P<0.05),与上述研究结果相符。这是由于纳武利尤单抗能稳定肿瘤局部微环境,增强免疫细胞增殖能力,更好杀伤癌细胞,抑制癌细胞生长,从而取得满意疗效。
免疫功能方面,细胞免疫发挥重要作用,T淋巴细胞在免疫内环境调节与维持中意义重大,NSCLC患者免疫功能受损严重,加之化疗药物在杀灭癌细胞的同时,也会减弱免疫功能,导致CD3+、CD4+明显减少,CD8+明显增加,NK细胞是介导免疫应答主要细胞,在癌细胞发生免疫逃逸过程中其功能明显下降,数量明显减少[9-10]。本研究数据说明,相较于单一使用化疗药物,纳武利尤单抗与化疗联用能改善老年中晚期NSCLC患者免疫功能。分析原因可能为纳武利尤单抗既能减轻化疗药物带来的免疫抑制作用,增强机体耐受性,又能提高NK细胞的活性,从而改善机体免疫功能。
肿瘤标志物方面,CEA、CA125、CY211在NSCLC诊断、疗效与预后判断中敏感度与特异度较高,相关文献报道,NSCLC患者CEA、CA125、CY211水平明显较健康人群高,且与临床分期成正比[11-13]。本研究还对SIRT1阳性率、miR-21表达量进行探讨,SIRT1属SIRTUIN家族,正常情况下发挥细胞保护作用,还参与肿瘤发生与发展,在癌组织中呈高表达,并与淋巴结转移与分期等情况相关;miR-21是miRNA家族成员,参与细胞分化、增殖等机体重要生理过程,相关研究证实,其在肺癌患者肿瘤组织中表达异常,其表达水平与淋巴结分期呈正相关[14-15]。本研究使用纳武利尤单抗联合化疗药物培美曲塞治疗NSCLC,结果显示联合组CEA、CA125、CY211水平与SIRT1阳性率、miR-21表达量均低于单一组(P<0.05),提示该治疗方案能降低肿瘤标志物水平,抑制SIRT1与miR-21表达,可能在于纳武利尤单抗能抑制肿瘤血管内皮细胞增殖与迁移,减少新生血管生成,达到抑制肿瘤发生与发展的目的。本研究还发现,两组骨髓抑制、恶心呕吐、肝肾功能受损、血小板减少、白细胞减少、贫血等发生率比较差异均无统计学意义(P>0.05),说明纳武利尤单抗的应用不增加不良反应,患者耐受程度高,更易于患者接受。
综上所述,常规化疗联合纳武利尤单抗方案应用于老年中晚期NSCLC治疗中效果显著,能改善患者免疫功能,降低肿瘤标志物水平,抑制SIRT1与miR-21表达,且安全性高。但本研究也有一定不足之处,如纳武利尤单抗在我国上市时间较短,费用高昂,临床应用较少,后续需扩大样本量深入研究本治疗方案。
