鳜鱼内脏副产物中鱼油的精炼及其品质分析
2022-10-20吴永祥吴丽萍胡长玉
吴永祥 雍 张 王 茵 吴丽萍 胡长玉
(黄山学院生命与环境科学学院,安徽 黄山 245041)
鳜鱼(Sinipercachuatsi)是鮨科(Serranidae)鳜属(SinipercaGill)的鱼类,具有较高的经济价值[1-2]。据统计[3],2018年鳜鱼年产量达到31.59万t,其市场需求量和养殖规模逐年递增。目前,鳜鱼主要以鲜食或加工成臭鳜鱼等方式进行销售[4-5],由此产生约占鱼体40%~55%的副产物,其中以内脏为主[6]。鳜鱼内脏含有蛋白质、氨基酸、微量元素以及不饱和脂肪酸等营养物质[7-8],有较高的潜在开发价值。但目前除部分加工成宠物饲料,大多被直接丢弃或掩埋,造成了严重的资源浪费和环境污染[9-10]。
鱼内脏中以油脂居多,能提取出丰富的鱼油,鱼油富含的n-3系多不饱和脂肪酸,具有预防心血管疾病、抗炎、抗肿瘤、维护血脂平衡以及免疫增加等作用[11-14]。内脏粗提油往往酸价偏高,存在磷脂、蛋白质及色素沉淀等杂质,并伴有较重的鱼腥味,严重影响其品质及应用价值[15-16]。
目前,国内外学者对鳜鱼的研究主要集中在鳜鱼发酵工艺及其质构特性、挥发性成分的动态变化[17-20],对鳜鱼内脏副产物中鱼油的精炼及品质研究仍然缺乏。基于此,研究拟采用蒸煮法提取鳜鱼内脏副产物中粗鱼油,在单因素试验的基础上,利用响应面设计试验对脱胶、脱酸、脱色等关键精炼步骤进行工艺优化,确定最佳的精炼条件,并对精炼前后鳜鱼鱼油的理化指标及脂肪酸组成进行分析,以期为鳜鱼内脏副产物的有效开发与利用提供一定的数据参考。
1 材料与方法
1.1 材料与试剂
新鲜鳜鱼内脏:由黄山市胡兴堂桃花流水食品有限公司提供,保存于-18 ℃备用;
碘化钾:天津博迪化工股份有限公司;
三氯甲烷、硫代硫酸钠:分析纯,国药集团化学试剂有限公司;
硫酸、氢氧化钠、磷酸、重铬酸钾:分析纯,西陇科学股份有限公司;
无水乙醇:分析纯,上海玻尔化学试剂有限公司。
1.2 主要仪器与设备
高速冷冻离心机:Allegra 64R型,贝克曼库尔特商贸(中国)有限公司;
电热恒温水浴锅:HWS-28型,上海一恒科学仪器有限公司;
电子天平:AR124CN型,奥豪斯仪器(常州)有限公司;
浊度计:WGZ-800型,上海昕瑞仪器仪表有限公司;
鼓风干燥箱:DKL410C型,北京安捷来勒科技有限公司;
气相色谱—质谱联用仪:Agilent HP7890-5975C型,美国Agilent公司。
1.3 试验方法
1.3.1 鳜鱼内脏中粗鱼油的提取 将鳜鱼内脏除杂清洗干净,置于组织捣碎机中捣成糜状。取一定量内脏以料液比1∶5 (g/mL)加入蒸馏水,采用蒸煮法在85 ℃下恒温提取90 min,静置冷却后,取上清液,在以4 000 r/min 离心10 min,加入等体积的热水搅拌3 min,4 000 r/min 离心10 min得粗鱼油[21-22],置于4 ℃密封保存待用。
1.3.2 酸价的测定 参照GB 5009. 229—2016《食品安全国家标准 食品中酸价的测定》中的热乙醇指示剂滴定法,略加修改。量取50 mL 95%的乙醇与0.5 mL酚酞指示剂于1号锥形瓶中混匀,称取油样于2号锥形瓶中,油样质量记为m。将1号锥形瓶置于90~100 ℃的水浴中加热至乙醇微沸,用0.1 mol/L NaOH标准滴定液进行滴定,得到中和后的乙醇。将1号锥形瓶中的中和乙醇趁热倒进装有油样的2号瓶中形成悬浊液,置于90~100 ℃的水浴中加热至乙醇微沸,对热乙醇悬浊液进行滴定,至滴定终点停止,记录所消耗标准滴定液的毫升数,记作V。按式(1)计算酸价。
(1)
式中:
XAV——酸价,mg/g;
V——消耗的标准滴定液体积,mL;
40——NaOH的摩尔质量,g/mol;
c——标准滴定液的浓度,mol/L;
m——油样的质量,g。
1.3.3 过氧化值的测定 参照GB 5009. 227—2016《食品安全国家标准 食品中过氧化值的测定》中的滴定法,略加修改。取2 g油样置于碘量瓶中,加入30 mL CH3Cl3—冰乙酸轻摇混匀,加入1 mL KI震荡0.5 min并置于暗处3 min,后转移至250 mL锥形瓶,加入100 mL水。用硫代硫酸钠标准滴定液滴定析出的碘,至淡黄色停止,再加入1 mL淀粉指示剂,继续滴定至蓝色消失。记录消耗的标准滴定液的毫升数,记作V。按式(2)计算过氧化值。
(2)
式中:
X1——过氧化值,g/100 g;
V——消耗的硫代硫酸钠标准溶液体积,mL;
V0——空白试验消耗的标准溶液体积,mL;
c——标准滴定液的浓度,mol/L;
0.126 9——与1.00 mL硫代硫酸钠标准滴定溶液[c(Na2S2O3)=1.000 mol/L]相当的碘的质量;
m——油样质量,g;
100——换算系数。
1.3.4 脱色率的测定 取鱼油样品和正己烷溶液,按体积比1∶10混合均匀,以正己烷溶液作为参照,在400~650 nm下进行扫描,发现其最大吸收峰在448 nm处[9],故测定鱼油在448 nm下的吸光度,并按照式(3)计算脱色率。
(3)
式中:
T——脱色率,%;
A0——鱼油处理前的吸光度;
A1——鱼油处理后的吸光度。
1.3.5 理化指标的测定
(1) 感官评定:按SC/T 3502—2016执行。
(2) 水分及挥发物含量:按GB 5009. 236—2016中电热干燥箱法执行。
(3) 不溶性杂质含量:按GB/T 15688—2008中坩埚式过滤器法执行。
(4) 不皂化物含量:按GB/T 5535.2—2008中己烷提取法执行。
1.3.6 脂肪酸组成的测定
(1) 鱼油甲酯化:称取10 g精炼前后的鳜鱼鱼油,加入油重10%的无水硫酸钠进行干燥。取60 mg干燥后的鱼油于试管中,加入4 mL异辛烷溶解试样,溶解后加入0.2 mL 2 mol/L 氢氧化钾甲醇溶液,振摇30 s后静置至澄清。加入1 g硫酸氢钠,反应至有沉淀析出,吸取上清液进行GC-MS分析[23]。
(2) GC条件:采用HP-5MS毛细管柱(30 m×0.25 mm,0.25 μm),以不分流进样,柱流量1 mL/min,进样量0.5 μL,进样温度270 ℃。升温程序:初温100 ℃,保持13 min,以10 ℃/min速率升温至180 ℃,保持6 min,再以1 ℃/min 速率升温至200 ℃,保持20 min,然后以4 ℃/min 速率升温至230 ℃,保持10.5 min[23-24]。
(3) MS条件:电子轰击离子源,电子能量70 eV,扫描范围m/z为35~450 amu全离子扫描。
1.3.7 鱼油精炼工艺单因素试验
(1) 磷酸体积分数对鱼油品质的影响:称取一定量的粗鱼油,水浴加热至70 ℃,加入粗鱼油质量1%的不同体积分数(50%,55%,60%,65%,70%)的磷酸,搅拌均匀后70 ℃水浴1 min,再以10 000 r/min离心10 min,吸出上层油样,即得脱胶鱼油[25]。测定不同体积分数磷酸下鱼油的酸价和过氧化值,考察脱胶过程中磷酸体积分数对鱼油品质的影响。
(2) NaOH添加量对鱼油品质的影响:称取一定量的粗鱼油,加入粗鱼油质量0.5%,1.0%,1.5%,2.0%,2.5%的4 mol/L NaOH溶液,均匀搅拌,加热至70 ℃,保温30 min后冷却至室温,以10 000 r/min离心10 min,除去沉淀。加入鱼油体积10%的95 ℃热水,再以10 000 r/min离心5 min,吸出上层油样,即为脱酸鱼油[26]。测定NaOH溶液不同添加量下鱼油的酸价和过氧化值,考察脱酸过程中NaOH溶液添加量对鱼油品质的影响。
(3) 活性白土添加量对鱼油品质的影响:称取一定量的粗鱼油,水浴加热至60 ℃,加入鱼油质量5%,10%,15%,20%,25%的活性白土,搅拌30 min后,以10 000 r/min 离心10 min,吸出上层油样,即为脱色鱼油[23,27]。测定活性白土不同添加量下鱼油的酸价和过氧化值,考察脱色过程中活性白土添加量对鱼油品质的影响。
1.3.8 响应面试验 在单因素试验的基础上,选择磷酸体积分数、NaOH添加量、活性白土添加量为影响因素,采用Box-Behnken设计原理,以鱼油酸价和过氧化值为评价指标,设计三因素三水平的响应面试验,依次进行脱胶、脱酸、脱色,以优化鱼油精炼工艺条件。
1.3.9 浊度的测定 采用台式浊度仪测定鱼油精炼前后的浊度。将蒸馏水通过针筒过滤器进行二次过滤得到零浊度水,加入试样瓶内至十字刻度横线,并对准试样座上的白色定位线,调节调零旋钮,使显示为零。采用同样方法用100 UTU福尔马肼标准溶液进行校准,重复调零校准步骤。换用精炼前后的鱼油样品进行测定,读数稳定后记录数值。
1.3.10 黏度的测定 采用毛细管黏度计测定鱼油精炼前后的黏度。将毛细管黏度计倒置插入鱼油中,用食指堵住另一端的粗管口,用洗耳球连接支管口抽气吸取鱼油,将鱼油吸至毛细管最上方圈线,使鱼油在两圈线内充分填充,迅速将黏度计竖直放置,静置等待鱼油流下,待鱼油液面下降至与第1个圈线相切时,开始计时;待鱼油流出第2个圈线后,停止计时。按式(4)计算黏度。
KV=0.009 594×t,
(4)
式中:
KV——运动黏度,mm/s2;
0.009 594——黏度计常数,mm2/s2;
t——试样流动时间,s。
1.4 数据统计与分析
所得数据以均值±标准差表示。采用Design-Expert 8.0.6软件进行响应面设计及方差分析。运用SPSS 18.0统计软件中单因素方差分析的Duncan’s多重比较法分析数据间的显著差异,P<0.05表示差异显著。
2 结果与分析
2.1 磷酸体积分数对鱼油酸价和过氧化值的影响
由图1可知,鱼油酸价随着磷酸体积分数的增加呈先减小后增大的趋势,当磷酸体积分数达到55%时,鱼油酸价最低,为(6.255±0.163) mg/g,与未添加磷酸的对照组相比,鱼油酸价降低了8.35%。相比于对照组,添加磷酸后鱼油的过氧化值显著降低(P<0.05);当磷酸体积分数为55%,鱼油过氧化值达到最低,为(0.325±0.004) g/100 g,过氧化值降低了58.09%。然而,当磷酸体积分数过高时,酸性增强,鱼油的氧化程度增大,酸价和过氧化值也随之增大。综上,脱胶工艺处理可以有效去除鱼油中磷脂类胶体物质,使鱼油酸价和过氧化值显著降低,与陈转霞等[28]和李冲冲等[9]对鱼油脱胶的研究结果基本一致。

字母不同表示差异显著(P<0.05)
2.2 NaOH添加量对鱼油酸价和过氧化值的影响
由图2可知,鳜鱼内脏粗鱼油的酸价和过氧化值均随着NaOH添加量的增加呈显著下降的趋势(P<0.05)。当NaOH添加量为2%时,鱼油酸价最低,为(3.586±0.338) mg/g,与未添加NaOH的对照组相比(6.504±0.323) mg/g,鱼油酸价降低了44.86%;当NaOH添加量为1.5%时,鱼油过氧化值最低,为(0.572±0.001) g/100 g,与对照组相比,过氧化值降低了28.90%;这可能是由于NaOH添加量增大,碱液与游离脂肪酸能更好地中和,降低了鱼油酸价和过氧化值[29]。综上,NaOH的添加能有效去除鱼油中的游离脂肪酸,对鳜鱼内脏粗鱼油脱酸效果显著。

字母不同表示差异显著(P<0.05)
2.3 活性白土添加量对鱼油酸价、过氧化值和脱色效果的影响
如图3所示,鳜鱼内脏粗鱼油酸价随着活性白土添加量的增加呈先下降后上升的趋势,当活性白土添加量达到10%时,鱼油酸价达到最低值,为(5.556±0.320) mg/g,与未添加活性白土的对照组相比鱼油酸价降低了15.93%。相比于对照组,添加活性白土后鱼油的过氧化值显著降低(P<0.05);当活性白土添加量为15%,鱼油过氧化值为(0.537±0.007) g/100 g,过氧化值降低了26.94%。如表1所示,活性白土可以很好地吸附鳜鱼内脏鱼油中的色素类物质,随着活性炭添加量的增多,鱼油脱色效果显著提高,但继续增大活性炭的添加量,脱色率反而降低;这可能是活性炭添加过多时,活性炭会快速沉降,降低了吸附表面积,导致脱色率降低[9]。

字母不同表示差异显著(P<0.05)
2.4 回归模型的建立
在单因素试验基础上,进一步选择磷酸体积分数、NaOH添加量、活性白土添加量为考察因素,以鱼油酸价(Y1)、过氧化值(Y2)为响应值,设计三因素三水平Box-Behnken试验,试验因素与水平设计见表2,试验结果见表3。利用 Design-Expert Ⅴ 8.0.6 软件进行多元回归拟合分析,得到回归方程为:
Y1=1.93+0.15A-0.40B-0.13C+0.27AB+0.95AC+0.021BC+0.60A2+0.044B2+0.21C2,
(5)
Y2=0.16-0.02A-0.014B-0.027C-0.021AB+0.035AC-0.017BC+0.0095A2-0.0055B2+0.01C2。
(6)
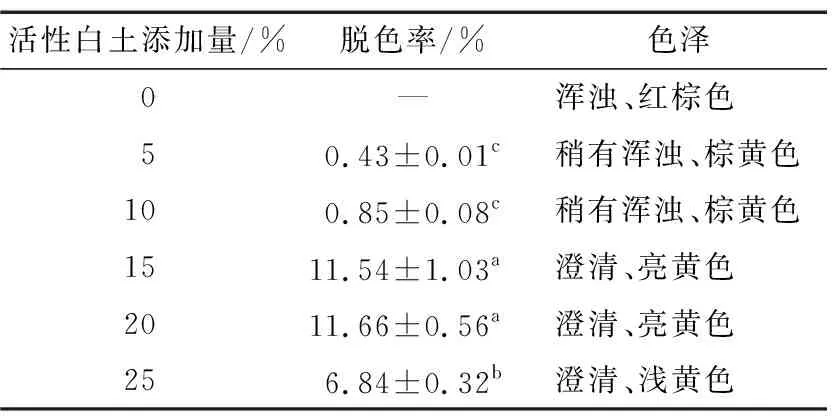
表1 活性白土添加量对鱼油脱色效果的影响†

表2 Box-Behnken试验设计试验因素与水平表

表3 酸价和过氧化值的响应面试验设计方案及结果
2.5 响应面试验的方差分析


表4 酸价的回归模型方差分析†
过氧化值的回归模型方差分析结果见表5。回归模型P<0.05,表明模型具有显著性;失拟项P值为0.232 3>0.05,失拟项不显著,说明未知因素对试验的结果影响较小。因此,该模型在试验范围内,能够适用于鳜鱼内脏鱼油精炼最佳工艺的分析预测。经统计学分析可知,在此试验设计中,一次项A对鱼油过氧化值的影响达到了显著水平(P<0.05),C对鱼油过氧化值的影响达到了极显著水平(P<0.01),交互项AC对鱼油过氧化值的影响也达到了显著水平(P<0.05),其他因素的影响不显著。
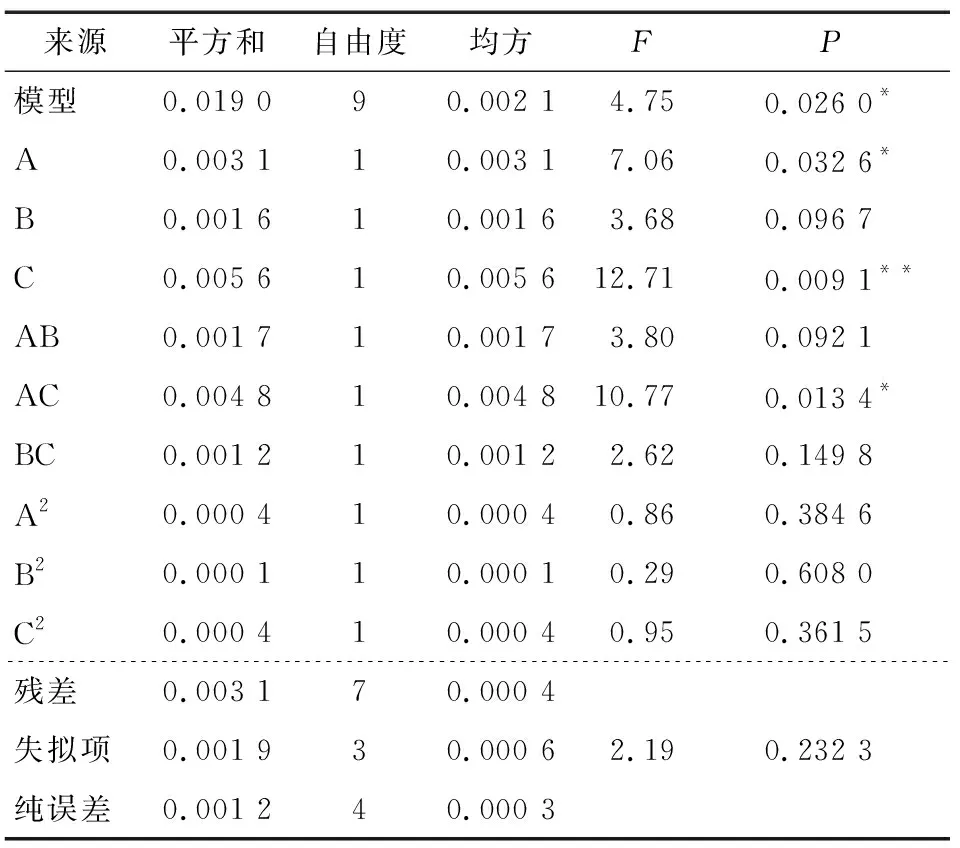
表5 过氧化值的回归模型方差分析†
2.6 验证实验
利用Design-Expert V 8.0.6软件对工艺条件进行优化,得到鳜鱼内脏鱼油最佳精炼条件:磷酸体积分数为50%、NaOH添加量为2%、活性白土添加量为15%。采用上述条件进行验证实验,测得酸价为(0.94±0.03) mg/g、过氧化值为(0.12±0.01) g/100 g,与酸价预测值0.951 mg/g、过氧化值预测值0.116 g/100 g的相对误差分别为1.68%和3.88%,进一步说明此模型对试验的拟合度较好,得到的回归方程在试验中有实际意义。
2.7 鱼油精炼前后品质的变化分析
通过测定鱼油的感官品质、理化指标及物理特性,对鳜鱼内脏粗鱼油和精炼鱼油的品质进行对比分析,结果如表6所示。经活性白土脱色工艺优化,鱼油色泽呈亮黄色,澄清透明,达到一级精制鱼油的质量标准(SC/T 3502—2016)。经脱酸工艺优化,酸价降低至(0.94±0.03) mg/g,达到一级精制鱼油的质量标准;精炼后鱼油的过氧化值降低至(0.12±0.01) g/100 g,达到二级精制鱼油的质量标准。经脱胶工艺优化,不溶性杂质和不皂化物的含量显著降低,达到一级精制鱼油的质量标准。精炼后鱼油的浊度为(5.15±0.07) NTU,相比于精炼前降低了99.07%;精炼后鱼油的黏度为(66.52±0.01) mm2/s,相比于精炼前降低了13.79%。以上结果显示,鳜鱼内脏鱼油经脱胶、脱酸及脱色工艺精制后的感官品质、理化指标及物理特性等品质特性均得到有效改善,说明该条件下的精炼工艺可行。

表6 鱼油精炼前后品质的比较
2.8 鱼油精炼前后脂肪酸含量的变化
按最佳工艺条件对鳜鱼内脏鱼油进行精炼,并对粗鱼油、精炼鱼油的脂肪酸组成及含量进行了对比分析,结果如表7所示。鳜鱼内脏鱼油主要是由C16~C18脂肪酸组成,包括饱和脂肪酸2种、单不饱和脂肪酸3种、多不饱和脂肪酸1种。精炼鱼油的不饱和脂肪酸主要为十八碳烯酸(36.73%)和共轭亚油酸(27.02%),还含有少量的6-十八烯酸、9-十六烯酸,共占总脂肪酸含量的68.25%。鳜鱼内脏鱼油在精炼过程中,各脂肪酸组成及含量变化不明显,说明精炼过程没有引起脂肪酸的氧化分解。陈转霞等[28]和林煌华等[29]也有相同的发现,脱胶、脱酸及脱色等精炼工艺对粗鱼油脂肪酸组成及含量的影响不显著,这可能与残留物以及皂类的去除有关。

表7 鱼油精炼前后脂肪酸组成的分析
3 结论
试验采用蒸煮法提取鳜鱼内脏副产物中粗鱼油,在单因素试验的基础上,通过响应面法优化鱼油精炼工艺,得到其最优加工参数:磷酸体积分数50%,NaOH添加量2%,活性白土添加量15%。在此条件下,预测值与实际值相符,表明得到的回归方程在试验中有实际意义。精制后的鳜鱼内脏鱼油的感官品质、理化指标及物理特性等品质特性均得到有效改善,达到了水产行业精制鱼油的一级、二级标准(SC/T 3502—2016)。精炼前后鱼油的各脂肪酸组成及含量无显著差异,说明精炼过程没有引起脂肪酸的氧化分解。研究结果揭示了鳜鱼内脏鱼油的精炼工艺及其品质变化,然而鱼油在贮藏过程中具有易氧化的特性,如何增强鱼油的抗氧化特性,需要进一步的探索。
