液相色谱法测定饮料中诱惑红含量的 不确定度评定
2022-10-20许智彪
诱惑红是一种食用性的合成色素,能够在水中溶解,具有较强的着色牢度,毒性小。《食品安全国家标准 食品添加剂使用标准》(GB 2760—2014)规定,诱惑红能够添加到糖果、冷饮以及固体饮料当中,但其添加剂量必须控制在规定范围内。近年来,诱惑红也开始被应用于肉灌肠、西式火腿、果冻等食品中,使用范围越来越广。由于诱惑红属于人工合成色素,不能过量添加,否则会对食用者产生危害,因此必须要加强对此种色素的应用剂量检测,确保其处于合格范围内。在测定饮料中诱惑红含量时,常用液相色谱法,该方法效果显著,测定过程简单快速,且准确性高,结果满意[4-5]。因此,本文结合《测量不确定度评定与表示》(JJF 1059.1—2012)[1]和《化学分析中不确定度的评估指南》(CNAS-GL006-2019)[2]中规定的基本因素,对高效液相色谱法测定饮料中诱惑红的含量进行不确定度分析[6],找出影响不确定度的因素,对不确定度进行评估,给出不确定度,如实反映测量的置信度和准确度,为检测结果的准确性、可靠性提供真实、有效的依据[7-9]。
1 材料与方法
1.1 检验标准
根据《食品中诱惑红、酸性红、亮蓝、日落黄的含量检测 高效液相色谱法》(SN/T 1743—2006)进行测定。
1.2 主要仪器设备、标准物质、试剂
LC-20A岛津高效液相色谱仪配紫外检测器;艾杰尔Venusil XBP C18色谱柱;赛多利斯电子分析天平;超声波水浴;刻度吸管;移液器;甲醇(色谱纯,上海安谱科技有限公司);乙酸铵(色谱纯,天津市科密欧化学试剂有限公司);水,均为一级水。
食用合成色素诱惑红溶液标准物质[GBW(E)100164],中国计量科学研究院。
1.3 检测步骤与色谱条件
1.3.1 色谱条件
流动相:甲醇:0.02 mol·L-1乙酸铵溶液(5+95);梯度洗脱: 0~3 min,甲醇5%→20%;3~8 min,甲醇20%→35%;8~15 min,甲醇35%→98%;15~21 min,甲醇98%;检测波长:254 nm;柱温:室温;进样量:10 μL。
1.3.2 检测步骤
用液相色谱法测定饮料中的诱惑红,将一定量样品注入液相色谱仪,利用紫外检测器进行检测,通过对被测样品中色谱峰的保留时间来定性,根据样品峰面积与标准比较用外标法来定量。
2 数学模型的建立与不确定度来源
2.1 诱惑红的含量计算
用外标法计算饮料中诱惑红的含量,其数学模型为

式中:X为样品中诱惑红的浓度,g·kg-1;Cs为诱惑红标准溶液的浓度,μg·mL-1;Ai为样品中诱惑红的峰面积;As为诱惑红标准的峰面积;V为提取溶液的总体积,mL;m为样品称样量,g。
2.2 不确定度来源
根据测定饮料中诱惑红含量的数学模型,其测量不确定度的来源主要有样品称量引入的不确定度;样品定容引入的不确定度;标准溶液配制引入的不确定度;标准工作曲线拟合求浓度引入的不确定度;样品重复测定引入的不确定度。
3 不确定度分量的评定
3.1 样品制备引入的不确定度
(1)试样称量,电子天平的允许偏差为±0.002 mg,k=2,样品量m=5.052 g,相对标准不确定度为
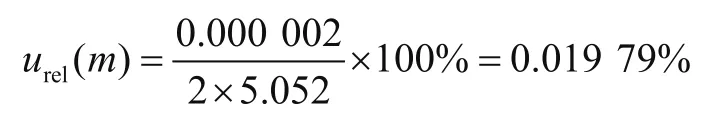
(2)试样稀释。A级10.0 mL容量瓶,误差为±0 mL,按矩形分布,k=,相对标准不确定度为

故试样称量和稀释的相对不确定度为
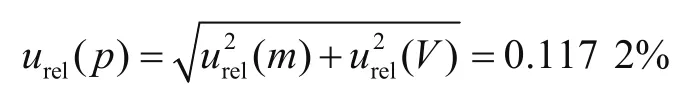
3.2 标准溶液配制引入的不确定度
(1)标准物质引入的不确定度。从标准物质证书中查得诱惑红标准溶液的相对不确定度urel(S1)为2.0%。
(2)配制标准储备溶液引入的不确定度。用5 mL的刻度管移取2.5 mL至10 mL容量瓶中定容。5 mL刻度管允差为0.015 mL,10 mL容量瓶(A)级容量允差为0.02 mL,按照均匀分布,引入的相对不确定为
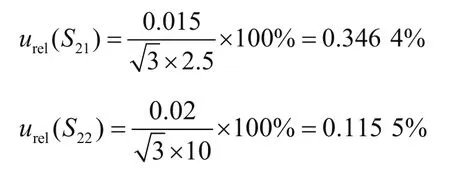
故配制标准储备溶液引入的不确定度为
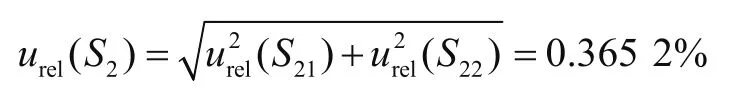
(3)配制标准工作溶液引入的不确定度。用1 mL的刻度管移取1 mL至10 mL容量瓶中定容。1 mL刻度管允差为0.007 mL,10 mL容量瓶(A)级容量允差为0.02 mL,按照均匀分布,引入的相对不确定为
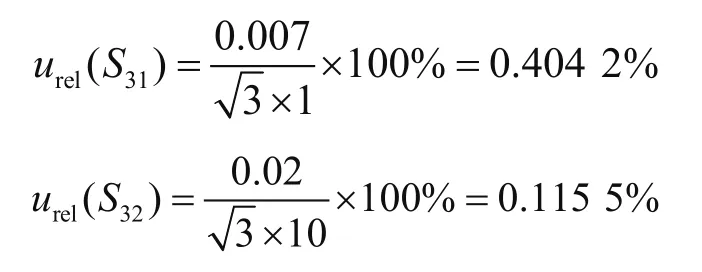
故配制标准工作溶液引入的不确定度为
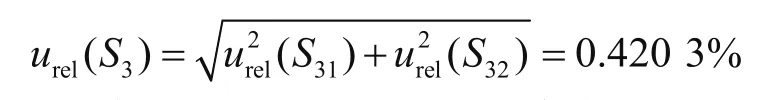
因此标准物质引入的不确定度为

3.3 标准曲线拟合引入的不确定度
由表1、表2可知,标准系列工作液按色谱条件进行进样,以保留时间定性,根据标准溶液的浓度和对应的峰面积,用最小二乘法拟合标准曲线,得到线性回归方程为y=21 999x,相关系数0.999 9。标准系列工作溶液峰面积的标准偏差为S=2 226.454 452,标准系列工作溶液的相对标准不确定度为urel(c0)=0.701 72%。
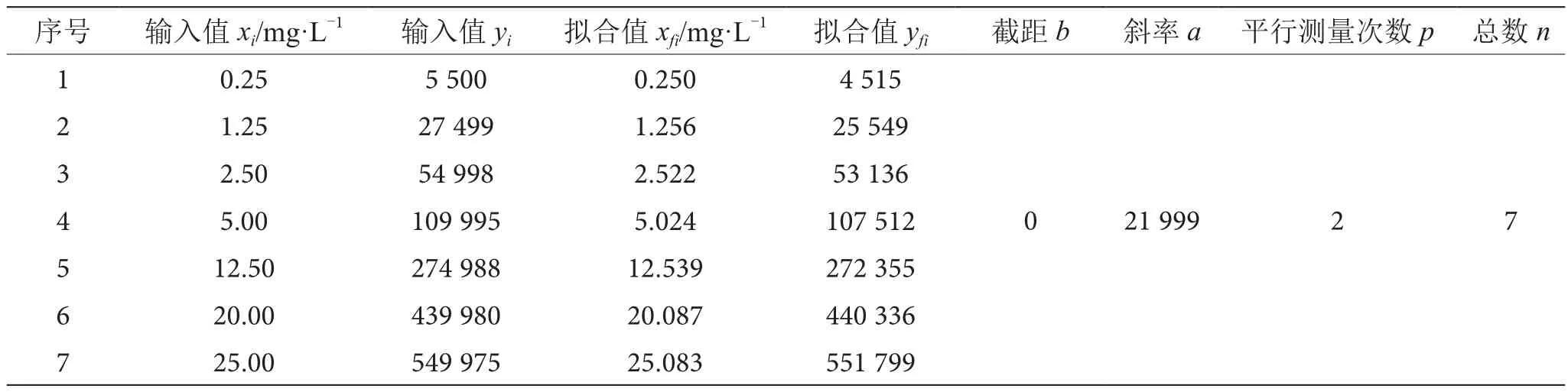
表1 拟合标准曲线数据表

表2 标准工作曲线引入的不确定度表
3.4 重复试验引入的不确定度
称取6份饮料各5 g,按相同的提取步骤进行提取,相同的测量参数上机测定,测量结果分别为0.023 2 g·kg-1、0.023 0 g·kg-1、0.023 1 g·kg-1、0.022 9 g·kg-1、0.023 1 g·kg-1和 0.023 2 g·kg-1,平均值c=0.023 0 g·kg-1,重复测量的标准偏差s=0.000 26 g·kg-1,相对标准不确定度为
4 合成相对不确定度评定
由于上述各个不确定度为积和商的关系,且相互独立,故合成相对不确定度为
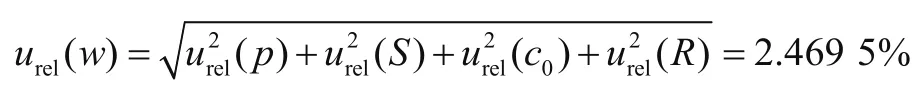
5 扩展不确定度
取包含因子k=2,则高效液相色谱法测定饮料中诱惑红的相对扩展不确定度为Urel=k×urel(w)=2×2.469 5%=4.939 0%。故扩展不确定度为U=0.023×4.939 0%=0.001 1 g·kg-1。
6 测量结果不确定度
用高效液相色谱法测定饮料中诱惑红含量,测定结果为X=(0.023±0.001 1)g·kg-1;k=2。
7 结论与讨论
本实验采用《食品中诱惑红、酸性红、亮蓝、日落黄的含量检测 高效液相色谱法》(SN/T 1743—2006)[3]方法测定饮料中诱惑红含量,其不确定度为X=(0.023±0.001 1)g·kg-1;k=2。根据评定结果,影响不确定因素由大到小依次为标准溶液配制、样品的重复测定、标准曲线拟合求浓度和样品制备。其中标准溶液配制过程引入的不确定度贡献最大。因此,在实际工作中,尽量选择纯度高的标准品,在配制过程中规范操作,选用高级别的量具,并定期对其进行检定校准,以减少不确定度分量,提高测量值的准确性和可信度,以保证检测数据的科学性和合理性。
