不同剂量钙敏感受体抑制剂对磨损颗粒诱导小鼠骨溶解及炎症因子表达的影响
2022-10-20钟艳春叶勇军刘午阳
钟艳春 叶勇军 刘午阳
赣南医学院第一附属医院骨科,江西赣州 341000
有限的使用寿命是人工关节置换手术最大的缺陷,产生这一缺陷的主要原因是术后出现的关节假体无菌性松动。目前,对于人工关节无菌性松动,非手术治疗疗效差,最终均需行翻修手术,而翻修手术费用昂贵,创伤大,术后并发症多,给患者带来巨大痛苦。因此,探索出更安全有效的人工关节无菌性松动防治方法意义重大。钙敏感受体(calcium-sensing receptor,CaSR)是一种细胞表面受体,属于G 蛋白偶联受体家族。研究发现,CaSR 参与了多种骨关节炎症疾病的发生、发展过程,如骨关节炎、类风湿性关节炎等,通过抑制CaSR 可以有效减轻炎症反应。 同时,CaSR 还在单核细胞、破骨细胞等多种细胞的成熟、分化及凋亡中起重要调控作用。 磨损颗粒诱导的骨溶解也是一种炎症性骨溶解过程,而通过抑制CaSR 是否可以减轻磨损颗粒诱导的炎症反应及骨溶解,目前尚不清楚。本实验通过建立人工关节无菌性松动小鼠颅骨模型,给予不同浓度CaSR 抑制剂(NPS2390)干预后,观察其对磨损颗粒诱导骨溶解及炎症因子表达的影响,为人工关节无菌性松动的防治提供新思路。
1 对象与方法
1.1 实验动物
40 只8~10 周龄C57BL/6J 雄性小鼠,体重19~22 g,购于上海斯莱克动物实验有限责任公司,许可证号码:SCXK(沪)2017-0005,饲养于SPF 实验动物房内。 动物实验通过赣南医学院第一附属医院动物实验伦理委员会审核通过,实验过程符合医学伦理规范(伦理审批号:ABRLLSC2021-0112)。
1.2 主要仪器及试剂
磨损颗粒:取人工髋关节翻修术取出的金属关节假体柄,参照前期研究文献制备(激光粒度仪分析显示: 颗粒平均粒径2.93 μm,98%颗粒粒径<6.67 μm,主要成分为钛、铜、铬)。 CaSR 抑制剂NPS2390(美国Sigma 公司,226878-01-09); 小鼠白细胞介素-1β(in terleukin-1β,IL-1β)ELISA 检测试剂盒(上海江莱生物科技有限公司,JL18442);小鼠肿瘤坏死因子α(tumor necrosis factor-α,TNF-α)ELISA 检测试剂盒 (上海江莱生物科技有限公司,JL10484);抗酒石酸酸性染色液(solarbio 公司,G1942);Micro-CT(SCANCO MEDICAL,瑞士,vivaCT40);图像分析软件(Image-Pro Plus 6.0)。
1.3 实验分组及处理
1.3.1 磨损颗粒制备 将制备的磨损颗粒用75%乙醇溶液冲洗并浸泡48 h 后,生理盐水反复清洗。 经鲎试剂盒检测内毒素含量小于0.02 EU/ml 后, 采用PBS配制成浓度为600 mg/ml 颗粒悬液备用。
1.3.2 实验动物分组 将40 只8~10 周龄C57BL/6J 雄性小鼠按照随机数字表法分成空白对照组、 颗粒组、低剂量治疗组、高剂量治疗组,每组10 只。
1.3.3 磨损颗粒诱导骨溶解颅骨模型建立 所有分组后小鼠按照400 mg/kg 的剂量腹腔注射10%水合氯醛麻醉后,剪去小鼠颅顶部毛发,碘伏消毒三遍皮肤后,以小鼠外耳根内侧部连线中点为中心,作一经颅正中矢状线长约0.5 cm 的手术切口,逐层切开皮肤、皮下组织,剥离颅骨骨膜,于颗粒组、低剂量治疗组、高剂量治疗组小鼠骨膜下植入30 mg(50 μl)预先配备好的关节假体磨损颗粒悬浮液,空白对照组以等量PBS 溶液替代。 3-0 丝线缝合手术切口,检查切口无漏液后碘伏消毒切口,手术结束。
1.3.4 实验干预及建模成功的标准 建模手术后第2天开始,低剂量治疗组、高剂量治疗组小鼠分别隔日接受0.2、2.0 mg/kg NPS2390 腹腔注射; 空白对照组和颗粒组以等量生理盐水替代,干预持续14 d。 实验过程中,仔细观察各组小鼠头部术口,进食及活动情况,以及小鼠颅顶磨损颗粒悬浮液有无外漏。小鼠在处死前,术口无红肿、渗液、流脓,无磨损颗粒外漏,进食及活动正常,属模型建立成功。
1.3.5 标本采集 药物干预14 d 后处死各组小鼠,去除颅底组织及颅骨表面植入磨损颗粒。 行Micro-CT检测后将每组标本分2 份,一份颅骨用10%的甲醛固定,用于组织学检测,一份放置2 ml DMEM 培养基浸泡24 h,取上清检测炎症因子含量。
1.4 观察指标及检测方法
1.4.1 Micro-CT 检测 将Micro-CT 参数设定为:X线能量70 kV,200 μA, 扫面层厚20 μm, 激发时间300 ms。 获得断层图像后对颅盖骨进行三维结构重建。在颅盖骨标本正中央选取5 mm的正方形区域进行骨矿物质密度、骨孔隙率和骨体积分数检测。
1.4.2 HE 染色 标本中性甲醛固定24 h, 流水冲洗后放置10%乙二胺四乙酸中脱钙, 每3 天更换浸泡液1次,直至颅骨变软,细针能轻易穿透为止。 标本经脱水、石蜡包埋,切片,片厚5 μm,HE 染色。通过显微镜在200×下观察颅骨HE 染色切片并拍照。 使用美国Image-Pro Plus 软件分析正中矢状线区域骨面积。
1.4.3 TRAP 染色 TRAP 标本经脱水浸蜡包埋后切成4~5 μm 厚切片,放入TRAP 固定液4℃固定3 min,清水冲洗。再将切片放入TRAP 孵育液中置于37℃温箱染色60 min,水洗。最后,苏木素染色液中染色5 min,水洗。 通过显微镜在200×下观察颅骨TRAP 染色切片并拍照,将细胞染成暗红色,多核的定为阳染细胞,即为破骨细胞。 使用美国Image-Pro Plus 软件分析破骨细胞数。
1.4.4 ELISA 检测 将标本放置于2 ml DMEM 培养基浸泡24 h,取上清,按ELISA 试剂盒操作说明书检测其中IL-1β、TNF-α 含量。
1.5 统计学方法
2 结果
2.1 Micro-CT 检测
CT 扫描图像重建后显示空白对照组颅骨表面光滑平整,颅骨缝连接紧密(图1A)。颗粒组磨损颗粒放置区域颅骨显得粗糙,凹凸不平,表面布满坑坑洼洼的骨吸收孔隙,颅骨正中连接缝增宽(图1B)。 低剂量组颅骨重建图像仍可见较多骨吸收陷窝,但较颗粒组稍少(图1C)。 高剂量组颅骨表面骨吸收空隙明显较少,较光滑,重建图像与空白对照组较相似(图1D)。
在颅盖骨标本正中央选取特定区域进行骨参数定量检测后显示: 颗粒组颅骨孔隙率高于空白对照组, 而颅骨矿物质密度和骨体积分数低于空白对照组,差异有统计学意义(P<0.05)。 低剂量组骨矿物质密度高于颗粒组,差异有统计学意义(P<0.05)。 高剂量组骨孔隙率低于颗粒组,而骨矿物质密度和骨体积分数明高于颗粒组,差异有统计学意义(P<0.05)。 高剂量组骨矿物质密度及骨体积分数高于低剂量组,差异有统计学意义(P<0.05)(图1E~G)。
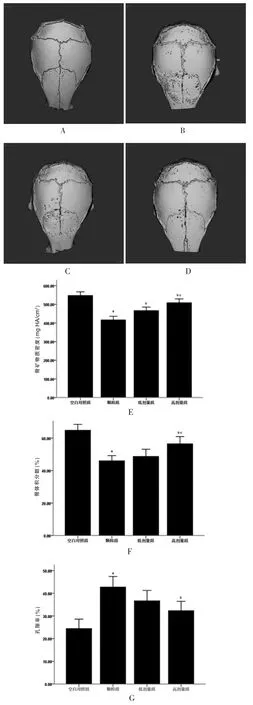
图1 小鼠颅骨Micro-CT 扫描及骨参数分析
2.2 HE 染色
空白对照组颅骨冠状面切片染色可见颅骨完整性较好,颅骨缝连接紧密,骨膜菲薄,细胞浸润少,多为梭形成纤维细胞(图2A)。 颗粒组可见少量残留的磨损颗粒,颅骨缝连接处骨破坏最明显,周围见大小不等的骨溶解缺孔,骨膜反应强烈,明显增厚,大量炎症细胞浸润(图2B)。 低剂量组、高剂量组亦可见少量未能冲洗干净的颗粒,炎症细胞浸润减少,骨膜较薄,骨结构相对完整,骨侵蚀面积均减少(图2C~D)。经图像分析显示,颗粒组骨面积小于空白对照组,高剂量组骨面积高于颗粒组, 差异有统计学意义 (P<0.05)(图2E)。
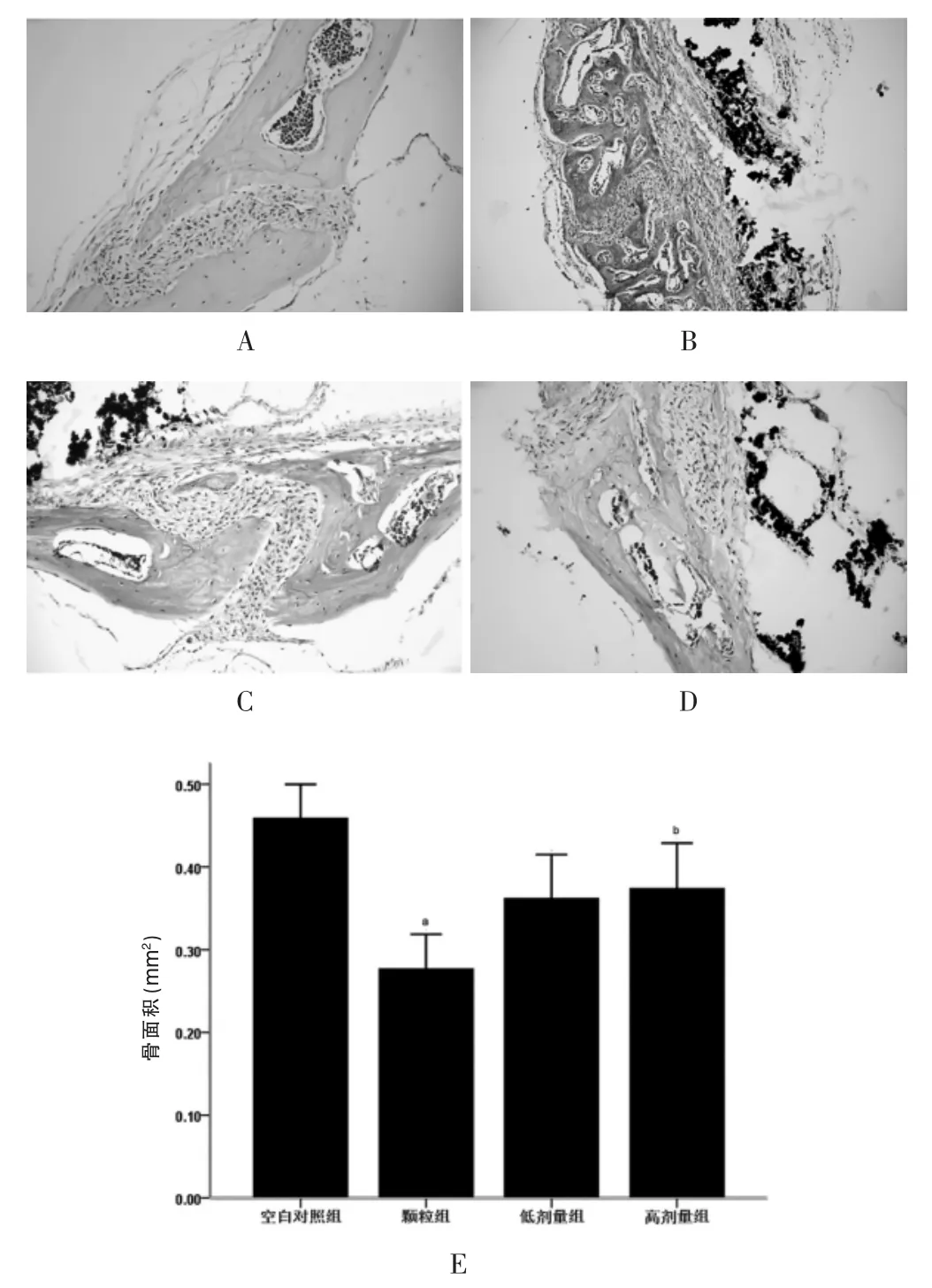
图2 小鼠颅骨HE 染色及骨面积分析结果
2.3 TRAP 染色
空白对照组颅骨平整,骨皮质边缘零星分布少量染成暗红色不规则形的破骨细胞(图3A)。 颗粒组骨侵蚀明显,形态不规则,结构不完整,骨破坏边缘分布大量红色深染的多核破骨细胞(图3B),低剂量组、高剂量组骨破坏减轻,红色深染的破骨细胞数较少(图3C、D)。 经图像分析显示,颗粒组破骨细胞数高于空白对照组,低剂量组和高剂量组破骨细胞数均少于颗粒组,差异有统计学意义(P<0.05)(图3E)。
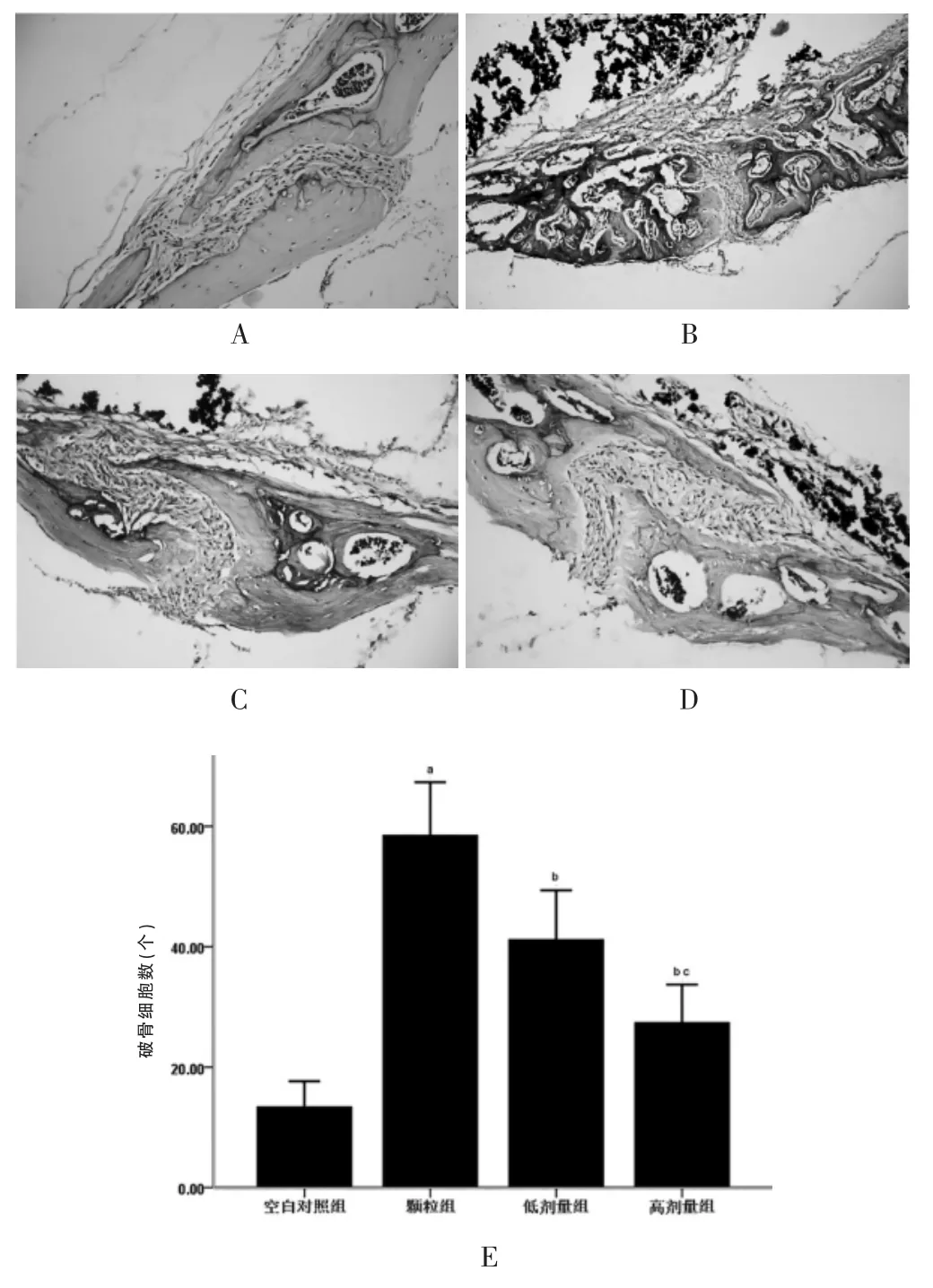
图3 小鼠颅骨TRAP 染色及阳染细胞数分析结果
2.4 ELISA 检测
颗粒组炎症因子IL-1β、TNF-α 表达量高于空白对照组,差异有统计学意义(P<0.05)。 低剂量治疗组、高剂量治疗组IL-1β、TNF-α 表达均低于颗粒组,以高剂量组降低最为明显,低剂量组次之,高、低剂量组之间比较,差异有统计学意义(P<0.05)(图4)。
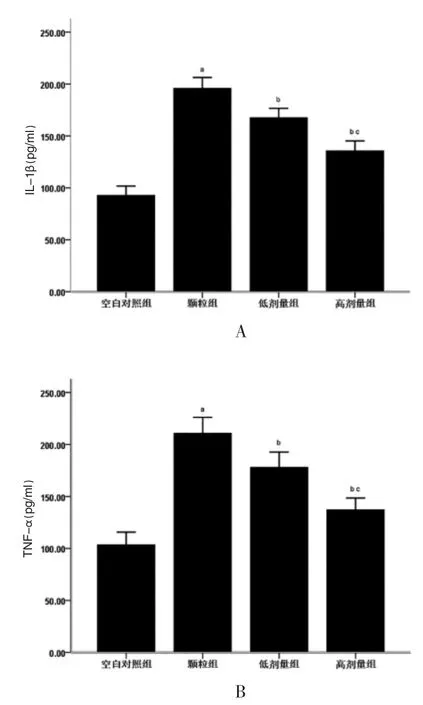
图4 ELISA 检测炎症因子表达量
3 讨论
随着生物医学材料研究的发展,人工关节假体材质由金属升级到了陶瓷,关节的耐磨性得到了很大提升,但是仍然难以做到关节界面零磨损。 关节的长期使用依然会源源不断产生磨损颗粒, 由此产生的磨损颗粒聚集在假体周围, 诱导无菌性炎症反应及破骨细胞过渡活化、 骨吸收, 最终导致假体周围骨缺损、松动。从磨损颗粒的产生到关节假体松动是一个复杂的炎症性骨溶解过程,涉及多种炎症细胞聚集浸润及炎症因子分泌,其中,单核巨噬细胞在该炎症反应过程中起重要作用。体外实验发现不同材质的磨损颗粒均能刺激外周血单核细胞分泌炎症因子和趋化因子,并存在剂量依赖性;其中钛合金颗粒的生物学活性最强, 其次是钴铬合金和聚甲基丙烯酸甲酯颗粒,超高分子量聚乙烯颗粒最低弱。 刘子歌等则认为钴铬钼合金颗粒对巨噬细胞细胞的刺激更为强烈,能更显著增强巨噬细胞的吞噬功能及骨溶解相关因子的释放。 席向东等在人工关节无菌性松动假体周围界膜组织中发现含有大量异物巨噬细胞,且基质金属蛋白酶-9、TNF-α、IL-1 的表达明显高于初次人工置换患者滑膜组织。单核细胞可吞噬粒径小于10 μm的磨损颗粒,并融合成多核异物巨噬细胞,活化后产生大量炎症因子TNF-α、IL-1β、单核细胞趋化蛋白1(Monocyte chemoattractant protein-1,MCP-1)等,以维持假体周围慢性炎症反应。 CaSR 参与了多种炎症反应过程,并在多种炎症细胞中均有表达。 D′Espessailles 等发现巨噬细胞表达CaSR,当受到CaSR 激动剂刺激后,巨噬细胞核苷酸结合寡聚化结构域样受体蛋白3(NOD-like receptor protein 3,NLRP3)、IL-1β及半胱氨酸酶-1 的表达明显增加,而加入CaSR 拮抗剂后,炎症因子表达明显得到抑制。 Jager 等发现类风湿性关节炎患者单核细胞CaSR 表达明显上调,并通过激活NLRP3 炎症使IL-1β 释放增加, 维持炎症反应, 通过抑制CaSR 可减轻类风湿患者炎症反应。Su发现大肠杆菌大鼠睾丸炎模型中睾丸单核巨噬细胞CaSR 表达明显增加,并通过激活NLRP3 炎症小体上调IL-1β 的表达,而CaSR 抑制剂可明显减轻炎症反应。 Lee 等证实CaSR 抑制剂NPS2143 可以抑制脂多糖诱导的急性肺水肿小鼠肺内炎症细胞浸润和MCP-1、TNF-α、白细胞介素-6 等炎症细胞因子的表达,对脂多糖诱导的急性肺损伤有保护作用。 由此可见,单核巨噬细胞表达的CaSR 有助于炎症因子的释放,炎症反应的扩大及维持,而通过阻断CaSR 可抑制炎症反应。本研究中,与空白对照组相比,颗粒组局部炎症反应明显加重,骨膜增厚,大量炎症细胞浸润,可见多核巨噬细胞,同时,TNF-α、IL-1β 表达量也明显增加,且无红肿、渗液等感染迹象,这说明,动物模型的建立是成功的,很好地模拟了磨损颗粒诱导的骨溶解体内变化。给予CaSR 抑制剂NPS2390 干预后, 颅骨骨膜炎症细胞的浸润明显减少, 炎症因子TNF-α、IL-1β 表达明显被抑制, 这种抑制效果随NPS2390 浓度增加而越发明显, 其机制很有可能是NPS2390 阻断了周围单核巨噬细胞CaSR 信号通路,抑制了炎症因子的释放,阻断了磨损颗粒引发的炎症瀑布反应。
磨损颗粒不仅可以通过炎症细胞间接影响骨组织细胞,也可以直接影响骨细胞,导致骨代谢失衡。体外培养的破骨细胞前体细胞可吞噬磨损颗粒,并融合分化成为有骨吸收能力的成熟破骨细胞,参与假体周围骨吸收过程。 同时,磨损颗粒还可以增加假体周围核因子κB 受体活化因子配体(receptor activator of NF-κB ligand,RANKL)的表达,抑制骨保护素(osteoprotegerin,OPG)表达,通过强化RANKL/核因子κ B受体活化因子(receptor activator of NF-κB,RANK)信号通路促进破骨细胞成熟、分化,外源性给予OPG 干预后可以抑制磨损颗粒诱导的炎症反应及骨溶解。磨损颗粒可抑制成骨细胞生长、 成熟及功能的发挥,诱导其凋亡,通过刺激成骨细胞功能,可有效抑制磨损颗粒诱导的骨溶解。 CaSR 也参与了多种骨组织细胞成熟、分化及凋亡的调控,但在不同疾病中起不一样的作用。 雷群等发现Ca通过与CaSR 结合在体外能促进人成骨细胞的增殖、成骨分化与矿化,CaSR拮抗剂降能阻断这一作用。雷尼酸锶是一种抗骨质疏松药物,因其中锶离子和钙离子理化性质相仿,有报道雷尼酸锶通过激活CaSR,促进破骨细胞凋亡和成骨细胞分化,从而加强骨组织,达到抗骨质疏松疗效。Liu 等报道雷尼酸锶还可通过阻断炎症因子TNF-α、IL-1β 释放,促进OPG 表达,抑制破骨细胞生成,从而减轻磨损颗粒诱导炎症骨溶解。 Liu 等发现肺癌组织中CaSR 表达明显高于癌旁正常组织,存在骨转移的肺癌CaSR 表达明显高于无骨转移肺癌。 高表达的CaSR 可以促进破骨细胞前体细胞成熟分化,抑制成骨细胞功能,CaSR 拮抗剂可抑制肺癌骨转移的骨破坏。 Boudot 等发现CaSR 的过表达在可促进乳腺癌细胞分泌表皮调节素,从而抑制OPG 的表达,促进破骨细胞成熟分化,骨破坏。董冰子等发现CaSR 拮抗剂溶钙素可以制造低钙血症的假象,促进甲状旁腺激素的分泌,从而刺激成骨,增强骨密度。
在本研究中,磨损颗粒组破骨细胞数量多于空白对照组,骨体积分数、骨矿物质密度明显降低,骨孔隙率增加和骨溶解明显,提示磨损颗粒在体内诱导了破骨细胞激活并发挥了骨溶解作用。 给予CaSR 抑制剂NPS2390 干预后,破骨细胞数量明显减少,颅骨骨溶解也受到抑制。 其作用机制可能两方面。 一方面是NPS2390 抑制了局部炎症反应及单核巨噬细胞的浸润,而单核细胞是破骨细胞的前体来源来细胞,是磨损碎屑诱导的破骨细胞活化的基础, 前体细胞减少了, 成熟的破骨细胞自然就少了。 另一方面是CaSR在磨损颗粒诱导骨溶解中的作用和转移瘤中的作用相似, 是激活破骨细胞, 促进骨溶解的作用,而NPS2390 抑制了这种作用。当然,本实验未检测CaSR的表达,所以具体作用机制仍不明确。
综上所述,CaSR 抑制剂可有效减轻磨损颗粒诱导的骨溶解及炎症因子的表达,但其具体分子机制仍需进一步深入研究
