PD-1抑制剂导致甲状腺毒症1例及文献复习
2022-10-14张立宽赵中华张强郝建斌郝延璋章丽芳
张立宽 赵中华 张强 郝建斌 郝延璋 章丽芳
1滨州医学院附属医院肿瘤科,滨州 256600;2南京鼓楼医院集团安庆石化医院内分泌科,安庆 246000
近年来,随着抗肿瘤治疗的发展,免疫疗法迎来了里程碑式的发展,免疫检查点是免疫系统的负向节器,防止过度激活免疫反应。免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)的单克隆抗体已被开发用于封锁这些调控因子,包括细胞毒性T淋巴细胞抗原4(cytotoxic T lymphocyte antigen-4,CTLA-4)和程序性死亡受体-1(programmed death-1,PD-1)以及其配体程序性死亡配体-1(programmed death-ligand-1,PD-L1)。这些药物通过克服免疫耐受,增强肿瘤微环境的免疫,对多种肿瘤均表现出显著的抗肿瘤作用。抗CTLA-4抗体(ipilimumab)已被美国食品和药物管理局(FDA)批准用于治疗黑色素瘤。此外,PD-1抑制剂(pembrolizumab和nivolumab)和PD-L1抗体(atezolizumab、durvalumab和avelumab)已被证明可以改善各种癌症患者的总生存率,也已被FDA批准[1]。ICIs在激活免疫系统的同时,也会诱发自身免疫相关性疾病,通常称为免疫相关不良反应(immune-related adverse events,IrAEs)[2]。众所周知,IrAEs会影响内分泌器官,如垂体、甲状腺和胰腺[3-4]。甲状腺功能障碍尤其与PD-1或PD-L1抑制剂的使用有关。在一项使用nivolumab、pembrolizumab、atezolizumab治疗的患者的系统综述和荟萃分析中,甲状腺功能减退的发生率分别为7.0%、3.9%和13.2%,甲状腺功能亢进的发生率分别为3.2%、0.6%和8.0%[5]。在一项回顾性研究中,有191例患者接受了PD-1抑制剂的治疗。其中亚临床甲状腺功能减退10例(5.2%),明显甲状腺功能减退15例(7.9%),亚临床甲状腺功能亢进6例(3.1%),明显甲状腺功能亢进9例(4.7%)[6]。本文报道了1例喉鳞癌患者应用PD-1抑制剂信迪利单抗后出现甲状腺毒症的临床表现及诊疗情况,以提高医师对该疾病的认识。
病例资料
1、一般资料
患者,男,72岁,2016年行气管切开+环舌会厌吻合术,术后病理:中分化鳞状细胞癌,术后因疾病进展提示左侧颈动脉鞘区淋巴结较前增大,考虑肿瘤复发,于2019-09-20行左侧颈部重大淋巴结局部放射治疗,DT 60 Gy∕30f。后因左锁骨上窝新发肿大淋巴结行CT引导下放射性粒子植入治疗。此后行紫杉醇+顺铂(TP)联合PD-1抑制剂治疗2周期,具体药物及剂量:信迪利单抗200 mg,d1+顺铂40 mg,d1-3+紫杉醇注射液240 mg,d1,每21 d为1周期,患者距第1次使用信迪利单抗时间为45 d,患者出现窦性心动过速、胸闷、心悸、多汗、食欲增加,无双手颤抖及腹泻等症状。患者首次使用信迪利单抗之前甲状腺相关激素水平均处于正常水平范围。患者于2022-04-25就诊于滨州医学院附属医院肿瘤科进一步治疗,入院体格检查:体温36.2℃,呼吸频率25次∕min,血压154∕74 mmHg(1 mmHg=0.133 kPa),心率100次∕min。心电图提示:窦性心动过速,轻度ST改变。面部多汗、无突眼及眼睑水肿、甲状腺正常,质地软,触之无压痛,未触及结节,未闻及震颤及血管杂音。胸腹查体无异常。实验室检查:白细胞计数5.7×109∕L,红细胞计数4.1×1012∕L,血红蛋白130 g∕L,血小板计数218×109∕L,总白蛋白62.60 g∕L,白蛋白38.40 g∕L,肝肾功能等相关指标无异常。甲状腺相关指标见表1。
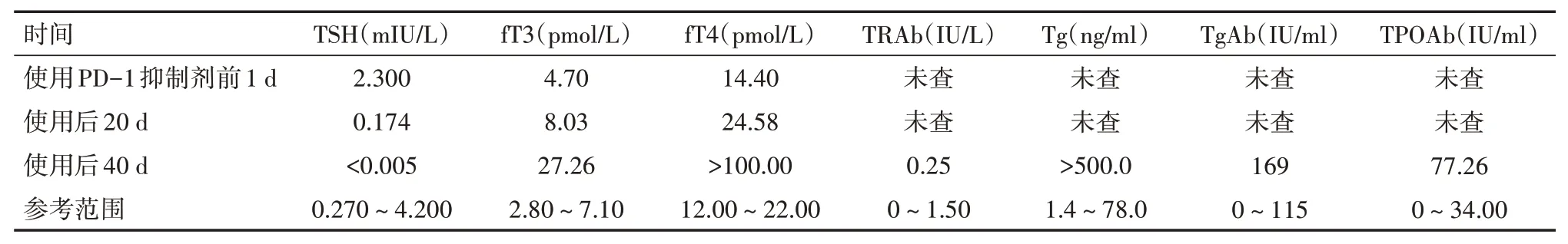
表1 1例喉中分化鳞状细胞癌患者首次使用程序性死亡受体-1抑制剂前后甲状腺功能相关指标水平
2、诊断及治疗
患者使用信迪利单抗前甲状腺激素水平处于正常范围,使用后患者伴有高代谢症状。游离三碘甲状腺原氨酸(fT3)、游离甲状腺素(fT4)水平升高,促甲状腺激素(TSH)水平降低,抗甲状腺球蛋白抗体(TgAb)及甲状腺球蛋白(Tg)升高,促甲状腺激素受体抗体(TRAb)水平正常;甲状腺及颈部淋巴结超声:甲状腺实质回声不均匀。考虑为ICIs导致的自身免疫性甲状腺炎。自确诊之日起给予患者琥珀酸美托洛尔缓释片47.5 mg qd,甲巯咪唑片10.0 mg bid,原抗肿瘤治疗方案不变。患者服用药物后门诊随诊,自诉心悸、多汗症状较前明显好转,目前仍在规律复查中。
甲状腺毒症定义为TSH下降,fT4或总T3升高,相对短暂的过程,通常发生在ICIs开始后4~8周。本文报道了1例PD-1抑制剂导致甲状腺毒症患者,究其原因考虑为ICIs使机体免疫系统过度激活,损伤正常的腺体组织,以甲状腺最易受累[7]。一项研究指出:ICIs影响的内分泌器官包括甲状腺(18∕23,78.3%)、胰岛(17∕23,73.9%)、垂体(11∕23,47.8%)和肾上腺(2∕23,8.7%),65.2%的患者检出相关自身抗体[8]。一项回顾性分析中,有93例患者使用帕博利珠单抗,甲状腺炎发生率为7.5%[8]。同样在一项荟萃分析中指出,使用ipilimumab的患者发生与胃肠道系统相关的潜在IrAEs(腹泻,29%;结肠炎,8%)和皮肤(皮疹,31%;瘙痒症,27%;皮炎,10%),垂体炎占4%[9]。Nivolumab最常见的潜在风险为黄斑丘疹(13%)、红斑(4%)、肝炎(3%)和输液相关反应(3%),而pembrolizumab则为关节痛(12%)、甲状腺功能减退(8%)和高血糖(6%)。关于甲状腺炎的数据仍然有限,但发病率范围从nivolumab单药治疗的1.6%到PD-1和CTLA4抑制剂联合治疗的4.6%[10]。本例患者在使用信迪利单抗后45 d出现甲状腺功能异常,与文献报道的ICIs引起的甲状腺毒症可持续21~60 d相符合。自身免疫性甲状腺疾病是一组常见的内分泌系统疾病,可导致甲状腺激素过度分泌以及随之而来的全身代谢功能障碍,从而影响全身多个器官系统,临床主要包括桥本甲状腺炎(HT)和Graves病(GD)。此患者诊断为自身免疫性甲状腺炎,因其发生甲状腺毒症时伴随TgAb、TPOAb及Tg阳性,TRAb阴性,并且在给予患者美托洛尔治疗后复查fT3、fT4、TSH较前好转。该患者既往有过颈部淋巴结放射治疗及放射性粒子植入病史。有研究表明,放疗产生的电离辐射不仅会直接损伤患者的甲状腺细胞,而且还会损伤其周围的血管以及免疫介导,产生刺激因子,引起甲状腺组织本身产生免疫反应,从而导致甲状腺功能减退发生[11]。乳腺癌根治术后进行胸锁联合野放疗结束12个月后TGAb可升高。在一项83例鼻咽癌患者调强放疗的回顾性分析中指出:83例患者中有56例发生甲状腺功能减退(包括临床型和亚临床型),占67.5%,27例未发生甲状腺功能减退,占32.5%,并未出现自身免疫性甲状腺炎的患者[12]。此例患者颈部淋巴结放疗为2019年,虽然伴有TGAb升高,但该患者临床表现更倾向于甲状腺功能亢进的临床表现,故临床诊断为信迪利单抗引起自身免疫性甲状腺炎。
ICIs引起甲状腺炎的机制尚不明确,但多认为这是继正常免疫调节通路封锁后的自身免疫反应。该患者在使用信迪利单抗后甲状腺球蛋白水平明显增加,说明甲状腺受到炎症损伤,并且伴有甲状腺过氧化物酶抗体、甲状腺球蛋白抗体水平较基线升高,和甲状腺毒症一起出现,说明甲状腺的自身抗体可能参与ICIs导致的甲状腺炎出现。大多数免疫检查点抑制剂导致甲状腺功能障碍多为轻症,不用调整免疫检查点抑制剂的剂量。从这个病例中我们可以得到一定的启发,在患者使用ICIs前后须定期复查甲状腺功能
讨论及文献复习
相关指标,发现甲状腺功能异常时应及时采取治疗措施,必要时可停药处理,同时定期复查甲状腺功能及甲状腺超声以明确甲状腺功能恢复情况,根据临床情况适时加减剂量。
