血清25(OH)D及矿物质水平与产后出血的关联性研究
2022-10-12尼牙孜汗依明
张 颖,马 艳,尼牙孜汗·依明,刘 海,陈 梅
(1.新疆生产建设兵团第十三师红星医院产科,新疆 哈密 839000;2.新疆维吾尔自治区哈密市伊州区哈密市中心医院产科,新疆 哈密 839000)
产后出血(postpartum hemorrhage,PPH)是临床多见的妇产科严重并发症,迅速且过量出血易造成失血性休克,甚至导致凝血功能障碍,并发弥散性血管内凝血综合征,目前仍是导致国内产妇死亡的关键因素之一。有研究指出,引发PPH的首要因素为宫缩乏力、胎盘残留、软产道受损等[1]。且有分析指出,维生素D(vitamin D,VD)及矿物质的缺乏也会导致产妇的不良妊娠结局[2-3]。VD是机体必不可少的维生素之一,参与机体钙磷的摄入及代谢,对保持骨骼健康有着关键的意义[4]。但随着更深层次的研究,愈来愈多的报道认为因VD缺乏受累的群体十分宽泛,诸如代谢性疾病、心血管病及免疫系统病等均与其相关[5]。血清25羟维生素D[25 hydroxyvitamin D,25(OH)D]是能够用于评估机体VD水平的关键指标之一。妊娠期女性相关激素水平及糖代谢等情况有别于非孕期女性,多存在VD缺乏的现象,即25(OH)D小于50nmol/L[6]。因当前有关孕妇VD、矿物质水平和PPH间的相关性研究偏少,故本研究分别对产后正常与PPH妇女的25(OH)D及矿物质水平进行了观察与比较,以研究血清25(OH)D及矿物质水平与PPH的相关性,现将结果报告如下。
1 资料与方法
1.1 一般资料
选取2017年11月至2020年11月新疆生产建设兵团第十三师红星医院收治的297例孕妇为研究对象。依据PPH相关诊断标准[7],即分娩后24h内阴道出血量是否大于500mL分为产后出血组(n=21)与产后正常组(n=276)。纳入标准:①产后出血组患者PPH的诊断符合《产后出血预防与处理指南(2014)》中PPH相关诊断标准[7];②均在本院自然分娩;③均为单胎妊娠;④年龄20~40周岁;⑤产次低于3次;⑥获得研究对象的知情同意。排除标准:①研究对象的基本临床信息有缺失;②分娩前2周内有接受过影响机体营养素的药物;③合并有凝血功能障碍等血液病;④妊娠期出现肝功能异常;⑤有严重妊娠期合并症;⑥同时参与其他项目研究者。
产后出血组中年龄23~35岁,平均(26.65±3.48)岁;产时体质量指数(body mass index,BMI)24~31kg/m2,平均(27.61±3.09)kg/m2;初产妇16例,经产妇5例。产后正常组中年龄21~34岁,平均(26.43±3.34)岁;产时BMI为24~30kg/m2,平均(27.01±2.63)kg/m2;初产妇248例,经产妇28例。两组孕妇一般资料比较差异无统计学意义(P>0.05)。本研究获我院医学伦理委员会批准(伦理批号2017-21号)。
1.2 研究方法
所有研究对象入组后均采集一般资料,包括年龄、产次、月经初潮年龄、不良孕产史等,并采集所有孕妇空腹外周血5mL,以2 000r/min低温离心5min分离上清液,置于-80℃冰柜存储备用。使用全自动生化分析仪(7600型,日本日立)以酶联免疫法测定25(OH)D水平,检测试剂盒由英国IDS Ltd公司提供;使用电解质分析仪(DH505型,武汉中达公司)以离子选择电极直接法检测血清矿物质(血清钙、血清磷、血清铁)水平,所有检测操作均严格按仪器和试剂盒说明书操作,待孕妇分娩后采集产时BMI、孕周与脐带缠绕的临床资料。
1.3 观察指标
①对比两组孕妇临床资料及实验室指标差异;②分析25(OH)D、血清钙、血清铁预测孕妇发生PPH的价值;③将两组有统计学差异的变量纳入Logistic回归模型,行量化赋值,以是否发生PPH作为因变量(是=1分,否=0分),以25(OH)D、血清钙、血清铁为自变量,明确孕妇发生PPH的危险因素。
1.4 统计学方法
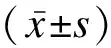
2 结果
2.1 孕妇发生PPH的单因素分析
产后出血组不良孕产史占比高于产后正常组,25(OH)D、血清钙、血清铁水平低于产后正常组,差异均有统计学意义(χ2/t值分别为4.129、6.526、8.317、7.517,P<0.05);产后出血组年龄、产时BMI、产次、孕周、月经初潮年龄、脐带缠绕、血清磷与产后正常组比较,差异无统计学意义(P>0.05),见表1。

表1 孕妇发生PPH的单因素分析
2.2 25(OH)D、血清钙、血清铁预测孕妇发生PPH的ROC曲线分析
经ROC曲线分析,25(OH)D、血清钙、血清铁预测孕妇发生PPH的曲线下面积分别为0.905、0.853、0.860,见表2、图1。

表2 25(OH)D、血清钙、血清铁预测孕妇发生PPH的ROC曲线分析

图1 25(OH)D、血清钙、血清铁预测孕妇发生PPH的ROC曲线
2.3 孕妇发生PPH的多因素Logistic回归分析
多因素Logistic回归分析显示有不良孕产史、25(OH)D<41.905nmol/L、血清钙<2.165mmol/L、血清铁<12.265mmol/L是孕妇发生PPH的危险因素,其OR值及95%CI分别为3.261(1.298~8.193)、3.999(1.658~9.645)、3.654(1.449~9.214)、4.225(1.574~11.341),P<0.05,见表3。

表3 孕妇发生PPH的多因素Logistic回归分析
3 讨论
3.1 不良孕产史及血清25(OH)D、钙、铁低水平均是孕妇发生PPH的危险因素
孕期女性所摄入的营养成分除了用以维系本身的需要,还要考虑妊娠期胎儿的发育[8]。为能够满足妊娠期女性的自身健康及胎儿生长的双向需求,妊娠期女性对各种维生素的需求明显增多,目前研究表明约一半以上的女性怀孕以后存在维生素缺乏的状况[9],且有研究进一步指出VD缺乏与不良妊娠结局之间具备显著相关性[10]。此外,妊娠期矿物质缺乏会增加胎儿发育不良、贫血或发育畸形等发生率,还会造成孕妇产后出血量增多[11]。本研究结果显示,产后出血组不良孕产史占比显著高于产后正常组,25(OH)D、血清钙、血清铁水平均显著低于产后正常组,且有不良孕产史、25(OH)D<41.905nmol/L、血清钙<2.165mmol/L、血清铁<12.265mmol/L均是孕妇发生PPH的危险因素,提示不良孕产史及孕妇血清25(OH)D、血清钙、血清铁水平均与是否发生PPH有显著相关性。
3.2 不良孕产史及血清25(OH)D、钙、铁低水平影响孕妇PPH发生的机制探讨
既往有研究证实,发生PPH的孕妇不良孕产史比例显著高于未发生PPH的孕妇,并指出不良孕产史是孕妇发生PPH的危险因素[12]。原因可能为流产与引产次数增加可造成子宫壁变薄,同时降低子宫肌的收缩力,从而增加出血的可能性。而25(OH)D是VD的中间代谢物,因其具备较好稳定度与较长半衰期等特点,常被作为一种体现身体VD水平的标志物。在人体生理条件下,VD与其受体相结合,能增加体内钙水平[13]。近来有研究发现,宫缩功能与钙离子有关,孕期子宫肌细胞肥大,细胞质内富含具有收缩活性作用的肌凝与肌动蛋白,而钙离子进到子宫肌细胞后可结合肌凝与肌动蛋白,推动收缩及舒张子宫,以减少出血,且子宫璧间血管也可因肌肉收缩反应复始而受到有效挤压,便于血流被阻滞[14]。另外,钙离子在参与血液凝固过程中对应的是第Ⅳ凝血因子,能加速子宫内胎盘与子宫壁剥离面形成血栓,减少出血[15]。既往研究也认为,低水平25(OH)D是产妇阴道分娩发生PPH的关键危险因素之一,且其浓度与产妇发生PPH呈显著负相关[12]。本研究结果进一步从侧面证明了VD缺乏会明显提升产妇PPH的发生率,为孕期妇女需要更多VD摄入的研究提供了理论依据,同时也证实了血清钙水平与孕妇发生PPH的显著相关性。
血清铁是机体必需的微量元素,在人体内分布范围广,参与能量代谢及造血功能,如参与血红蛋白携氧及输送,而部分激素与酶的生成也有铁参与其中。临床上有研究表明随着妊娠期的增长,女性体内血清铁会逐步降低,在孕晚期达到最低水平[16]。血红蛋白水平的下降提升了PPH发生的风险,且携氧能力的降低也可造成分娩临产时子宫肌收缩不能正常进行,继而发生子宫收缩乏力性出血。
综上,不良孕产史、25(OH)D<41.905nmol/L、血清钙<2.165mmol/L、血清铁<12.265mmol/L均是孕妇发生PPH的危险因素,与是否发生PPH有显著相关性,对预防产后出血发生率具有重要参考意义。
