地塞米松玻璃体内植入剂联合抗VEGF药物治疗视网膜静脉阻塞
2022-10-11王晓波吴国基
王晓波,吴国基,刘 丛
0 引言
视网膜静脉阻塞(RVO)是仅次于糖尿病视网膜病变的第二大常见视网膜血管性疾病[1]。RVO的特点是视网膜静脉扩张迂曲,沿静脉分布区域的视网膜出血、水肿和渗出,累及黄斑区时引起黄斑水肿(macular edema,ME)。视网膜静脉阻塞继发黄斑水肿(macular edema secondary to retinal vein occlusion,RVO-ME)是导致视力下降的最主要原因[2]。黄斑水肿的产生被认为与静脉阻塞以后缺血缺氧诱导的血管内皮生长因子(vascular endothelial growth factor,VEGF)以及炎症因素导致的血-视网膜屏障破坏相关,因此目前临床上主要采用玻璃体腔内注射抗VEGF药物或糖皮质激素类药物的治疗方式[3]。抗VEGF药物起效快,半衰期短,在玻璃体腔维持时间约2~3wk,需要频繁给药;而地塞米松玻璃体内植入剂(Ozurdex,0.7mg)依靠其缓释装置可持续释放地塞米松长达3~6mo[3],合理假设两者联合治疗可降低注射次数同时又达到不低于单药治疗的效果。本研究旨在比较地塞米松玻璃体内植入剂联合抗VEGF药物与抗VEGF药物单药治疗RVO-ME的疗效和安全性。
1 对象和方法
1.1对象前瞻性随机对照研究。本研究纳入2019-06/2020-12在厦门大学附属厦门眼科中心接受治疗的RVO-ME患者133例133眼,其中男71例,女62例。纳入标准:(1)年龄>18岁;(2)结合广角眼底照相、眼底荧光素血管造影(fundus fluorescein angiography,FFA)与光学相干断层扫描(optical coherence tomography,OCT)仪检查,明确诊断为RVO-ME,包括视网膜中央静脉阻塞( central retinal vein occlusion,CRVO)和视网膜分支静脉阻塞(branch retinal vein occlusion,BRVO);(3)治疗前中央视网膜厚度(central retinal thickness,CRT)>250μm;(4)治疗前非接触式眼压计测得眼压10~21mmHg。排除标准:(1)妊娠及哺乳期妇女;(2)近期有心脑血管意外或症状的患者;(3)有青光眼病史或高危房角的患者;(4)影像学检查存在无灌注区,且既往未行视网膜光凝治疗、未行玻璃体腔注射曲安奈德或抗VEGF药物治疗。本研究经本院伦理委员会批准并取得所有患者知情同意。
1.2方法
1.2.1治疗方法
1.2.1.1治疗方案所有操作或手术均在患者知情同意后开始。单药治疗组接受每月注射康柏西普0.05mL (10mg/mL) 1次,连续3mo,每月复诊,如果达到再治疗标准,则再注射康柏西普1针,继续每月复诊。联合治疗组接受地塞米松玻璃体内植入剂注射1次,1wk后注射康柏西普0.05mL (10mg/mL)1次,每月复诊,如果达到再治疗标准,则再注射地塞米松玻璃体内植入剂1针(如果距注射地塞米松玻璃体内植入剂未超过3mo者,则改为注射康柏西普1针),继续每月复诊。再治疗标准:CRT>250μm或最佳矫正视力(BCVA)降低≥5个Snellen字母和/或CRT增加>50μm。
1.2.1.2手术步骤(1)术前3d开始局部滴5g/L左氧氟沙星滴眼液,每天4次,每次1滴;(2)术前给予复方托吡卡胺滴眼液充分散瞳(即对光反射消失),分别给予50g/L聚维酮碘溶液1mL浸泡消毒结膜囊约2min和生理盐水20mL冲洗结膜囊,盐酸丙美卡因滴眼液行表面麻醉;(3)采用30G注射针头在距离角膜缘3.5~4.0mm的巩膜处穿刺至眼球中心,注入康柏西普0.05mL(10mg/mL);或采用地塞米松玻璃体内植入剂自带的22G无菌专用给药器,在距离角膜缘3.5~4.0mm的巩膜处穿刺,注入地塞米松玻璃体内植入剂0.7mg;(4)按压穿刺口至穿刺口闭合,且无渗血渗液;(5)予3g/L氧氟沙星眼膏,包眼。
1.2.2观察指标观察两组患者治疗前(首次玻璃体腔注射前)、治疗后1、2、3、6mo时的BCVA(Snellen)、CRT情况,并观察联合治疗组患者地塞米松玻璃体内植入剂注射1wk后抗VEGF药物注射前的BCVA、CRT情况,记录首次玻璃体内注射至治疗6mo时康柏西普注射次数。此外,观察两组患者眼压升高和伴随使用的降眼压药物情况及白内障、感染性眼内炎、结膜出血、视网膜脱落等眼部并发症发生情况,并观察与玻璃体腔注射治疗相关的全身不良事件发生情况。
2 结果
2.1两组患者基本资料比较将纳入患者随机分配至两个治疗组,其中单药治疗组66例66眼接受玻璃体腔注射康柏西普治疗,联合治疗组67例67眼接受地塞米松玻璃体内植入剂联合玻璃体腔注射康柏西普治疗。治疗前两组患者基本资料比较,差异无统计学意义(均P>0.05,表1),具有可比性。

表1 两组患者基线资料比较
2.2两组患者治疗后BCVA及CRT改善情况治疗后1、2、3、6mo时,两组患者BCVA和CRT改善情况具有时间差异性(BCVA:F组间=0.676,P组间=0.413,F时间=132.250,P时间<0.001,F组间×时间=0.904,P组间×时间=0.379;CRT:F组间=0.711,P组间=0.401,F时间=177.009,P时间<0.001,F组间×时间=1.490,P组间×时间=0.228),治疗后1、2、3、6mo两组患者BCVA和CRT均较治疗前显著改善,见表2,图1。此外,联合治疗组在地塞米松玻璃体内植入剂注射1wk后(抗VEGF药物注射前)BCVA较治疗前提高8.28±1.27字母,CRT较治疗前降低311.34±24.53μm。
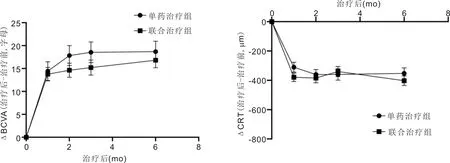
图1 治疗后两组患者BCVA和CRT改善情况比较 A:BCVA改善情况;B:CRT改善情况。

表2 两组患者治疗后BCVA及CRT改善情况
按照RVO类型进行亚组分析,BRVO患者中,治疗后1、2、3、6mo时,两组患者BCVA和CRT改善情况具有时间差异性(BCVA:F组间=0.052,P组间=0.821,F时间=88.600,P时间<0.001,F组间×时间=0.330,P组间×时间=0.624;CRT:F组间=3.529,P组间=0.064,F时间=111.731,P时间<0.001,F组间×时间=2.813,P组间×时间=0.069),治疗后1、2、3、6mo两组患者BCVA和CRT均较治疗前显著改善,见表3。CRVO患者中,治疗后1、2、3、6mo时,两组患者BCVA和CRT改善情况具有时间差异性(BCVA:F组间=0.937,P组间=0.338,F时间=43.732,P时间<0.001,F组间×时间=0.873,P组间×时间=0.408;CRT:F组间=0.287,P组间=0.595,F时间=75.534,P时间<0.001,F组间×时间=1.483,P组间×时间=0.232),治疗后1、2、3、6mo两组患者BCVA和CRT均较治疗前显著改善,见表4。

表3 BRVO患者治疗后BCVA及CRT改善情况

表4 CRVO患者治疗后BCVA及CRT改善情况
2.3两组患者康柏西普注射次数比较首次玻璃体腔注射至治疗6mo时,单药治疗组和联合治疗组康柏西普注射次数分别为3.56±0.12、2.96±0.17次,联合治疗组显著低于单药治疗组,差异有统计学意义(t=2.936,P=0.004)。BRVO患者中,联合治疗组康柏西普注射次数(2.59±0.15次)显著低于单药治疗组(3.39±0.12次),差异有统计学意义(t=4.117,P<0.001)。CRVO患者中,单药治疗组和联合治疗组康柏西普注射次数差异无统计学意义(3.84±0.23次vs3.65±0.36次,t=0.444,P=0.659)。
2.4不良反应随访至治疗后6mo,联合治疗组有18眼(26.9%)出现高眼压,其中2眼眼压≥35mmHg;单药治疗组有4眼(6.1%)出现高眼压,但无眼压≥35mmHg,两组患者高眼压发生率差异有统计学意义(χ2=10.425,P=0.001)。所有眼压升高患者局部使用降眼压滴眼液后眼压均恢复正常,无1例需要进行抗青光眼手术治疗。随访过程中,联合治疗组发生白内障加重4眼,均未行白内障手术,单药治疗组无患者出现白内障进展;两组患者均无玻璃体积血、眼内炎、视网膜脱离等不良反应发生,均未观察到全身不良事件发生。
3 讨论
RVO-ME的发生机制至今尚未完全阐明,RVO患者由于视网膜循环障碍,静脉迂曲扩张,沿视网膜静脉分布区域缺血、缺氧,造成血-视网膜屏障(blood retinal barrier,BRB)破坏,导致进入视网膜的液体增加,同时,Müller细胞和视网膜色素上皮(retinal pigment epithelium,RPE)细胞损伤,使得视网膜下空间和视网膜组织间液体的转运障碍,导致视网膜液体进入和流出之间的平衡被打乱,进而引起ME,其过程伴随多种复杂的细胞和细胞因子参与,在ME患者眼内液中发现VEGF和白细胞介素(IL)-1、IL-6、IL-8、单核细胞趋化蛋白-1(monocyte chemotactic protein-1,MCP-1)、肿瘤坏死因子(tumor necrosis factor-α,TNF-α)等炎症因子水平升高,这些因子在炎症和血管通透性增加方面发挥重要作用[4-5]。目前临床上抗VEGF药物单药治疗RVO-ME给药频次高,给药次数的增加不仅在客观上增加了注射相关并发症如玻璃体积血、视网膜脱离等的发生,在新型冠状病毒肺炎疫情情况下也给患者带来了较重的随访负担和经济负担。约42%的患者期望在保持疗效的前提下,尽量减少注射次数[6]。糖皮质激素与抗VEGF药物在RVO-ME的治疗中作用机制不同,联合用药可在降低玻璃体腔内VEGF浓度的同时抑制多种炎性细胞因子的产生,此外,两种药物在玻璃体腔内持续时间存在差异,联合用药可能实现更少的玻璃体腔内注射次数和更低的治疗负担,因此探索联合给药方案很有意义。
由于在RVO-ME的临床治疗中抗VEGF药物与糖皮质激素联合用药尚未有明确的给药剂量、给药时间间隔及频次的指南或共识推荐,既往国内外研究中联合给药方案不尽相同,与抗VEGF药物单药治疗对比的结果也存在些微差异。Fan等[7]和袁诗曼等[8]分别比较了雷珠单抗单药与雷珠单抗联合曲安奈德玻璃体腔内注射的有效性及安全性,结果发现玻璃体腔单独注射雷珠单抗或联合曲安奈德均可减轻RVO患者的黄斑水肿并改善视力,联合治疗虽能减少注药次数,但两者治疗效果无明显差异。部分学者为了降低高眼压及白内障等激素相关不良反应发生率,在治疗时尝试玻璃体腔注射抗VEGF药物联合Tenon囊注射曲安奈德给药方案,李婷婷等[9]和Moon等[10]研究结果发现在给药后1、3mo,联合治疗组黄斑中心凹厚度(central macular thickness,CMT)改善明显优于单药组,但治疗后6mo两治疗组间CMT变化差异无统计学意义。随着玻璃体内缓释制剂Ozurdex的上市,更多学者开始探索抗VEGF药物联合不同激素制剂的临床效果。Maturi等[11]在一项前瞻性临床研究中纳入30例RVO患者,按1∶1随机分配至贝伐单抗单药治疗组和联合地塞米松玻璃体内植入剂组(联合组)。初始治疗所有患者均接受1次玻璃体腔贝伐单抗(1.25mg)注射,1wk后,单药组接受假注射,而联合组进行1次地塞米松玻璃体内植入剂注射。结果发现,与接受单药治疗的患者相比,联合组患者虽然在视力较基线的平均变化方面无差异,但仅需更少的贝伐单抗再注射次数(2次vs3次,P=0.02),且CRT平均降低幅度更大(-56μmvs+45μm,P=0.01)。
本研究中对比了抗VEGF单药“3+PRN”给药方案与地塞米松玻璃体内植入剂联合抗VEGF药物“1+1+PRN”给药方案治疗RVO-ME的疗效和安全性,结果显示联合治疗组在地塞米松玻璃体内植入剂注射1wk后(抗VEGF药物注射前)BCVA和CRT均较治疗前显著改善,说明地塞米松玻璃体内植入剂治疗RVO-ME能够快速起效,1wk即可显著改善BCVA和CRT,这与其药代动力学曲线相符[12]。治疗后单药治疗组和联合治疗组患者的BCVA、CRT均较治疗前显著改善,提示两种给药方案均可在RVO-ME中获得良好疗效。在治疗后任何时间点两组间BCVA和CRT改善均无统计学差异,但联合治疗组注射次数显著低于单药治疗组,说明该联合治疗方案可在减少抗VEGF药物注射次数的同时达到与抗VEGF药物单药治疗相似的疗效,这与既往研究结果[11]一致。在安全性方面,联合治疗组高眼压和白内障发生率均高于单药治疗组,这也是激素类药物最常见的眼部并发症,对于这部分患者需严密监控眼压升高和白内障进展情况,及时干预。
本研究还进一步分析了不同治疗方案分别在BRVO和CRVO患者中的疗效差异。结果发现,在BRVO患者中,两种治疗方案下治疗后任意时间点的BCVA改善情况均无统计学差异,但联合治疗组抗VEGF药物注射次数显著低于单药治疗组(P<0.001),说明BRVO联合治疗组患者在治疗后6mo内通过更少的玻璃体腔内注药获得了更优的解剖学结局。值得注意的是,本研究表明BRVO患者治疗后6mo时CRT的减轻和视力的提高并不是同步的,考虑可能原因为目前对于BCVA提高和CRT下降的关系并没有明确共识,也就是说,有可能两者的关系本身就不是同步的;其次,由于样本量较小且随访时间短,远期疗效的数据并没有纳入本研究统计分析中。亚组分析中CRVO患者在两种治疗方案下治疗后所有随访时间点BCVA和CRT改善情况均无统计学差异,且两组间抗VEGF药物注射次数也无差异,这可能是由于CRVO发病机制较BRVO更为复杂,全身影响因素更多[1,2,13-14],ME易反复所致。
综上所述,地塞米松玻璃体内植入剂联合抗VEGF药物是治疗RVO-ME的有效方法,可显著改善视力,降低CRT,该治疗方案可在减少抗VEGF药物注射次数的同时达到与抗VEGF药物单药治疗相似的疗效,但需要监控眼压变化及白内障进展情况。由于本研究纳入的样本量较少、随访时间短,存在一定的局限性,但研究结果仍提示值得进一步开展多中心、大样本量、长期随访的随机对照研究,为临床治疗RVO-ME探索更加科学、安全、经济的联合给药方案。
