南葶苈子及炒南葶苈子标准饮片的均匀化方法研究*
2022-10-10丁明雅张雅倩杨玉乔李晋何俊常艳旭
丁明雅,张雅倩,杨玉乔,李晋,何俊,常艳旭
(天津中医药大学,天津市现代中药重点实验室,天津 301617)
中药标准饮片是按照一定的技术规范制成,能体现中药整体性和专属性的标准物质形式,是衡量中药饮片质量最合适的“标准物质”[1]。当前可以被用作标准物质的化学对照品、对照药材及对照提取物仍无法反映中药饮片的科学内涵和特征属性[2]。中国药典中中药饮片标准多数参考药材的标准,缺乏专属性和客观性。因此建立中药饮片专属标准,健全中药饮片标准体系是及其必要的。通常来说标准饮片质量均匀是其质量稳定的重要表现[3-4]。标准饮片均匀化研究可确保中药临床用药的安全性和有效性,为建立健全中药标准体系提供基础性研究方案。
南葶苈子为十字花科植物播娘蒿Descurainia sophia(L.)Webb ex Prantl.的干燥成熟种子,其最早记录在《神农本草经》中。南葶苈子有下气行水、清热活血、利尿消肿[5-6]的功效。主治痰液积聚,咳嗽痰多,呼吸困难,胸腹水肿等症。南葶苈子中化学成分主要有强心苷类、黄酮类、脂肪油类及有机酸类等[7-9],其对呼吸系统、泌尿系统、循环系统疾病的治疗都具有积极作用[10-11]。但有关南葶苈子及炒南葶苈子制备标准饮片的相关报道较少。开展南葶苈子及炒南葶苈子标准饮片制备研究有利于其市场质量监管,其标准饮片的均匀化方法研究同时有利于保障饮片安全性、有效性和质量可控性[1,12-14]。本文以出粉率、3种黄酮类化合物的总含量及指纹图谱峰总面积为指标,考察了粉碎时间、粉碎次数、投料量对于标准饮片均匀化方法的影响[12-14],优化南葶苈子及炒南葶苈子粉碎工艺,为南葶苈子和炒南葶苈子标准饮片均匀化技术规范的制定提供了参考依据。
1 仪器和试剂
1.1 仪器 Waters ACQUITY超高效液相色谱仪(美国Waters公司);AX205型十万分之一电子天平(瑞士METTLER TOLEDO公司);小型粉碎机(天津市泰斯特仪器有限公司);SB-1000YDTD型超声清洗槽(宁波新芝生物科技股份有限公司);Mill-Q II型超纯水器(Millipore公司);3K15型离心机(半径11 cm,德国Sigma公司);XW-80A型旋涡混合器(上海沪西分析仪器厂)。
1.2 试剂 乙腈来自Merk公司、甲醇来自Fisher公司、甲酸来自Tedia公司,所有有机试剂均为色谱纯;实验用水均由Millipore超纯水系统制得。
2 药品与方法
2.1 药材与标准品 南葶苈子和炒南葶苈子药材于2016年购买于安国药材市场,经天津中医药大学马琳教授鉴定为十字花科植物播娘嵩Descurainia sophia(L.)Webb.ex Prantl.的干燥成熟种子,并按照2015版药典进行净制和炮制,获得南亭苈子饮片和炒葶苈子饮片。所有样品干燥24 h后,在规定目数筛子下筛分备用(干燥温度:60℃;筛子:65目)。黄酮类标准品槲皮素-3-O-β-D-吡喃葡萄糖-7-O-β-D-龙胆双糖苷(批号:PCS0375)、槲皮素-3-O-β-D-吡喃葡萄糖苷(批号:CHB160912)、异鼠李素-3-O-β-D-吡喃葡萄糖(批号:PS14012301)均来自德思特生物科技有限公司(成都),高效液相分析纯度均≥98%。
2.2 正交实验采用设计L9(34)正交实验表(表1),考察粉碎时间(A)、粉碎次数(B)和投料量(C)均对饮片出粉率有影响。
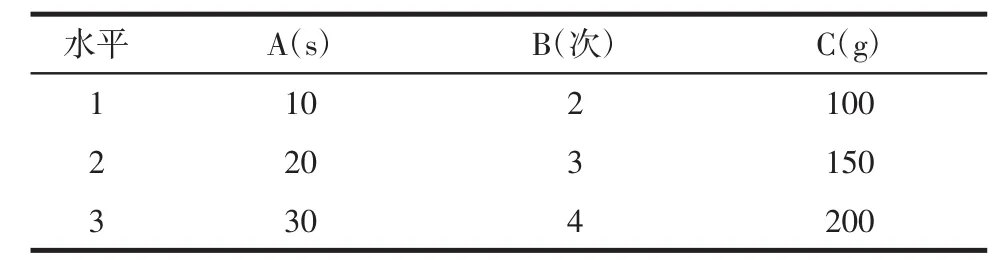
表1 正交试验因素与水平Tab.1 Factors and levels of orthogonal test
2.3 3种黄酮成分含量测定
2.3.1 标准品溶液的制备 3种黄酮类成分分别加甲醇制成质量浓度均为1.00 mg/mL的对照品母液。分别精密量取各母液适量配制成浓度分别为500 μg/mL(槲皮素-3-O-β-D-吡喃葡萄糖-7-O-β-D-龙胆双糖)、50 μg/mL(槲皮素-3-O-β-D-吡喃葡萄糖苷)、50 μg/mL(异鼠李素-3-O-β-D-吡喃葡萄糖苷)的混合标准品溶液,按照一定比例向下逐级稀释成所需浓度,备用。
2.3.2 样品的制备 精密称取0.750 g样品粉末于锥形瓶中,超声30 min进行样品提取(提取溶剂为60%的甲醇,10 mL),超声前后对具塞锥形瓶总质量进行称质量,用提取溶液补足质量差,混匀后14 000 rpm离心10 min,离心半径为8 cm,取上清,经0.22 μm针式过滤器过滤后进样分析[15]。
2.3.3 色谱条件色谱柱:ACQUITYBEHC18(1.7μm,2.1×100mm);保护柱:Waters C18柱(2.1 mm×12.5 mm,5 μm);流速:0.3 mL/min;进样量:2 μL;柱温:30 ℃;波长扫描:265 nm;检测时间:16 min;流动相:含0.1%甲酸的水溶液(A)- 乙腈(B);采用梯度洗脱。见表2。

表2 梯度洗脱程序表Tab.2 Gradient elution procedure
2.3.4 出粉率的测定 对已称质量样品粉末进行粉末化处理,粉碎尽可能完全,过4号筛(65目),分离粉末和药渣,计算出粉率。
3 结果
3.1 单因素考察 以出粉率为指标,考察了饮片投料量、打粉时间、打粉次数对饮片粉碎工艺的影响。研究结果表明,当南葶苈子投料量为100 g和150 g时,饮片出粉率没有明显差异,综合考虑以150 g投料量为最佳,出粉率为74.0%。考察不同打粉时间(10 s、20 s、30 s)对粉碎工艺的影响,结果显示单次打粉20 s出粉率最高,为72.8%。考察打粉次数(2次、3次、4次)对粉碎工艺的影响,发现打粉4次时饮片出粉率较其他组高,为83%。因此,通过单因素实验确定了南葶苈子最佳粉碎工艺为:投料量150 g,打粉4次,单次打粉时间20 s。按照相同的方法,确定了炒南葶苈子最佳粉碎工艺为:投料量100 g,打粉4次,单次打粉时间20 s。
3.2 3个黄酮类化合物的含量测定
3.2.1 标准曲线及线性范围 将配置好的混合标准溶液用甲醇逐级稀释成不同浓度的混合标准溶液,分别进样分析,按横、纵坐标分别为浓度(μg/mL)和峰面积进行线性拟合,结果见表3。

表3 3种黄酮类成分的线性回归方程Tab.3 Linearity and regression equations of three flavonoids
3.2.2 精密度实验 精密吸取同一批供试品溶液于1日内连续进样6次,结果显示3种黄酮类化合物6次进样峰面积相对标准差(RSD)分别为1.38%、0.40%、0.84%,表明仪器精密度良好。
3.2.3 稳定性实验 准确吸取适量供试品溶液,分别于1日内不同时间点进样分析,加样第1个点设置为0 h,依次按照选取的时间间隔进样分析供试样品,共记录24 h,实验结束后依次计算供试品溶液中3个黄酮类化合物在不同时间点峰面积的相对标准偏差,结果显示3个化合物连续24 h内不同时间点进样峰面积 RSD 分别为:1.43%、1.87%、2.06%,表明样品溶液24 h内稳定。
3.2.4 重复性实验 精密称取同一批次南葶苈子样品粉末,平行制备6份样品溶液,连续进样分析。计算所得峰面积换算成化合物浓度,分别计算6份样品中3种黄酮类化合物的含量,结果显示3种黄酮类化合物含量的RSD值分别为 3.72%、4.92%、3.82%,说明供试品样品处理方法重复性良好。
3.2.5 指纹图谱测定 取正交实验9份样品粉末,分别检测指纹图谱,计算UPLC指纹图谱峰面积大于3 000的指纹峰总面积结果见表4[18]。南葶苈子生品与炮制品指纹图谱结果分别见图1和图2。并通过标准品对其共有指纹峰进行比对,指认了其中5个色谱峰分别为槲皮素-3-O-β-D-吡喃葡萄糖-7-O-β-D-龙胆双糖苷、槲皮素-3-O-β-D-吡喃葡萄糖苷、异鼠李素-3-O-β-D-吡喃葡萄糖、芥子酸和异鼠李素(图3B)。

表4 南葶苈子和炒南葶苈子样品L9(34)正交实验设计结果Tab.4Results for orthogonal test L9(34)of raw and stir-fried Descurainiae Semen

图1 南葶苈子样品超高效液相色谱指纹图谱Fig.1 Ultra high-performance liquid chromatography fingerprint of Descurainiae Semen

图2 炒南葶苈子样品UPLC指纹图谱Fig.2 Ultra high-performance liquid chromatography fingerprint of stir-fried Descurainiae Semen

图3 典型色谱图谱Fig.3 Typical chromatography
3.3 3个黄酮类化合物的总含量测定 按照正交实验计算出的9组制备工艺分别制备南葶苈子及炒南葶苈子样品粉末,采用UPLC法测各组样品粉末中所含3种黄酮类化合物的总含量。按照上述色谱条件进样分析南葶苈子及混合对照品典型色谱图见图3。
3.4 正交实验结果
3.4.1 综合评分法分析正交实验结果 本实验采用加权法对正交实验结果进行综合评分,选用出粉率(D)、3个黄酮类化合物的总含量(E)、指纹图谱总峰面积(F)作为均匀化方法考察的指标,根据所测指标在南葶苈子饮片均匀化工艺中的主次顺序确定各指标权重[17],系数分别为:0.3、0.4、0.3。

3.4.2 数据处理与分析 南葶苈子及炒南葶苈子综合评分结果见表4,方差分析结果见表5。南葶苈子和炒南葶苈子方差分析结果显示粉碎时间对实验结果影响较小。在α=0.05条件下,粉碎时间、粉碎次数和投料量对粉碎工艺没有显著性的影响可能是因素间交互作用或误差自由度小的原因。因此,根据直观分析结果,影响南葶苈子饮片均匀化因素的主次顺序为:C(投料量)>B(粉碎次数)>A(粉碎时间),A2>A3>A1,B3>B1>B2,C2>C1>C3。为节省生产成本,最佳均匀化方法选择A1B3C2,即用150 g南葶苈子饮片,粉碎4次,每次10 s。同理直观分析结果显示,影响炒南葶苈子综合评分因素的主次顺序为:B(粉碎次数)>C(投料量)>A(粉碎时间),A2>A3>A1,B2>B3>B1,C1>C3>C2。综合考虑,最佳均匀化方法为A1B2C1,即用100 g炒南葶苈子饮片,粉碎3次,每次10 s。
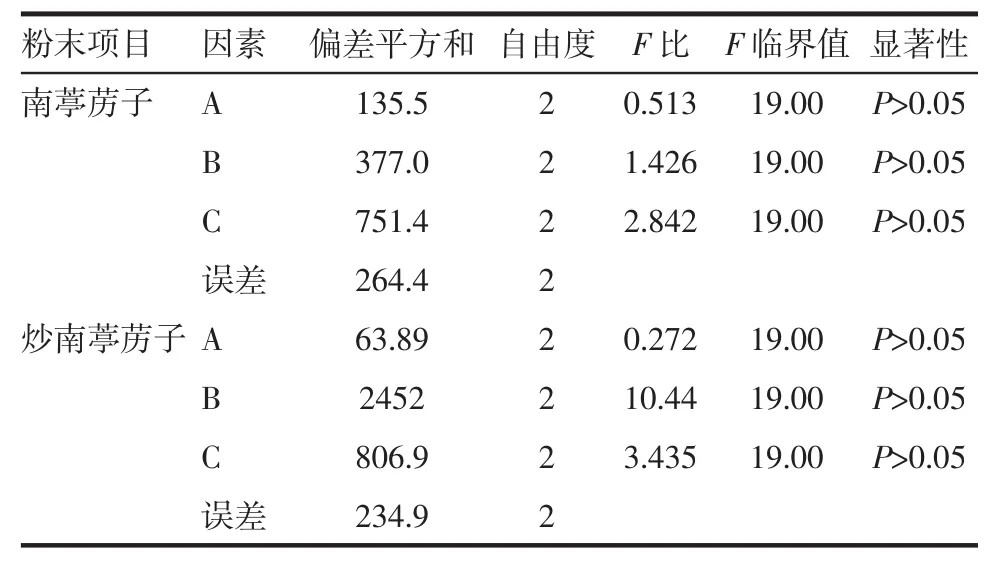
表5 南葶苈子和炒南葶苈子标准饮片均匀化粉碎工艺方差分析结果Tab.5 Analysis of variance of homogenization crushing process of standard decoction pieces of raw and stir-fried Descurainiae Semen
3.4.3 南葶苈子和炒南葶苈子最佳均匀化工艺验证实验 根据正交实验所得的最优均匀化工艺对南葶苈子及炒南葶苈子样品进行粉碎,实验平行3次,计算每份粉末的出粉率,并测定指纹图谱总峰面积和3个黄酮类化合物的总含量。最佳粉碎工艺验证结果见表6。
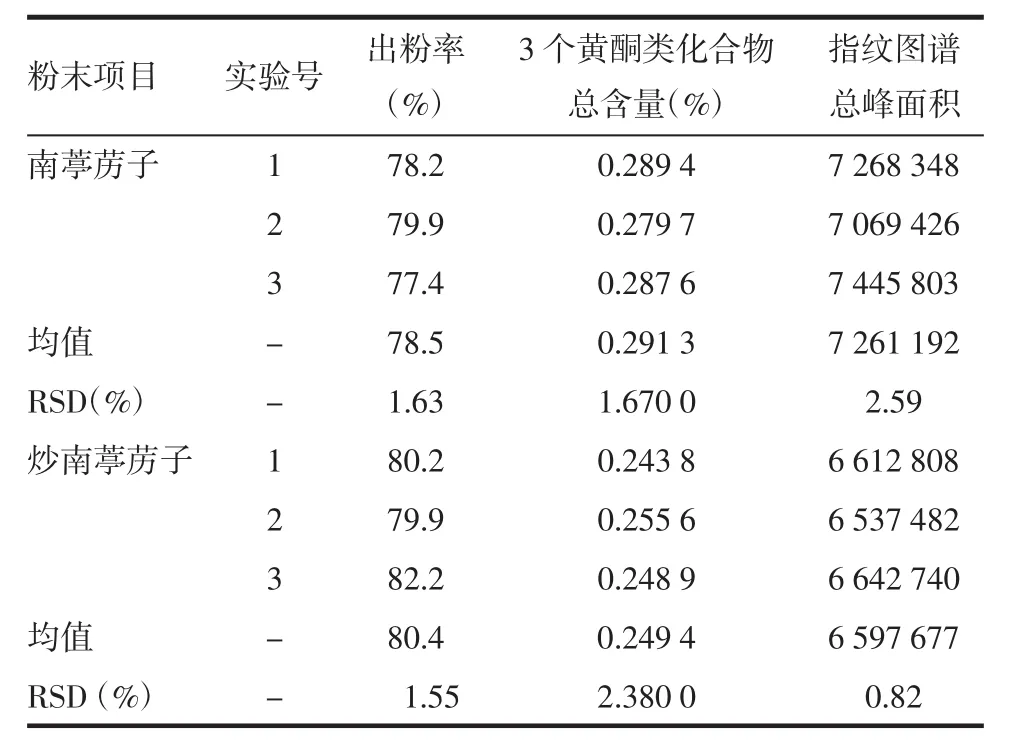
表6 南葶苈子和炒南葶苈子最佳均匀化工艺验证实验Tab.6 Verification test of optimal homogenization process of raw and stir-fried Descurainiae Semen
4 讨论
中药标准饮片处理是否均匀对于药物性质、属性的表达具有关键的作用,而粉碎工艺在标准饮片均匀化工艺中占绝对的比重,对粉碎工艺进行研究是中药饮片标准制定的基础也是必不可少的步骤。本文通过正交实验对中药南葶苈子及其炮制品进行粉碎均匀化研究,经验证发现最佳均匀化方法制备的样品其不同测定指标值均可以稳定实现,研究结果准确可靠,为南葶苈子标准饮片进一步研究提供基础性研究材料。
单一指标通常会导致优化结果的不准确,多指标优化不仅避免单指标优化的缺陷,还可以较为合理地优选南葶苈子及炒南葶苈子标准饮片均匀化方法,使研究更具有专属性,说服性[18-19]。本研究选择3个关键考察指标对标准饮片均匀化工艺进行优选,其中饮片出粉率反映了饮片的粉碎效率,通过调节粉碎过程的关键因素来实现出粉率最大化;本研究所选的槲皮素-3-O-β-D-葡萄糖-7-O-β-D-龙胆双糖苷、槲皮素-3-O-β-D-葡萄糖苷、异鼠李素-3-O-β-D-葡萄糖苷3个含量测定的化合物是南葶苈子样品中含量相对较高且又具有代表性的黄酮类成分,将其作为南葶苈子药材质量控制的指标性成分[20];指纹图谱可以较好地反映药材中化合物信息,为饮片中化学成分系统的研究提供了研究方法,同时在265 nm波长下测定的色谱峰响应值高,出峰较多,各色谱峰之间分离度较好,保留时间适中,故选择265 nm下总峰面积,更能相对全面地评价南葶苈子的饮片质量[21]。研究选用多指标优化均匀化工艺不仅填补了研究空白,也为后期标准饮片相关质量控制提供可资借鉴的案例。南葶苈子及炒南葶苈子标准饮片粉碎工艺研究,为中药标准饮片均匀化技术研究提供支撑材料[22]。
5 结论
以出粉率、3个黄酮类化合物的总含量、指纹图谱总峰面积作为指标,对投料量、单次粉碎时间、粉碎次数3个因素进行考察,优化南葶苈子和炒南葶苈子标准饮片的均匀化方法,确定南葶苈子最佳均匀化工艺:投料量150 g,单次粉碎时间10 s,粉碎4次;炒南葶苈子饮片最佳均匀化工艺:投料量100 g,单次粉碎时间10 s,粉碎3次。标准饮片均匀化研究确保了中药临床用药的安全性和有效性,为建立健全中药标准体系提供基础性研究方案。
