枸杞环肽调控NLRP3及NF-κB信号通路减轻BaP诱导的气道上皮细胞炎性损伤
2022-10-09赵传欣李叶婷卜凡莉郑曼
赵传欣,李叶婷,卜凡莉,郑曼
(东营市人民医院,山东东营 257091)
苯并芘(Benzopyrene,BaP)是重要的大气污染物,化石燃料的燃烧及烧烤、油炸过程会产生大量的苯并芘[1]。苯并芘吸入或皮肤接触会导致机体DNA损伤,造成呼吸系统及皮肤炎症,持续大量苯并芘暴露会导致肺癌[2]、皮肤癌[3]等疾病。
炎症是机体对外界刺激的一种防御反应,大多数情况下是有益的,但当炎症朝着不受控制的情况发展就会损害机体健康[4]。支气管炎是一种常见的气道炎症,临床表现以咳嗽为主,常伴有咽痛、鼻塞等症状,对患者的生活质量造成很大影响[5]。同时,慢性支气管炎还有可能发展成为慢性阻塞性肺疾病[6]、肺源性心脏病[7]等,严重危害患者的身体健康。研究发现,苯并芘暴露会诱发或加重支气管炎、慢性支气管炎及慢性阻塞性肺疾病等疾病[8],但现代医学对于支气管炎等相关呼吸道疾病尚未有良好对策。
枸杞是茄科枸杞属植物,广泛分布于亚、欧及北美干旱和半干旱地区[9]。在中国,枸杞作为药物使用的历史可追溯到2300年前,人们日常生活中常见的枸杞子多是由宁夏枸杞的果实制成[10]。《本草纲目》记载,枸杞子能够补肝明目;现代医学证实,枸杞含有多种多糖、类胡萝卜素、类黄酮、生物碱等活性物质[11],具有抗炎[12,13]、免疫调节[14]、抗氧化[15]等活性。人们前期的研究主要集中在枸杞中的多糖类物质,同样具有免疫调节、抗氧化、降血压等功能的糖肽、ACE抑制肽等肽类物质很容易被忽视[16,17],而针对枸杞环肽能否抑制BaP导致的气道上皮细胞损伤的活性及机制鲜有报道。因此,本实验将构建BaP暴露气道上皮细胞模型并通过活性追踪方法分离枸杞活性肽,在此基础上进一步研究其潜在的活性及机制,以期为枸杞活性肽类物质的研究奠定一定的实验基础。
1 材料与方法
1.1 材料与试剂
人支气管上皮16-HBE细胞,中国科学院上海细胞生物研究所;苯并芘,阿拉丁试剂有限公司;DMEM基础培养基、胎牛血清-FBS和青霉素-链霉素混合液,美国Gbico;BCA蛋白质浓度测定试剂盒,碧云天生物技术研究所;Human PGE2Elisa Kit、一氧化氮(NO)含量检测试剂盒,北京索莱宝科技有限公司;Human IL-1β(白细胞介素-1β)和Human TNF-α(肿瘤坏死因子-α)ELISA试剂盒,北京四正柏生物科技有限公司;IκB、p-IκB、p65、p-p65、NLRP3、ASC、COX-2和iNOS的一抗抗体,美国CST。
1.2 仪器与设备
SW-CJ-IC超净工作台,苏州;INCO2108 CO2培养箱,德国Memmert;2K15低温高速离心机,美国Sigma公司;Waters R2487高效液相色谱(High Performance Liquid Chromatography,HPLC),美国沃特世;液质联用(Liquid Chromatography-Mass Spectrometry,LC/MS),美国Agilent Technologies;组织匀浆器,Ultra-Turrax;IKALabortechnik,德国Staufen;Epics Altra型流式细胞仪,美国Beckman;3-30 K高速台式冷冻离心机,美国Sigma公司。
1.3 方法
1.3.1 枸杞活性肽的分离、鉴定
1.3.1.1 枸杞粗蛋白制备
将干枸杞(1.0 kg)匀浆与异丙醇按1:5(m/V)的比例混合,断搅拌2 h。收集沉积物,冷冻干燥并储存在-80 ℃。脱脂沉淀物(205 g)溶解在0.25 mol/L磷酸盐缓冲溶液(PBS,pH值7.3)中(10%,m/V)。离心(9 000g,12 min),上清液冻干,作为枸杞总蛋白。
1.3.1.2 超滤、疏水层析
超滤色谱法:采用分子量为1 ku的超滤膜对枸杞总蛋白进行超滤分离。收集LBP-A(Mw<1 ku)和LBP-B(Mw>1 ku)两个组分,冷冻干燥。评价LBP-A和LBP-B对BaP暴露的16-HBE细胞的保护活性,收集具有最佳保护活性部分。
1.3.1.3 疏水色谱法
将LBP-A(27.3 g)溶解于用30 mmol/L磷酸盐缓冲液(pH值7.3)制备的1.60 mol/L (NH4)2SO4中。苯基Sepharose CL-4B疏水色谱柱(3.0 cm×100 cm),30 mm磷酸盐缓冲液(pH值7.3)2.5 mL/min的流速梯度[1.60、0.80和0 mol/L (NH4)2SO4]洗脱。300 nm监测,收集10个组分(LBP-A-1~10,每个组分500 mL),并将组分进行冷冻干燥。评价LBP-A-1~10对BaP暴露的16-HBE细胞的保护活性,收集具有最佳保护活性部分。
1.3.1.4 阴离子交换色谱法
将LBP-A-4溶液(3 mL,2.27 g/mL)上样于DEAE-52纤维素阴离子交换柱(Sigma-Aldrich,上海,3.0 cm×100 cm),去离子水预平衡。2.0 mL/min的流量,0、0.20、0.40和0.80 mol/L (NH4)2SO4溶液梯度洗脱。300 nm监测,收集10个组分(LBP-A-4-1~10,每个组分500 mL),并将组分进行冷冻干燥。评价LBP-A-4-1~10对BaP诱导的16-HBE细胞的保护活性,收集具有最佳保护活性部分。
1.3.1.5 凝胶过滤色谱法
LBP-A-4-4溶液(1.5 mL,366 mg/mL)上样于Sephadex G-15柱(Sigma-Aldrich,上海,3.0 cm×100 cm),2.0 mL/min的流量用0.40 mol/L (NH4)2SO4溶液洗脱。300 nm监测,收集10个组分(LBP-A-4-4-1~10,每个组分300 mL),并将组分进行冷冻干燥。评价LBP-A-4-4-1~10对BaP暴露的16-HBE细胞的保护活性,收集具有最佳保护活性部分。
1.3.1.6 RP-HPLC法
LBP-A-4-4-1通过RP-HPLC(Agilent 1200 HPLC)分析制备,Zorbax,SB C-18柱(4.6×250 mm,5 µm)。洗脱溶剂体系为水-三氟乙酸(溶剂A;100:0.1,V/V)和乙腈-三氟乙酸(溶剂B;100:0.1,V/V)。以2.0 mL/min的流量从30%到60%的溶剂B梯度洗脱60 min,检测波长设置为300 nm。将分离得到的化合物组分进行冷冻干燥,最终分离获得两个枸杞肽类活性化合物枸杞活性肽-1(LBP-1)及枸杞活性肽-2(LBP-2)。
1.3.1.7 LBP-1~2的分子量测定及氨基酸序列分析
SCIEX500R Q-TOF质谱仪(Framingham,美国)进行HPLC-ESI-MS分析。质谱条件:ESI源质量范围设为m/z50~1 500,以正离子模式采集Q-TOF-MS数据。MS分析条件为:CAD气体流量7 L/min;干燥气体温度,550 ℃;离子喷涂电压,5 500 V;去聚电位,80 V。软件生成的数据文件:SCIEX OS 1.0。
1.3.2 细胞培养
将质量分数分别为10%的FBS、1%的青霉素-链霉素混合液和89%的DMEM基础培养基混合后配置成DMEN完全培养基用于后续实验;将16-HBE细胞接种于含有DMEM完全培养基的T75细胞培养瓶中,隔日换液;待细胞处于对数生长期后即可以1:3的比例进行传代或收集细胞进行后续实验。
1.3.3 细胞活力检测
将16-HBE细胞密度调整为每毫升1×105个细胞,于96孔板中每孔接种100 μL,37 ℃、体积分数5% CO2的培养箱中培养,隔日换液。分为4组,每组6个复孔,第1组细胞不做任何处理,第2~4组的细胞培养基中分别加入不同浓度的LBP-1、LBP-2,培养箱中孵育48 h后,每孔加入CCK-8试剂10 μL,温育4 h,酶标仪测定450 nm处的吸光度,检测LBP-1、LBP-2的细胞毒性。
将16-HBE细胞密度调整为每毫升1×105个细胞,于96孔板中每孔接种100 μL,37 ℃、5% CO2的培养箱中培养。分为4组,每组6个复孔,第1组细胞不做任何处理,第2~4组加入终浓度为10 μmol/L的BaP,孵育12 h后,第3、4组分别加入终浓度为10 μmol/L的LBP-1及LBP-2,培养箱中孵育12 h。每孔加入CCK-8试剂10 μL,温育4 h,酶标仪测定450 nm处的吸光度,评价LBP-1、LBP-2的保护活性。
1.3.4 ELISA检测16-HBE细胞炎症因子分泌
将16-HBE细胞密度调整为每毫升1×105个细胞,于24孔板中每孔接种1 mL,37 ℃、体积分数5% CO2的培养箱中培养。分为4组:①空白对照组(Control),②B aP 组(BaP),③10 μmol/L LBP-1组,④50 μmol/L LBP-1组,每组3个复孔。①不做任何处理,②③④加入终浓度为10 μmol/L的BaP,孵育12 h后,③加入终浓度为10 μmol/L的LBP-1,④加入终浓度为50 μmol/L的LBP-1。再次孵育12 h,收集细胞培养基,1 400 r/min离心5 min,收集上清液。参照IL-1β、TNF-α、NO和PGE2的ELISA试剂盒说明书检测细胞上清液中炎症因子含量。
1.3.5 Western Blot检测相关蛋白的表达
将16-HBE细胞密度调整为每毫升3×105个细胞,于6孔板中每孔接种3 mL,37 ℃、体积分数5% CO2的培养箱中培养。参照方法1.3.4分组处理,收集细胞,加入适量RIPA裂解液提取细胞总蛋白。参考文献方法,Western Blotting检测NF-κB信号通路及NLRP3炎症小体相关蛋白的表达。
1.3.6 数据处理
所有数据采用SPSS 18软件进行统计。对阴性对照和阳性对照采用独立样本t检验,对LBP-1处理效应进行回归分析。p<0.05表明具有显著差异,p<0.01表明具有极显著差异,结果均以平均值±标准差表示。
2 结果与分析
2.1 枸杞环肽的分离鉴定
LBP-1:白色粉末,m/z564.245 0离子是[M+H]+,确定分子式为C29H33N5O7;m/z546.234 3离子是[M-H2O+H]+;m/z463.197 7离子是[M-Thr+H2O+H]+;m/z435.200 6离子是[M-Glu+H2O+H]+;m/z417.183 3离子是[M-Phe+H2O+H]+;m/z378.166 0离子是[M-Trp+H2O+H]+;m/z316.129 0离子是[Glu-Trp-H2O+H]+;m/z288.134 4离子是[Thr+Trp-H2O+H]+;m/z249.123 0离子是[Phe-Thr-H2O+H]+;m/z187.086 5离子是[Trp-H2O+H]+;m/z159.091 5离子是[Trp-COOH+H]+;m/z102.055 4离子是[Glu-COOH+H]+;m/z74.061 9离子是[Thr-COOH+H]+;最终,确认LBP-1是环-(Trp-Glu-Phe-Thr)肽。
LBP-2:白色粉末,m/z497.284 3离子是[M+H]+,确定分子式为C26H36N6O4;m/z469.289 7离子是[M-CO+H]+;m/z398.216 4离子是[M-Val+H2O+H]+;m/z384.201 2离子是[M-Leu+H2O+H]+;m/z380.205 3离子是[M-Val+H]+;m/z350.216 8离子是[M-Phe+H2O+H]+;m/z285.132 5离子是[His-Phe-2H2O+H]+;m/z261.158 2离子是[Leu-Phe-2H2O+H]+;m/z237.133 2离子是[His-Val-2H2O+H]+;m/z212.116 9离子是[Val-Leu-2H2O+H]+;m/z138.065 6离 子 是[His-H2O+H]+;m/z110.070 8离子是[His-COOH+H]+;m/z86.097 5离子是[Leu-COOH+H]+;最终,确认LBP-2是环-(Leu-Val-His-Phe)肽。
2.2 LBPs对16-HBE细胞的保护作用
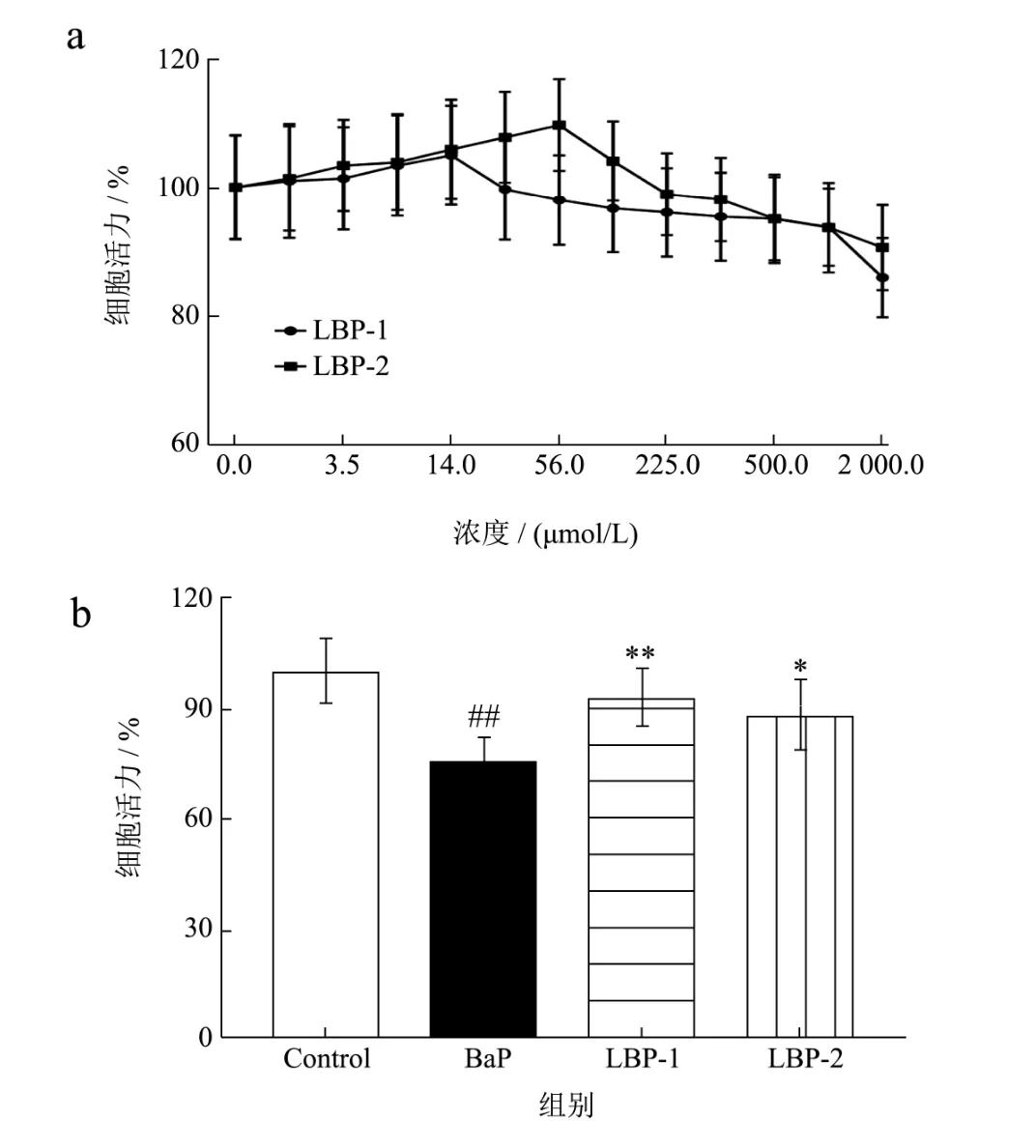
图2 LBP-1、LBP-2的细胞毒性及对16-HBE细胞的保护活性Fig.2 Cytotoxicity of LBP-1 and LBP-2 and their protective activity on 16-HBE cells
本研究检测了LBP-1、LBP-2的细胞毒性。结果如图2a,LBP-1、LBP-2的浓度低于1.0 mmol/L时,16-HBE细胞活力与空白对照组相比均无显著差异(p>0.05)。表明,LBP-1、LBP-2的浓度低于1.0 mmol/L时,无显著细胞毒性,因此后续实验将LBP-1、LBP-2的浓度设置为低于1.0 mmol/L。
由图2b可知,相比于空白对照组,经10 μmol/L的BaP处理12 h后,16-HBE细胞的活力降低24.84%(p<0.01);而经LBP-1及LBP-2处理12 h后,BaP暴露导致的16-HBE细胞活力降低被显著抑制。相比于BaP组,LBP-1、LBP-2组细胞活力分别提高了17.83%(p<0.01)及12.78%(p<0.05)。考虑到LBP-1的保护活性比LBP-2更佳,因此选择LBP-1进行后续研究。
2.3 LBP-1抑制BaP诱导的16-HBE细胞炎症因子分泌

图3 LBP-1对BaP诱导的16-HBE细胞炎症因子分泌的影响Fig.3 Effect of LBP-1 on the secretion of inflammatory factors in 16-HBE cells induced by BaP
促炎因子是一类由机体的免疫和非免疫细胞合成和分泌的小分子多肽类物质,它们调节多种细胞生理功能,并在创伤、疼痛、感染等应激过程中起重要作用。促炎性细胞因子包括白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)和肿瘤坏死因子-α(TNF-α)等[14]。TNF-α主要由巨噬细胞和淋巴细胞分泌,以应对感染或其他外界刺激引起的细胞损伤[15],同时它也可由如上皮细胞等许多其他类型的细胞和组织分泌[18];IL-1β与TNF-α类似,是一种促炎细胞因子[19]。本研究中,BaP暴露使16-HBE细胞IL-1β与TNF-α分泌显著增加,而LBP-1干预后,BaP诱导的IL-1β与TNF-α过量分泌被显著抑制。
BaP会导致炎症的发生[20],结果如图3所示,BaP暴露会诱发16-HBE细胞炎性细胞因子(TNF-α、IL-1β、IL-18和IL-6)的过量分泌。相比于空白对照组,BaP暴露使16-HBE细胞TNF-α、IL-1β、IL-18和IL-6炎性细胞因子分泌分别增加了556.15%(p<0.01)、690.72%(p<0.01)、476.53%(p<0.01)和286.45%(p<0.01)。表明,BaP暴露会造成16-HBE细胞炎性损伤,并诱发炎症因子大量分泌。研究表明,多种生物活性肽具有抑制炎症的功能[21],本研究中,50 μmol/L的LBP-1处理后,相比于BaP组,细胞培养上清液中TNF-α、IL-1β的质量浓度分别降低了34.93%(p<0.05)及27.41%(p<0.05);IL-18和IL-6的质量浓度降低了31.05%(p<0.05)、35.28%(p<0.02)。本文推测,BaP暴露造成的16-HBE细胞炎性损伤被LBP-1显著减轻。
2.4 LBP-1对16-HBE细胞PGE2、NO分泌及COX-2、iNOS表达的影响
iNOS在细胞中通常不表达,但会响应细胞的炎症刺激(如细胞因子)而产生,一旦表达就会产生高水平的NO,而高水平的NO则会产生细胞毒性,对炎症和宿主免疫产生持久影响[22];花生四烯酸从生物膜中释放出来后,被迅速氧化成不稳定的PGG2,随后被还原为PGH2,这两个过程均由COX-2催化,随后,PGH2会被一组末端合成酶迅速转化为PGE2[23],而COX-2在许多组织中可通过促炎因子诱导高表达,从而产生大量的PGE2[24],同时PGE2在炎症的初期会促进中性粒细胞、巨噬细胞和肥大细胞从血流中流入组织,导致感染或组织损伤部位肿胀和水肿,从而促进炎症的发生和发展[25]。本研究中,BaP暴露使16-HBE细胞iNOS与COX-2表达显著增加,同时,NO及PGE2含量显著升高。而LBP-1干预后,BaP诱导的iNOS与COX-2高表达及NO、PGE2过量分泌被显著抑制。提示LBP-1具有预防BaP暴露所致的气道上皮细胞炎症反应,从而缓解和改善细胞活力减弱细胞损伤。
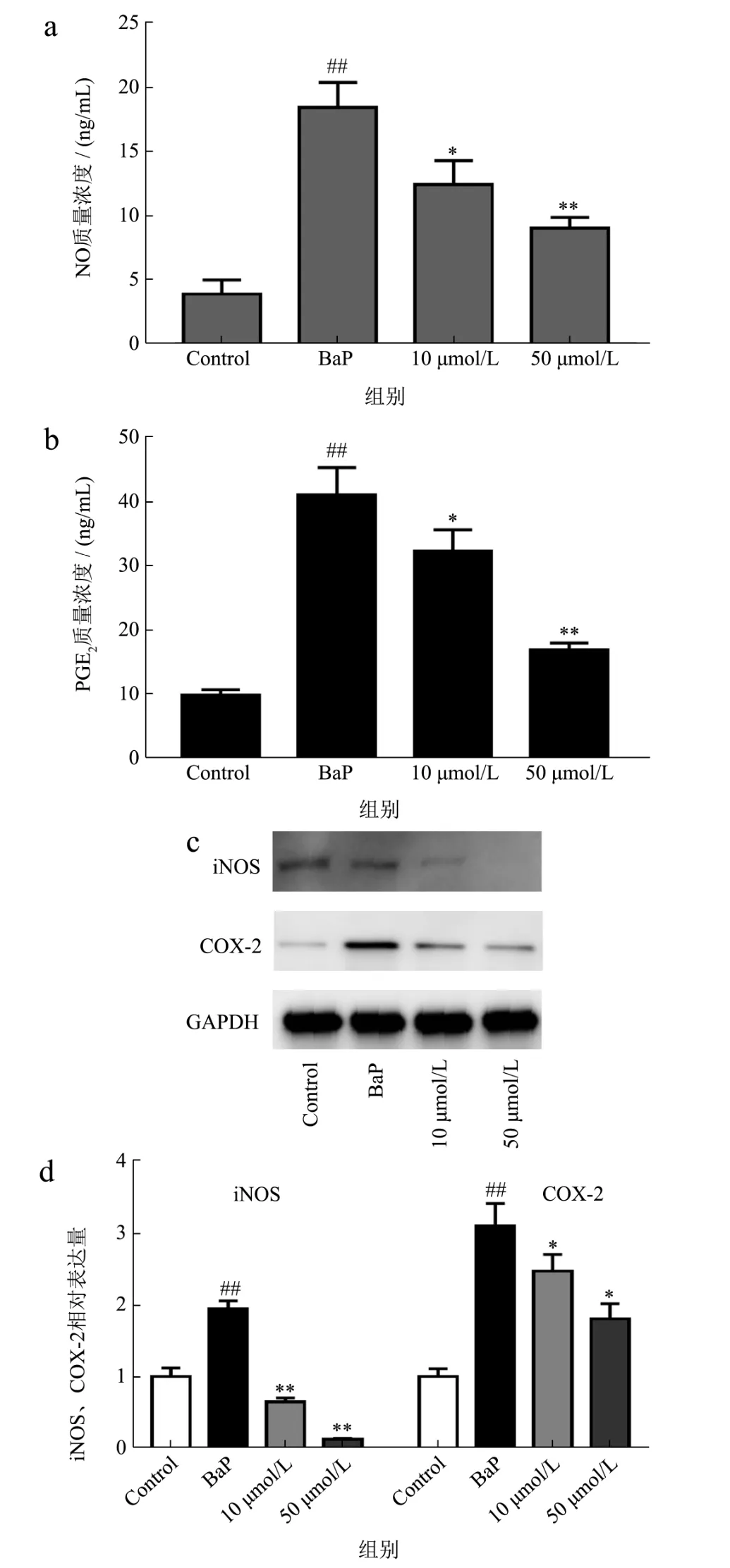
图4 LBP-1对BaP诱导的16-HBE细胞NO、PGE2分泌及iNOS、COX-2表达的影响Fig.4 Effects of LBP-1 on the secretion of NO and PGE2 and the expression of iNOS and COX-2 in 16-HBE cells induced by BaP
结果如图4a、4b所示,BaP暴露会诱发16-HBE细胞NO、PGE2的过量分泌。相比于空白对照组,BaP暴露使16-HBE细胞NO、PGE2分泌分别增加475.34%(p<0.01)、414.77%(p<0.01)。而50 μmol/L的LBP-1处理后,相比于BaP组,细胞培养上清液中NO、PGE2的浓度分别降低了51.15%(p<0.01)及27.46%(p<0.01)。COX-2及iNOS是细胞合成PGE2和NO的关键酶,BaP诱导的PGE2和NO过量分泌被LBP-1显著抑制。从海马中纯化出的一种生物活性肽可以抑制iNOS和COX-2的表达,从而抑制LPS诱导的炎症[26],BaP及LBP-1对COX-2和iNOS表达的影响的结果如图4c、4d所示,BaP暴露使16-HBE细胞中iNOS和COX-2表达显著升高。10 μmol/L LBP-1处理后,16-HBE细胞iNOS及COX-2的表达量有所下降,但不具有显著性差异。而50 μmol/L LBP-1处理后,16-HBE细胞iNOS及COX-2的表达显著下降。相比于BaP组,50μmol/L LBP-1组iNOS及COX-2表达降低81.72%(p<0.01)和41.70%(p<0.05)。LBP-1可通过抑制BaP诱导的COX-2及iNOS的表达进而抑制PGE2及NO的过量分泌。
2.5 LBP-1抑制BaP诱导的16-HBE细胞NLRP3和NF-κB信号通路激活
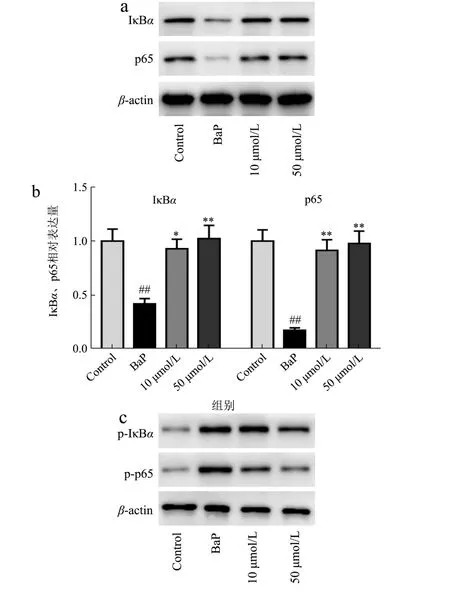
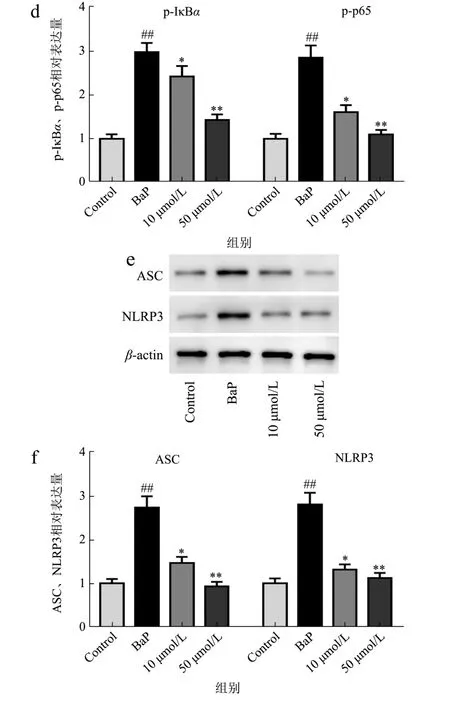
图5 LBP-1对BaP暴露诱导16-HBE细胞NF-κB、NLRP3信号通路相关蛋白表达影响Fig.5 Effect of LBP-1 on the expression of NF-κB and NLRP3 signaling pathway related proteins in 16-HBE cells induced by BaP exposure
核转录因子κB(NF-κB)是细胞中重要的转录调节因子,通常以p50-p65异二聚体的形式与其抑制性蛋白(inhibitorκB,IKB)结合而呈非活化状态;NF-κB通过刺激因子(肿瘤坏死因子、淋巴毒素、环境污染物等)的活化进而诱导多种基因的表达,产生多种细胞因子参与炎症反应[27]。因此,NF-κB信号通路是经典的炎症通路,也是抗炎药物的经典靶点。NLRP3也叫NOD样受体蛋白3,属于炎性复合体的传感蛋白,当细胞受到感染刺激时,被激活的NLRP3形成NLRP3炎性小体,在炎性小体的作用下,促进下游炎性细胞因子IL-1β和IL-18的释放从而引起炎症反应[28]。
因此本文检测了LBP-1对BaP暴露诱导的16-HBE细胞NF-κB和NLRP3信号通路相关蛋白的影响。Bap可通过激活NF-κB信号通路从而导致炎症[20],如图5a、5b和5c、5d所示,BaP暴露会使IκBα和p65表达降低,诱导IκBα和p65磷酸化;与此同时,BaP暴露使NLRP3及ASC表达显著增高。说明,BaP暴露激活了NF-κB和NLRP3信号通路。活性肽也可通过NF-κB信号通路抑制炎症[26],本研究中50 μmol/L的LBP-1处理16-HBE细胞后,BaP暴露导致的NF-κB和NLRP3信号通路激活被显著抑制。IκBα和p65表达升高,IκBα和p65磷酸化水平降低,NLRP3及ASC表达也被显著抑制。通过结果推测,LBP-1可通过抑制NF-κB和NLRP3信号通路相关蛋白的表达抑制BaP暴露导致的16-HBE细胞NF-κB和NLRP3信号通路激活,进而发挥抗炎活性。
3 结论
多环芳烃化合物(PAHs)及其衍生物已经被证明在环境污染所引起的癌症的发生发展过程中起着非常重要的作用。苯并芘及其代谢产物能够诱导生物有机体产生炎症反应,进而表现出较强的致癌性,在慢性肺炎及肺部肿瘤的形成过程中发挥重要作用。本研究构建BaP诱导的气道上皮细胞损伤模型,通过活性追踪方式从枸杞中分离获得具有保护活性的环肽类化合物。发现枸杞环肽-1(LBP-1,环-(Trp-Glu-Phe-Thr)肽)能够显著抑制BaP暴露导致的细胞活力降低,进一步的研究显示LBP-1能够抑制BaP暴露诱发的炎性细胞因子分泌,抑制IκBα磷酸化及ASC高表达。本文推测LBP-1抗BaP诱导的气道上皮细胞炎症损伤可能是通过抑制BaP暴露诱导的炎性细胞因子分泌及介导的NF-κB/NLRP3信号通路激活有关。
本研究发现BaP暴露会激活NF-κB信号通路,同时NLRP3炎症小体的NLRP3及ASC蛋白表达增加,而LBP-1处理后,BaP暴露诱导的p65与IκBα磷酸化及NLRP3炎症小体激活收到显著抑制。说明,LBP-1可通过调控NLRP3及NF-κB信号通路相关蛋白表达发挥抗BaP诱发的气道上皮细胞炎性损伤。总之,LBP-1可通过抑制BaP诱导的气道上皮细胞NF-κB/NLRP3信号通路激活及iNOS、COX-2酶活性从而抑制炎症因子IL-1β、NO等的释放,进而有效抑制炎症反应。本研究为将为新型活性枸杞活性肽的开发及抗环境污染物多环芳烃诱导的呼吸道损伤药物研发提供新的研究思路和实验依据。
