心脏磁共振诊断妊娠期急性冠状动脉非梗阻型心肌梗死一例
2022-10-08张凯璐曹玉坤史河水
张凯璐,曹玉坤,史河水*
作者单位:1.华中科技大学同济医学院附属协和医院放射科,武汉 430022;2.湖北省分子影像重点实验室,武汉 430022
本研究经华中科技大学同济医学院医学伦理委员会批准,免除受试者知情同意,伦理批文号:[2019]伦审字(S878)号。
患者女,32岁,孕32周,2021年7月12日因间断胸痛2天,加重16 h 入院。患者7 月10 日无明显诱因间断出现胸痛,可自行缓解,未予重视,2 天后无明显诱因再次出现胸骨中下段后方疼痛,伴出汗、气短、乏力。急诊心电图显示:aVR 导联上抬,胸导联ST 段广泛压低。入院后体检:心率109 次/min,心律齐,无杂音,胸肺听诊未闻及湿啰音,双下肺呼吸音低;腹软,肝脾肋下未及,双下肢无明显水肿。入院后予以地塞米松、营养及对症治疗,与患者及家属沟通后,于入院第3 天行子宫下段横切口剖宫产术。术后复查心电图可见Q 波(Ⅲ、aVF导联)和异常T波(图1)。

图1 心电图示窦性心律,Q波(Ⅲ、AVF导联),T波异常(前壁)。 图2 冠状动脉计算机断层扫描血管造影(CTA)—多平面重建(MPR)。2A~2D:分别显示右冠、左主干与回旋支、第1对角支和前降支管腔无明显狭窄。Fig. 1 Electrocardiogram (ECG) showing sinus rhythm, Q-wave (Ⅲ, AVF leads) , abnormal T-wave (anterior wall). Fig. 2 Coronary artery computed tomographic angiography (CTA)-multiplanar reformation (MPR) showed no significant stenosis in the lumen of the right coronary artery, left main and circumflex artery, first diagonal branch and anterior descending branch.
实验室检查:7 月12 日凌晨急诊查TnI 10.205 ng/mL,CK-MB 64.84 ng/mL,同 日8 h 后 复 查TnI 3033.00 pg/mL,CK-MB 225.1 ng/mL。7 月12 日入院当天:肌酸激酶1867 U/L,CK-MB 121.4 ng/mL,TnI 32086.6 ng/L,血NT-ProBNP 1400.0 pg/mL。总胆固醇(TC)7.60 mmol/L、甘油三酯(TG)2.94 mmol/L、高密度脂蛋白胆固醇(HDL-C)1.76 mmol/L、低密度脂蛋白胆固醇(LDL-C)4.71 mmol/L。7月22日出院当天:肌酸激酶65 U/L,CK-MB 1.0 ng/mL,TnI 381.6 ng/L。
影像学检查:急诊冠状动脉计算机断层扫描血管造影(computed tomographic angiography, CTA)示冠状动脉主干与主要分支未见明显斑块及管腔狭窄,冠状动脉疾病报告和数据系统(Coronary Artery Disease Reporting and Data System, CAD-RADS)评分为0;左前降支中段长约2.2 cm 表浅型壁冠状动脉(图2)。全主动脉CTA 未见明显异常。剖宫产术后3天行心脏磁共振(cardiac magnetic resonance, CMR)、心脏电影示左心室中间—心尖段间隔壁室壁运动相对减弱,基底段舒缩运动正常;舒张末期短轴位测左室基底—中间段间隔壁心肌轻度增厚(12~14 mm)。静息态心肌首过灌注示左心室间隔壁心内膜下局部线样低信号灌注缺损影。心肌延迟显像示左心室中间—心尖段间隔壁心内膜下线样延迟强化(late gadolinium enhancement, LGE)(图3)。采用CVI 42 软件测量心功能指标和左心室心肌应力指标,左心功能:左室射血分数(LVEF)41.17%、舒张末期容积(EDV)114.73 mL、收缩末期容积(ESV)67.49 mL、心搏量(SV)47.23 mL;右心功能:右室射血分数(RVEF)50.93%、EDV 108.09 mL、ESV 53.04 mL、SV 55.05 mL;根据左心室平均3D 周向应力峰值、纵向应力峰值、径向应力峰值数据生成AHA16节段模型图(图4)。
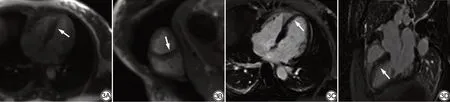

图3 心脏磁共振成像图。3A、3B:静息态心肌首过灌注图像,室间隔左心室内膜下局部低信号心肌灌注缺损(箭);3C、3D:钆延迟显像,间隔壁心内膜下线样高信号延迟强化(箭)。图4 左心室AHA16 节段模型图。4A:平均3D 周向应力峰值,心尖段间隔壁周向应力为10.6%,提示有矛盾运动;4B:平均3D纵向应力峰值,基底段前壁和前侧壁纵向应力分别为-9.1%和-10.9%,中间段前侧壁和下侧壁纵向应力分别为-7.6%和-8.7%,心尖段间隔壁纵向应力为-10.6%,相比其他节段稍减低;4C:平均3D径向应力峰值。Fig. 3 Cardiac magnetic resonance (CMR) images. 3A, 3B: The resting myocardial first-pass perfusion images, subendocardial low-signal myocardial perfusion defect (arrow) in the left ventricle of the interventricular septum; 3C, 3D: The delayed gadolinium-enhanced imaging, subendocardial linear delayed hypersignal enhancement of septal wall (arrow). Fig. 4 The AHA 16-segment model of the left ventricle. 4A: The mean 3D peak circumferential strain, the circumferential strain of apical septum wall was 10.6%, suggesting myocardial paradoxical movement; 4B:The mean 3D peak longitudinal strain, the longitudinal strain of anterior wall and anterior lateral wall of the basal segment was-9.1%and-10.9%,anterior and inferior lateral wall of the middle segment was-7.6%and-8.7%,and apical septum wall was-10.6%,which was slightly lower than that of other segments;4C:The mean 3D peak radial strain.
结合病史、冠状动脉CTA 和实验室检查,排除急性心肌炎和应激性心肌病,诊断为急性冠状动脉非阻塞型心肌梗死(myocardial infarction with no obstructive coronary atherosclerosis, MINOCA)。术后应用瑞舒伐他汀、依折麦布片、地尔硫卓、肝素钠及缩宫素等对症与支持治疗,同时予以头孢孟多酯钠预防性抗感染,患者病情逐渐好转并出院。
讨论 急性心肌梗死(acute myocardial infarction,AMI)是妊娠期一种罕见但极具潜在危害的并发症,发生率为3~10/10 万人,5%~7%的孕产妇死亡与此相关,同时也严重危害胎儿健康。现有研究表明,高脂血症、肥胖、慢性高血压、糖尿病、高龄是妊娠期AMI 的独立危险因素[1-3]。本例患者32 岁,实验室检查提示高脂血症,可能是发生MINOCA 的原因之一。MINOCA 作为一种病因各异的综合征,是冠状动脉造影显示冠状动脉正常或接近正常(狭窄程度<50%)的AMI,在AMI患者中发生率为5%~6%。目前MINOCA的发病机制和病因尚未完全阐明,可能病因有斑块破裂、心外膜下冠脉痉挛、冠脉微血管功能障碍、冠脉栓塞或血栓形成、自发性冠脉夹层等[4-5]。另外,妊娠期机体处于高动力循环状态,总血容量和心输出量逐渐增加,至妊娠32~34 周达高峰,心率也逐渐增加,至妊娠晚期每分钟平均增加10~15 次,同时心脏发生心肌重塑和/或轻度离心肥大。相比于非妊娠期,孕妇血容量与血流动力学变化增加了患心力衰竭和AMI 的风险。而常规用于治疗心肌梗死的药物,包括血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体阻滞剂(ARB)和他汀类药物禁止用于孕妇,这更增加了治疗难度与风险。因此,对可疑MINOCA 的孕妇进行及时诊断与适当干预非常重要。
本例患者妊娠晚期32 周,无病毒感染和发热等炎症相关病史,冠状动脉CTA 显示主干与主要分支无明显粥样硬化斑块与管腔狭窄(图2),CMR 未见心外膜下或透壁性延迟强化,可排除急性心肌炎和应激性心肌病。钆延迟显像示左室间隔壁内膜下延迟强化(图3),相应层面纵向应力值减低(图4),且临床存在妊娠状态等高危因素,支持MINOCA 诊断。此外,患者心脏电影显示舒张末期短轴位测左室基底—中间段间隔壁心肌轻度增厚,可能由于妊娠状态高负荷代偿所致,但仍需结合临床相关指标(如基因检测)除外肥厚型心肌病。
CMR 基于无创、无辐射、一站式定量评估心脏结构和功能的优势,是临床上诊断MINOCA 的关键检查之一,可鉴别心肌炎、Takotsubo 综合征和其他非缺血性心肌病,并明确AMI 的影像学诊断。但CMR 上没有心肌梗死表现并不一定能排除MINOCA[6],例如在肌钙蛋白异常升高的情况下,患者出现心肌缺血症状、心电图上出现缺血性表现和/或病理性Q 波,冠脉造影发现冠脉血栓等结果满足至少一项即可诊断AMI。研究表明,MINOCA 患者通常比患有阻塞性冠状动脉疾病(coronary artery disease, CAD)的AMI 患者更年轻,预后更好[7]。目前妊娠期MINOCA 的治疗尚未有明确指南,治疗方案和终止妊娠时机的选择主要取决于孕妇及胎儿状态。本例及时行剖宫产术终止妊娠,缩短产程,尽快结束分娩,一方面避免了长时间子宫收缩引起心肌耗氧量增加,导致梗死范围的进一步扩大;另一方面也减轻疲劳和疼痛等引起的心脏负荷增加,利于减轻心肌损伤和缺血。术后改善循环、控制心率、降脂等对症及支持治疗也有助于减轻心脏负荷和抗心肌重塑。
尽管CMR 已在缺血性心脏病中广泛应用,但关于妊娠期MINOCA的报道较少,放射科医师应熟悉此疾病的影像表现,以便及时提供正确诊断,而对于被诊断为MINOCA 的患者,在排除其他导致肌钙蛋白升高的原因后,医生应确定导致MINOCA的具体病因和发病机制,以便进行有针对性的治疗。
作者利益冲突声明:全部作者均声明无利益冲突。
