猪乙型脑炎传代细胞活疫苗保护剂的效力试验
2022-09-29刘艳彬潘春刚周建民
韩 伟 , 刘艳彬 , 蒋 利 , 潘春刚 , 周建民
(1. 中牧实业股份有限公司 , 北京 丰台 100070 ; 2. 农业农村部兽用生物制品与化学药品重点实验室 ,北京 海淀 100095 ; 3. 北京市兽用多肽疫苗设计与制备工程技术中心 , 北京 海淀 100095)
乙型脑炎病毒又称日本脑炎病毒(Japanese encephalitis virus,JEV),简称乙脑病毒,所引起的疾病称乙型脑炎,是最常见的以三带喙库蚊为主要传播媒介的病毒性脑炎,它是严重威胁人畜健康的一种中枢神经系统的急性传染病[1]。JEV是引起母猪繁殖障碍的主要病原之一。猪是JEV的重要储存宿主和扩增宿主,是乙型脑炎的主要传染源。预防和控制猪乙型脑炎的最有效方法是接种疫苗。而疫苗在保存、运输和使用过程中均需要使用冻干保护剂。传统的疫苗保护剂主要配方为脱脂牛奶、蔗糖、明胶等,组方简单、配制简便、易溶性良好,但热稳定性和保护功能差,产品的保存条件较为苛刻,大多需要在-15 ℃以下保存。在疫苗生产、运输和使用过程中,如果冷链系统控制不当,疫苗保存环境温度升高,常常导致疫苗效力下降或失效,造成免疫失败。耐热冻干保护剂比传统冻干保护剂更周到地考虑了具有生物活性的制品在较高温度和较长时间保存的情况下,冻干物质可能产生的物理和化学变化对活疫苗存活的影响,通过填充、防冻、抗氧化、酸碱调整、羟基中和等一系列机制,确保病毒在2~8 ℃条件下保存期可达24个月,效价无明显下降,即使在较高的常温甚至37 ℃也可以保存10 d以上,因而其保护性能要比传统保护剂更为优良,从而使活苗的储存、运输和使用更方便、经济[2]。而JEV在环境中极不稳定,在-20 ℃条件下仅可保存1年,且病毒滴度下降较快。因此研制猪乙型脑炎耐热冻干保护剂对该疫苗的保存和运输具有重要的作用和意义,有利于预防该病毒的流行和传播。
1 材料与方法
1.1 细胞与毒种 Vero细胞、BHK-21细胞和JEV(SA14-14-2株,第10代)、JEV P3株,均由中牧实业股份有限公司保存、提供。
1.2 实验动物 ICR小鼠,10~12 g,购自北京维通利华实验动物技术有限公司,生产许可证号:SCXK(京)2016—0006。
1.3 主要试剂 甲基纤维素,购自Sigma公司;DMEM培养液、胎牛血清和0.25%胰蛋白酶,均购自Gibco公司;结晶紫、明胶、蔗糖、乳糖、甘氨酸、谷氨酸钠、海藻糖等试剂,均为北京市化学试剂公司产品。
1.4 方法
1.4.1 抗原液的制备 用3 L转瓶将Vero细胞培养72~96 h,接种3 mL JEV毒液(病毒含量为1.2×107PFU/mL),37 ℃吸附60 min,补加含2%胎牛血清的DMEM维持液(pH 7.8),35 ℃ 12 r/h旋转培养96 h后收获毒液,冻融1次,-70 ℃保存备用。
1.4.2 病毒含量的测定 采用病毒蚀斑试验进行病毒含量的测定。将疫苗用疫苗稀释液稀释至1头份/mL,然后进行10倍系列稀释,取10-2、10-3和10-4共3个稀释度,分别接种于生长BHK-21单层细胞的12孔细胞板中,每个稀释度设3个重复孔,0.1 mL/孔。病毒接种后于37 ℃吸附90 min,加覆盖物(含1.5%甲基纤维素、2%小牛血清的DMEM培养基),5 d后用结晶紫染色、固定30 min,流水冲洗,干燥后在低倍显微镜下计数各孔蚀斑数,根据公式可计算出病毒含量(Log PFU/mL)。
病毒含量(Log PFU/mL)=Log某稀释度平均蚀斑数×稀释倍数×10。
1.4.3 保护剂的配制 耐热冻干保护剂的配制:根据冻干活疫苗的质量要求和各类型原材料的作用机理,将明胶、蔗糖、海藻糖、聚乙烯吡咯烷酮K90(PVP-K90)、山梨醇、甘露醇、聚乙二醇-6000(PEG-6000)、吐温-80、谷氨酸钠等物质按照一定配方比例溶于注射用水中,116 ℃灭菌 30~40 min,使用前调pH至7.5。传统冻干保护剂的配制:明胶20 g、蔗糖100 g,加入注射用水定容至1 000 mL,116 ℃灭菌 30~40 min,于2~8 ℃保存备用。
1.4.4 保护剂耐老化试验 取制备的抗原液与耐热冻干保护剂按1∶1比例混合,定量分装,以传统冻干保护剂作对照,用同一冻干曲线进行冻干。比较耐热冻干保护剂制备的乙型脑炎活疫苗和传统冻干保护剂制备的乙型脑炎活疫苗的物理性状、真空度、剩余水分测定、冻干前后疫苗病毒含量损失(重复3次测定)、2~8 ℃保存24个月后抗原病毒含量下降情况(重复3次测定)、25 ℃常温保存2个月后疫苗病毒含量下降情况(重复3次测定)、37 ℃保存10 d后抗原病毒含量下降情况(重复3次测定)等指标。
1.4.5 冻干曲线 冻干曲线主要参数:预冻阶段疫苗最低温度-40 ℃,疫苗达到最低温度后维持时间2 h;升华干燥阶段疫苗最终温度-20 ℃,疫苗达到最终温度的运行时间16 h,冻干箱真空控制压力0.18 mbar;解析干燥阶段疫苗的最终温度28 ℃,冻干箱真空压力0.005 mbar,运行时间8 h。
1.4.6 对小鼠免疫原性试验 免疫组取上述耐热冻干保护剂制备的疫苗(疫苗1)和传统冻干保护剂制备的疫苗(疫苗2)分别用含2%胎牛血清的DMEM培养基进行10倍系列稀释,取10-2、10-3和10-4共3个稀释度,每个稀释度取0.1 mL皮下接种ICR小鼠10只,免疫1次,全部小鼠于免疫后14 d用JEV P3株腹腔攻毒,每只小鼠腹腔注射0.3 mL[不低于500 半数致死量(LD50)],同时脑内空刺,破坏血脑屏障,另设同批次攻毒对照组小鼠10只,不进行免疫,但与免疫组同时进行攻毒。攻毒后3 d内死亡小鼠不计,其余观察14 d,对照组小鼠应出现脑炎综合症,且死亡率达80%,计算各免疫组半数有效剂量(ED50)。
2 结果
2.1 抗原液的制备和病毒含量测定 用3 L转瓶进行抗原液的培养,抗原液病毒含量为6.8 Log PFU/mL。
2.2 耐热冻干保护剂配方 按重量百分比计,明胶1.0%~1.4%、蔗糖9%~11%、海藻糖9%~11%、PVP-K90 0.15%~0.35%、山梨醇0.3%~0.8%、甘露醇0.3%~ 0.8%、PEG-6000 0.1%~0.2%、吐温-80 0.01%~0.02%、谷氨酸钠0.8%~1.2%,余量为注射用水,并用1 N盐酸调节pH至7.5,通过高温灭菌步骤制备耐热冻干保护剂。
2.3 保护剂耐老化试验
2.3.1 物理性状 耐热冻干保护剂制备的乙型脑炎活疫苗和传统冻干保护剂制备的乙型脑炎活疫苗均呈现淡红色、质地均匀一致的疏松体(冻干块无皱缩、分层现象),复溶后快速溶解为无异物的粉红色澄清液体。
2.3.2 真空度的测定 按现行《中华人民共和国兽药典》[3]对耐热冻干保护剂制备的乙型脑炎活疫苗和传统冻干保护剂制备的乙型脑炎活疫苗进行真空度测定,均出现紫色辉光,真空度合格。
2.3.3 剩余水分测定 按现行《中华人民共和国兽药典》[3]对耐热冻干保护剂制备的乙型脑炎活疫苗和传统冻干保护剂制备的乙型脑炎活疫苗进行剩余水分测定,剩余水分均不超过4.0%,分别为2.7%和3.1%。
2.3.4 冻干前后疫苗病毒含量的测定 耐热冻干保护剂制备的乙型脑炎活疫苗冻干前后抗原的病毒含量下降不超过0.5 Log PFU/mL,传统冻干保护剂制备的乙型脑炎活疫苗冻干前后抗原的病毒含量下降超过0.5 Log PFU/mL(表1)。

表1 使用不同保护剂冻干前后病毒含量的变化Table 1 Changes of virus content before and after freeze-drying with different lyophilized protective agents (Log PFU/mL)
2.3.5 2~8 ℃保存24个月后抗原病毒含量的测定 经2~8 ℃保存24个月后,耐热冻干保护剂制备的乙型脑炎活疫苗的抗原病毒含量下降不超过1.0 Log PFU/mL,传统冻干保护剂制备的乙型脑炎活疫苗的抗原含量下降超过3.0 Log PFU/mL(表2)。

表2 使用不同保护剂2~8 ℃保存24个月后病毒含量的变化Table 2 Changes of virus content after 24 months of storage at 2-8 ℃ with different lyophilized protective agents (Log PFU/mL)
2.3.6 25 ℃保存2个月后抗原病毒含量的测定 经25 ℃保存2个月后,耐热冻干保护剂制备的乙型脑炎活疫苗的抗原病毒含量下降不超过1.0 Log PFU/mL,传统冻干保护剂制备的乙型脑炎活疫苗的抗原含量下降约2.0 Log PFU/mL(表3)。

表3 使用不同保护剂25 ℃保存2个月后病毒含量的变化Table 3 Changes of virus content after 2 months of storage at 25 ℃ with different lyophilized protective agents (Log PFU/mL)
2.3.7 37 ℃保存10 d后抗原病毒含量的测定 经37 ℃保存10 d后,耐热冻干保护剂制备的乙型脑炎活疫苗的抗原病毒含量下降不超过1.5 Log PFU/mL,传统冻干保护剂制备的乙型脑炎活疫苗的病毒含量下降超过1.5 Log PFU/mL(表4)。

表4 使用不同保护剂37 ℃保存10 d后病毒含量的变化Table 4 Changes of virus content after 10 d of storage at 37 ℃ with different lyophilized protective agents (Log PFU/mL)
2.4 对小鼠免疫原性试验 使用耐热冻干保护剂制备的活疫苗(疫苗1)和使用传统冻干保护剂制备的活疫苗(疫苗2)对小鼠的免疫原性相当,半数有效剂量分别为10-3.12/0.1 mL和10-3.11/0.1 mL(表5)。
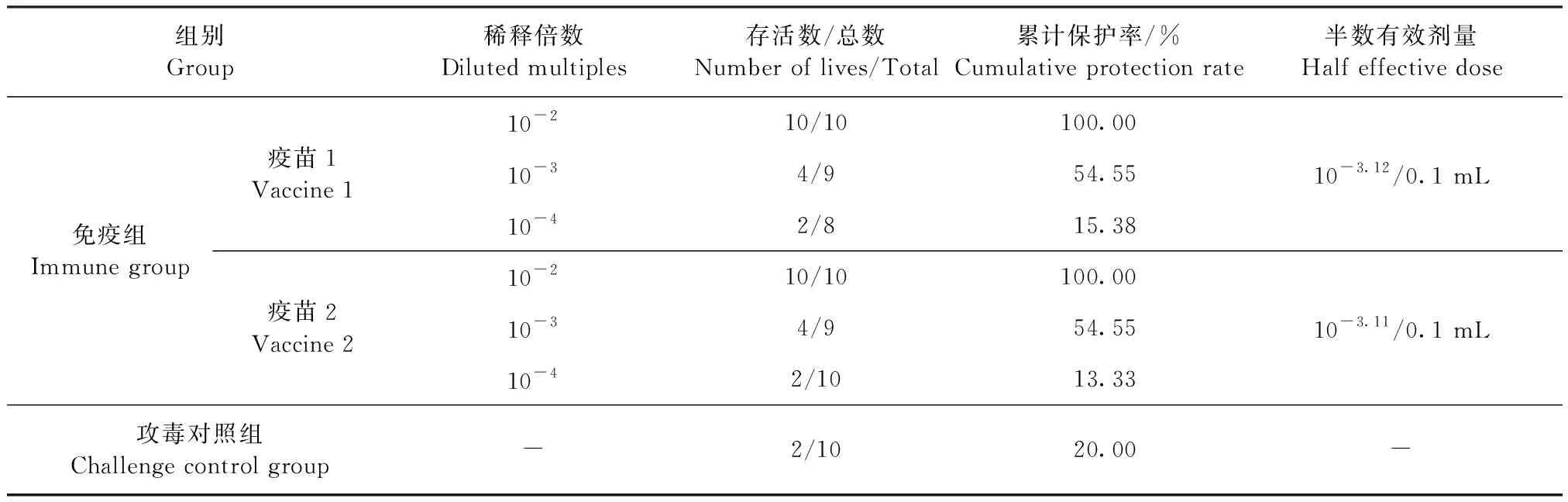
表5 接种小鼠死亡情况及半数有效剂量测定Table 5 Death of inoculated mice and half effective dose determination
3 讨论
猪乙型脑炎是由JEV引起的一种动物和人类共患的传染病,疫苗接种是防控猪乙型脑炎的最有效方法之一。我国已批准的猪乙型脑炎活疫苗(SA14-14-2株)在2~8 ℃条件下的有效期只有6个月[4]。疫苗耐热性能差,使得保存、运输和使用效果大大降低。目前,国内大多采用传统的疫苗保护剂,主要配方为脱脂牛奶、蔗糖、明胶等,组方简单、配制简便、易溶性良好,但热稳定性和保护功能差,产品大多在-15 ℃以下保存。国外采用低聚糖、多元醇、蛋白、抗氧化剂、缓冲剂、填充剂等复合组方配伍的耐热冻干保护剂,制备的冻干活疫苗在2~8 ℃条件下保存期可达24个月[5],其保护性能比传统保护剂更优良,使活苗的储存、运输和使用更方便、经济。已有耐热保护剂应用于乙型脑炎疫苗的制备中,潘春刚等[2]研制了一种猪JEV活疫苗耐热冻干保护剂,将其与猪JEV活疫苗病毒液混合,冷冻干燥后即得冻干疫苗,疫苗冻干前后病毒含量下降不超过1.0 Log PFU/mL,疫苗经2~8 ℃保存24个月后抗原病毒含量下降不超过1.0 Log PFU/mL,疫苗经37 ℃保存10 d后抗原病毒含量下降不超过1.5 Log PFU/mL,同本试验结果一致。耐热冻干保护剂配方简单,制备简易,适于大规模生产,对疫苗具有良好的保护功效。巢伟等[6]研发了一种活疫苗的耐热冻干保护剂,与传统的保护剂相比,其更能有效地保护疫苗中病毒的活力,37 ℃耐热超过20 d,2~8 ℃能保存2年以上,每头份病毒含量均高于国家标准[每头份病毒含量≥105.7半数细胞培养物感染量(TCID50)][3],同本试验结果一致。
耐热冻干保护剂应用前景广阔,国外许多生物疫苗公司都会加入耐热冻干保护剂制备疫苗[7]。国内兽用生物制品保护剂的研发相对滞后,近几年也有许多科研单位正致力于耐热保护剂的研究并取得了一定的成果。王颖等[8]选用谷氨酸钠、L-精氨酸盐酸盐、D-山梨醇、酶解酪蛋白、海藻糖、明胶、蔗糖、牛血清白蛋白等组分配制耐热保护剂冻干猪伪狂犬病病毒,经37 ℃保存7 d及2~8 ℃保存24个月,三批疫苗病毒滴度分别下降0.55、0.62、0.47 Log TCID/0.1 mL及0.47、0.51、0.41 Log TCID/0.1 mL,表明该疫苗热稳定性良好。赵艳红等[9]采用耐热冻干保护剂冻干鸭肝炎病毒,于37 ℃保存10 d、15 d,病毒损失分别为0.35 Log、0.61 Log,于2~8 ℃可保存2年。孙德君等[10]应用海藻糖、葡萄糖、明胶、硫脲和聚乙烯吡咯烷酮K30(PVP-K30)等组分制备鸡传染性支气管炎活疫苗,使冻干时间由48 h缩短至24 h,且耐热后疫苗病毒滴度下降减少,疫苗2~8 ℃保存期达36个月,疫苗的效力更加稳定,安全性更好。孙德君等[11]应用海藻糖、甘露醇、多聚蛋白胨等制备鸡痘耐热保护剂活疫苗,使冻干时间缩短至24 h,疫苗在2~8 ℃条件下可以保存36个月,耐热后疫苗病毒滴度下降减少,效力更加稳定。陈生雷等[12]应用耐热冻干保护剂制备鸡新城疫、支气管炎二联活疫苗,置37 ℃ 10 d后病毒含量下降幅度均不超过1个滴度,保护剂的性能稳定。李自波等[13]应用耐热冻干保护剂制备鸡新城疫活疫苗(Lasota株),其可在2~8 ℃保存24个月,且在37 ℃可至少保存1周,可有效减少运输、使用过程中的损失。万成燕等[14]应用明胶、海藻糖、蔗糖、L-谷氨酸钠、精氨酸、PVP-K30、甘露醇等组分制备伪狂犬耐热冻干活疫苗,37 ℃放置15 d病毒含量降低小于0.3个滴度,滴度降低少,保存时间长。张述斌等[15]应用聚乙烯吡咯烷酮、山梨醇、谷氨酸钠等制备羊口疮活疫苗,使得活疫苗冻干粉在25 ℃可保存2个月,2~8 ℃条件下可保存24个月。丁旭娜等[16]应用明胶、海藻糖、L-精氨酸、谷氨酸钠、聚乙烯吡咯烷酮等组分制备猪传染性胃肠炎病毒、猪流行性腹泻病毒二联冻干活疫苗,在37 ℃放置14 d后病毒含量下降不超过0.5个滴度,在2~8 ℃保存30个月后,疫苗仍保持冻干后的外形,病毒含量仍≥105.0TCID50/mL。
疫苗免疫小鼠后用强毒进行攻击,为传统的乙脑疫苗免疫效果评价的方法之一。孔嫄嫄[17]使用市售弱毒SA14-14-2株疫苗免疫小鼠后腹腔攻毒,保护率为70%,结果表明该疫苗具有很好的免疫原性。贾丽丽等[18]用小鼠保护力试验测定乙脑活疫苗SA14-14-2株对国内外不同野毒株的攻击保护作用,结果表明该疫苗具有广谱和良好的免疫原性。岳广智等[19]比较乙型脑炎活疫苗与灭活疫苗对小鼠的免疫原性,结果表明活疫苗免疫后小鼠中和抗体水平虽然很低,但仍有很强的保护力。本试验采用耐热冻干保护剂制备的乙型脑炎活疫苗与上述报道一致,可以刺激小鼠机体产生良好的免疫应答,对小鼠有免疫保护作用。
本试验制备的耐热冻干保护剂能够减少疫苗制品在冷冻干燥过程中各种理化因素对病毒活性的损伤,使冻干后病毒的损失率降低,不超过1.0 Log PFU/mL。有效解决了传统保护剂活疫苗需冷冻运输、储存不便等问题。
