卡培他滨联合贝伐珠单抗治疗晚期结直肠癌的效果
2022-09-26廖国龙欧阳鹏刘文东
廖国龙 欧阳鹏 刘文东
晚期结直肠癌患者多通过化疗的方式延长生存期。卡培他滨是最常用于治疗晚期结肠癌的化疗药物,可有效抑制肿瘤细胞增殖,但其也可同时抑制正常细胞的增殖,有严重的药物毒副作用,对于肿瘤病灶的靶向性较差,临床效果欠佳[1]。近十年来,抗血管内皮生长因子(VEGF)分子靶向药物——贝伐珠单抗在肺癌、子宫颈癌等癌症治疗中逐渐得到应用[2-3]。其可阻断VEGF,使肿瘤血管退化,联合卡培他滨治疗晚期结直肠癌,可能会有助于提高治疗效果,从而改善患者预后。基于此,本研究纳入惠州市第三人民医院2018年1月-2019年12月收治的晚期结直肠癌患者,探讨卡培他滨联合贝伐珠单抗的治疗效果,现将研究结果报道如下。
1 资料与方法
1.1 一般资料
选择本院2018年1月-2019年12月收治的60例晚期结直肠癌患者作为研究对象。纳入标准:(1)符合结直肠癌的诊断标准[4];(2)TNM分期:Ⅲ~Ⅳ期;(3)入组前7 d未接受任何免疫治疗或输注血液成分;(4)预计生存期超过3个月;(5)ECOG评分为1~2分。排除标准:(1)合并有恶性消化道穿孔;(2)伴有活动性出血;(3)合并肠梗阻;(4)癌细胞已转移至脑组织。按照随机数字表法将其分为对照组和观察组,每组30例。对照组男14例,女16例;年龄54~67岁,平均(61.73±4.07)岁;Ⅲ期20例,Ⅳ期10例;体重指数(BMI):19~25 kg/m2,平均(22.63±2.04)kg/m2。观察组男17例,女13例;年龄55~66岁,平均(60.48±4.20)岁;Ⅲ期 16例,Ⅳ期 14例;BMI:19~24 kg/m2,平均(21.93±1.71)kg/m2。两组一般资料比较差异无统计学意义(P>0.05),有可比性。本研究经医院伦理委员会批准,患者及家属签订知情同意书。
1.2 方法
对照组给予卡培他滨片(上海罗氏制药有限公司,国药准字H20073023,规格:0.15 g/片)治疗,每天早晚各口服1次,每次用量1 000 mg/m2。第1~14天用药,第15~21天不用药,21 d为1个周期,接受6个周期的治疗。
观察组给予卡培他滨片(用法同对照组)联合贝伐珠单抗注射液(Roche Diagnostics GmbH,国药准字SJ20170035,规格:100 mg/瓶)治疗,每次用量 7.5 mg/kg,静滴 60~90 min,第 1~14 天用药,第15~21天不用药,21 d治疗为1个周期,接受6个周期的治疗。
1.3 观察指标及评价标准
(1)治疗效果:于治疗结束后参考文献[5]《实体瘤治疗疗效评价标准-RECIST》,记录两组疗效,完全缓解(CR)为靶病灶完全消失;部分缓解(PR)为靶病灶最长直径比入组前减少≥20%;疾病稳定(SD)为处于PR与PD之间;疾病进展(PD)为靶病灶最长直径比入组前增加≥20%。疾病控制率=(CR+PR+SD)/总例数×100%。(2)肿瘤标志物及VEGF:于治疗前后,采集两组患者的空腹静脉血3 ml,采用酶联免疫吸附试法(ELISA)测定血清糖类抗原 199(CA199)(正常值 <37.00 U/ml)、CA242(正常值<20 IU/ml)、CA125(正常值≤40 U/ml),应用免疫分析法测定癌胚抗原(CEA)(正常值<5.0 ng/ml)、VEGF(正常值<290 pg/ml)。(3) 相关蛋白表达:于治疗前后,采集两组患者结直肠癌黏膜的组织标本,所有标本均行免疫组织化学染色,统计B淋巴细胞瘤2(Bcl-2)蛋白阳性细胞(超过25%判定为Bcl-2阳性)、人体抑癌基因p53蛋白阳性细胞(超过20%判定为阳性)、Bax阳性细胞(超过51%判定为阳性)的患者例数。(4)安全性:记录两组治疗期间的药物毒副反应,包括骨髓抑制(中性粒细胞下降、贫血、凝血异常等)、胃肠道反应(恶心呕吐、便秘、食欲减退等)、肝肾功能异常、外周神经毒性(感觉异常或迟钝)。
1.4 统计学处理
本研究数据采用SPSS 22.0统计学软件进行分析和处理,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组治疗效果比较
观察组疾病控制率为90.00%,高于对照组的66.67%(P<0.05),见表 1。
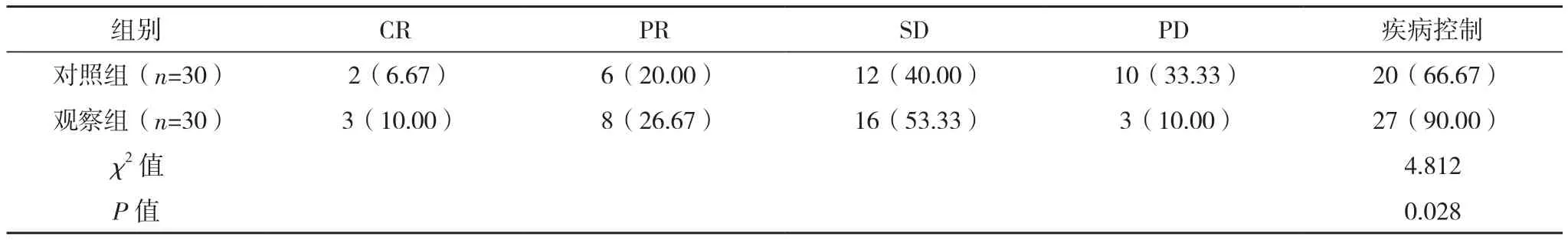
表1 两组治疗效果比较[例(%)]
2.2 两组肿瘤标志物及VEGF比较
治疗前,两组CA199、CA125、CEA、VEGF、CA242水平比较差异均无统计学意义(P>0.05),治疗后,两组CA199、CA125、CEA、VEGF、CA242水平均较治疗前下降,观察组CA199、CA125、CEA、VEGF、CA242水平均低于对照组(P<0.05),见表2。
表2 两组肿瘤标志物及VEGF比较(±s)
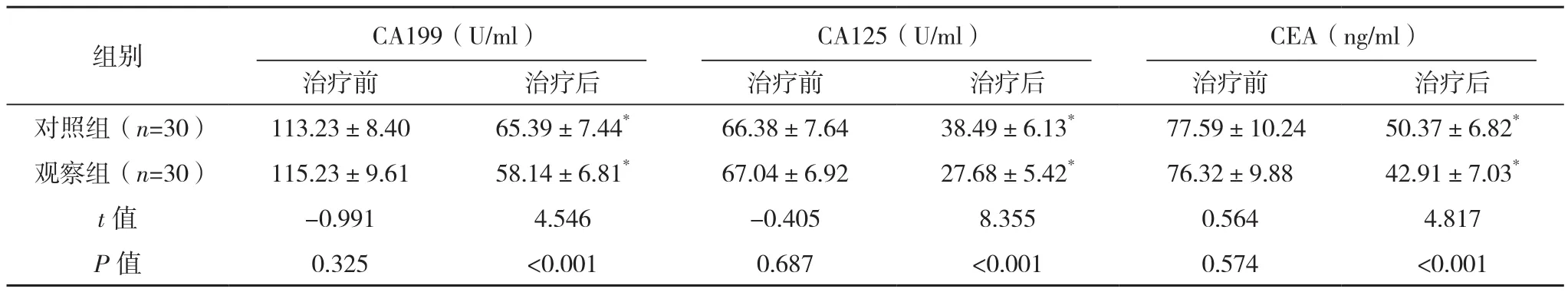
表2 两组肿瘤标志物及VEGF比较(±s)
组别 CA199(U/ml)CA125(U/ml)CEA(ng/ml)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后对照组(n=30) 113.23±8.40 65.39±7.44* 66.38±7.64 38.49±6.13* 77.59±10.24 50.37±6.82*观察组(n=30) 115.23±9.61 58.14±6.81* 67.04±6.92 27.68±5.42* 76.32±9.88 42.91±7.03*t值 -0.991 4.546 -0.405 8.355 0.564 4.817 P值 0.325 <0.001 0.687 <0.001 0.574 <0.001

表2(续)
2.3 两组相关蛋白表达阳性率比较
治疗前,两组Bcl-2蛋白、p53蛋白、Bax的阳性率比较差异均无统计学意义(P>0.05),治疗后,观察组p53蛋白、Bcl-2蛋白阳性率低于对照组,Bax阳性率高于对照组(P<0.05),见表3。
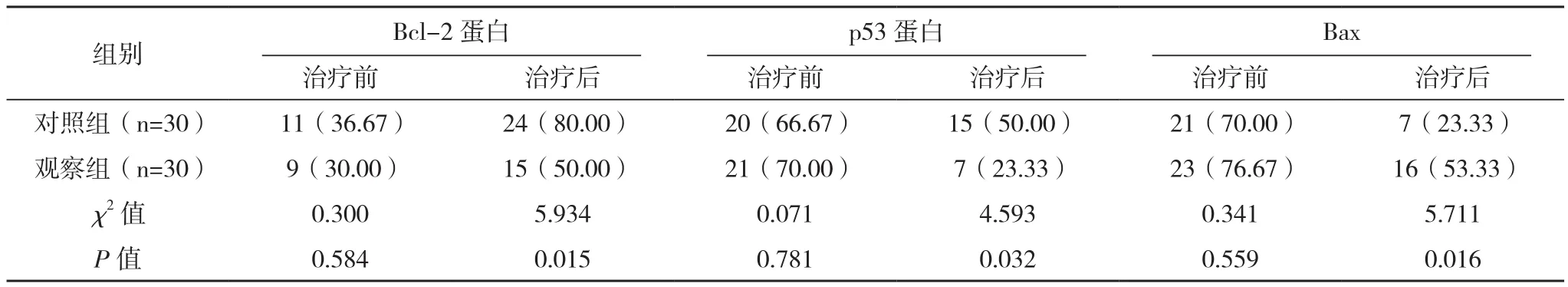
表3 两组相关蛋白表达阳性率比较[例(%)]
2.4 两组安全性比较
观察组与对照组的不良反应发生率分别为40.00%、30.00%,两组不良反应发生率比较差异无统计学意义(P>0.05),见表4。
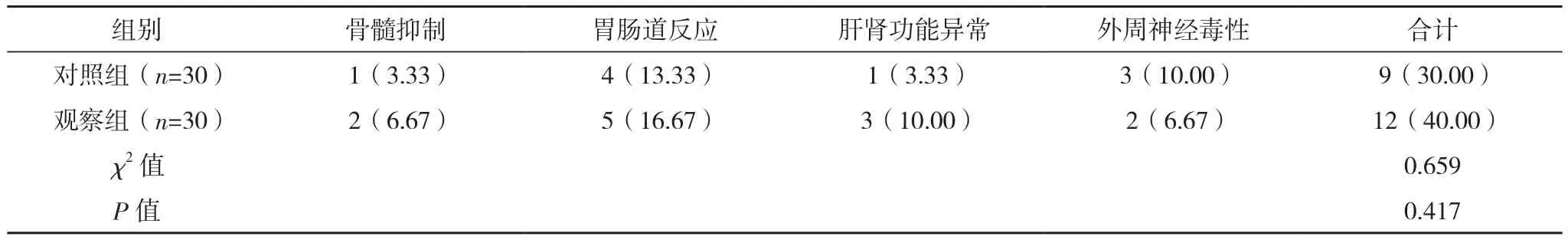
表4 两组安全性比较[例(%)]
3 讨论
结直肠癌的发病率逐年增高,每年增长3%~4%,约有80%的患者确诊时已是Ⅲ~Ⅳ期[6]。此阶段患者的癌细胞极易发生转移,化疗替代手术成为首选治疗方法。目前,化疗方案多应用卡培他滨,其通过抑制癌细胞的增殖以阻止疾病进展,虽可达到一定疗效,但在杀伤肿瘤细胞的同时也可抑制正常细胞增殖,常规化疗方案治疗的效果不理想[7]。贝伐珠单抗是特异性抗肿瘤血管生成的分子靶向药物,其联合常规治疗方案,可破坏肿瘤组织内的新生血管网、抑制新生血管,可能会有效提高晚期结直肠癌的治疗效果,缓解疾病。
Bcl-2蛋白为细胞凋亡过程中的重要抑制因子,Bax是凋亡促进基因,p53蛋白为细胞增殖的重要调控因子[8]。本研究结果显示:治疗后,观察组CA199、CA125、CEA、VEGF、CA242水平均低于对照组(P<0.05)。治疗后,观察组p53蛋白、Bcl-2蛋白阳性率低于对照组,Bax阳性率均高于对照组(P<0.05),说明卡培他滨联合贝伐珠单抗治疗晚期结直肠癌,可有效降低患者的血清肿瘤标志物水平和调节相关蛋白表达。卡培他滨口服后进胃肠道吸收,经羧酸酯酶水解为5-DFCR,经胞嘧啶脱氨酶转换为5-DFUR,达到癌组织后转化为5-氟尿嘧啶,通过干扰RNA和蛋白质的合成抑制癌细胞分裂,达到抗肿瘤的作用。贝伐珠单抗可选择性与VEGF结合,并阻断其生物活性,抑制VEGF与血管内皮上的Fms样酪氨酸激酶-激酶插入结构域受体(Flt-KDR)结合,使得VEGF失去生物活性,减少血管内皮细胞的迁移与增殖,从而减少肿瘤病灶处组织血管生成、发展及远处转移,同时使肿瘤血管退化,减少对肿瘤组织的供给,促进肿瘤细胞凋亡和自噬,抑制肿瘤细胞增殖,随着肿瘤病灶的控制,患者机体的Bax表达增多,Bcl-2蛋白和p53蛋白表达减少。亦有罗文杰等[9]应用FOLFOX化疗方案联合贝伐珠单抗可有效降低晚期结肠癌患者的血清癌胚抗原,且安全性较高,本研究与之相似。
本研究结果显示:观察组疾病控制率为90.00%,高于对照组的66.67%(P<0.05)。两组不良反应发生率比较差异无统计学意义(P>0.05),说明在卡培他滨基础上增加贝伐珠单抗不会降低治疗晚期结直肠癌患者的安全性,且能提高治疗效果。卡培他滨通过5-氟尿嘧啶抑制癌细胞分裂,从而抑制癌细胞增殖[10]。再联合贝伐珠单抗,抑制肿瘤组织内的血管增生、促进血管退化凋亡,使得肿瘤病灶的营养供给减少,进而萎缩退化。两者联合能从抑制肿瘤增殖、促使肿瘤病灶退化方面,起到抗肿瘤作用,提高临床疗效,这一发现与贾建宾[11]的结果相符。其表示贝伐珠单抗联合FOLFOX-6化疗方案治疗3个月的肿瘤缓解率高于单独FOLFOX-6化疗方案(观察组48.89%,高于对照组的31.11%,P<0.05)。另外,因贝伐珠单抗为人源化的VEGF抗体,为靶向药物,只与相应受体结合产生作用,安全性高[12]。
综上所述,相较于单药卡培他滨治疗晚期结直肠癌,联合贝伐珠单抗可有效降低血清肿瘤 因子水平和调节相关蛋白表达,促进疾病控制,且不会增加不良反应,安全性较高。
