纳米复合凝胶AgNPs@Gel的制备及催化性能研究
2022-09-24陈汝盼李云龙欧阳娜吕明旭
陈汝盼,李云龙,欧阳娜,吕明旭
(1.黎明职业大学 新材料与鞋服工程学院,福建 泉州 362000;2.先进高分子材料福建省高校应用技术协同创新中心,福建 泉州 362000)
0 引 言
4-氨基苯酚(4-AP)是一种重要的化工和医药中间体[1],主要应用于制备退烧药、止痛药、染料、橡胶助剂和石油添加剂等方面[2-5].目前,4-AP主要采用4-硝基苯酚(4-NP)铁粉还原法来制备,但是铁粉还原法生产成本高、规模小,对环境污染严重.因而,以纳米贵金属(如Pd、Au、Ag等)为催化剂,通过催化加氢还原得到4-AP近些年来成为学者研究的热点[6-12].但是,纳米金属粒子易团聚,将纳米金属粒子负载在一定载体上,可克服该缺点.Pinar Ilgin[13]制备了含有硫醚官能团的水凝胶,并以硫醚功能化的水凝胶为载体对Au3+进行选择性吸附,负载AuNPs后的复合水凝胶对4-NP有良好的催化活性.王尚霞[14]采用原位法制备了纳米银/还原氧化石墨@硅藻土(Ag/RGO@DE)复合微粒.结果表明,纳米银的引入显著提高了RGO基体对可见光的吸收及其光生电子-空穴对的分离效率;当银质量分数为2.5%,RGO质量分数为26.6%时,Ag/RGO@DE表现出最佳的光催化还原活性,对4-NP的还原反应具有高效催化活性.Hava Ozay[15]通过酶介导的Au ( III )离子还原,合成了由交联凝胶结构支撑的Au@Gel.固定在交联凝胶结构中的葡萄糖氧化酶确保了凝胶内扩散的Au(III)离子被还原为AuNPs.考察了Au@Gel中AuNPs粒子的催化活性,在还原剂NaBH4存在下,Au@Gel催化4-硝基苯酚(4-NP)还原反应的催化活化Ea为30.16 kJ/mol.
目前,将纳米银负载在智能凝胶上,并以纳米银智能凝胶作为催化剂载体,通过外界环境的刺激作用来控制纳米银粒子催化活性的研究较少.本文以P(AMPS-co-DMAA)智能凝胶为载体,通过原位还原反应引入纳米银粒子,制备纳米复合凝胶AgNPs@Gel,并探讨不同条件下AgNPs@Gel对4-NP的催化性能.
1 实验部分
1.1 试剂与仪器
2-丙烯酰胺基-2-甲基丙磺酸(AMPS,C7H13NO4S,CP,山东寿光煜源化学有限公司);N,N-二甲基丙烯酰胺(DMAA,C5H9NO,AR,江苏南通沃兰化工有限公司);N,N-亚甲基双丙烯酰胺(C7H10N2O2,CP,阿拉丁试剂有限公司);过硫酸铵((NH4)2S2O8,AR,西陇化工有限公司);硝酸银(AgNO3,AR,国药集团化学试剂有限公司);对硝基苯酚(C6H5NO3,AR,国药集团化学试剂有限公司);硼氢化钠(NaBH4,AR,上海展云化工有限公司).
Tensor27型傅立叶红外光谱仪(德国Bruker公司);LEO-1530型扫描电子显微镜(德国里奥电镜有限公司);TU-1901型紫外可见分光光度计(北京普析通用仪器设备有限公司);X,Pert 型X射线衍射仪(荷兰Panalytical公司).
1.2 纳米复合凝胶AgNPs@Gel的制备
以AMPS、DMAA为单体,通过水溶液聚合法制备P(AMPS-co-DMAA)凝胶[16].将已合成的P(AMPS-co-DMAA)凝胶切成一定的形状并干燥后,浸泡在不同浓度AgNO3溶液中.充分浸泡12 h后,取出放入0.05 mol/L NaHB4溶液中进行原位还原反应.将反应产物置于去离子水中,每间隔一定时间换一次去离子水,浸泡2 d后,制备一系列纳米复合凝胶AgNPs@Gel.
1.3 结构表征
FTIR:将干凝胶研磨成粉末后和溴化钾混合压制成膜,采用Tensor27型傅立叶红外光谱仪,在500~4 000 cm-1波长范围内测试;SEM:将冷冻干燥后的水凝胶进行表面喷金处理,采用LEO-1530型扫描电子显微镜观察其表面形态;XRD:将干凝胶研磨成粉末,在X’Pert 型X射线衍射仪进行测试,采用Cu靶Kα辐射线,工作电压40 keV, 工作电流30 mA,2θ扫描范围为10°~ 85°.
1.4 催化性能测试
称取0.05 g NaHB4和0.005 g 4-NP,溶解于50 mL去离子水中.将凝胶切成1 cm×1 cm×1 cm的方块放入到配制的溶液中,每间隔一定时间取出0.5 mL溶液,并稀释一定倍率,用TU-1901型紫外-可见分光光度计测定其吸光度随时间的变化.4-NP的转化率(α)由式(1)进行计算:
α=(1-At/A0)×100%
(1)
式中:A0代表起始吸光度值;At代表t时刻吸光度值.
2 结果与讨论
2.1 FTIR分析
P(AMPS-co-DMAA)凝胶和AgNPs@Gel的红外光谱如图1所示.
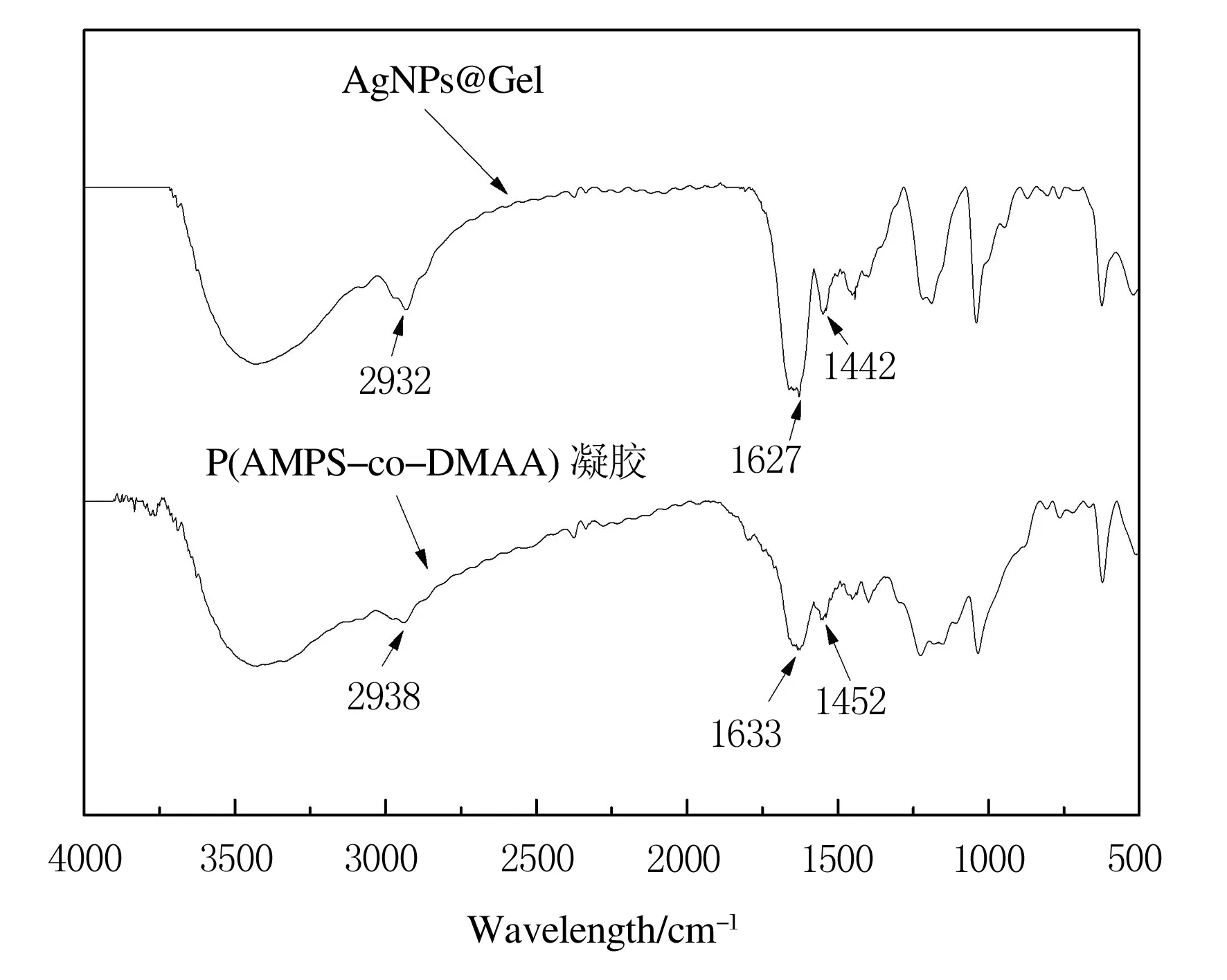
图1 P(AMPS-co-DMAA)凝胶和AgNPs@Gel的红外光谱图
从图1中可以看出,P(AMPS-co-DMAA)凝胶和AgNPs@Gel的特征吸收峰位置基本相似,说明成功制备了AgNPs@Gel.2 932 cm-1处是C—H伸缩振动吸收峰;在1 627 cm-1和1 442 cm-1处分别出现了酰胺基团的C=O伸缩振动吸收峰和C—N伸缩振动吸收峰.但AgNPs@Gel各基团上的特征吸收峰明显比P(AMPS-co-DMAA)凝胶增强.这主要是因为纳米银粒子特有的高表面活性及表面能,能够产生表面增强效应;另一方面,纳米银粒子和AgNPs@Gel的酰胺基团存在相互作用,电子转移向了酰胺基团,导致酰胺基团的伸缩振动频率升高,吸收峰移向低波数.因而AgNPs@Gel比P(AMPS-co-DMAA)凝胶对红外光谱的吸收能力增强.
2.2 SEM分析
P(AMPS-co-DMAA)凝胶、AgNPs@Gel的扫描电镜图和元素分析图如图2所示.
由图2(a)可知,P(AMPS-co-DMAA)凝胶的表面比较平整,未出现明显相分离,凝胶因未浸泡在AgNO3溶液中,故没有检测到元素银的存在;由图2(b)可知,AgNPs@Gel的表面有轻微的褶皱,AgNPs被原位还原后固定在凝胶网络中,数目较少,银的含量为2.95%,粒径大约为200 nm;由图2(c)可知,AgNPs@Gel的表面不平整,有明显的褶皱,且附着着较多的AgNPs颗粒,分散较均匀,银的含量为6.62%,粒径大约为200 nm.这是因为随着AgNO3浓度的增大,P(AMPS-co-DMAA)凝胶吸附更多的Ag+离子于凝胶网络结构中,经原位还原生成的纳米银粒子也增多.
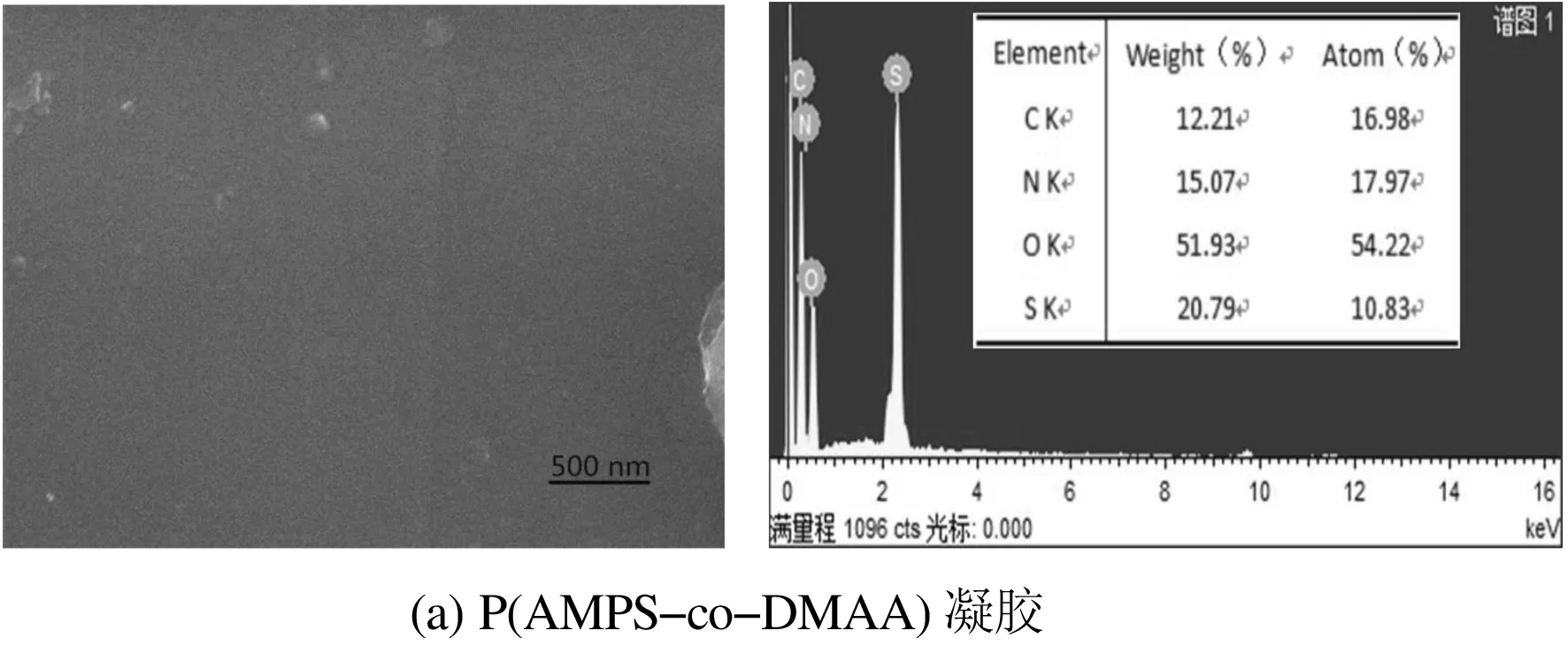


图2 P(AMPS-co-DMAA)凝胶、AgNPs@Gel的SEM图和元素分析图
2.3 X射线衍射图谱分析
AgNPs@Gel的XRD图谱如图3所示.

图3 AgNPs@Gel的XRD图谱
从图3中可以看出,AgNPs@Gel分别在2θ=38.22°,44.46°,64.58°,77.54°处出现4个明显的衍射峰.衍射峰的位置与JCPDS卡上(NO.4-0783)[106]数据相符,分别对应单质金属银的(111)、(200)、(220)和(311)晶面.XRD图谱说明通过原位还原反应,在P(AMPS-co-DMAA)凝胶中生成了具有面心立方晶体结构的纳米银粒子.
2.4 催化性能
以NaBH4为还原剂,测定AgNPs@Gel对4-NP的催化活性.BH4-在AgNPs@Gel的催化下,把反应体系中的硝基还原成氨基,生成4-AP.AgNPs@Gel催化还原对硝基苯酚的紫外吸收光谱图如图4所示.

图4 AgNPs@Gel催化4-NP的紫外吸收光谱图
从图4中可以看出,4-NP的特征吸收峰在400 nm处,随着催化还原反应的进行,4-NP的吸收峰强度逐渐减弱,而在298 nm处出现了新的特征吸收峰,并逐渐增强,这是因为生成物4-AP生成量逐渐增多.当催化还原反应进行120 min后,400 nm处的特征吸收峰基本消失.催化前4-NP溶液呈浅黄色,催化后溶液呈无色透明.在不加AgNPs@Gel催化的对照实验中,发现溶液一直呈浅黄色且不发生变色,其紫外吸光度值不随时间的变化而变化.说明AgNPs@Gel对4-NP的催化活性效果良好.
2.4.1 AgNO3浓度的影响
不同浓度的AgNO3制备的AgNPs@Gel催化4-NP的ln (At/A0)-t曲线如图5所示,对曲线进行线性拟合,并通过计算曲线的斜率可得不同反应条件下的催化反应速率常数Kc.
从图5中可以看出,ln (At/A0)随时间t的变化基本呈线性关系,说明AgNPs@Gel催化还原4-NP的反应基本符合一级动力学.
从图5还可以看出,随着AgNO3浓度的增加,所制备的AgNPs@Gel催化还原4-NP的斜率逐渐增加,催化反应速率逐渐增大,催化转化率也逐渐增大.当AgNO3浓度为0.005 mol/L时,反应平衡时间为200 min,转化率为78.35%,催化速率常数值为0.76×10-2min-1;当AgNO3浓度为0.03 mol/L时,反应平衡时间为120 min,转化率为96.30%,催化速率常数值为2.75 ×10-2min-1;AgNO3浓度≥0.03mol/L,催化反应速率及转化率变化不大.这是因为,随着AgNO3浓度的增加, AgNPs@Gel网络内的纳米银粒子增多,迁移进入凝胶网络内的 BH4-及4-硝基苯氧离子与纳米银粒子接触的机会增多,催化反应速率加快,转化率增加,催化速率常数增加.
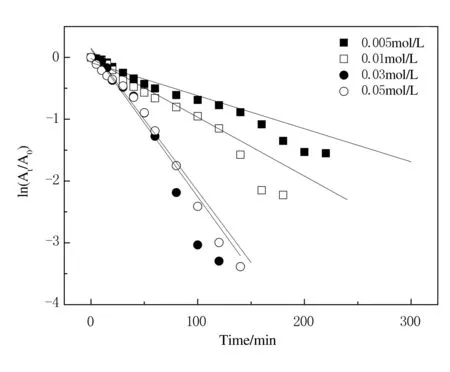
图5 AgNPs@Gel催化4-NP的ln (At/A0)-t线性拟合曲线
2.4.2 凝胶用量的影响
凝胶用量对AgNPs@Gel催化转化率的影响曲线如图6所示.

图6 AgNPs@Gel用量对转化率的影响曲线
从图6中可以看出,随着AgNPs@Gel用量增加,催化反应速率呈增长的趋势,催化转化率也逐渐增大.从表2的数据得出,凝胶用量为10 mg时,反应平衡时间为220 min,转化率为72.76%,催化速率常数值为0.63×10-2min-1;凝胶用量为50 mg时,反应平衡时间为120 min,转化率为96.30%,催化速率常数值为2.75×10-2min-1;AgNPs@Gel用量≥50mg,催化速率常数及转化率变化不大.这是因为,AgNPs@Gel的催化活性是由凝胶中纳米银粒子与反应物接触的数量来决定的.AgNPs@Gel用量的增加,一方面凝胶的体积增大,凝胶表面的纳米银粒子与反应物溶液接触的几率增加;另一方面,凝胶网络内的纳米银粒子增多,扩散进入凝胶网络内的 BH4-及4-硝基苯氧离子与纳米银粒子接触的机会增多.故催化反应速率加快,转化率增加,催化速率常数增加.
2.4.3 电场的影响
外加电场对AgNPs@Gel催化转化率的影响曲线如图7所示.

图7 电场对转化率的影响曲线
从图7中可知,随着电压的增大,催化反应速率呈增长的趋势,催化转化率变化不大.未施加电场时,反应平衡时间为120 min,转化率为96.30%,催化速率常数值为2.75×10-2min-1;电压为30 V时,反应平衡时间为50 min,转化率为96.67%,催化速率常数值为6.81×10-2min-1.这是因为, AgNPs@Gel具有电场敏感性,在电场作用下凝胶发生溶胀,凝胶与反应液的接触面积增大;且电场是离子迁移的驱动力,随着电压的增加,加速了 BH4-及4-硝基苯氧离子扩散进入凝胶网络内,使其与纳米银粒子接触的机会增多,故催化反应速率加快,催化速率常数增加.
2.4.4温度的影响
温度对AgNPs@Gel催化转化率的影响曲线如图8所示.
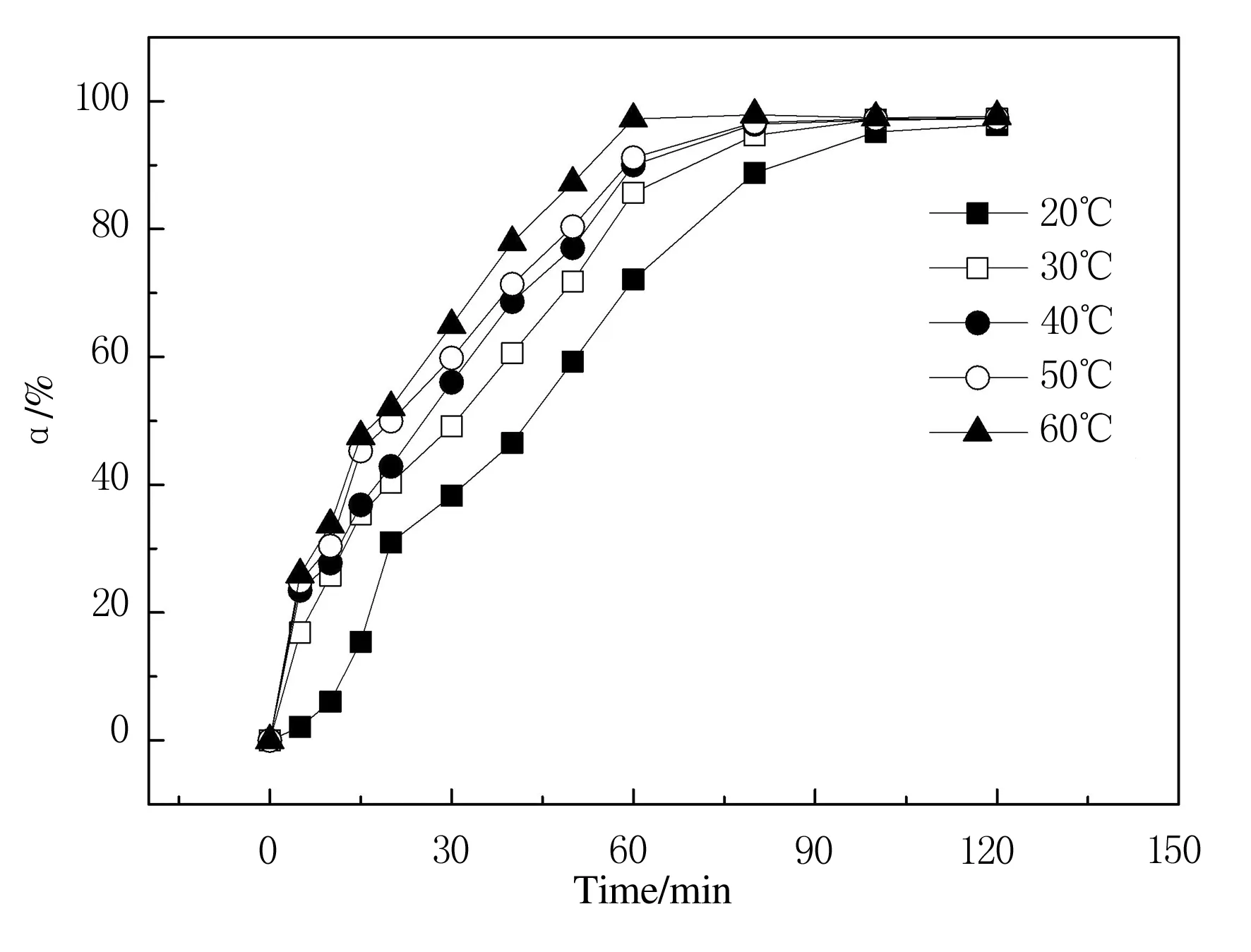
图8 温度对转化率的影响曲线
从图8中可以看出,随着温度的增大,催化反应速率不断增大,催化转化率变化不大.当温度为20 ℃时,反应平衡时间为120 min,转化率为96.30%,催化速率常数值为2.75×10-2min-1;温度为60℃时,反应平衡时间为60 min,转化率为97.22%,催化速率常数值为5.46×10-2min-1.这是因为,反应温度增加,反应体系的熵增加,AgNPs@Gel的催化活性增强,扩散进入凝胶网络内的 BH4-及4-硝基苯氧离子与纳米银粒子接触的几率增加,故催化反应速率加快,催化速率常数增加.
2.4.5 催化重复使用性能
在每次催化反应结束后对AgNPs@Gel进行沉淀分离,用去离子水和有机溶剂进行交替洗脱后再进行下一次催化反应,考察AgNPs@Gel的重复使用性能,如表1所列.

表1 AgNPs@Gel的催化循环使用性能
从表1中可知,第1次催化转化率为96.30%,第3次转化率为93.26%,催化性能下降比较缓慢,随着循环使用次数的增加,催化转化率下降加快,但在第5次时,催化转化率仍达到86.62%.说明AgNPs@Gel具有较好的催化稳定性及重复使用性能.
3 结论
以P(AMPS-co-DMAA)凝胶为模板,吸附Ag+进入凝胶网络内,通过原位还原法制备得到橙黄色的AgNPs@Gel.FT-IR分析表明成功制备了AgNPs@Gel;SEM和XRD分析表明,AgNPs@Gel网络内的纳米银粒子没有团聚,分散较均匀,具有较好的稳定性,粒径尺寸在100~200 nm之间.AgNO3浓度、凝胶用量、外加电场、反应温度均能影响AgNPs@Gel的催化性能,因而可以通过不同的反应条件控制AgNPs@Gel的催化活性.AgNPs@Gel对4-NP有较好的催化活性及重复使用性能,可以应用于生物医药领域,有一定的应用价值.
