库仑滴定法快速测定白酒中总酯的含量
2022-09-22王为民
王为民
(济源市质量技术监督检验测试中心,济源 459000)
白酒作为中国特有饮品,因香味浓郁、口感醇厚而在人们的日常饮食生活中广受欢迎,其中酯类化合物,如乙酸乙酯、己酸乙酯等对白酒的香味与口感具有突出性贡献,决定了白酒的感官品质[1-2]。因此,如何简便、快速、准确地测定白酒中总酯含量,已成为酒类品质分析的研究热点。
目前测定白酒总酯含量的分析方法主要有酸碱滴定法[3-4]、电位滴定法[5]、红外光谱法[6-7]、比色法[8]及气相色谱法[9]。其中电位滴定法作为国家标准规定方法,应用最为广泛,但需提前配制、标定相关溶液且测定耗时较长;红外光谱法在近红外与中红外光谱区均可测定,无需对样品采取预处理和使用对照品,但需建立相关数学模型计算,过程复杂且设备较昂贵,推广难度较大;比色法生成的有色络合物稳定性较差;气相色谱法专属性虽好,可快速分离酒中不同酯类化合物,但因不易获得全部对照品,而难以准确定量。库仑滴定法是控制电解电流生成滴定剂,准确灵敏地快速测定样品中常量、微量及痕量组分的电化学分析方法,已被广泛用于食品、卫生、环保等领域[10-11]。
本工作借鉴酸碱滴定法的原理,探讨了库仑滴定法快速测定白酒中总酯的含量的分析条件,从而为白酒的品质控制提供参考。
1 试验部分
1.1 仪器与试剂
ZDJ-5型库仑滴定仪;ZD-2 型自动电位滴定仪;ME 204E型电子天平;BWS-10型恒温水浴锅;铂丝辅助电极[Ф0.6 cm×5 cm,外套玻璃管,装有10%(质量分数)氯化钾溶液,底部为陶瓷砂芯];E-201-D 型pH 复合玻璃电极;213型铂片电极。
乙酸乙酯标准溶液:2.70 g·L-1,准确移取3 mL乙酸乙酯溶于1 000 mL 无水乙醇中。其余质量浓度的乙酸乙酯标准溶液(0.45~4.5 g·L-1)同法配制。
氢氧化钠标准溶液:0.10 mol·L-1,称取一定质量的氢氧化钠,加水溶解至一定浓度后,采用邻苯二甲酸氢钾标定,即得。
硫酸标准溶液:0.05 mol·L-1,移取一定体积的硫酸加水稀释至一定体积后,采用碳酸钠标定,即得。所用试剂均为分析纯;试验用水为去离子水。白酒样品按品牌的不同分别标记为1,2,3。
1.2 试验原理
样品中的酯类化合物经过量的碱溶液皂化处理后,通过电解液生成的H+消耗样品中剩余的OH-,间接测得皂化反应消耗的碱量,计算出样品中总酯的含量。
1.3 仪器工作条件
213型铂片电极与铂丝辅助电极作电解电极对,E-201-D 型pH 复合玻璃电极作指示电极,0.80 mol·L-1硫酸钾溶液为支持电解质,滴定终点pH 7.70。
1.4 试验方法
1.4.1 样品预处理
准确移取50.0 mL 样品置于回流瓶中,加入适量氢氧化钠标准溶液至pH 7.0,消耗样品中游离酸后,定量加入12.0 mL氢氧化钠标准溶液,于60 ℃水浴回流30 min,冷却后,转移至100 mL 容量瓶中,加水定容,即得样品溶液。
1.4.2 库仑滴定法
将分别置有30 mL的0.80 mol·L-1硫酸钾溶液电解池的阳极区与阴极区通过盐桥相连,另将不同电极连接库仑滴定仪,并预滴定至pH 7.70。随后准确加入1.0 mL 预处理后的样品溶液至电解池阳极区内,搅拌均匀后,自动电解至滴定终点,记录电解时间,通过下式计算样品的总酯含量(以乙酸乙酯含量计)。
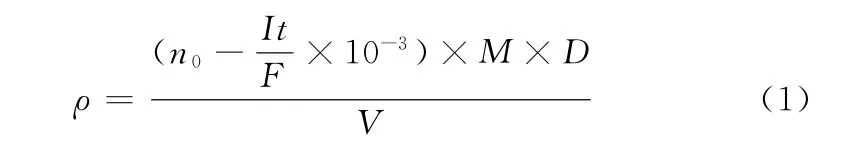
式中:n0为皂化反应加入的氢氧化钠的物质的量,mol;I为电解电流,m A;t为电解时间,s;F为法拉第电解常数,96 500 C·mol-1;M为乙酸乙酯的摩尔质量,88 g·mol-1;D为稀释倍数;V为样品体积,L;ρ为总酯质量浓度,g·L-1。
1.4.3 电位滴定法
参照国家标准GB/T 10345-2007《白酒分析方法》,准确移取20 mL 样品溶液至100 mL 烧杯内,利用硫酸标准溶液自动电位滴定至终点,记录消耗的硫酸标准溶液体积,计算样品中总酯的含量。
2 结果与讨论
2.1 支持电解质浓度的选择
支持电解质的浓度影响滴定过程的电流效率,因此固定电流100.0 m A,分别考察了0.10~1.0 mol·L-1硫酸钾溶液(支持电解质)对2.70 g·L-1乙酸乙酯标准溶液测定结果的影响,并计算回收率和测定值的相对标准偏差(RSD),结果见表1。
由表1可知:当硫酸钾溶液浓度过低时,电解池无法形成回路;随着硫酸钾溶液浓度逐渐增高,测定结果的RSD 逐渐减小至1.0%内。为节约成本,综合考虑,选择支持电解质硫酸钾溶液浓度为0.80 mol·L-1。
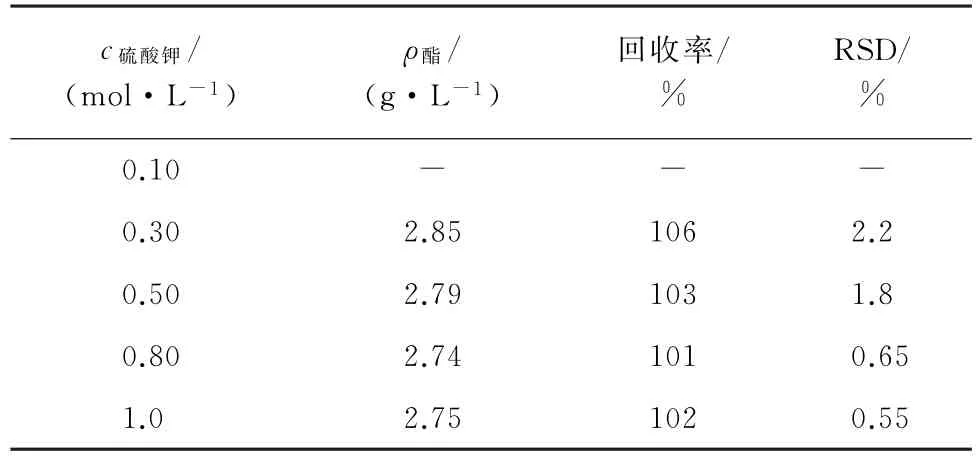
表1 支持电解质浓度对酯测定结果的影响(n=5)Tab.1 Effect of supporting electrolyte concentration on ester determination results(n=5)
2.2 电解电流的选择
若电流过高,单位时间电解生成的H+含量较高,滴定时间过短,可能造成结果误差较大,而电流过低,则滴定时间延长[12]。因此,试验考察了在0.80 mol·L-1硫酸钾溶液中不同电流对2.70 g·L-1乙酸乙酯标准溶液测定结果的影响,结果见表2。
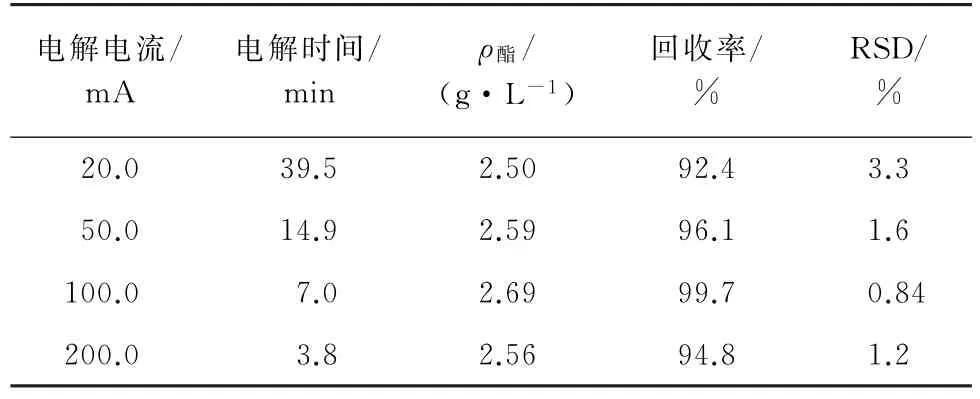
表2 电解电流对酯测定结果的影响(n=5)Tab.2 Effect of electrolytic current on ester determination results(n=5)
由表2可知,电解电流过大或过小,均不利于提高测定结果的准确度与精密度,而且当电流为20.0 m A 时,电解时间较长,接近40.0 min。试验最终确定:当样品总酯质量浓度大于2.00 g·L-1时,电解电流选择100.0 m A,总酯质量浓度小于2.00 g·L-1时,电解电流选择200.0 m A,测定过程控制在10 min内完成。
2.3 滴定终点的选择
以样品1为研究对象,电解电流为200.0 m A,确定实际样品的滴定终点p H,结果见图1。
由图1可知,通过对滴定曲线进行一阶求导得到滴定曲线的突跃点pH 约为7.70,因此选择pH 7.70作为测定样品溶液剩余OH-的滴定终点。
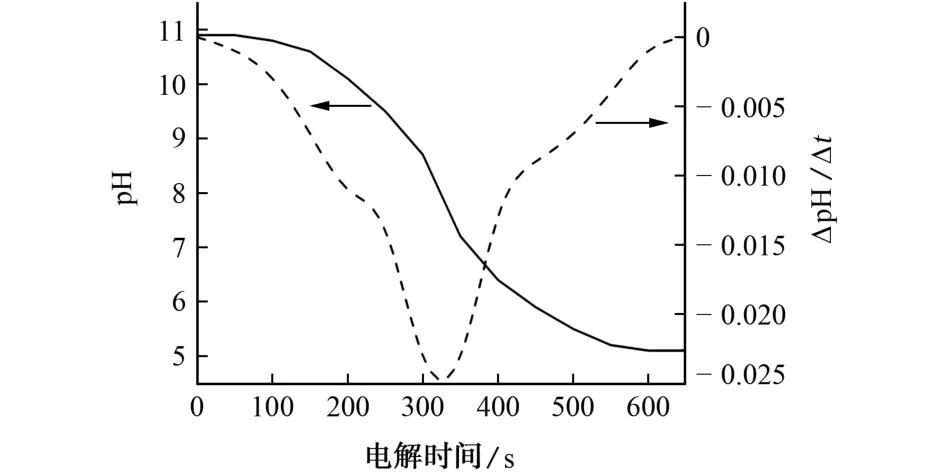
图1 样品1中剩余碱的滴定曲线Fig.1 Titration curves of residual alkali in sample 1
2.4 预滴定与溶解氧的影响
文献[13]采用库仑滴定法测定六氟磷酸锂电解液中游离酸时发现预滴定操作和电解液中的溶解氧可能对测定结果的准确度与精密度造成影响。为此,以2.70 g·L-1乙酸乙酯标准溶液为研究对象,固定电流100.0 m A,考察了测定前进行预滴定和通氮除氧操作对测定结果的影响,结果见表3。
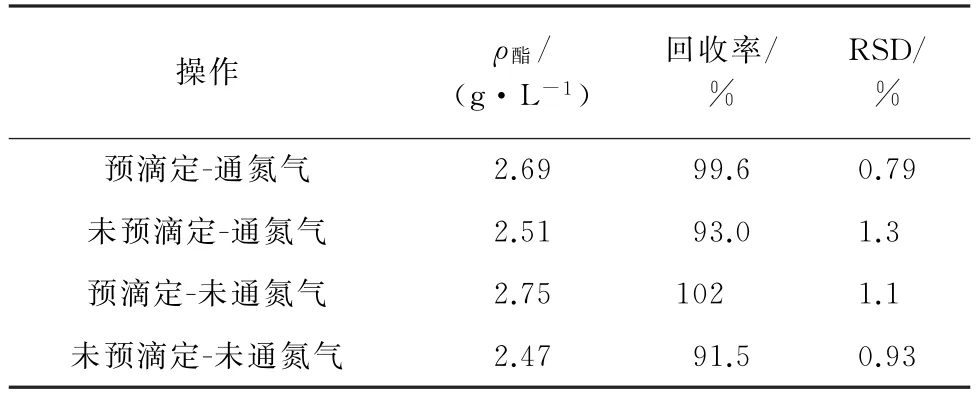
表3 预滴定与通氮除氧对酯测定结果的影响(n=5)Tab.3 Effect of pre-titration and removal oxygen by nitrogen on ester determination results(n=5)
由表3可知,是否通入氮气对回收率结果影响较小,而未采取预滴定操作,会使得测定结果偏低,因此测定样品前,需预滴定溶液pH 至7.70,无需通入氮气去除溶解氧。
2.5 共存物质的干扰
传统固态法制得的白酒未加入食品添加剂,组分中主要为乙醇与水,而液态法或固液结合法制得的白酒中会添加少量增香、增味物质[14],因此以样品1为研究对象,加入0.1%(质量分数)常用添加剂(甜蜜素、甘油、β-胡萝卜素)后,测定其中总酯的含量,结果见表4。
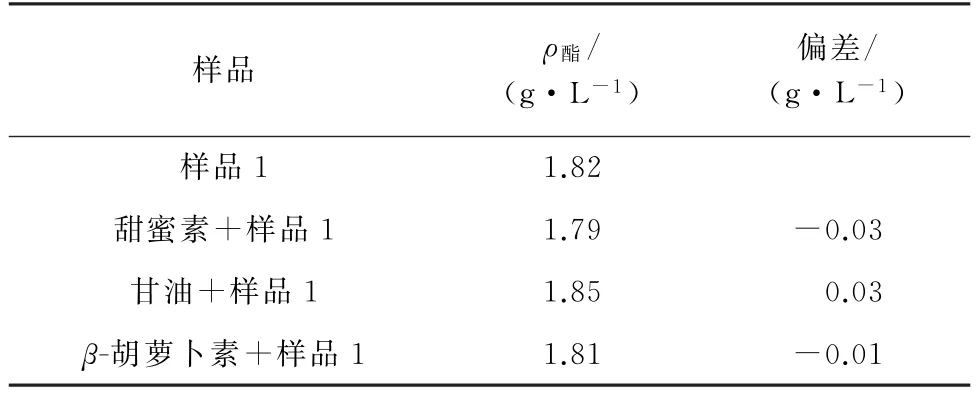
表4 添加剂对酯测定结果的影响(n=5)Tab.4 Effect of additive on the ester determination results(n=5)
由表4可见,添加不同添加剂的样品测定结果相近,与样品1 测定结果的偏差的绝对值均低于0.05 g·L-1,表明上述添加剂对白酒中总酯含量的测定无干扰。
2.6 准确度试验
向50 mL 样品1中加入不同浓度水平的乙酸乙酯标准溶液,并进行预处理,加水稀释定容至100 mL,按照库仑滴定法测定总酯含量后,计算回收率,结果见表5。
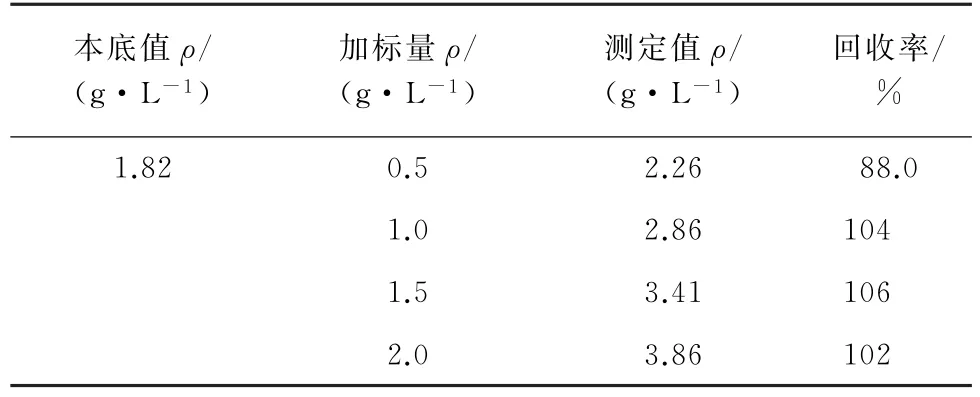
表5 准确度试验结果Tab.5 Results of test for recovery
由表5可知,不同加标量的样品溶液中总酯回收率为88.0%~106%,表明库仑滴定法准确可行。
2.7 方法比对
采用库仑滴定法与电位滴定法分别测定样品1,2,3中总酯的含量,结果见表6。
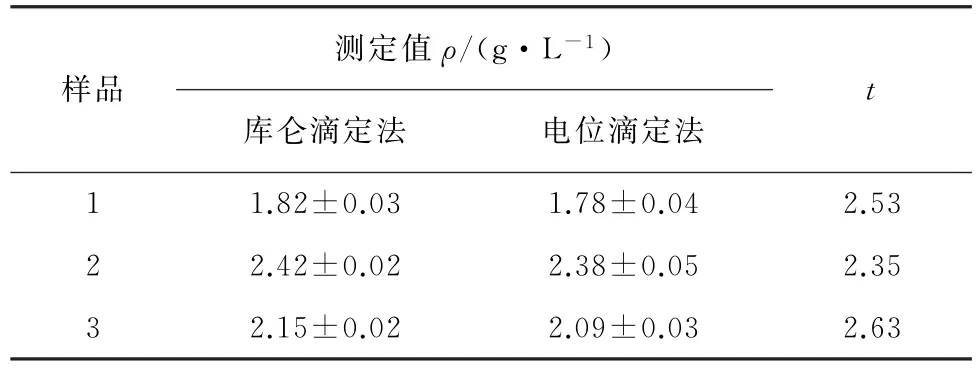
表6 不同方法所得测定结果的比较(n=5)Tab.6 Comparison of determination results of different methods(n=5)
由表6可知,两种方法测得结果相近。在95%置信度下,对两组结果进行t检验分析,计算得到所有t值均低于临界值ttab(2.78),表明不同方法结果之间无显著性差异。
本工作采用库仑滴定法测定白酒中总酯的含量,利用电解生成的H+与预处理后样品中剩余OH-定量反应,根据法拉第电解定律计算出白酒中总酯的含量。与国家标准规定的电位滴定法相比,无需提前过多准备标准溶液,操作较为简便,并可通过控制电解电流,选择合适的电解时间,测定结果具有较好的精密度与准确度,因此适用于相关产品的质量控制。
