利用模型认知探讨综合实验方案设计专题解题策略
2022-09-22江苏省南通市市直学校教育管理中心226019徐小健
江苏省南通市市直学校教育管理中心(226019) 徐小健
模型认知是指通过分析、推理等方法认识研究对象的本质特征、构成要素及其相互关系,建立认知模型,并能运用模型解释化学现象,揭示现象的本质和规律的一种认识方法。
近年来,化学综合实验方案设计的题型以其独有的魅力越来越受到命题者青睐,这类试题可以较好地考查学生获取加工信息、综合运用所学化学知识解决实际问题的能力,需要学生有物质间转化、物质检验、物质分离与提纯等基础知识,并能建立以物质性质为依据的试剂选择、混合顺序等,能够根据实验目的、实验试剂,运用比较分析、类比迁移等科学方法,以“身临其境”的状态严谨地设计每一步实验操作,还要能根据实验步骤所要达到的目的结合现象准确描述试剂用量。在语言表达上有些类似于语文中的小作文,所以解这类试题需要学生有较好的语文素养和化学素养。试题通常以工业上某种重要的无机物的制备、含量测定等为背景,体现了化学是“真实的”“有用的”[1]。
《普通高中化学课程标准(2017年版2020年修订)》中要求学生“学习研究物质性质,探究反应规律,进行物质分离、检验和制备等不同类型化学实验及探究活动的核心思路与基本方法。由于这类试题是基于真实问题情境下的实验设计,所以在设计时要考虑得较为细致、具体、全面。综合实验方案设计题对学生的思维能力要求较高,主要涉及信息加工的整合能力、实验方案优劣的评价能力、实验数据的分析处理能力、实验方案的设计能力、规范的语言表达能力[2]。学生在这类试题的解决中会遇到较多问题,在教学中如何引导学生突破呢?实践证明构建解题模型能有效帮助学生有条不紊地解决此类问题。
1 设计物质制备路线,建构物质转化模型
1.1 路线格式
要想设计一个较为复杂的实验方案,需要对整个实验原理有一个清晰的认识。我们可以依照有机合成路线设计的格式,结合原料及所给试剂来设计物质转化路线,其格式如图1所示,其中控制的条件包括温度、溶液的pH值等,实验操作包括过滤、结晶等。设计时可以从原料出发,最终得到单一产品溶液(后续分离操作暂时可以不写出)。

图1 物质制备路线示意图
1.2 典型例题
例1:工业废铝屑(主要成分为铝,还含有少量氧化铁、氧化铝)可用于制取硫酸铝晶体[Al2(SO4)3·18H2O]。请补充完整由废铝屑为原料制备硫酸铝晶体的实验方案:取一定量废铝屑,放入烧杯中,____,得硫酸铝晶体。[已知:pH=5时,Al(OH)3沉淀完全;pH=8.5时,Al(OH)3沉淀开始溶解。须使用的试剂:3 mol·L-1H2SO4溶液、2 mol·L-1NaOH溶液、冰水]
1.3 思维建模
对比原料与产品可知,此处需要的元素是铝元素,所以氧化铁为杂质。结合所给试剂可知有两种方式:(1)用3 mol·L-1H2SO4溶液溶解废铝屑后,再用2 mol·L-1NaOH溶液调节溶液pH除去Fe3+,但题中未给出Fe3+完全沉淀时的pH,所以排除此方式;(2)用2 mol·L-1NaOH溶液溶解废铝屑并过滤除去氧化铁后,再用3 mol·L-1H2SO4溶液调节溶液pH,此时又有两种选择:①调至pH为5~8.5,使Al(OH)3完全沉淀,过滤后再加入3 mol·L-1H2SO4溶液将沉淀完全溶解,②直接滴加3 mol·L-1H2SO4溶液,使生成的Al(OH)3沉淀恰好溶解,但显然此方式中会混有Na2SO4杂质,排除此方式。所以在分析转化过程时,不仅要从所给试剂等信息揣摩命题意图,还要通过对比判断哪种方式更可控、更能使最终的产品纯净,进而确定最终路线。本题最终确定如图2所示的物质制备路线图。
1.4 拓展练习
例2:某研究性学习小组欲从蚀刻镀铜电路板所得废液(溶质为FeCl2、CuCl2、FeCl3)中制备出单质铜和FeCl3·6H2O。请补充完整由蚀刻废液制备单质铜和FeCl3·6H2O的实验步骤:向废液中加入足量铁粉,充分反应后过滤;________;调节溶液pH,将溶液蒸发浓缩、冷却结晶、过滤、洗涤干燥得FeCl3·6H2O。(可选用的试剂:铁粉、盐酸、NaOH溶液和H2O2溶液)
点拨:本题中铁元素与铜元素都是所需要的,向废液中加入足量铁粉,充分反应后过滤得到的滤渣中含有金属铜和过量的铁粉,所以要进一步将过量铁粉分离出来并参与后续反应,以提高原料的利用率,可以得到如图3所示的物质制备路线图。
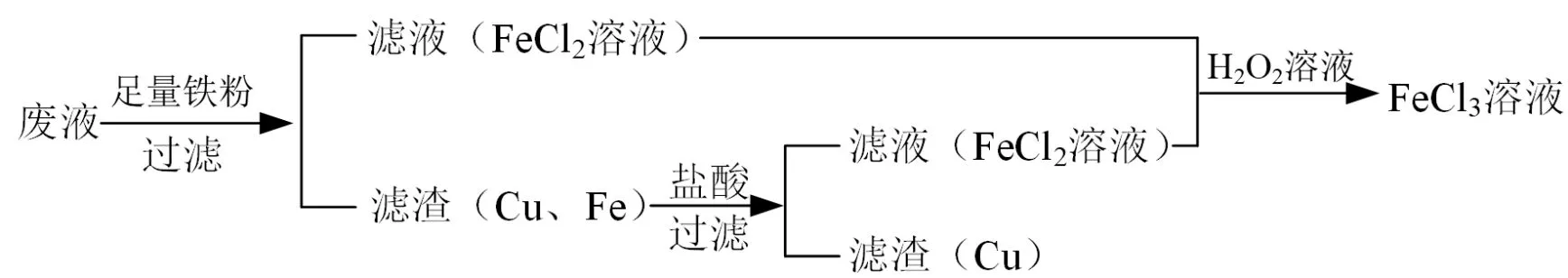
图3 废液制备铜和六水合氯化铁的物质制备路线图
2 结合实验操作细节,建构方案设计模型
有了物质转化路线图就有了实验方案设计的主线,相当于写作文拟的提纲。此时再结合具体实验操作细节,从实验操作层面分析每个环节需要注意的问题,即可设计出较完美的实验方案。
2.1 盘点操作细节
参照工业流程图,将整个实验设计划分为提供原料、核心反应和目标产品三个部分进行分析。
2.1.1 从提供原料角度
提供的原料一般是固体原料,若已结块则先粉碎,若含有受热易分解的杂质则先灼烧至固体质量不再变化。其他情况则一般先溶解制得溶液,为确保固体中的有效成分完全溶解而又不至于浪费过多溶液,在实验操作时应分批加入。
提供的原料如果全部是溶液,为确保X溶液中的有效成分完全反应而又不至于浪费过多Y溶液,在实验操作时应逐滴加入,直至反应结束。文字可描述为“边搅拌边向X溶液中滴加Y溶液直至固体完全溶解(或不再减少)”,可从以下几个角度指明反应完成的特征:①沉淀不再增多(产生大量沉淀后,静置,向上层清液中继续滴入少量X溶液,无沉淀产生);②不再产生气泡;③颜色变为*色;④溶液pH在a~b之间。如果没有明显的完成特征,则要指明将哪种物质完全转化。
此外,务必关注题中提供的是“须使用的试剂”还是“可选用的试剂”,可借助这些试剂的性质和作用分析制备的流程。
2.1.2 从核心反应角度
在进行核心反应设计时要考虑:是否要注意加料方式?是否要控制反应条件?若生成污染性气体,则要进行尾气处理。文字描述可参考2.1.1中的文字描述。
2.1.3 从目标产品角度
如果目标产品是难溶性固体,则一般流程是:在制备反应完成后,静置、过滤,再充分洗涤滤渣直至向最后一次的洗涤滤液中加入Y溶液无沉淀产生,低温干燥。
如果目标产品是可溶性固体,则一般流程是:在制备反应完成后,根据溶质溶解度随温度的变化情况和溶质热稳定性选择合适的结晶方式,对溶解度随温度升高而缓慢增大的晶体,采用蒸发溶液至出现较多晶体时(趁热)过滤的方式,对溶解度随温度升高而迅速增大或热稳定性差的晶体,采用蒸发浓缩(至溶液表面产生一层晶膜)、冷却结晶、过滤,然后用冰水或无水乙醇洗涤,再低温干燥的方式。
如果目标产品是溶液,则在制备反应完成后进行除杂即可。
2.2 建构思维导图
在教学中,教师可以将综合实验方案设计各环节列出,然后让学生尽可能多地罗列出各环节注意事项,建构思维导图,这样可以让整个过程一目了然,更有利于整体架构。比如物质制备综合实验设计可以建构图4所示的思维导图。
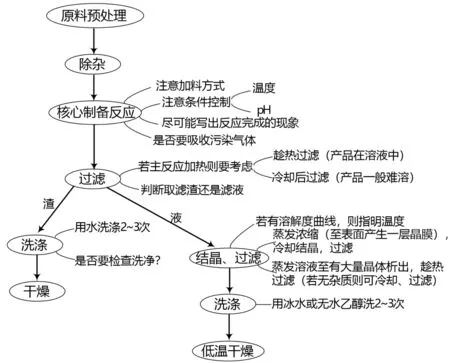
图4 物质制备综合实验设计思维导图
2.3 设计实验方案
有了实验操作细节的经验后,就可以沿着物质转化路线图这一主线进行实验方案设计了。例1可设计为“边搅拌边分批加入2 mol·L-1NaOH溶液,直至不再有气泡产生,过滤;搅拌时向滤液中滴加3 mol·L-1H2SO4,调至pH为5~8.5,过滤,洗涤滤渣2~3次;将滤渣转移至烧杯中,边搅拌边分批加入稍过量的3 mol·L-1H2SO4至固体完全溶解;将溶液蒸发浓缩、冷却结晶、过滤、用少量冰水洗涤滤渣,干燥”。例2可设计为“边搅拌边向滤渣中分批加入稍过量盐酸至不再产生气泡,过滤、洗涤、干燥得铜粉;将两次过滤所得滤液合并,向其中加入适量H2O2溶液至Fe2+全部生成Fe3+”。
3 参照方案评价要点,完善实验设计细节
3.1 评价目的
《普通高中化学课程标准(2017年版2020年修订)》中提出“积极倡导‘教、学、评’一体化,使每个学生化学学科核心素养得到不同程度的发展。化学日常学习评价不能游离于化学教与学之外,应与化学教与学活动有机融合在一起。”在综合实验方案设计教学中,教师可以在学生独立完成的基础上,给出评分依据,让学生根据评分标准在小组内互评,这样学生就可以站在阅卷者视角来审视别人的实验方案并反思优化自己设计的方案。评分后选择代表进行展示,师生进一步交流和优化评价的合理性,这样操作既减轻了教师逐一批阅的困难,又让学生了解到阅卷的标准,进而提升了实验设计水平,提高了课堂教学效果。
3.2 评价角度
评价时一般可以从以下六个方面进行:①试剂的选择、使用顺序是否正确(即实验原理是否正确)?若不正确,则不得分。②反应完成的特征描述是否准确?若没有描述或描述不准确,则不得分。③实验基本操作是否规范、完整?若不完整或不规范,则酌情评分。④条件控制是否正确?若没有或不准确,则不得分。⑤实验步骤中,对象描述是否明确?若没有指明对象,则酌情评分。⑥文字描述是否完整?若文字描述不完整,则酌情评分。
3.3 分点评分
为了让学生在评分时有可操作性,需要给出分点评分标准。如果将综合实验设计题分值设为4~5分,可以将得分细化。
实践证明,学生抓住物质制备路线图主线,结合各环节注意事项,语言学术化、操作程度化、试剂定量化[3],一定能够设计出较为完整的实验方案,教师要引导学生不断进行归纳、总结、发散、创新,使学生从设计实验的学习中深化和发展知识,发展创新思维,增强思维的严谨性、全面性、逻辑性[4],培养学生的学科核心素养。
