乙二醇法合成海藻糖脂肪酸酯
2022-09-21李殷
李 殷
(常州工学院化工与材料学院,江苏 常州 213000)
海藻糖是由两分子的葡萄糖通过α,α-1,1糖苷键结合的非还原性二糖[1],是合成非离子表面活性剂海藻糖脂肪酸酯的重要原料。海藻糖脂肪酸酯由海藻糖(亲水性基团)和脂肪酸(疏水性基团)两部分结合而成,故影响反应产率的关键因素是溶剂对两种原料的溶解性。由于海藻糖具有多个羟基可供酯化反应,所以选择不同的催化剂,海藻糖酯化的羟基会不同[2-3]。目前海藻糖脂肪酸酯的主要合成方法有微生物发酵法[4]、酶催化合成法[5-7]和化学合成法(脱水法、酰氯酯化法和酯交换法)[8-9]:李智斌等[5]以脂肪酶Lipozyme 435为催化剂,叔丁醇/吡啶为溶剂,由海藻糖与脂肪酸的酯化反应可高选择性地合成海藻糖单脂肪酸酯;微生物和酶促发酵时间长,不利于工业化;Paul等[8]采用O-苯并三氮唑-N,N,N′,N′-四甲基脲四氟硼酸为催化剂和DMF溶剂合成出指定构型的海藻糖脂肪酸酯,但由于催化剂和溶剂有毒性,不能用于食品工业。
本工作以食品级原料合成海藻糖脂肪酸酯,采用无毒溶剂和催化剂进行酯交换,解决了目前制备过程中溶剂、催化剂毒性较大的技术问题。
1 实 验
1.1 主要试剂与仪器
海藻糖,食品级,溧阳维信生物科技有限公司;硬脂酸(n=18),分析纯,成都市科龙化工试剂厂;碳酸钾,分析纯,宜兴市第二化学试剂厂;乙酸乙酯,分析纯,江苏强盛功能化学有限公司;氯化钠、无水乙醇、乙二醇,分析纯,江苏永丰化学试剂有限公司;溴化钾,光谱纯,国药集团化学试剂有限公司。
IR-960傅里叶变换红外光谱仪,天津瑞岸科技有限公司;Varian 00M超导核磁共振波谱仪(CD3OD,500 MHz),美国瓦里安有限公司;Waters e2695液相色谱仪,美国沃特斯公司。HLB值比色管,自制。
1.2 合成步骤
1.2.1 硬脂酸乙酯的制备与纯化
在向装有温度计和冷凝管的250 mL三口烧瓶中加入硬脂酸,在搅拌下缓慢加入浓硫酸,滴加无水乙醇,加热升温并搅拌,在70 ℃回流反应4 h。反应停止后蒸出多余乙醇,冷却至室温,加入2%碳酸钠水溶液进行洗涤,用水洗至中性[10-11];静置分层,取上层油状有机层,干燥后冷却,得到透明状固体,即硬脂酸乙酯。
1.2.2 乙二醇溶剂法制备海藻糖酯
向装有温度计和冷凝管的250 mL三口烧瓶中加入16 g硬脂酸乙酯和150 mL醇类溶剂乙二醇,搅拌,加入研磨烘干的37 g海藻糖粉末和0.8 g催化剂K2CO3粉末,减压蒸馏,升高温度至130 ℃,在真空度0.09 MPa下反应5 h,反应过程中将反应生成的甲醇和溶剂乙二醇蒸出,得到24 g产物海藻糖硬脂酸单酯。
1.2.3 海藻糖酯的纯化
向反应产物中加入10%NaCl溶液,再加入乙酸乙酯溶液,加热至80 ℃,搅拌至产物充分溶解;将溶液冷却静置,减压抽滤,即得粗产物。用热的乙醇溶液溶解粗产物,冷却后海藻糖酯重结晶析出,即得纯化产物。通过定量分析海藻糖残留量计算海藻糖酯纯度。
1.3 性能测试方法
1.3.1 HLB值的测定
采比色管中,以Tween80、Span85以及Tween40作HLB标准曲线,通过式(1)计算混合物的HLB值[12]。用各种不同HLB值为横坐标,耗水体积为纵坐标作标准曲线,计算得到海藻糖脂肪酸酯HLB值。
(1)
式中:HLBA、HLBB分别为AB混合物中物质A和物质B的HLB值;WA、WB分别为AB混合物中物质A和物质B的质量分数。
1.3.2 起泡性和泡沫稳定性的测定
在25 ℃,将质量浓度为0.2 g/L的海藻糖脂肪酸酯溶液和对照物Tween80、Span80以及Tween60加入50 mL离心管中,记录溶液起始高度(H0)。用高速剪切机于1 500 r/min下分散均质2 min,立即测定每组试样的泡沫高度(H2)和液体总高度(H1),分别静置20、40、60、80 min后,再分别记录泡沫高度(H3)[13]。依照式(2)和式(3)计算起泡性与泡沫稳定性:
发泡性,%=(H1+H2-H0)/H0×100%
(2)
发泡稳定性,%=H3/H1×100%
(3)
1.3.3 乳化性和稳定性的测定
在25 ℃、1 500 r/min条件下,将20 mL海藻糖脂肪酸酯水溶液与10 mL大豆油均质5 min制备乳液,记录乳液相高度(h1)和系统总高度(h2),按式(4)计算海藻糖脂肪酸酯的乳化性(EA):
EA,%=h1/h2×100%
(4)
静置45 min后,将乳剂以1 000 r/min搅拌5 min,然后测量乳液相的高度(h3)和体系的总高度(h4),按式(5)计算乳化稳定性(ES):
ES,%=h3/h4×100%
(5)
2 结果与讨论
2.1 产物表征
2.1.1 红外光谱
图1为试样的红外光谱(溴化钾法压法)。

图1 海藻糖和海藻脂肪酸酯的IR光谱

与海藻糖的红外光谱相比,海藻糖脂肪酸酯在1 737 cm-1附近出现了一个较强的羰基峰;与硬脂酸乙酯的红外光谱相比海藻糖脂肪酸酯在3 405 cm-1附近出现了一强而宽的缔合O—H吸收峰,在990 cm-1处出现了苷键的特征峰。故由此推断产物为海藻糖与硬脂酸乙酯进行酯交换反应合成了海藻糖脂肪酸酯。
2.1.21H NMR
图2为海藻糖脂肪酸酯的1H NMR谱。

图2 海藻脂肪酸酯的1H NMR谱
由图2可见,δ:5.04(dd, 2H, 1-H, 1′-H), 4.36(dd, 1H, 6-H), 4.19(dd, 1H, 6-H), 3.78~3.66 (m, 4H, 2-H, 2′-H, 5′-H, 6′-H), 3.66(dd, 1H, 6′-H), 3.48~3.46(m, 2H, 3-H, 3′-H), 3.34~3.30(m, 2H, 4-H, 4′-H), 2.89(t, 2H, 2″-H), 1.61(m, 2H, 3″-H), 1.28 (m, 30H, 4″-H~16″-H), 0.90(t, 3H, 8″-H)。可见,该图谱与理论氢谱出峰位置基本相同,亦可以判断产物为海藻糖脂肪酸单酯。
2.2 海藻糖残留量
采用液相色谱法,根据海藻糖标准品定量曲线(图3)计算纯化产物中残留海藻糖为6.2 g/100 g,海藻糖酯含量为93.8%(图4)。
2.3 反应条件的优化
2.3.1 糖酯摩尔比对产率的影响
由于海藻糖与硬脂酸乙酯的酯交换反应是可逆的,故糖酯摩尔比对产率的影响很大。在回流温度100 ℃、碳酸钾用量为1.5%(催化剂与原料的质量比,下同)、反应时间为5 h的条件下,考察糖酯摩尔比对产率的影响,结果见图5。
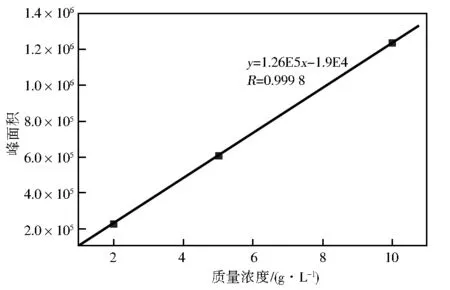
图3 海藻糖标准曲线回归方程

图4 海藻糖试样的HPLC
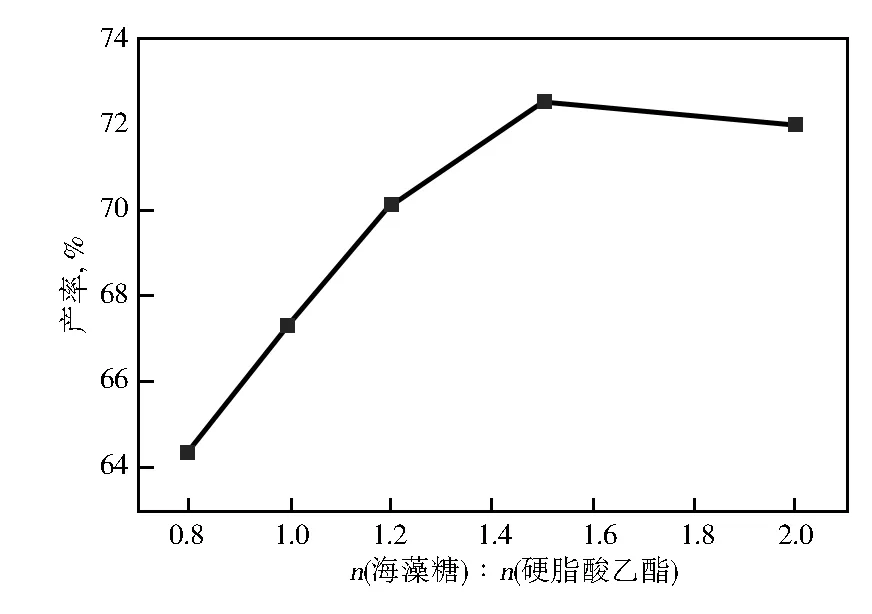
图5 n(海藻糖)∶n(硬脂酸乙酯)对产率的影响
由图5可知,产率随糖酯摩尔比的增大而增加,当超过一定的比例后,产率变化不大。因此,适宜的n(海藻糖)∶n(硬脂酸乙酯)为1.5∶1。
2.3.2 催化剂用量对产率的影响
在回流温度100 ℃、n(海藻糖)∶n(硬脂酸乙酯)=1.5∶1、反应时间为5 h的条件下,考察催化剂碳酸钾用量对产率的影响,结果见图6。
由图6可知,产率随催化剂的增大而增加,当催化剂用量为1.5%时,产率基本达到最大值,继续增加催化剂用量,产率提高不明显。因此,适宜的催化剂碳酸钾用量为1.5%。

图6 催化剂用量比对产率的影响
2.3.3 反应时间对产率的影响
在回流温度100 ℃、n(海藻糖)∶n(硬脂酸乙酯)=1.5∶1、碳酸钾用量为1.5%条件下,考察反应时间对产率的影响,结果见图7。由图7可知,适宜的反应时间为5 h。
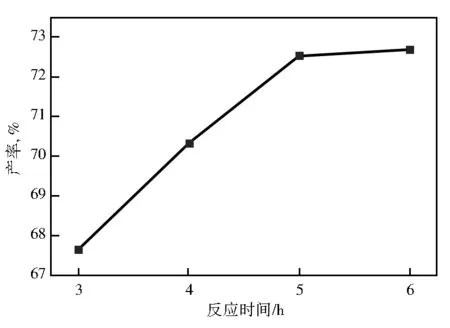
图7 反应时间对产率的影响
2.4 海藻糖脂肪酸酯的性能
2.4.1 HLB值
图8是HLB值的标准曲线。由图8可见,海藻糖脂肪酸酯的HLB值为15.36。

图8 海藻糖脂肪酸酯的HLB标准曲线
2.4.2 起泡性和发泡稳定性
图9是海藻糖脂肪酸酯与对照物的起泡性。
由图9可见,Span80具有极低的发泡性,这可能与其HLB值过低(4.3),疏水性强有关。相对而言,具有较高HLB值的Tween80、海藻糖脂肪酸酯以及Tween60则具有较好的发泡性。
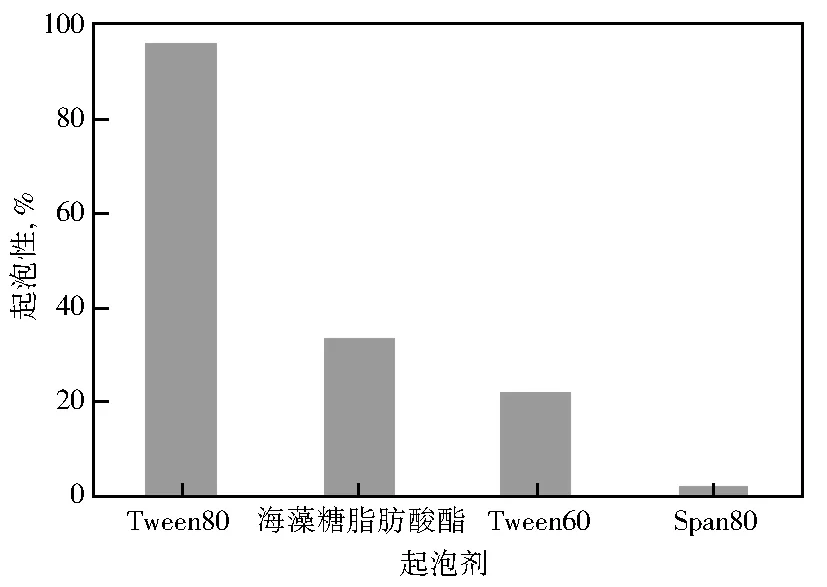
图9 海藻糖脂肪酸酯与对照物的起泡性
图10是海藻糖脂肪酸酯与对照物的发泡稳定性。从图10可以看出,随着时间的延长,Tween80、Tween60以及海藻糖脂肪酸酯的泡沫稳定性逐渐降低。可见,海藻糖脂肪酸酯可用作一些条件要求不高的发泡剂。
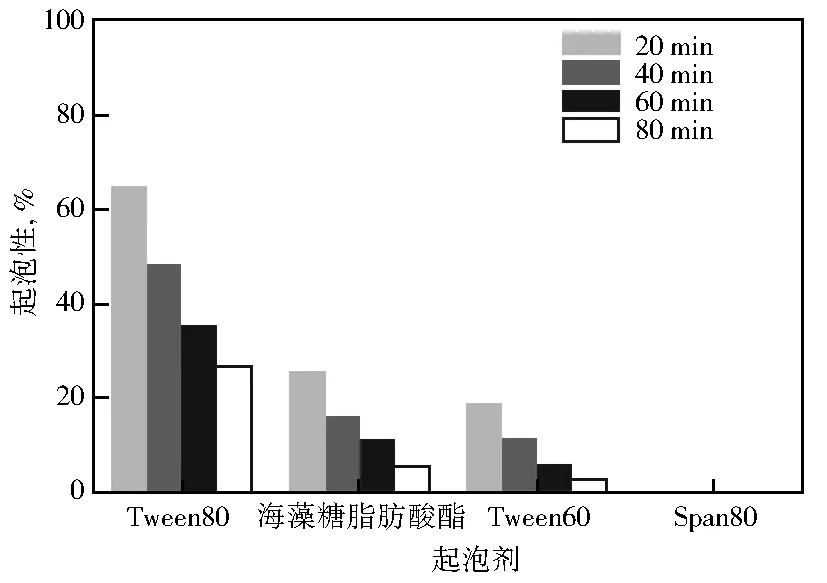
图10 海藻糖脂肪酸酯与对照物的发泡稳定性
2.4.3 乳化性能
海藻糖脂肪酸酯的乳化性能见表1。
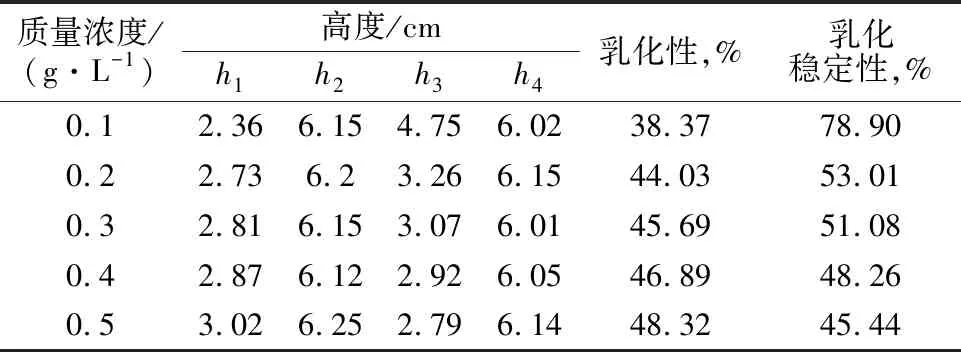
表1 海藻糖脂肪酸酯的乳化性及乳化稳定性
由表1可见,海藻糖脂肪酸酯的乳化性能和乳化稳定性随着质量浓度的增加而逐渐增加,当质量浓度大于0.2 g/L时,趋势逐渐趋于平缓。
3 结 论
a.采用酯交换法合成海藻糖脂肪酸单酯,较佳的工艺条件为:反应温度100 ℃,n(海藻糖)∶n(硬脂酸乙酯)=1.5∶1,催化剂碳酸钾用量1.5%,反应时间5 h,产率72.5%,海藻糖酯含量大于99.6%(HPLC)。
b.海藻糖脂肪酸酯的HLB值为15.36,具有较高的亲水性,可用作增溶剂。海藻糖脂肪酸酯具有较好的发泡性能,在质量浓度0.1~0.5 g/L范围内具有较好的乳化性能,可用作发泡要求条件不高的发泡剂。该合成工艺采用食品添加剂乙二醇作为溶剂,合成海藻糖脂肪酸酯工艺简单,生产成本低,易于工业化生产。
