基于网络药理学及分子对接探讨参苓白术散对慢性肾小球肾炎和抑郁症异病同治的作用机制
2022-09-20郑舒文王柏森李志明王圣治
郑舒文,王柏森,李志明,王圣治
(辽宁中医药大学 1.研究生学院,沈阳 110847;2.附属医院肾内科,沈阳 110032)
慢性肾小球肾炎(chronic glomerulonephritis,CGN)是我国最常见的慢性肾脏病之一,病程较长者可致慢性肾衰竭,其病理机制尚未明确且无特效药物[1-2]。抑郁症主要表现为情绪低落,对周边事物漠不关心,产生自责心理[3-4],严重影响患者的健康和生活质量[5],其发病可能与多种因素有关[6-10]。抗抑郁药治疗在短期具有一定作用,但其不良反应亦不容忽视[11-12]。CGN和抑郁症目前均无明确病理机制及特效药,而中医在慢性疾病治疗方面具有一定的优势。中医异病同治是中医基础重要理论之一,不同疾病其病机相同即可用同一药方治疗。参苓白术散出自《太平惠民和剂局方》[13]。已有研究[14]表明,加味参苓白术散治疗脾肾两虚型CGN,疗效确切,改善临床症状效果显著;也有研究[15]表明,以参苓白术散为底方,运用健脾益气法治疗老年抑郁症患者,总有效率91%。由于CGN和抑郁症均有脾虚证,而参苓白术散有益气补脾的作用,为异病同治提供了理论依据。
网络药理学主要通过建立“成分-靶标-通路-疾病”网络的方法分析药物的作用机制[16],由此可知一种靶点可调控多种疾病,这种调控过程和中医的异病同治类似。参苓白术散治疗CGN和抑郁症均效果良好,因此,本研究拟通过网络药理学及分子对接的方法分析其异病同治的作用机制,以证明中医药在2种疾病中的作用。
1 材料与方法
1.1 参苓白术散化学成分及靶点的搜寻
运用中药系统药理学(Traditional Chinese Medicine Systems Pharmacology,TCMSP)数据库和分析平台(http://tcmspw.com/tcmsp.php),搜索参苓白术散方组成中10种中药的活性成分,以口服生物利用度(oral bioavailability,OB)≥30%和类药性指数(drug like index,DL)≥0.18[17]为条件,对收集的信息进行筛选。并利用 Uniprot数据库(https://www.uniprot.org)的注释文件将药物靶点基因规范化。
1.2 参苓白术散治疗CGN和抑郁症共同靶点的筛选
利用GeneCards数据库(https://www.genecards.org)和OMIM数据库(https://www.omim.org),获取CGN和抑郁症的对应靶点。将该靶点及参苓白术散对应的靶点导入在线软件Venny 2.1.0(https://bioinfogp.cnb.csic.es/tools/venny/)取交集,并绘制韦恩图。
1.3 “中药-活性成分-共同靶点”网络的构建
用Cytoscape3.8.2软件构建参苓白术散治疗CGN和抑郁症的“中药-活性成分-共同靶点”网络。对上述网络进行拓扑分析,其中,度的数值越大,该成分越有可能为参苓白术散治疗的潜在活性成分。
1.4 关键靶点的筛选
在STRING数据库(http://string-db.org)中上传共有靶点,并将物种设置成人类,取最高置信度,数值0.900,其余参数设置为默认,获得蛋白质-蛋白质相互作用(protein-protein interaction,PPI)网络。将结果导入Cytoscape软件可视化,拓扑分析后选取度值较高的前10个靶点,即参苓白术散异病同治的核心靶点。
1.5 通路分析
将共同靶点导入DAVID 6.8数据库(https://david.ncifcrf.gov/),限定物种为人类,对参苓白术散“异病同治”的作用靶点进行富集分析,按P值从小到大排序,绘制排名前20的结果图。
1.6 分子对接
从TCMSP数据库和RCSB蛋白质数据库(https://www.rcsb.org/)分别下载活性成分的分子结构,以及核心靶点对应蛋白的晶体结构,并导入Sybyl-X2.1.1软件进行分子对接。若对接得分>4.25,表明分子与蛋白具有对接活性;若对接得分>5,表明具有较好的对接活性;若对接结果>7,则认为具有高度的对接活性。
2 结果
2.1 参苓白术散的活性成分和靶点筛选
从TCMSP数据库中获得参苓白术散中10味中药的活性成分,其中,人参22种、白术7种、茯苓15种、桔梗7种、白扁豆1种、甘草92种、莲子心11种、薏苡仁9种、山药16种、砂仁10种,将活性成分对应靶点删除重复后获得225个靶点,将结果绘制“成分-靶点”网络图(图1)。

图1 “成分-靶点”网络图Fig.1 "Component-target" network diagram
2.2 CGN和抑郁症的靶点预测
在GeneCards数据库和OMIM数据库中,CGN对应删除重复后靶点1 806个,抑郁症对应删除重复后靶点12 997个。在Venny2.1.0中得到参苓白术散异病同治2种疾病潜在作用靶点共计103个,并绘制韦恩图(图2)。
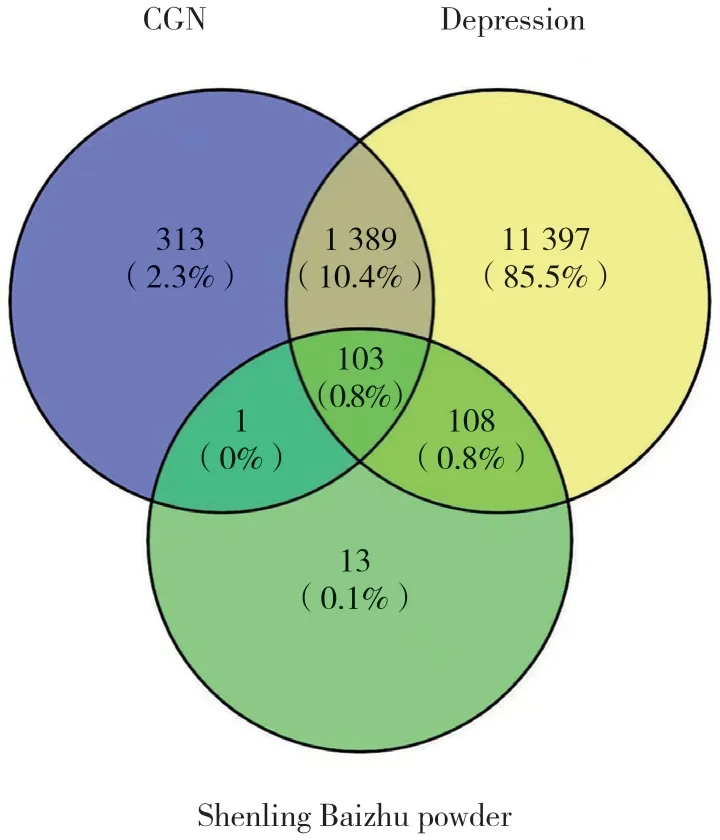
图2 共有作用靶点韦恩图Fig.2 Venn diagram of common action target
2.3 “中药-活性成分-共同靶点”网络结构
在参苓白术散异病同治2种疾病的“中药-活性成分-共同靶点”网络图(图3)中,活性成分槲皮素(MOL000098)、木犀草素(MOL000006)、山奈酚(MOL000422)为参苓白术散异病同治的关键活性成分,其中,槲皮素作用于75个靶点,网络度最好。
2.4 PPI网络构建与关键靶点筛选
构建的PPI网络图共有节点97个,边912个。其中,参苓白术散异病同治的核心靶点是STAT3、JUN、RELA、MAPK1、TP53、AKT1、HSP90AA1、MAPK14、IL6、ESR1。
2.5 通路分析
共获得参苓白术散与疾病共有靶点的基因本体论(gene ontology,GO)富集结果508条(P<0.05),共同靶点主要影响生物学结果(biological process,BP)383条,主要包括DNA模板转录的正调节、RNA聚合酶Ⅱ启动子转录的正调控、对药物的反应;结果中,细胞的组成(cellular component,CC)43 条,主要包括胞外区、细胞质、细胞外间隙;分子功能(molecular function,MF)的结果82条,主要包括蛋白质结合、转录因子结合、酶结合等。
京都基因和基因组数据库(Kyoto Encyclopedia of Genes and Genomes,KEGG)分析涉及信号通路109条(P<0.05),其中,肿瘤坏死因子(tumor necrosis factor,TNF)信号通路、Toll样受体信号通路、缺氧诱导因子1(hypoxia-inducible factor-1,HIF-1)信号通路、以磷脂酰肌醇 3-激酶/蛋白激酶 B(phosphatidylinositol 3 kinase-protein kinase B,PI3K-Akt)信号、核苷酸结合寡聚化结构域(nucleotide-binding oligomerization domain,NOD)样受体信号通路为参苓白术散异病同治的主要的“明星通路”。
2.6 分子对接
对接结果显示,分子与晶体均具有结合活性。其中α-丝氨酸/苏氨酸蛋白激酶(RAC-alpha serine/threonine-protein kinase,AKT)1与3种蛋白晶体均具有较好的对接活性,与槲皮素对接得分7.617,具有高度的对接活性。依据对接得分值绘制热图(图4),同时绘制AKT1与3种活性成分对接构象(图5)。
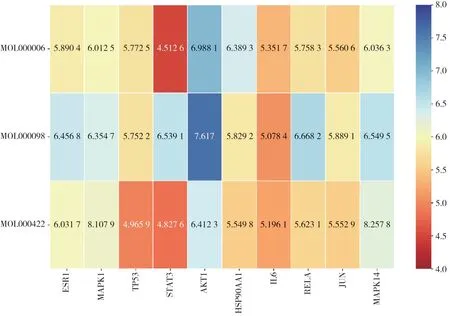
图4 对接得分值热图Fig.4 Docking scoring value heat map
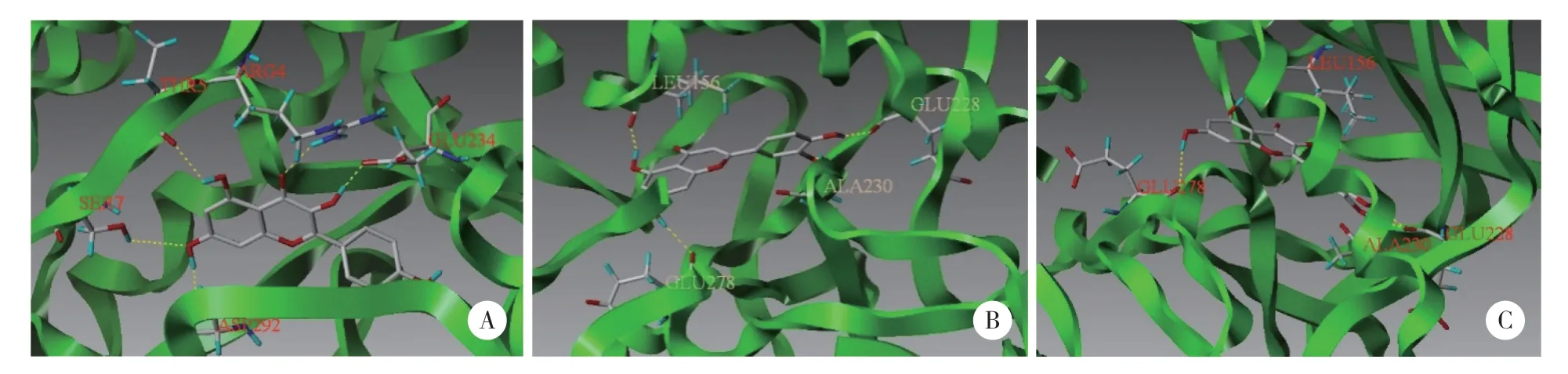
图5 AKT1与槲皮素、木犀草素、山奈酚对接构象Fig.5 Docking conformation of AKT1 with quercetin,luteolin and kaempferol
3 讨论
中医理论认为,CGN与抑郁症的共同发病机制在于脾失健运。参苓白术散作为补益脾胃的经典方剂,已被临床广泛应用。异病同治是中医辨证论治的基本特点之一,也是《黄帝内经》原文中“治病必求于本”的重要体现[18]。在古代医书中虽未记载CGN病名,但根据其症状,可从医家经典中发现一些线索。如《黄帝内经》中有“慢肾风”“风水”“水胀”等病名;《金匮要略》中也提到十一类水肿;这些疾病的临床表现与CGN类似[19-21]。脾虚是CGN的核心病机,正所谓“四季脾旺不受邪”[22]。脾失固摄则精微物质下泄,尿中出现蛋白等物质[23],脾虚则土不制水故出现水肿。海派名医童少伯从脾论治CGN,认为CGN病本在脾,脾在中焦调控肺肾两脏[24]。《黄帝内经》有云“脾在志为思”“思伤脾”,忧思过度则会伤及脾脏,脾的运化功能与西医消化系统相似,现代研究[25-26]表明肠道菌群可影响神经递质、HPA轴等,从而导致抑郁症。
槲皮素是参苓白术散中对应靶点最多的核心成分。已有研究[27-28]表明,槲皮素有抗炎、抗氧化、预防神经凋亡等作用,戴恩来等[29]研究表明槲皮素干预可修复足细胞损伤,进而保护肾小球滤过膜。华深等[30]通过对小鼠进行应激刺激并用槲皮素进行干预,阐明了槲皮素对抑郁症的治疗效果及机制。
本研究中,KEGG分析结果发现,参苓白术散作用于109个信号通路,其中TNF信号通路等5种信号通路相关性较高。TNF信号通路作为一种炎症信号通路,介导多种炎症反应,调控多种炎性细胞因子的表达,TNF信号通路及其下游白细胞介素-6等炎性细胞因子在抑郁症患者外周血中浓度增加[31],在肾组织中TNF信号通路及下游表达升高则会导致细胞因子失衡,进而增加CGN的疾病进展的风险[32]。Toll样受体可触发产生免疫复合物,与肾脏损伤有一定的联系[33]。研究[34]发现,慢性肾炎患者外周血淋巴细胞中,Toll样受体表达显著上调,引起炎症损伤。通过调控Toll样受体信号通路可修复神经损伤,达到抗抑郁的效果[35]。HIF-1和NOD样受体信号通路参与多种炎症反应,NOD样受体信号通路可以激活下游核因子κB信号通路[36],这些炎症反应均参与CGN和抑郁症发生和发展,调控上述2种信号通路在疾病抗炎治疗中起重要的作用。PI3K-AKT信号通路参与多种自身免疫性疾病,在多种慢性肾脏病中显著上调并参与炎症和增殖,且该通路与抑郁症的关系明确,多种抗抑郁药物通过该通路发挥作用,如文拉法辛可通过该通路抑制神经元凋亡[37],从而发挥抗抑郁的作用。
本研究通过2种技术对参苓白术散治疗CGN及抑郁症的作用机制进行了分析,与异病同治理论相对应。将参苓白术散治疗2种疾病的共同靶点构建PPI网络,发现10个核心靶点作用于RNA聚合酶Ⅱ启动子转录的正调控、DNA模板转录的正调节、对药物的反应等生物学过程,调节多种信号通路,继而调控CGN与抑郁症。分子对接结果显示,上述10个核心靶点与参苓白术散的主要活性成分都具有对接活性,也从侧面证明了参苓白术散主要是通过这些核心靶点对CGN及抑郁症发挥异病同治的作用。值得注意的是,AKT1与这3种活性成分都具有最高的对接得分。AKT1也是PI3K-AKT信号通路的重要组成部分,该通路也是参苓白术散异病同治过程中的“明星通路”,也从一定程度上反映了参苓白术散可以通过这些核心靶点发挥异病同治的作用。
综上所述,本研究在微观上证明了异病同治理论的可行性,丰富了其内涵。虽然应用网络药理学和分子对接的方法可以探究中药在CGN与抑郁症的作用机制,但其本身具有一定的局限性,因此,仍然需要进一步研究验证。
