硫酸根对聚合氮化碳光催化活性的影响
2022-09-17马炳香申云霞韦尧意
马炳香,申云霞,李 娜,李 敏,韦尧意,赵 宇
(1.中国海洋大学化学化工学院,山东青岛266100;2.烟台高新技术产业开发区环境执法大队)
当前环境问题日益突出,印染废水是造成严重水污染的工业废水之一,具有易致畸、易致癌、高毒性、高残留等多种危害[1]。合理利用太阳光在光催化剂作用下降解水中污染物是解决水污染问题的重要方法之一[2]。氮化碳因其相对中等的能带隙、合适的能带位置和化学稳定性,在光催化领域应用广泛[1,3]。然而,块状氮化碳由于光利用率低、光生电子-空穴对快速复合、比表面积小等因素,光催化活性较低[4]。为进一步提高氮化碳的可见光催化活性,研究人员采用元素掺杂[5]、与其他材料复合[6]、酸处理[7]等多种方法提高其光响应范围和抑制光生电子-空穴对复合,从而达到提高光催化活性的目的[8]。其中,用无机酸处理的氮化碳光催化活性有明显提升。
WANG等[9]通过将三聚氰胺在稀释的H2SO4溶液中经水热处理形成的前驱体进行煅烧,制备得到超薄2D氮化碳纳米片,其光催化产氢性能明显提升,产氢速率可达2 590 μmol(/h·g),是在相同条件下块状氮化碳的9.9倍。HUANG等[10]通过煅烧由H2SO4/甲醇重结晶合成的三聚氰胺前驱体,制备了高比表面积、高孔隙率以及低缺陷浓度的氮化碳纳米管,表现出增强的光催化析氢性能,产氢速率为5 236 μmol(/h·g)。TANG等[11]用H2SO4、HNO3、HCl预处理的类氢键有机骨架的三聚氰胺前驱体,在N2条件下煅烧得到了3种具有良好收集可见光和分离光生电子-空穴能力的氮化碳,H2SO4预处理的氮化碳具有最高的析氢速率,为81.01 μmol/h。上述文献都表明,H2SO4处理的氮化碳光催化效果明显增强,但是SO42-对氮化碳光催化活性的影响未见有进一步探讨。
笔者以罗丹明B(RhB)作为目标污染物,考察了聚合氮化碳对RhB的光催化降解性能,以此评价其光催化活性。以不含氧的HCl提供H+,在相同pH条件下比较了SO42-、NO3-、PO43-对三聚氰胺前驱体制备的聚合氮化碳光催化活性的影响,考察了SO42-的最佳用量、材料的稳定性以及光催化降解RhB的机理。
1 实验部分
1.1 试剂和仪器
试剂:三聚氰胺(C3H6N6)、盐酸(HCl)、硫酸钠(Na2SO4)、硝酸钠(NaNO3)、十二水合磷酸三钠(Na3PO4·12H2O)、罗丹明B(RhB,C28H31ClN2O3)、乙二胺四乙酸二钠(EDTA-2Na,C10H14N2Na2O8)、异丙醇(IPA,C3H8O)、对苯醌(BQ,C6H4O2),均为分析纯。
仪器:SX2-2.5-10NP型可程式电阻箱;300 W氙灯;UltimaⅣ型X射线衍射仪(XRD);TESCAN MIRA4型扫描电子显微镜(SEM);K-Alpha型X射线光电子能谱仪(XPS);ASAP 2460型比表面与孔隙度分析仪;U-4100型紫外-可见漫反射光谱仪(UVVis DRS);F-4600型荧光光谱仪(PL);UV 1880型紫外-可见分光光度计(UV-Vis)。
1.2 光催化剂制备
1.2.1 CN、CN-0.02SO42-、CN-0.02NO3-、CN-0.02PO43-的制备
取3 g三聚氰胺分散于250 mL去离子水中,搅拌加热到80℃至其完全溶解。分别加入0.06 mol的Na2SO4、NaNO3和Na3PO4·12H2O,再加入一定量1 mol/L的盐酸溶液调节pH为1。搅拌加热60 min后自然冷却12 h,有白色沉淀析出。将白色沉淀过滤收集,用去离子水洗涤多次,然后置于60℃烘箱中干燥24 h。
取2.5 g上述样品分别置于带盖的刚玉瓷舟中,在空气条件下在马弗炉中以2℃/min的速率加热至550℃,保温2 h后自然降温。将得到的样品分别标记为CN-0.02SO42-、CN-0.02NO3-、CN-0.02PO43-。取2.5 g三聚氰胺以相同的条件在马弗炉中煅烧得到CN样品。
1.2.2 Cl-CN、CN-xSO42(-x=0.01、0.04、0.06)的制备
在相同制备条件下分别加入0.00、0.03、0.12、0.18 mol的Na2SO4,得到不同SO42-含量的盐酸处理的三聚氰胺前驱体。取2.5 g上述样品在相同煅烧条件下分别得到Cl-CN、CN-0.01SO42-、CN-0.04SO42-、CN-0.06SO42-。
1.3 光催化实验
称取10 mg光催化剂加入50 mL质量浓度为10 mg/L的RhB溶液中,通入回流冷却水,使反应容器的温度维持在25℃左右。在光反应箱内在黑暗条件下搅拌30 min,使光催化剂在RhB溶液中达到吸附与脱附平衡。随后打开光源,用300 W氙灯(λ>420 nm)照射,间隔一定的时间取样。用高速离心机对3 mL的反应液离心分离,上清液用紫外-可见分光光度计测定553 nm处的吸光度,计算RhB的降解率。空白实验在相同条件下进行。对CN-0.04SO42-样品在相同条件下进行3次循环降解实验,将降解后的样品离心收集,用乙醇和去离子水多次洗涤,置于60℃烘箱中干燥后用于下一次降解实验。
1.4 活性物种捕获实验
以EDTA-2Na、IPA和BQ作为自由基捕获剂,分别检测空穴(h+)、羟基自由基(·OH)和超氧自由基(·O2-)。其他光催化实验条件不变,加入1 mmol/L自由基捕获剂后在可见光下对RhB进行降解实验。
2 结果与讨论
2.1 结构及形貌分析
2.1.1 XRD分析
图1为CN、Cl-CN、CN-0.02NO3-、CN-0.02PO43-的XRD谱图(a)以及CN-xSO42-(x=0.01、0.02、0.04、0.06)的XRD谱图(b)。从图1看出,所有样品的XRD谱图相似,这些样品在2θ为13.1°都存在一个弱的特征峰,对应氮化碳的(100)晶面,这是由3-s-三嗪环结构的面内排序导致的[12]。在2θ为27.6°左右存在明显的层间堆叠特征峰,对应氮化碳(002)晶面。XRD表征结果表明,这些样品都是氮化碳。相较于CN,其他样品的特征峰由2θ为27.3°移至27.6°,这表明层间距离减小,形成了更为紧实的层间堆积结构的聚合氮化碳[13]。

图1 CN、Cl-CN、CN-0.02NO3-、CN-0.02PO43-的XRD谱图(a);CN-xSO42-(x=0.01、0.02、0.04、0.06)的XRD谱图(b)Fig.1 XRD patterns of CN,Cl-CN,CN-0.02NO3-and CN-0.02PO43-(a);XRD patterns of CN-xSO42-(x=0.01,0.02,0.04,0.06)(b)
2.1.2 SEM分析
通过SEM观察了CN、Cl-CN、CN-0.04SO42-的形貌,结果见图2。从图2a看出,CN呈现层状堆叠的块状形貌,表面略粗糙,与文献报道的氮化碳典型结构特征相符[14]。从图2b~c看出,Cl-CN呈现不规则层状堆叠形状,表面较CN更为平滑。从图2d~f看出,引入SO42-经盐酸预处理的聚合氮化碳与CN、Cl-CN在形貌上有较大差别,CN-0.04SO42-呈现不规则块状形态,粒径约为30 μm,存在大量薄层褶皱;CN-0.04SO42-表面松散且凹凸不平,有明显的孔道存在。

图2 CN(a)、Cl-CN(b、c)、CN-0.04SO42-(d、e、f)的SEM照片Fig.2 SEM images of CN(a);Cl-CN(b,c);CN-0.04SO42(-d,e,f)
为进一步研究样品形貌的差异,对CN、Cl-CN、CN-0.04SO42-进行了比表面及孔隙度分析,结果见图3。从图3看出,3个样品的氮气吸附-脱附等温线均为Ⅳ型吸附等温线,表明3个样品均存在介孔;CN与Cl-CN的比表面积相差不大,而CN-0.04SO42-的比表面积明显高于CN、Cl-CN,具有较大的平均孔径。CN-0.04SO42-具有高比表面积和大的平均孔径,反应活性位点的数量多,有利于光催化反应[15]。

图3 CN、Cl-CN、CN-0.04SO42-的氮气吸附-脱附等温线(a)和孔径分布曲线(b)Fig.3 Adsorption isotherms(a)and pore diameter distribution curves(b)of CN,Cl-CN and CN-0.04SO42-
2.1.3 XPS分析
CN-0.04SO42-的XPS图见图4。从图4a看出,样品的主要元素为C、N、O。样品的全谱XPS图中没有S、Cl元素特征峰,可能是由于煅烧过程中样品存在大量损失,导致S、Cl的含量较低不能被检测出来。从图4b看出,288.02 eV处为一强窄峰,该特征峰来自于sp2杂化的C原子,主要是氮化碳骨架中的C—N=C[12];284.80 eV处为一弱宽峰,该特征峰可归于C—C或C=C[16]。从图4c看出,400.97 eV处为一弱宽峰,该特征峰来自于C—N—H的N原子[17];400.04 eV处为一弱宽峰,该特征峰被认为是与3个C原子相连的桥接N原子[18];398.54 eV处为一强窄峰,来自于3-s-三嗪环结构的C—N=C的sp2杂化的N原子[4,19]。XPS表征结果进一步证明CN-0.04SO42-是典型的氮化碳。通过测定样品的价带X射线光电子能谱(VB-XPS)(见图4d),得出CN-0.04SO42-的价带值(EVB-XPS)约为1.88 eV。CN-0.04SO42-相对于标准氢电极的价带值(EVB,NHE),可由以下公式计算:
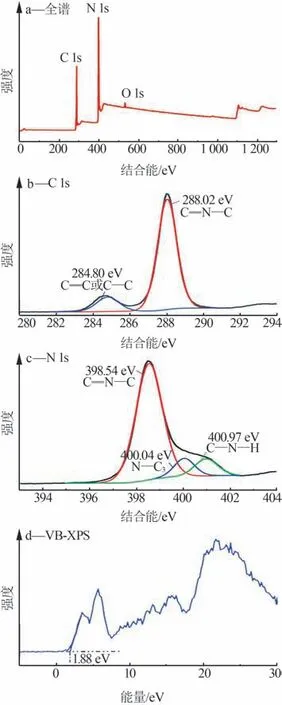
图4 CN-0.04SO42-的XPS图Fig.4 XPS spectra of CN-0.04SO42-
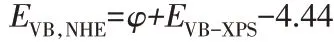
式中:φ为仪器的功函数(4.20 eV)[20]。经上式计算,CN-0.04SO4
2-的EVB,NHE为1.64 eV。
2.2 光催化活性分析
2.2.1 光催化降解RhB
在可见光照射下,用RhB作为污染物进行了光催化降解实验,结果见图5。从图5a看出,在无光催化剂时RhB的降解率为0.3%,降解率极低,可忽略不计;CN、Cl-CN对RhB的降解率分别为11.7%、14.4%。为考察不同酸根阴离子对聚合氮化碳光催化活性的影响,分别向三聚氰胺溶液中加入0.06 mol的Na2SO4、NaNO3、Na3PO4·12H2O,用盐酸提供H(+pH=1)形成不同的前躯体,高温煅烧后分别得到CN-0.02SO42-、CN-0.02NO3-、CN-0.02PO43-。它们对RhB的降解率分别是97.7%、18.7%、14.1%,伪一级动力学常数分别为0.049 0、0.004 6、0.002 8 min-1。它们的伪一级动力学常数分别是Cl-CN的14.4、1.35、0.82倍,酸根阴离子对聚合氮化碳光催化活性的影响从大到小的顺序依次为SO42-、NO3-、PO43-。SO42-、NO3-、PO43-均可通过氢键与三聚氰胺分子形成不同结构的前体,然而加入NO3-、PO43-得到的聚合氮化碳光催化活性比SO42-差,这可能是由于其前体中的氢键不利于缩聚过程,导致CN-0.02NO3-、CN-0.02PO43-的聚合度低[7,21]。
考察了SO42-用量对pH=1盐酸预处理聚合氮化碳光催化活性的影响,结果见图5b。从图5b看出,CN-0.01SO42-、CN-0.02SO42-、CN-0.04SO42-、CN-0.06SO42-在光照45 min后对RhB的降解率分别为74.9%、97.7%、99.1%、98.9%。CN-0.04SO42-的伪一级动力学常数高于其他氮化碳样品,为0.078 3 min-1,是Cl-CN的23.0倍,其光催化降解性能最好。CN-0.06SO42-和CN-0.04SO42-随时间变化的降解曲线相似,CN-0.06SO42-的伪一级动力学常数也与CN-0.04SO42-的数值接近,这说明二者的光催化降解性能基本相同。随着SO42-用量的逐渐增加,聚合氮化碳的光催化降解性能逐渐提高后趋于稳定。SO42-的引入使聚合氮化碳的光催化活性明显增强。SO42-与三聚氰胺分子通过氢键可以形成大而稳定的前体结构。随着SO42-用量增加,SO42-与三聚氰胺分子形成的氢键数量逐渐接近饱和,再增加SO42-的用量对前体结构的影响不大。聚合氮化碳的光催化活性随着SO42-用量的增加逐渐提高后趋于稳定。煅烧过程中前体中的SO42-受热会生成SO2等气体逸出,使得到的聚合氮化碳具有高的比表面积[7]。CN-0.04SO42-的比表面积是Cl-CN的8.4倍左右,表现出较强的光催化活性,很好地证明了这一点。
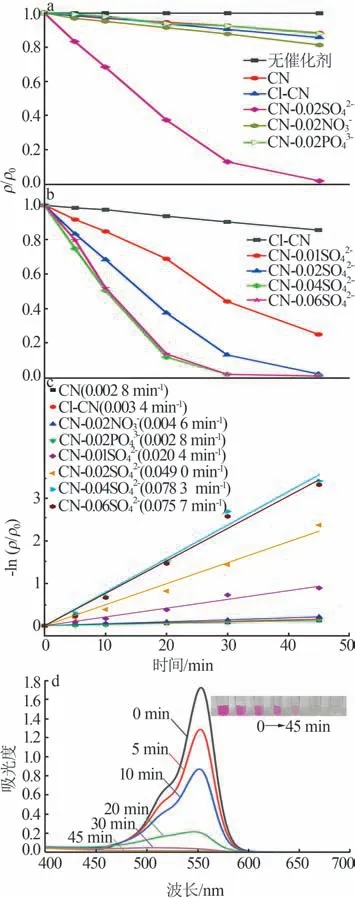
图5 无催化剂、CN、Cl-CN、CN-0.02SO42-、CN-0.02NO3-、CN-0.02PO43-光催化降解RhB曲线图(a);Cl-CN和CN-xSO42-(x=0.01、0.02、0.04、0.06)光催化降解RhB曲线图(b);所有样品伪一级动力学曲线(c);CN-0.04SO42-降解RhB的UV-Vis图(d)Fig.5 Photocatalytic degradation curves of RhB by catalystfree,CN,Cl-CN,CN-0.02SO42-,CN-0.02NO3-and CN-0.02PO43-(a);The photocatalytic degradation curves of RhB by Cl-CN and CN-xSO42-(x=0.01,0.02,0.04 or 0.06)(b);Pseudo first order kinetic curves for all samples(c);UV-Vis absorption curves of RhB degradation by CN-0.04SO42-(d)
图5d为CN-0.04SO42-在可见光下降解RhB的UV-Vis图。当加入CN-0.04SO42-进行可见光照射后,RhB溶液在553 nm处的吸光度迅速下降,紫外-可见吸收曲线整体也表现为下降趋势,反应溶液由粉红色逐渐变浅至无色,这表明CN-0.04SO42-对RhB具有优异的光催化降解作用。RhB溶液的最大吸收峰发生蓝移,这可能是RhB经历了脱N-乙基基团产生反应中间体造成的[22]。
2.2.2 光催化剂的稳定性
图6a为CN-0.04SO42-循环降解RhB曲线图。CN-0.04SO42-进行了3次循环降解RhB实验,光照30 min后CN-0.04SO42-对RhB的3次降解率分别为98.0%、85.6%、84.2%,光催化剂的降解性能有所下降。这极有可能是CN-0.04SO42-回收时有质量损失,以及RhB分子与CN-0.04SO42-存在吸附作用不能完全被洗脱干净,占据了部分反应活性位点,从而导致CN-0.04SO42-对RhB的降解率下降。图6b为CN-0.04SO42-循环实验前后的XRD谱图。从图6b看出,CN-0.04SO42-循环前后的XRD谱图基本一致,保持了原有的晶型结构,进一步说明了其具有高稳定性。
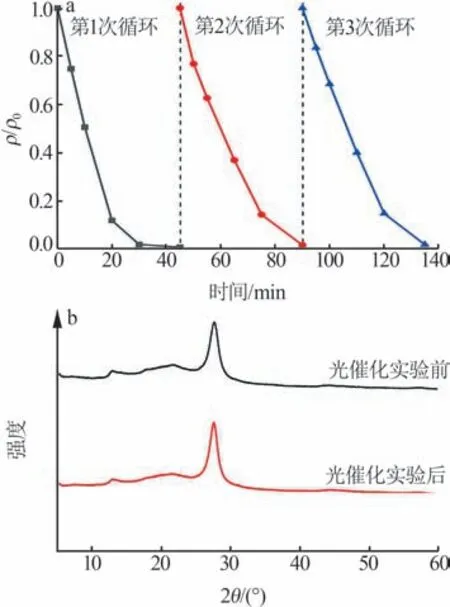
图6 CN-0.04SO42-循环降解RhB曲线图(a);CN-0.04SO42-循环实验前后XRD谱图(b)Fig.6 Cyclic degradation curves of RhB by CN-0.04SO42-(a);XRD patterns before and after cyclic experiments of CN-0.04SO42-(b)
2.3 光学性质分析
2.3.1 PL分析
图7为Cl-CN、CN-xSO42-(x=0.01、0.02、0.04、0.06)的PL光谱图。Cl-CN在445 nm处出现最强峰,CN-xSO42-在450 nm处出现最强峰,存在轻微红移。CN-xSO42-的PL光谱强度均弱于Cl-CN的光谱强度,特别是CN-0.04SO42-的强度最弱,表明该样品具有最低的光生载流子复合率。光生载流子能够在CN-0.04SO42-表面或内部快速迁移,SO42-的引入降低了光生电子与空穴的复合率,提高了电荷利用率,从而增强了光催化活性[12]。

图7 Cl-CN、CN-xSO42-(x=0.01、0.02、0.04、0.06)的PL光谱图Fig.7 Photoluminescence spectra of Cl-CN and CN-xSO42-(x=0.01,0.02,0.04,0.06)
2.3.2 UV-Vis DRS分析
通过UV-Vis DRS表征研究了SO42-的引入对聚合氮化碳光学特征的影响,结果见图8。从图8a可知,Cl-CN和CN-0.04SO42-从紫外光区到可见光区均有良好的吸光度,Cl-CN和CN-0.04SO42-的最大吸收波长分别约为462 nm和473 nm。在420~700 nm处CN-0.04SO42-的吸收值明显大于Cl-CN。SO42-的引入极大地拓宽了吸光范围并提高了吸光强度,这有利于光生电子和空穴的产生,也是光催化剂活性提高的原因之一[9]。图8b为Cl-CN和CN-0.04SO42-的(αhv)1/2-Eg曲线(Tauc plot方法)。从图8b看出,Cl-CN和CN-0.04SO42-的Eg分别为2.68 eV和2.62 eV。CN-0.04SO42-的禁带宽度比Cl-CN少0.06 eV,禁带宽度减少更有利于光催化剂对光的吸收。

图8 Cl-CN和CN-0.04SO42-的UV-Vis DRS(a)、(αhv)1/2-Eg图(Tauc plot方法)(b)Fig.8 UV-Vis DRS(a)and(αhv)1/2-Eg diagram(Tauc plot method)(b)of Cl-CN and CN-0.04SO42-
3 光催化机理研究
图9a为CN-0.04SO42-作为光催化剂时加入不同自由基捕获剂在光照20 min后对RhB的降解率。在没有添加自由基捕获剂时,CN-0.04SO42-对RhB的降解率为88.1%。当加入EDTA-2Na时,RhB的降解率有所提升,为95.3%,说明h+不是主要的反应物种,EDTA-2Na在抑制h+的同时可以提高电子-空穴对的分离率,从而加速了光催化降解[23];当加入IPA时,RhB降解率下降到41.5%;当加入BQ时,RhB降解率下降到24.1%。因此,影响CN-0.04SO42-光催化活性的主要活性物种是·O2-和·OH,影响程度从大到小的顺序依次为·O2-、·OH、h+。
CN-0.04SO42-的EVB,NHE为1.64 eV,小 于OH-/·OH的标准氧化还原电位(1.99 eV),CN-0.04SO42-产生的空穴(h+)不能氧化水中的OH-。结合活性物种捕获实验结果,光催化降解RhB的机理可能如图9b所示:CN-0.04SO42-的ECB为-0.98 eV,比O2/·O2-的标准氧化还原电位(-0.33 eV)更负,反应溶液中溶解氧可捕获电子(e-)发生还原反应得到·O2-[24]。部分·O2-可以直接氧化RhB分子,部分·O2-也可与H2O或H+进一步反应得到·OH[22]。·OH也具有强氧化性,可以氧化RhB分子。

图9 光照20 min时不同自由剂捕获剂对CN-0.04SO42-光催化降解RhB的影响(a);CN-0.04SO42-光催化降解RhB的机理示意图(b)Fig.9 Effect of different inhibitors on photocatalytic degradation of CN-0.04SO42-by illumination at 20 min(a);Mechanism diagram of CN-0.04SO42-photocatalytic degradation of RhB(b)
4 结论
通过高温煅烧分别加入SO42-、NO3-、PO43-的盐酸处理的三聚氰胺前体,得到了一系列聚合氮化碳,光催化活性影响程度从大到小的顺序依次为SO42-、NO3-、PO43-。SO42-能有效增强聚合氮化碳的光催化活性,随着SO42-用量的逐渐增加,聚合氮化碳的光催化活性逐渐提高后趋于稳定。CN-0.04SO42-的光催化降解速率最高,在45 min内对RhB的降解率可以达到99.1%,其伪一级动力学常数是Cl-CN的23.0倍。SO42-的引入降低了光生电子-空穴对的复合率,拓宽了吸光范围,提高了吸光强度。CN-0.04SO42-具有良好的稳定性,经过3次循环实验对RhB的降解率略有下降,晶型结构基本不变。·O2-和·OH是影响CN-0.04SO42-光催化降解RhB的主要活性物种。
