右美托咪定联用氢吗啡酮对癌性爆发痛的镇痛效果及安全性
2022-09-17潘燕萍王振红
潘燕萍 王 樱 王振红
1.江苏省人民医院溧阳分院麻醉科,江苏溧阳 213300;2.南京市第一医院麻醉科,江苏南京 210000
癌性爆发痛(breakthrough cancer pain,BTcP)专家共识中指出,80%的癌症患者在诊疗过程中均会出现癌性疼痛,其中BTcP 占比高达33%~95%[1]。BTcP 具有不可预测、机制复杂、药物治疗滞后的特点,导致治疗依从性、生活质量下降[2]。口服即释吗啡片是指南提出的最基础的爆发痛解救方法,但口服治疗往往无法及时起效,因此镇痛作用欠佳[3]。氢吗啡酮属于强效阿片类药物,镇痛作用明显,且代谢产物无活性,不良反应轻微[4];而右美托咪定是α2 肾上腺素受体激动剂,能通过激动交感神经末梢与脊髓α2 受体发挥镇痛镇静作用[5]。自控镇痛技术多用于术后急性疼痛的控制,相关研究表明,自控镇痛技术在癌症顽固性癌痛[6]、难治性疼痛[7]中均有一定的镇痛效果。因此,本研究旨在探讨右美托咪定联用氢吗啡酮的镇痛效果及安全性。
1 资料与方法
1.1 一般资料
选取2020 年2 月至2021 年2 月江苏省人民医院溧阳分院(以下简称“我院”)BTcP 患者96 例,按照随机数字表法将其分为对照组、观察组,各48 例。两组一般资料比较,差异无统计学意义(P >0.05),具有可比性,见表1。本研究经我院医学伦理委员会批准(批号:2020-ycj23-002)。
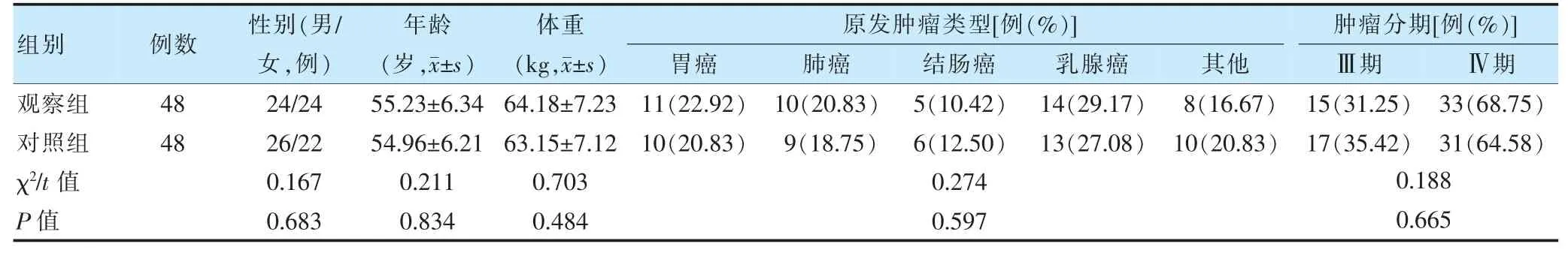
表1 两组一般资料比较
1.2 纳入及排除标准
纳入标准:符合《癌性爆发痛专家共识(2019 年版)》[1]中BTcP 的诊断标准;经病理学明确诊断为中晚期恶性肿瘤;过去1 周内存在持续性疼痛,且得到充分控制[数字评分法(numerical rating scale,NRS)[8]≤3 分],且存在短暂性疼痛加重现象(NRS 评分≥4 分);预计生存期>3 个月;同意采用皮下注射自控镇痛,且理解该方法的优势与风险;签署知情同意书。排除标准:合并心肝肾等重要脏器功能性障碍;合并感染性疾病;对本研究药物过敏或合并严重过敏性疾病;精神或意识障碍无法判定自身疼痛或自行操作镇痛泵;近4 周内参加过其他临床试验;体重指数≤18 kg/m2或≥30 kg/m2;有药物滥用史。
1.3 镇痛方法
两组均给予基础镇痛药物,口服盐酸吗啡片(青海制药厂有限公司,生产批号:1210802),5 mg/次,3 次/d,若24 h 内BTcP 次数>3 次,则增加基础镇痛药物剂量为10 mg/次。观察组常规静脉留置针于上肢内侧皮下部位,采用透明敷贴进行妥善固定,外接电子输液泵(河南驼人医疗器械集团有限公司,型号:TR-1-275),采用右美托咪定(江苏恒瑞医药股份有限公司,生产批号:21080431)联合氢吗啡酮(宜昌人福药业有限责任公司,生产批号:13A12011),其中右美托咪定剂量为2 μg/kg,氢吗啡酮剂量为0.1 mg/kg,用氯化钠注射液稀释至100 ml,自控按压每次0.5 ml,锁定时间为15 min,背景剂量为0。对照组采用氢吗啡酮,剂量为0.1 mg/kg,其余同观察组。若自控镇痛后患者仍主诉疼痛,且NRS 评分>4 分,则静脉注射氢吗啡酮0.01 mg/kg 进行补救镇痛。每日观察两组局部皮肤状态,若出现红肿、水肿、留置针堵塞等情况,应及时更换留置针与注射部位。治疗7 d 后评估镇痛效果。
1.4 观察指标
1.4.1 镇痛效果 比较两组镇痛效果,包括治疗7 d 内BTcP 发作次数、药物起效时间、药物作用时间、自控氢吗啡酮用量、补救镇痛用量、基线NRS 评分、BTcP发作时NRS 评分及疼痛程度。其中药物起效时间是指BTcP 到疼痛缓解的时间,药物作用时间指疼痛缓解的持续时间,NRS 评分总分0~10 分,0 分为无痛,1~3 分为轻度疼痛,4~6 分为中度疼痛,7~10 分为重度疼痛[8]。
1.4.2 睡眠质量及生活质量 比较两组治疗前、治疗7 d 后睡眠质量及生活质量。睡眠质量采用阿森斯失眠量表(Athens insomnia scale,AIS)评估,总分0~24 分,分数越高睡眠质量越差[9];生活质量采用Spitzer 生活质量指数(Spitzer quality of life index,SQOL)评估,总分0~10 分,分数越高生活质量越好[10]。
1.4.3 不良反应 比较两组治疗期间不良反应的发生情况,包括嗜睡、幻觉、瘙痒、恶心呕吐、小便困难、血压异常。
1.4.4 镇痛满意度 采用自制调查问卷方式调查患者对镇痛治疗的满意度,本问卷分为非常满意、满意、不满意,Cronbach’s α 系数为0.94,效度系数为0.86。
1.5 统计学方法
采用SPSS 22.0 软件进行数据分析,计量资料用均数±标准差()表示,组间比较采用t 检验;计数资料用例数或百分率表示,组间比较采用χ2检验;等级资料采用秩和检验。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组镇痛效果比较
两组BTcP 发作次数、基线NRS 评分比较,差异无统计学意义(P >0.05)。观察组药物起效时间短于对照组,药物作用时间长于对照组,自控氢吗啡酮用量及补救镇痛用量小于对照组,BTcP 发作时NRS 评分及疼痛程度低于对照组(P <0.05)。见表2。
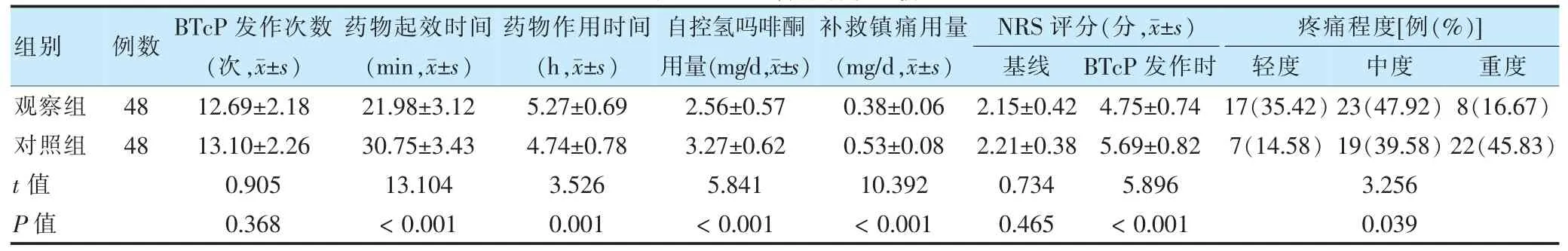
表2 两组镇痛效果比较
2.2 两组治疗前后AIS、SQOL 评分比较
治疗前,两组AIS、SQOL 评分比较,差异无统计学意义(P >0.05);治疗7 d 后,两组AIS 评分低于治疗前,SQOL 评分高于治疗前,且观察组AIS 评分低于对照组,SQOL 评分高于对照组(P <0.05)。见表3。
表3 两组治疗前后AIS、SQOL 评分比较(分,)
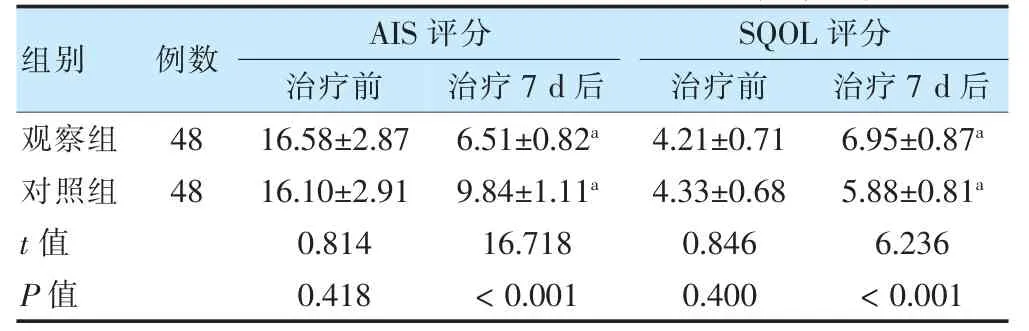
表3 两组治疗前后AIS、SQOL 评分比较(分,)
注 与同组治疗前比较,aP <0.05。AIS:阿森斯失眠量表;SQOL:Spitzer 生活质量指数
2.3 两组不良反应总发生率比较
两组不良反应总发生率比较,差异无统计学意义(P >0.05)。见表4。
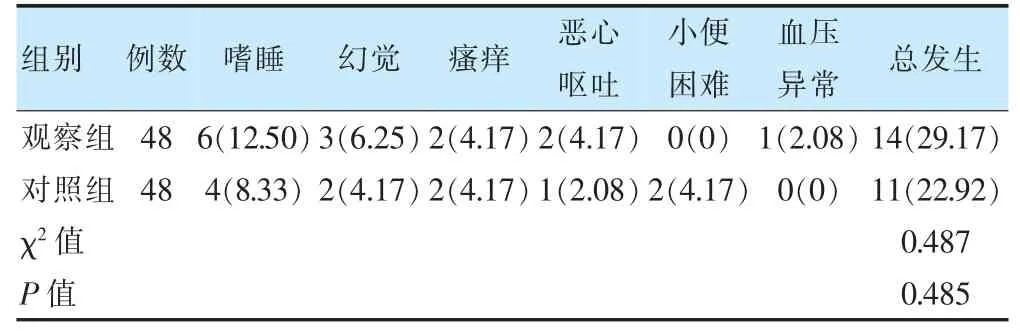
表4 两组不良反应总发生率比较[例(%)]
2.4 两组镇痛满意度比较
观察组镇痛满意度优于对照组(P <0.05)。见表5。
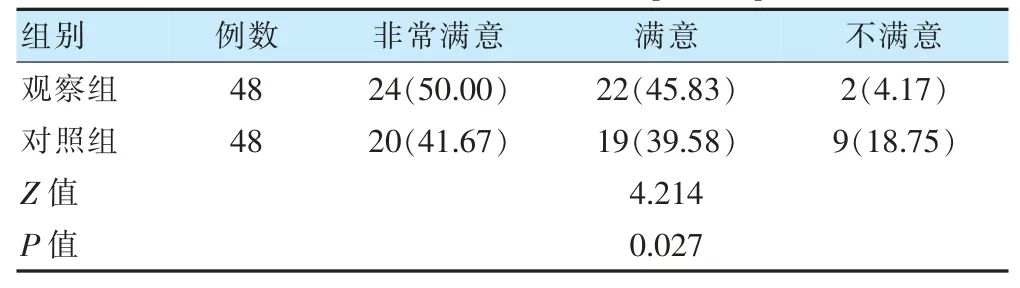
表5 两组镇痛满意度比较[例(%)]
3 讨论
BTcP 是晚期癌症患者突然出现的剧烈疼痛,国内多采用即释吗啡作为其解救药物,但口服起效时间为30~45 min,期间患者需忍受长时间的疼痛,因此其并非最佳治疗措施[11-12]。临床应积极探索新的解救方式提高镇痛效果。
自控镇痛技术出现近20 年,且多用于术后急性疼痛的控制,能够在医师的监控管理下,由患者自行控制镇痛药物的使用,缩短疼痛出现至控制时间,是个体化镇痛治疗的典型手段[13-14]。朱海萌等[15]研究显示,右美托咪定联合吗啡皮下注射自控镇痛用于BTcP 能快速缓解疼痛。而氢吗啡酮是吗啡的半合成衍生物,镇痛效果是吗啡的5~8 倍[16]。因此,本研究尝试以右美托咪定联合氢吗啡酮采用自控镇痛技术进行镇痛解救,结果显示观察组药物起效时间短于对照组,药物作用时间长于对照组,自控氢吗啡酮用量及补救镇痛用量小于对照组,BTcP 发作时NRS 评分低于对照组。提示二者联合应用于BTcP 能快速明显减轻疼痛,且持续时间更长。分析其原因为:右美托咪定能作用于脊髓背角的α2 肾上腺素能受体,阻止疼痛递质与疼痛信号的传递,与阿片类药物联合应用能发挥协同作用,增强其镇痛作用,缩短BTcP 缓解时间,减轻发作时疼痛强度[17-19]。同时,BTcP 患者由于无法预测的剧烈疼痛,必然会降低睡眠质量,影响日常生活[20-21]。本研究结果显示,治疗7 d 后,两组AIS 评分低于治疗前,SQOL 评分高于治疗前,且观察组AIS 评分低于对照组,SQOL 评分高于对照组。右美托咪定联用氢吗啡酮能明显增强镇痛效果,为睡眠质量提供一定保障,最低程度地影响日常生活,有助于生活质量的提升[22-24]。另外,两组不良反应总发生率比较,差异无统计学意义(P >0.05),提示右美托咪定联用氢吗啡酮不会增加不良反应的发生,具有一定安全性。基于上述研究结果,二者联合能通过提高镇痛效果,改善睡眠质量,且无明显嗜睡、恶心呕吐、瘙痒等不良反应出现,从而保证高护理满意度,也证实了本研究结果观察组镇痛满意度优于对照组的可信性。但本研究尚存在一定的不足之处,一是样本量有限;二是右美托咪定联用氢吗啡酮的最佳剂量尚不明确,临床需进一步扩大样本量、调整实验剂量进行深入分析与研究[25]。
综上所述,右美托咪定联合氢吗啡酮用于BTcP镇痛效果明显,能减轻疼痛程度,缩短缓解时间,提高睡眠质量与生活质量,不会增加不良反应的发生,患者镇痛满意度高,值得临床推广。
