均相催化湿式氧化技术对实际高浓有机废水处理研究
2022-09-16郑搏英丁鹏佳刘宏雁
郑搏英,路 青,丁鹏佳,刘宏雁
(河北海鹰环境安全科技股份有限公司,河北 石家庄 050001)
0 引 言
近年来,随着国民经济的快速提高,带动了石油、化工、焦化、制药、农药、造纸、食品等行业的高速发展,同时含有高浓度难生化降解有机污染废水以及高氨氮废水的排放量也不断增加,这一问题越来越引起社会各界和政府环保部门的重视。高浓度有机废水具有有机污染物浓度高、毒性强、难以生物降解、排放点分散、水量少、处理工艺复杂、投资和运行成本高及管理难等特点,同时其又是引发水体严重污染、生态环境恶化、威胁人体健康的主要污染物。由于常规的物理化学和生化处理方法难以或无法满足对此类废水净化处理的技术及经济要求,因此,难降解高浓度有机工业废水的高效处理技术,成为国内现阶段环境保护水处理技术领域亟待解决的一个难题。
湿式催化氧化法(catalytic wet air oxidation),又称CWAO技术,是指在高温(200~280℃)、高压(2~8 MPa)反应环境下,以富氧气体或氧气为氧化剂,利用催化剂的催化作用,降低反应的活化能,加快废水中有机物与氧化剂间的反应,使废水中的有机物快速氧化成CO2、N2、H2O及其它易降解的小分子有机物,达到净化的目的。对高COD或含生物难降解化合物的各种工业有机废水,COD及氨氮去除率最高可达到99%以上,不再需要进行后处理,只经一次处理即可达排放标准。
其中催化剂的加入,在不降低处理效果的情况下,可降低反应的温度和压力,提高氧化分解的能力,缩短反应的时间,提高反应效率,并能有效降低成本。用于湿式氧化处理的催化剂可分为均相催化剂和非均相催化剂两种。均相湿式氧化催化剂主要为可溶性的过渡金属盐类,以溶解离子的形式混合在废水中使用。最常用的和效果较为理想的是铜盐和Fenton试剂。常用的金属盐有FeSO4、CuSO4、Cu(NO3)2、CuCl2、MnSO4、Ni(NO3)2等。缺点是易于流失,存在二次污染问题,需对出水中的催化剂进行回收,由此增加了工艺的复杂化并提高了投资和运行成本。非均相催化剂容易和水分离,能有效控制催化剂组分的流失及带来的二次污染问题。其活性组分通常有铜、锰、铁、钴、镍、钌、铑、钯、铱、铂、金、铈、银等,可以是其中的一种金属或金属氧化物,也可以由多种金属、金属氧化物或复合氧化物所组成。缺点是催化剂原材料成本较高,制备工艺较复杂,使用过程中存在催化剂中毒失活问题,一定程度上限制了其应用范围。
湿式催化氧化技术在实际应用中,将污水通过贮存罐由高压泵打入热交换器,与反应后的高温氧化液体换热,使温度上升到接近于反应温度后进入反应器。反应所需的氧由压缩机打入反应器。在反应器内,污水中的有机物与氧发生放热反应。在较高温度下将污水中的有机物氧化成二氧化碳和水,或小分子有机酸等中间产物。反应后气液混合物经分离器分离,液相经热交换器预热进料,回收热能。高温高压的尾气首先通过再沸器产生蒸汽或经热交换器预热锅炉进水。其冷凝水由第二分离器分离后通过循环泵再打入反应器,分离后的高压尾气可产生机械能或电能。湿式催化氧化技术具有净化效率高、二次污染少、处理范围广、经济效益高等优点,是难降解工业废水处理技术领域前沿技术之一。目前,该技术已在国内外大量工业项目中得到有效应用,并达到明显稳定的处理效果。
本文中采用均相催化湿式氧化技术,针对3种不同领域的实际高浓度难降解有机工业废水进行处理,实验结果表明,针对3类高浓有机废水该技术均得到了明显的处理效果,具有较好的工程应用可行性及潜在价值。
1 实验部分
1.1 实验材料
盐酸分析纯,西陇化工股份有限公司。
硫酸分析纯,西陇化工股份有限公司。
氢氧化钠分析纯,天津市大茂化学试剂厂。
自配催化剂。
垃圾渗滤液浓水,江苏某公司。
环己二酮废水,浙江某公司。
丙烯酸废水,江苏某公司。
1.2 实验设备
电子分析天平,GL224-1SCN赛多利斯科学仪器有限公司。
pH计,FE-28梅特勒托利多仪器有限公司。COD快速消解测试仪,连华科技。
总有机碳检测仪,岛津公司TOC-LCPN型测试仪。
高压反应釜,自设计定制。
1.3 实验水质信息
实验所用实际工业废水各指标检测结果见表1。
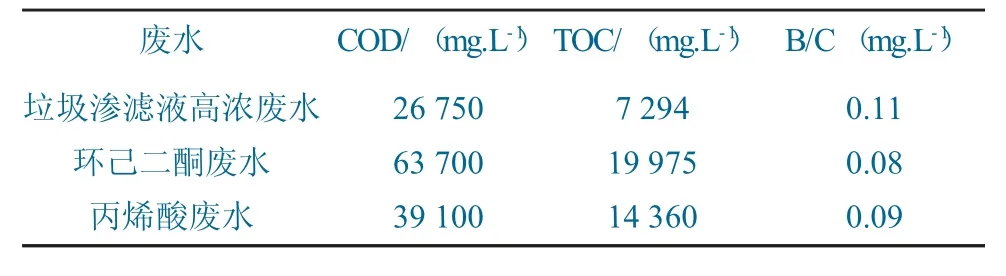
表1 废水水质信息表Table 1 Wastewater information
1.4 实验方法
将高压反应釜反复清洗干净,取固定量废水,用硫酸或氢氧化钠调节废水pH,加入固定量自配催化剂,搅拌均匀后倒入反应釜,上紧并通入氧气至固定气压以检查气密性,维持特定时间后确认气密性良好,调整出气背压阀,确保密封严密后开启搅拌,转速200~300 r/min,设定升温程序,套上加热套开始缓慢升温,升温速度低于5℃/min,达到预设反应温度后打开进气阀门,按照预设好的气体质量流量计控制进气流量,开始反应达到固定时间。反应结束后停止加热,关闭气路阀门,自然冷却至室温,缓慢开启反应釜通气阀门,至内外气压平衡后,开釜取样并检测特定指标,实验结束。
2 结果与讨论
2.1 反应温度对实验效果的影响
针对3种废水,分别考察不同反应温度条件下的处理效果。设定反应时间2 h,催化剂用量500 mg/L,进气量1.2倍,反应温度240~270℃,3种实际工业废水在不同反应温度下处理出水COD和TOC,反应温度对COD和TOC影响如图1所示。
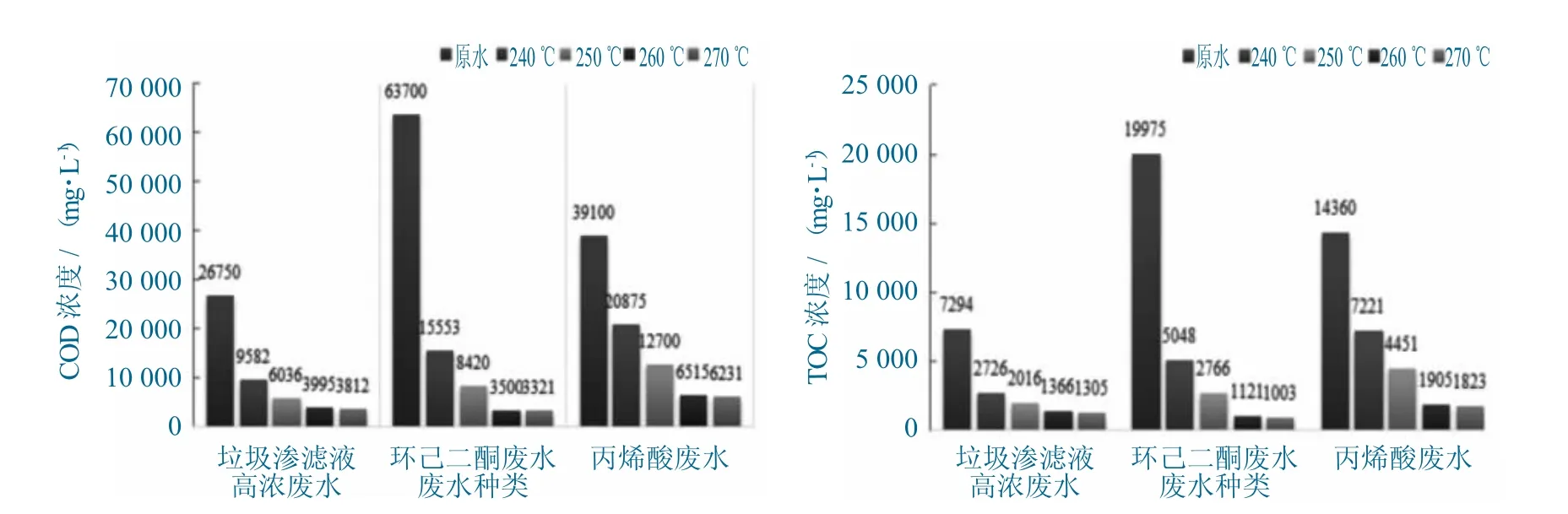
图1 反应温度对COD和TOC影响Fig.1 Effect of reaction temperature on COD and TOC
3种实际工业废水在不同反应温度下处理出水COD和TOC,反应温度对COD和TOC去除率影响如图2所示。

图2 反应温度对COD和TOC去除率影响Fig.2 Effect of reaction temperature on COD and TOC removal rate
由以上数据可知,在均相催化湿式氧化实验反应过程中,通过单因素实验考察,其他反应条件固定情况下,在一定范围内,随着反应温度的提升,3种实际工业废水水质指标COD和TOC去除率均呈现不同趋势的升高。在240℃下,整体处理效果一般,COD和TOC去除率均很低,分析原因为过低的反应温度条件下,体系内活化分子数量相对较少,反应物分子运动速率相对偏低,与氧化剂分子有效碰撞几率较小,未能达到最佳的反应状态。随着反应温度逐渐提升,反应体系中活化分子数量剧烈增多,分子运动速率加剧,氧化反应效率明显提升,对应的COD和TOC去除率也相应逐渐升高。当反应温度达到260~270℃时,COD和TOC去除率基本达到最高并趋于平稳。然而随着反应温度的升高,势必会带来反应器压力的大幅提高,这将导致反应过程的能耗明显增加,因此反应温度不宜选择过高。考虑反应过程中设备材质要求和能耗因素,根据实验结果,确定最佳反应温度为260℃。
2.2 反应时间对实验效果的影响
反应时间直接关系到实际处理过程中每天的废水处理量,而反应时间的判定须根据实际废水污染物的种类、浓度进行针对性试验确定。针对3种实际工业废水的处理情况要求及处理效果,设定反应时间1~3 h,催化剂用量500 mg/L,进气量1.2倍,反应温度260℃,3种实际工业废水在不同反应时间下处理出水COD和TOC,反应时间对COD和TOC影响如图3所示。

图3 反应时间对COD和TOC影响Fig.3 Effect of reaction time on COD and TOC
3种实际工业废水在不同反应时间下处理出水COD和TOC,反应时间对COD和TOC去除率影响如图4所示。
图4 反应时间对COD和TOC去除率影响Fig.4 Effect of reaction time on COD and TOC removal rate
由以上数据可知,在均相催化湿式氧化实验反应过程中,通过单因素实验考察,其他反应条件固定情况下,在一定范围内,随着反应时间的延长,3种实际工业废水水质指标COD和TOC去除率变化趋势相同,均呈现不同程度的升高。分析原因为当反应时间延长时,可有效增加体系内分子间有效碰撞的频次,延长有机物和氧化剂分子间反应作用的时长,促进氧化反应的有效进行,从而提高有机物去除效率。当反应时间达到2 h以上时,体系内有机污染物氧化程度达到峰值,COD和TOC去除率变化幅度已经很低,趋于稳定,考虑实际处理情况和处理效果要求,根据实验结果,确定最佳反应时间为2 h。
2.3 氧气量对实验效果的影响
氧气量的高低,直接影响着废水中有机污染物能否有效最大化氧化去除,同时关乎到实际应用过程中用量成本。针对3种实际工业废水,设定反应时间2 h,催化剂用量500 mg/L,进气量1~1.3倍,反应温度260℃,3种实际工业废水在不同氧气通气量条件下处理出水COD和TOC,氧气量对COD和TOC影响如图5所示。

图5 氧气量对COD和TOC影响Fig.5 Effect of oxygen on COD and TOC
3种实际工业废水在不同氧气通气量条件下处理出水COD和TOC,氧气量对COD和TOC去除率影响如图6所示。
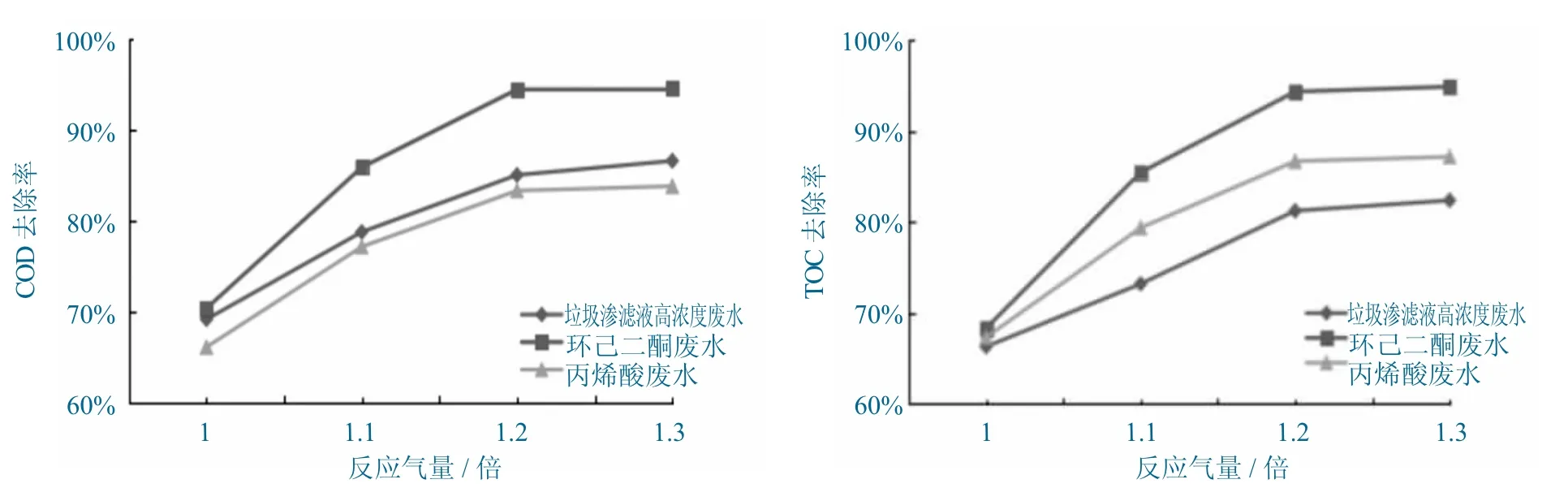
图6 氧气量对COD和TOC去除率影响Fig.6 Effect of oxygen on COD and TOC removal rate
由以上数据可知,在均相催化湿式氧化实验反应过程中,通过单因素实验考察,其他反应条件固定情况下,在一定范围内,随着通入反应体系内氧气量的增加,3种实际工业废水水质指标COD和TOC去除率变化趋势规律基本相近,均呈现不同程度的升高。分析原因为当通入反应系统的氧气量增大时,特定的空间内有机污染物分子和氧化剂分子碰撞频次增多,相互作用反应效率提高,从而实现有机物氧化效率的增大。当氧气量控制在理论用量的1.2~1.3倍下,对应的去除率变化已趋于平稳,考虑实际的处理要求及实际工程应用过程中的成本问题,根据实验结果,确定最佳实际进气量为理论用量的1.2倍即可。
2.4 催化剂用量对实验效果的影响
催化剂用量是保证废水在处理过程中达到最大化氧化的先决条件,且实际应用过程中按照废水的特定情况进行针对性的实验考察。针对3种实际工业废水,设定反应时间2 h,催化剂用量为100~700 mg/L,进气量1.2倍,反应温度260℃,3种实际工业废水在不同催化剂用量条件下处理出水COD和TOC,催化剂用量对COD和TOC影响如图7所示。
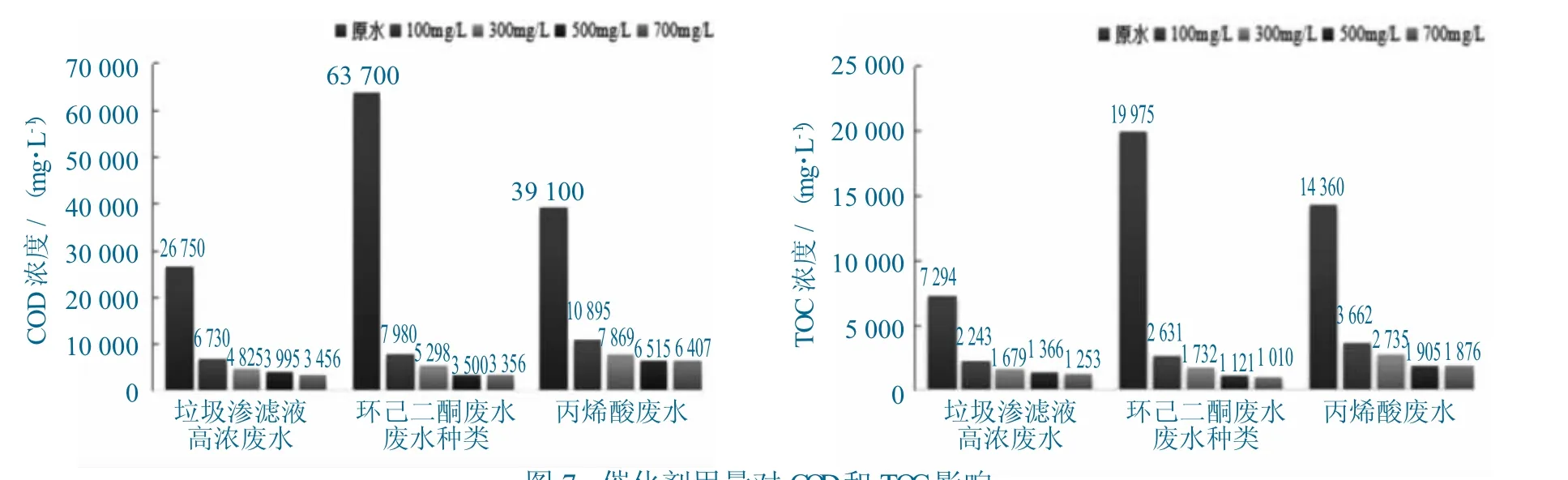
图7 催化剂用量对COD和TOC影响Fig.7 Effect of catalyst dosage on COD and TOC
由图7可知,在均相催化湿式氧化实验反应过程中,通过单因素实验考察,其他反应条件固定情况下,在一定范围内,随着体系催化剂用量的提高,3种实际工业废水水质指标COD和TOC去除率变化趋势规律大致相近,均随着催化剂量的增加而不断升高。分析原因为,较高的催化剂投加量可有效加大促进反应物分子自由基的生成,促进自由基和反应物分子之间的相互作用,加大自由基之间的相互碰撞,从而较好的降低反应所需的活化能,增大体系内有机物污染物的氧化效率,实现体系内有机物的深度最大化去除。同时因催化剂成本较高,考虑实际的处理效果要求及实际工程应用过程中原料成本等因素,根据实验结果,确定催化剂最佳用量为500 mg/L。
3种实际工业废水在不同催化剂用量条件下处理出水COD和TOC,催化剂用量对COD和TOC去除率影响如图8所示。

图8 催化剂用量对COD和TOC去除率影响Fig.8 Effect of catalyst dosage on COD and TOC removal rate
2.5 小 结
针对以上3类实际工业废水进行针对性催化湿式氧化实验处理后,确定大多数废水的最佳处理工艺条件为反应温度260℃,反应时间2 h,氧气量为理论用量的1.2倍,催化剂用量500 mg/L。在此反应条件下,其中垃圾渗滤液高浓废水和丙烯酸废水的COD和TOC去除率均达到80%以上,环己二酮废水的COD和TOC去除率达到90%以上,出水可生化性明显改善,处理效果明显。其他领域内的废水处理条件需根据特定水质性质、实际处理效果、实际工程要求及成本要求综合进行实验确认。处理后出水水质效果见表2。
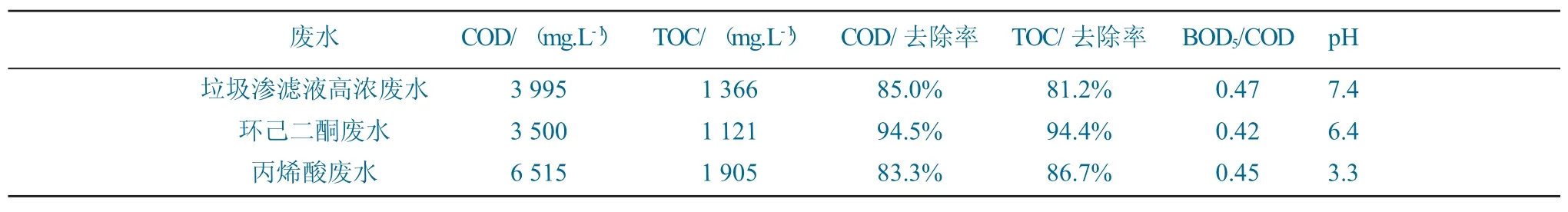
表2 处理后出水水质效果Table 2 Effluent effect after treatment
3 结 论
(1)针对垃圾渗滤液高浓废水、丙烯酸废水和环己二酮3类难降解的高浓有机工业废水,确定了均相催化湿式氧化技术最佳工艺条件为反应温度260℃,反应时间2 h,氧气量为理论用量的1.2倍,催化剂用量500 mg/L。
(2)均相催化湿式氧化技术针对实际难降解的高浓度有机废水处理效果优异,可生化性改善明显,解决了一般氧化技术难以处理达标的技术瓶颈,为后续传统技术的深度处理奠定了良好基础。
