主动及被动拘禁球囊技术应用于非左主干真性冠脉分叉病变的定量血流分数评价
2022-09-14王婧璞李晨光潘聪聪戴宇翔陈章炜吴轶常书福钱菊英葛均波
王婧璞,朱 丽,李晨光,袁 斌,潘聪聪,戴宇翔,陈章炜,陆 浩,吴轶 ,常书福,张 峰,*,钱菊英,葛均波
1.复旦大学附属中山医院心内科,上海 200032
2.国家放射与治疗临床医学研究中心,上海 200032
3.北京中医药大学孙思邈医院,铜川 727031
冠脉分叉病变占全部经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)病变的15%~20%[1-3],具有PCI 成功率低、边支急性闭塞发生率高[4]及术后主要心血管不良事件(major adverse cardiovascular event, MACE)发生率和靶病变血运重建率高等特点[5]。Provisional 策略能避免双支架技术相关的支架内再狭窄和支架内血栓风险[6-7],趋于成为指南和专家共识推荐[8-9]。但是,主支植入支架时常会引起血管嵴和斑块移位,同时有分支开口血流受限及闭塞风险[10-11]。因此,保护分支血流灌注功能是分叉病变介入治疗的关键。
拘禁导丝技术能为补救性处理提供指导,但无法有效预防分支闭塞[11]。拘禁球囊技术则提高了分支血流保留的成功率[12-13],其中主动球囊保护可相对降低分支急性闭塞比例并改善分支血流,但其有效性和安全性尚存争议。部分学者[14]认为分支球囊主动扩张可能导致分支夹层,造成分支闭塞或供血受累。
血流储备分数(fractional flow reserve, FFR)指导分叉病变治疗可显著改善预后,减少再次血运重建的发生[15]。但是,压力导丝通过分支血管时存在技术难度,且有分支夹层及血肿形成风险,导致FFR 评估拘禁分支功能难以广泛开展[16]。定量血流分数(quantitative flow ratio, QFR)为基于造影图像的新型功能学评价工具,与FFR 具有良好的一致性[17],可安全、便利地评估分支血管功能状态。因此,本研究旨在利用QFR 技术比较主动拘禁球囊技术和被动拘禁球囊技术治疗非左主干真性冠脉分叉病变的临床效果。
1 资料与方法
1.1 研究对象 连续纳入2019 年5 月至2020 年5 月于复旦大学附属中山医院经冠脉造影(coronary angiography, CAG)明确存在冠脉分叉病变并采用拘禁球囊技术治疗的292 例患者。排除标准:(1)根据Medina 分型定义为假性分叉病变;(2)左主干病变;(3)冠状动脉慢性完全闭塞;(4)既往接受冠状动脉旁路移植术;(5)靶血管扭曲、短缩及重叠等造成无法成功计算QFR。最终纳入255 例患者(261 个病变),其中主动拘禁球囊组171 例患者(177 个病变)、被动拘禁球囊组84 例患者(84 个病变)。本研究遵守《赫尔辛基宣言》相关准则,经医院伦理委员会审批(B2021-726R),所有患者均签署知情同意书。
1.2 冠脉造影 所有患者术前24 h 内常规接受负荷抗血小板处理,并由具有丰富PCI 经验的心脏病专科医师进行PCI 术:常规以1%利多卡因局部麻醉后穿刺桡动脉或股动脉,置入动脉鞘管。依照标准Judkins 法进行冠脉造影,常规多体位投照,显示左主干、左前降支、回旋支、右冠状动脉及其主要分支。记录手术情况及靶血管和靶病变特征:靶血管位置、靶病变类型、靶病变长度、靶病变狭窄程度、病变钙化程度、边支狭窄程度、心 肌 梗 死 溶 栓 试 验(thrombolysis in myocardial infarction, TIMI)血流情况及 Medina 分型。根据病变情况,选择合适的预扩球囊对靶病变主支血管进行预扩张处理,并记录预处理球囊类型、直径、大小及扩张压力,记录残余病变血管狭窄程度。对于狭窄程度≥50%的病变血管,由术者自主选择主动或被动拘禁球囊技术。
1.3 拘禁球囊技术 主动拘禁球囊技术:主支病变行支架植入时,分支血管预埋半顺应性球囊,同时以一定压力膨胀,预期能达到避免斑块移位、血管嵴移位的目的(图1)。被动拘禁球囊技术:在主支病变行支架植入时,分支预置半顺应性球囊但不常规扩张(图2);主支支架植入后分支血管病变加重或出现闭塞时予以分支预置球囊低压力扩张,以恢复血流,为后续重置导丝、球囊扩张或补救性支架植入赢得时间及给予影像指导。根据主支支架植入情况及分支血流情况,规范选择近端优化扩张技术和(或)分支补救性球囊后扩张技术对分叉病变进行优化处理,以最大程度保障主支支架贴壁满意及分支血流恢复。
1.4 QFR 计算流程 由培训合格人员运用AngioPlus 2.0 软件(博动医疗)对研究病变术前及术后即刻造影过程中主支和边支QFR 进行盲法分析。具体流程:导入造影图像,查看软件自动识别的关键帧,进行调整;重建病变血管轮廓及边支;检查及调整参考管腔,使正常段的参考管腔与实际管腔一致;获得研究病变主支及边支QFR(图1、图2)。
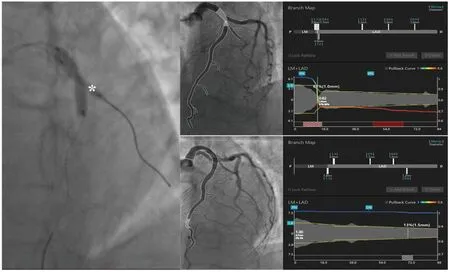
图1 主动拘禁球囊技术PCI 技术路线及QFR 分析示意

图2 被动拘禁球囊技术PCI 技术路线及QFR 分析示意
1.5 观察指标 记录对比剂剂量、靶病变处理时间、手术用药情况等。手术成功标准为靶病变主支残余狭窄<30%,TIMI 血流恢复至3 级。分支急性闭塞是指主支支架完全植入后,分支即刻TIMI 降低或分支内无血流[18]。
1.6 统计学处理 所有数据采用SPSS 25.0 软件进行分析。计量资料进行正态性检验,符合正态分布时以表示,组间比较采用独立样本t 检验;非正态分布资料以M(P25, P75)表示,组间比较采用Mann-Whitney U 检验。分类变量以 n(%) 表示,采用卡方检验或Fisher’s 确切概率法进行组间比较。检验水准(α)为0.05。
2 结 果
2.1 临床基线特征 结果(表1)显示:255 例患者以男性为主(200 例,78.4%),年龄34~88岁,平均(63.4±9.8)岁;稳定性冠心病119 例(46.7%),不稳定性心绞痛73 例(28.6%),非ST 段抬高型心肌梗死41 例(16.1%),ST 段抬高型心肌梗死22 例(8.6%)。两组患者人口学特点、危险因素及临床诊断差异无统计学意义。

表1 患者人口学及临床特点比较
2.2 冠脉造影特点 结果(表2)显示:261 个真性分叉病变主要分布于前降支-对角支(204个,78.2%),以Medina 1.1.1 型为主(232 个,88.9%)。两组病变特点及术前主支、边支TIMI血流分级差异无统计学意义。

表2 两组病变冠脉造影特点比较
2.3 PCI 治疗情况 结果(表3)显示:两组患者主支植入支架类型及大小、边支拘禁球囊大小、病变处理时间、术中对比剂剂量及血管内超声(intravascular ultrasound, IVUS)应用比例差异无统计学意义。所有患者PCI 术后主支TIMI 均为3 级;主动拘禁球囊组术后边支TIMI 分级明显高于被动拘禁球囊组(TIMI 3 级:96.0% vs 78.6%;P<0.001)。两组患者术中均未发生严重夹层(NHLBI 分型 C~F 型);主动拘禁球囊组边支急性闭塞发生率明显低于被动拘禁球囊组(0.6% vs 10.7%,P<0.001)。

表3 两组病变冠脉介入干预情况比较
2.4 定量冠脉造影特点 结果(表4、表5)显示:两组患者术前冠脉造影各项参数差异无统计学意义;术后主动拘禁球囊组分支血管开口直径[(1.41±0.42) mm vs (1.16±0.41) mm]及最小管腔直径[(1.14±0.32) mm vs (1.01±0.36) mm]均大于被动拘禁球囊组(P<0.01)。

表4 两组主支定量冠脉造影特点比较
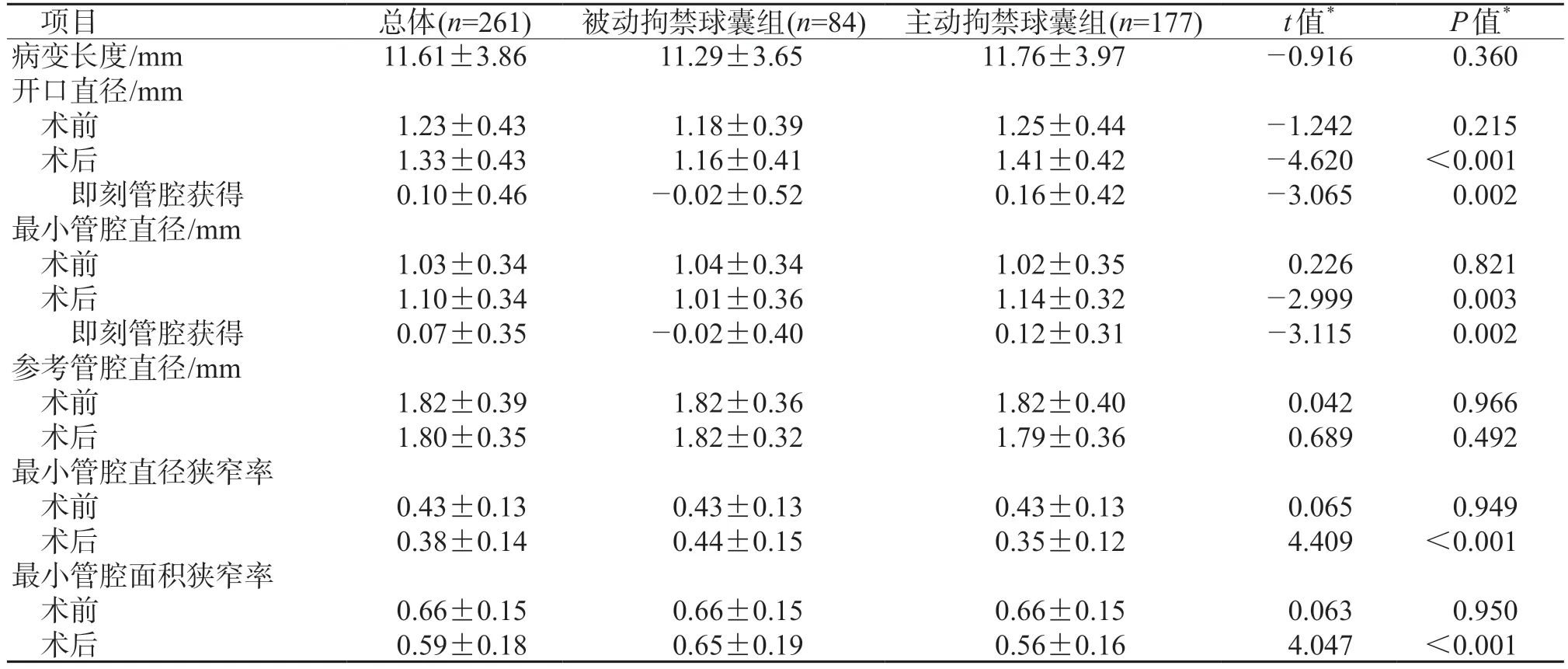
表5 两组分支病变定量冠脉造影特点比较
2.5 功能学评价 结果(表6)显示:两组患者术前主支及边支和术后即刻主支QFR 差异无统计学意义;主动拘禁球囊组术后即刻边支QFR 明显高于被动拘禁球囊组[0.90(0.84,0.95) vs 0.83(0.68,0.91),P<0.001]。
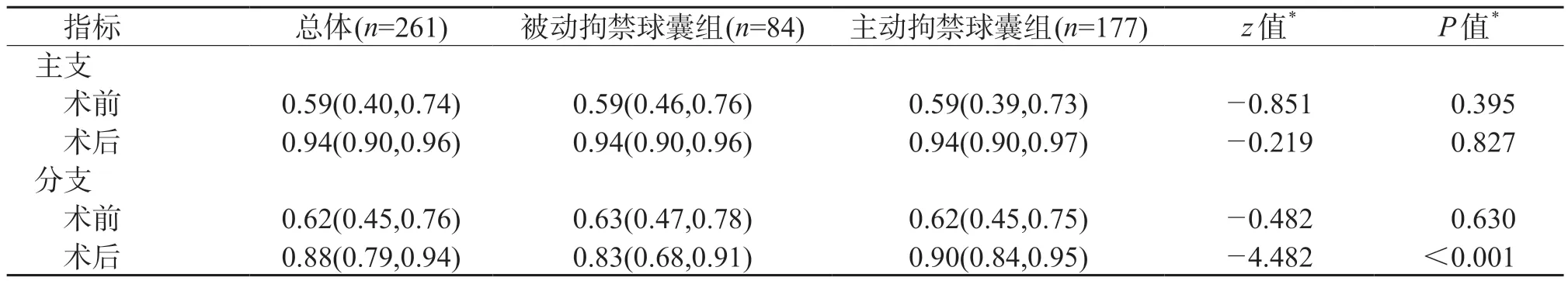
表6 两组病变定量血流分数比较
3 讨 论
关于分叉病变最佳术式选择尚无定论。近年来,以provisional 策略为主的单支架技术成为分叉病变的标准选择[19],但术后仍面临分支闭塞的风险。以Medina 分型确定的冠脉真性分叉病变尤其伴随更差的临床预后[13]。因此,分支保护成为分叉病变介入治疗近年的关注点。
传统的拘禁导丝技术无法避免分支急性闭塞,同时也存在重置导丝通过闭塞开口困难,造成再通失败的风险[3]。拘禁球囊技术是分叉病变PCI 术中分支保护的新方法[13,20]。与拘禁导丝相比,保护球囊可在分支血管开口占据更大的物理空间,防止血管嵴或斑块向分支开口移位。其中,被动拘禁球囊技术虽然在一定程度上减少了分支闭塞的发生,但仍有斑块移位风险,必要时仍须对受累分支血管进行补救性处理或植入支架[12,20]。以分支预置球囊扩张为特点的主动拘禁球囊保护方式旨在以更大的物理空间主动对抗主支支架释放时对血管嵴的压力,进一步降低分支丢失风险。有学者认为主动球囊扩张可能增加分支血管夹层[14]、主支支架膨胀不全[21]及支架变形风险[12],从而增加支架内血栓或支架内狭窄风险。本研究中,主动拘禁球囊技术在明显降低分支急性闭塞发生率的同时并没有增加分支夹层发生风险;而且,本中心术者应用主动拘禁球囊技术时常规进行后扩张,并于必要时采用近端优化技术扩张主支支架,因此主支支架因分支预置球囊主动扩张而贴壁不良或变形的情况少见。
既往研究[22-23]发现,单纯以冠脉造影评估分叉病变会因血管重叠或影像短缩等而受到限制。DKCRUSH-Ⅵ研究[24]显示 FFR 指导不增加 PCI 术后MACE,同时能明显减少分支血管支架植入数量;Lee 等的研究[25]则表明,FFR 指导可改善分叉病变PCI 术后患者的远期预后。然而,FFR 在分叉病变中的应用也有较大局限性,约有10%的患者因分支夹层或压力导丝无法通过等原因造成分支 FFR 获取失败[24,26]。
QFR 分析是基于造影的非侵入性冠脉生理功能学评估新方法,可避免压力导丝病变通过性不佳及使用冠脉扩张药物的缺点,易操作且实用。QFR 与FFR 具有较高一致性[17],且能优化分叉病变评估结果[27];同时,PCI 术后高QFR 是患者良好预后的预测因子[28]。本研究首次运用QFR 评估PCI 术前及术后即刻主支血管和分支血管的功能性血供情况,结果显示,主动拘禁球囊技术较被动拘禁球囊技术改善分支血管功能性血流的效果更佳[0.90(0.84, 0.95)vs 0.83(0.68,0.91),P<0.001],同时不影响主支血管血供,且分支急性闭塞风险更小。
综上所述,本研究首次应用QFR 技术对比主动拘禁球囊技术和被动拘禁球囊技术对非左主干真性冠脉分叉病变血运重建的效果,发现主动拘禁球囊技术可降低分支急性闭塞风险、改善分支血管血供的效果更佳,同时不影响主支血供。但是本研究中PCI 策略多由术者依据经验选择,且仅纳入术后即刻血流数据。因此,仍须进行前瞻性、大样本随机对照实验,并延长随访时间对本研究结果进行验证。
利益冲突:所有作者声明不存在利益冲突。
