中空硫球-MoS2/rGO材料的制备及其在锂硫电池中的应用
2022-09-13彭琳牛明鑫白羽孙克宁
彭琳,牛明鑫,白羽,孙克宁
(北京理工大学化学电源与绿色催化北京市重点实验室,北京 100081)
引 言
近些年,便携式电子设备、新能源汽车和大规模智能电网的广泛应用推动了新型储能设备的发展。目前商业化的锂离子电池由于受到理论能量密度的限制无法进一步满足更高能量密度、更长续航里程和更高储能能力的需求[1-3]。因此,锂硫电池凭借高理论比容量、高理论能量密度、低成本以及安全无污染等优点,成为极具发展前景的新一代二次电池[4-6]。然而,锂硫电池在商业化进程中,仍然存在许多需要克服的挑战:硫及放电终产物硫化锂(Li2S2/Li2S)的绝缘性,导致氧化还原动力学缓慢,从而降低电池的倍率性能并加快容量衰减;硫正极在放电过程的体积膨胀,导致活性材料脱落甚至电极结构粉化,影响电池的使用寿命;中间产物多硫化物溶解产生的“穿梭效应”,导致活性物质损失,从而降低电池的容量和库仑效率[7-11]。
为解决上述问题,研究人员在设计新型正极材料上做了大量的研究。其中,碳纳米管[12-13]、碳纤维[14]、石墨烯[15-16]等碳材料与硫单质复合是一种常见策略。利用碳材料的高导电性和高孔隙率能够改善正极材料的电子传输性能、缓解体积膨胀并物理限制多硫化物,从而提升电池的电化学性能。但是由于非极性的碳材料与多硫化物之间的范德华力结合较弱,无法有效限制多硫化物溶解[17]。因此,为了加强正极材料与多硫化物的相互作用,将极性的金属化合物(例如金属氧化物[18-19]、金属硫化物[20-23]、金属氮化物[24-25]、金属磷化物[26-27]等)与碳材料复合成为当下的研究热点。这些极性的金属化合物能够化学吸附多硫化物,同时催化多硫化物的转化,从而提高硫的利用率[28-30]。。
在众多金属化合物中,金属硫化物具有亲硫性以及优异的电催化活性[31],同时其低的锂化电压能够避免与锂硫电池的工作电压重叠,保持金属硫化物结构稳定[32-33],因此在锂硫电池中受到广泛的关注。其中MoS2凭借对多硫化物具有中等的吸附能力、通过S-Mo-S 键之间弱的范德华力提供更多的活性位点[34]以及材料表面能够实现快速的锂离子扩散[35-36]等优势,成为优异的正极宿主材料。此外,对于设计新型正极材料,不仅需要对材料的化学组成进行选择,同时还要对其进行合理的结构设计(例如多孔结构[37-38]、空心结构[39-40]、核壳结构[41-42]等),这也是能够缓解体积膨胀、限制多硫化物穿梭以及提高硫负载量的有效策略。
本研究通过低温液相法和水热法分别合成中空硫球(HS)和MoS2/rGO,随后将MoS2/rGO 包覆在HS表面得到HS-MoS2/rGO 复合材料。将HS-MoS2/rGO用作锂硫电池正极研究电池的放电比容量、倍率性能及循环稳定性,为锂硫电池正极材料的设计提供新的思路。
1 实验材料和方法
1.1 材料
五水合硫代硫酸钠(Na2S2O3·5H2O)、硫酸、醋酸,分析纯,北京化工厂;聚乙烯吡咯烷酮(PVP),分析纯,北京通广精细化工;盐酸,纯度36%~38%,新光化工试剂厂;二水合钼酸钠(Na2MoO4·2H2O)、硫脲(TU)、高锰酸钾、石墨、聚偏氟乙烯(PVDF),分析纯,阿拉丁试剂有限公司;升华硫,纯度99.95%,阿拉丁试剂有限公司;过氧化氢,纯度30%,阿拉丁试剂有限公司;壳聚糖,分析纯,国药集团化学试剂有限公司;无水乙醇,分析纯,科密欧化学试剂有限公司;N-甲基吡咯烷酮(NMP),纯度99%,阿法埃莎化学有限公司;导电炭黑(Super P),分析纯,太原市力之源电池销售部;聚丙烯隔膜(Celgard 2325),美国MTI公司;碳纸(CP),TGP-H-060,日本东丽(TORAY)公司;高纯锂片(直径14 mm,厚度1.1 mm),99.8%,天津中能锂业有限公司;锂硫电解液,上海松静能源科技有限公司;电池壳(CR-2025),深圳市天成和科技有限公司;泡沫镍(0.88 mm),加拿大Inco 有限公司;实验用水为双重去离子水。
1.2 HS-MoS2/rGO复合材料的制备
HS 的制备:首先,将2.00 g Na2S2O3·5H2O、0.04 g PVP 和100 ml 去离子水混合搅拌15 min 以形成均匀溶液。然后,将1.6 ml 浓盐酸(HCl)缓慢加入上述溶液中,溶液由无色逐渐变成乳白色。在室温下继续搅拌反应2 h 后,将得到的溶液低速离心,并分别用1.0%(质量)PVP 溶液和去离子水清洗2 次。最后,将离心收集的沉淀放入冷冻干燥机中冷冻干燥24 h,即得到HS。
MoS2/rGO 的 制 备:将125 mg Na2MoO4·2H2O、250 mg TU 和50 mg 氧化石墨烯(GO,由天然石墨薄片通过改良的Hummers方法制成)加入到50 ml去离子水中,超声2 h 以形成均匀分散液。然后将上述溶液倒入100 ml 高温高压水热釜,在烘箱中200℃下反应24 h。自然冷却至室温后,用去离子水洗涤3 次放入冰箱冷冻12 h。最后,将其放入冷冻干燥机冷冻干燥24 h,即得到产物MoS2/rGO。
HS-MoS2/rGO 的制备:HS 均匀分散到50 ml 去离子水中得到溶液A;40 mg MoS2/rGO 研磨后加入到40 ml 去离子水中超声分散2 h 得到溶液B;将溶液A 缓慢滴入至溶液B 中,加入2~3 滴0.3%(质量)壳聚糖(CS)溶液(含2~3 滴冰醋酸/10 ml)后搅拌2 h得到混合溶液C;最后,将溶液C 通过低速离心、去离子水洗涤2 次、冷冻干燥机干燥24 h 得到最终产物HS-MoS2/rGO。作为对照的HS-rGO 制备过程,除将溶液B 中的MoS2/rGO 替换成rGO 之外,其余步骤同上。图1为HS-MoS2/rGO制备过程示意图。

图1 HS、MoS2/rGO及HS-MoS2/rGO的制备过程Fig.1 Schematic illustration of the synthetic process of HS,MoS2/rGO and HS-MoS2/rGO
S-MoS2/rGO 的制备:将硫粉与MoS2/rGO 以8∶2(质量比)的比例混合,随后将混合好的粉末置于充满氩气的聚四氟反应釜中并置于烘箱中,在155℃下保温12 h,自然冷却至室温,得到S-MoS2/rGO 复合材料。
1.3 可视化吸附实验
在高纯氩气手套箱中按照摩尔比为5∶1 称取S和Li2S,溶解到DOL/DME 溶剂(体积比1∶1)中,得到1.4 mmol·L-1的Li2S6溶液。随后将相同质量(10 mg)的rGO 和MoS2/rGO 分 别 加 到6 ml 1.4 mmol·L-1的Li2S6溶液中,静置12 h后观察各个溶液的颜色变化。
1.4 正极极片的制备
对称电池极片的制备:将MoS2/rGO 超声分散在无水乙醇中,在剧烈搅拌下形成均匀的悬浮液。随后滴加在直径为12 mm 的碳纸(CP)上,60℃下真空干燥12 h 后得到MoS2/rGO 电极片,面载量约为0.50 mg·cm-2。对照组rGO极片制备方法同上。
扣式电池极片的制备:HS-MoS2/rGO、Super P和PVDF 按照7∶2∶1 的质量比溶于适量NMP 溶剂,搅拌均匀后将浆料涂刮在导电碳纸上,于50℃真空干燥24 h。随后在切片机上裁成直径为12 mm的圆形正极极片,控制硫面载在2.0~2.5 mg·cm-2范围内。对照组HS-rGO 和S-MoS2/rGO 正极极片制备方法同上。
1.5 电池的组装
对称电池的组装:采用负载在碳纸上的MoS2/rGO 用作工作电极和对电极组装对称电池,其中隔膜为Celgard 2325(PP/PE/PP)隔膜,电解液为包含1.0 mol·L-1的LiTFSI 和2.0% LiNO3的Li2S6([S]=2.5 mol·L-1)溶液,溶剂为DOL/DME(体积比为1∶1),电解液用量为40 μl。对照组rGO 的对称电池组装方法同上。
扣式电池的组装:采用HS-MoS2/rGO为正极,负极为厚度1 mm 的金属锂片,隔膜为Celgard 2325(PP/PE/PP)隔膜,电解液为包含1.0 mol·L-1双三氟甲基磺酸酰亚胺锂(LiTFSI)的乙二醇二甲醚(DME)和1,3-二氧戊环(DOL)的混合溶液(体积比1∶1),其中含有2%(质量分数)的LiNO3,电解液用量为60 μl。电极壳型号为CR2025,组装过程在高纯氩气气氛下的手套箱(水<1×10-6,氧<1×10-6)中进行,密封后静置12 h。对照组HS-rGO 和S-MoS2/rGO 的扣式电池组装方法同上。
1.6 测试仪器及方法
原料结构和形貌表征:采用X 射线衍射仪(XRD,Rigaku Ultima IV 型,Cu Kα,日本Rigaku 公司)测定样品的晶体结构,扫描范围为10°~80°,扫描速率为10(°)·min-1。采用扫描电子显微镜(SEM,FEIQuanta FEG 250 型,美国FEI 公司)对材料的微观形貌和尺寸进行分析。通过透射电子显微镜(TEM,JEOL-2100FS 型,日本JEOL 公司)对材料精细结构及元素的分布进行表征。采用拉曼光谱(Raman Spectra,RM 2000 型,英国Renishaw 公司) 对样品中碳材料性质进行表征。X 射线光电子能谱测试(XPS,PHI QUANTERA-ⅡSXM 型,日本ULVACPHI 公司) 对样品组成和元素价态进行分析,按照C 1s 的峰值284.8 eV 进行校正。采用热重分析(TGA,10℃·min-1,TG209 型,德国Netzsch 公司)测定硫的质量分数。采用紫外可见分光光度计(UV,波长范围200~700 nm,TU-1901 型,北京普析通用仪器有限责任公司) 测定样品吸附多硫化锂溶液后,上层清液中多硫化锂溶液的浓度。
电化学性能测试:循环伏安(CV)测试采用上海辰华仪器有限公司的CHI650B 电化学工作站,对称电池的扫描电压为-1.0~1.0 V,扫描速率100 mV·s-1;扣式电池的扫描范围为1.6~2.8 V,扫描速率为0.1 mV·s-1。电化学交流阻抗测试(EIS)采用美国普林斯顿大学的PARSTAT2273 型电化学测试系统对电池进行EIS 测试,交流信号的频率扫描范围为100 mHz~100 kHz,振幅为5 mV。使用Zsimp Win拟合软件对电化学阻抗谱进行拟合分析。恒流充放电分析测试使用深圳市新威尔电子有限公司的电池性能测试系统,电压范围1.6~2.8 V,电流密度以活性物质质量以及充放电倍率(1 C=1675 mA·h·g-1)计算。
2 实验结果与讨论
2.1 HS-MoS2/rGO的表征
2.1.1 HS-MoS2/rGO 的XRD 和拉曼光谱表征 通过XRD 测试表征材料的晶体结构,MoS2/rGO、HSrGO 和HS-MoS2/rGO 的XRD 谱图如图2 所示。由图可知,MoS2/rGO 在14.4°和33.6°处显示的衍射峰对应标准MoS2图谱(PDF#73-1508)的(002)和(101)晶面,在20°~30°出现的宽峰对应于无定形的rGO,表明MoS2/rGO 成功合成。当MoS2/rGO 和rGO 与HS 复合后,复合材料中HS 以高度结晶的立方硫形式存在(PDF#08-0247),但是较难观察到rGO 的无定形峰,这可能是由于rGO 的弱峰与硫的特征峰重叠导致的[43]。同时在HS-MoS2/rGO中能够观察到MoS2的(002)晶面特征峰,表明HS 成功与MoS2/rGO 复合。此外,拉曼光谱(Raman)测试用于表征MoS2/rGO 和rGO 中碳材料的性质。如图3 所示,在1332 cm-1(D带)和1590 cm-1(G 带)处出现两个特征峰,分别代表有缺陷的碳和石墨碳。D峰与G峰强度的比值(ID/IG)通常可以反映碳材料的无序度[44]。MoS2/rGO 和rGO的ID/IG分别为1.29 和1.07,说明MoS2/rGO 中rGO 的缺陷程度增加,这有利于锚定多硫化锂,抑制反应过程中的穿梭效应。

图2 MoS2/rGO、HS-rGO和HS-MoS2/rGO的XRD谱图Fig.2 XRD patterns of MoS2/rGO,HS-rGO and HS-MoS2/rGO

图3 MoS2/rGO和rGO的拉曼光谱图Fig.3 Raman spectra of MoS2/rGO和rGO
2.1.2 HS-MoS2/rGO 的微观形貌表征 HS、MoS2/rGO 和HS-MoS2/rGO 的微观形貌通过扫描电子显微镜(SEM)表征。如图4(a)所示,HS 呈纳米球状,其尺寸为500~600 nm。右上角插图为超声后硫球的SEM 图,显示出硫球为空心结构,且硫层厚度为30~50 nm,硫球的内部空间可以在放电过程中缓解体积膨胀。图4(b)是MoS2/rGO 的SEM 图,可以看出MoS2纳米花直径约为500 nm,其均匀地嵌入在rGO纳米片中。rGO 片层形成了导电骨架,可以提供快速的电子传输通道,从而有利于电化学反应的进行。HS-MoS2/rGO 的SEM 图 如 图4(c)所 示,HS 被MoS2/rGO 包覆且分布均匀。此外,材料复合后HS纳米球和MoS2纳米花的形貌保持不变。透射电子显微镜(TEM)和高分辨透射电子显微镜(HRTEM)用于进一步研究MoS2/rGO 的精细微观结构及元素分布,如图5所示。从MoS2/rGO 的TEM 图[图5(a)]可以看出,MoS2纳米花直径约为500 nm,其嵌入在褶皱起伏的rGO 纳米薄片中,这与SEM 图中观察到的结果一致。MoS2/rGO的HRTEM 图[图5(b)]显示出明显的晶格条纹,条纹间距为0.61 nm 对应于MoS2的(002)晶面,与XRD 测试结果对应。图5(c)是高角环形暗场像-扫描透射电子显微镜图像(HAADFSTEM)及相应的元素分布图,可以看出MoS2/rGO 中Mo、S和C三种元素均匀分布。

图4 HS、MoS2/rGO和HS-MoS2/rGO的SEM图Fig.4 SEM images of HS,MoS2/rGO and HS-MoS2/rGO

图5 MoS2/rGO的TEM图、HRTEM图和HAADF-STEM 图及相应的元素分布Fig.5 TEM image,HRTEM image and HAADF-STEM image and the corresponding EDS elemental analysis image of MoS2/rGO
2.1.3 MoS2/rGO 的XPS 表征 XPS 用于表征MoS2/rGO 的元素组成和化学状态。图6(a)为MoS2/rGO 的Mo 3d光谱,在232.4 eV 和229.1 eV 处观察到的两个峰分别对应于Mo4+3d3/2和Mo4+3d5/2
[39]。此 外,在235.8 eV 处出现了Mo6+(MoO3)的峰,这是由于在水热过程中GO 和溶液相互作用引起Mo4+发生部分氧化形成的[45-46]。图6(b)显示了MoS2/rGO 的S 2p XPS 光谱,在163.5 eV 和161.9 eV 处的峰分别对应S2-2p1/2和S2-2p3/2。而在168.8 eV 处的峰代表硫酸盐(/),是由于MoS2在空气中被部分氧化形成的。

图6 MoS2/rGO的XPS谱图Fig.6 XPS spectra of MoS2/rGO
2.1.4 HS-MoS2/rGO 的热重分析 通过热重分析(TGA)测试HS-MoS2/rGO 和HS-rGO 中的硫含量。如图7所示,在100~400℃之间的失重与材料内部的硫升华有关,因此由TGA 曲线可以测得HS-MoS2/rGO 和HS-rGO 中的硫含量分别为76.5% 和76.7%。

图7 HS-MoS2/rGO和HS-rGO的热重分析曲线Fig.7 TGA curves of HS-MoS2/rGO and HS-rGO
2.1.5 Li2S6吸附实验 为直观揭示MoS2/rGO 对多硫化物的吸附能力,将MoS2/rGO 和rGO 分别浸入Li2S6溶液中进行可视化吸附实验并进行紫外可见分光光度测试。从图8(a)中可以看出,加入MoS2/rGO的Li2S6溶液由黄色变为无色,而加入rGO 的Li2S6溶液无明显颜色变化,说明MoS2/rGO 对Li2S6有强化学吸附能力。随后,对不同样品吸附Li2S6的上清液进行紫外可见分光光度测试,如图8(b)所示,加入MoS2/rGO 的上清液的光吸收强度峰最弱,再次验证了MoS2/rGO与Li2S6之间更强的化学相互作用。

图8 rGO和MoS2/rGO的可视化吸附实验(a)及相应的紫外-可见吸收光谱(b)Fig.8 Visual adsorption experiments of rGO and MoS2/rGO(a)and corresponding ultraviolet/visible absorption spectra(b)
2.2 电化学性能分析
2.2.1 Li2S6对称电池测试 研究表明,极性材料不仅能够吸附多硫化物,同时还能够加速多硫化物的转化过程,从而有效抑制穿梭效应。因此,为了探究MoS2/rGO 对多硫化物的催化活性,组装了Li2S6对称电池并进行CV 测试,如图9 所示。不含Li2S6的MoS2/rGO 对称电池的CV 曲线几乎没有电流通过,说明无氧化还原反应发生。而含Li2S6的对称电池均表现出明显的电流响应,对应于Li2S6的氧化还原反应过程。相比于rGO,MoS2/rGO 的氧化还原电流值更大,表明多硫化物在MoS2/rGO 表面具有更快的电化学反应速率。进一步说明,MoS2/rGO 不仅具有强多硫化物吸附能力,同时能够促进多硫化物氧化还原反应动力学。

图9 rGO和MoS2/rGO的Li2S6对称电池CV曲线Fig.9 CV curves of Li2S6-symmetric cells employing rGO and MoS2/rGO as electrodes
2.2.2 电池的循环伏安测试(CV)和EIS 测试 为了研究HS-MoS2/rGO 对锂硫电池电化学性能的影响,组装了扣式电池并首先进行了循环伏安测试。循环伏安曲线如图10(a)所示,在1.6~2.8 V的电压范围内有两个还原峰(2.3 V 和2.0 V),分别代表S8到可溶 性Li2Sx(4≤x≤8)和Li2Sx(4≤x≤8)进 一 步 到 不 溶 性Li2S/Li2S2的还原过程。此外,HS-rGO 和HS-MoS2/rGO 对应的CV曲线有两个氧化峰,分别代表不溶性Li2S/Li2S2到可溶性Li2Sx(4≤x≤8)和Li2Sx(4≤x≤8)到S8的氧化过程。同时,与HS-rGO 相比,HS-MoS2/rGO 对应的CV 曲线峰电流值更高,峰形更尖锐且极化更小,说明MoS2/rGO 能够加速多硫化物的氧化还原反应。
电化学阻抗测试(EIS)用于研究电池的电化学动力学过程。图10(b)是电化学阻抗图和对应的等效电路图,图中半圆在横轴上的截距对应电池的欧姆电阻Re,半圆直径代表电池的电荷转移电阻(Rct)。对曲线进行拟合得到Re和Rct的值并总结到表1 中,可以看出两种电池的Re基本一致。此外,相比于HS-rGO 电 极(40.49),HS-MoS2/rGO 的Rct值 更 小(30.09),表明在MoS2/rGO 和多硫化物界面处电荷转移更快。
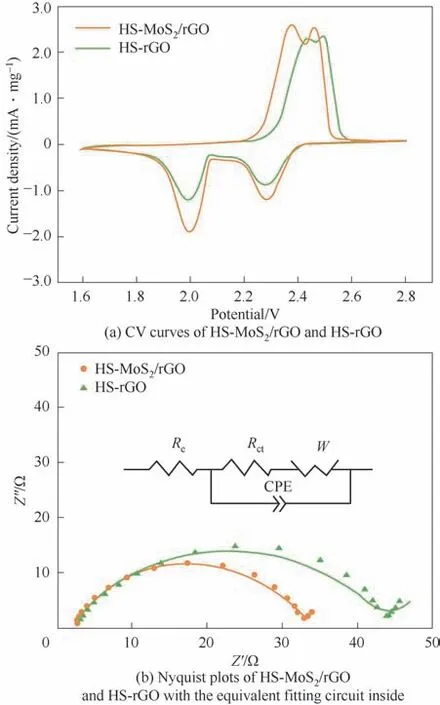
图10 HS-MoS2/rGO和HS-rGO的循环伏安曲线和电化学阻抗谱图(插图为拟合电路图)Fig.10 CV curves and Nyquist plots of HS-MoS2/rGO and HSrGO with the equivalent fitting circuit inside

表1 HS-MoS2/rGO和HS-rGO电池EIS结果对比Table 1 The EIS results of HS-MoS2/rGO and HS-rGO electrodes
2.2.3 电池的倍率性能测试 HS-MoS2/rGO 和HSrGO 倍率性能如图11(a)所示。HS-MoS2/rGO 电极在0.2、0.5、1、2 和3 C 倍率下,初始比容量分别达到1335.2、1108.3、1015.4、937.3 和822.2 mA·h·g-1,当倍率切换至0.2 C 时,放电比容量仍可以恢复到1060.6 mA·h·g-1,表明其优异的倍率性能。相比之下,HS-rGO 电极的初始比容量分别只有1135.4、1057.3、900.4、810.5 和727.8 mA·h·g-1,均低于HSMoS2/rGO 电极的放电比容量。HS-MoS2/rGO 电极优异的倍率性能归因于其表面的电荷转移更快,同时MoS2/rGO 能够加速多硫化物的氧化还原反应动力学。HS-MoS2/rGO 电池在不同倍率下的首圈充放电曲线如图11(b)所示,其存在两个放电平台和一个充电平台,位于2.30 V 左右较高的放电平台对应着单质硫向可溶多硫化物Li2Sx(4≤x≤8)转化的过程,位于2.08 V 左右较低的放电平台对应可溶的多硫化物Li2Sx(4≤x≤8)向不可溶的Li2S 和Li2S2的转化过程,而充电平台则对应放电产物Li2S和Li2S2向长链多硫化物及硫单质的转化过程。图中的ΔE代表充电和低放电平台间的电压差,是衡量电池极化程度和反应动力学的重要指标,其数值小说明极化程度低,电化学反应动力学较快。进一步对比了HS-MoS2/rGO和HS-rGO 电极在不同倍率下充放电曲线的极化大小,结果如图11(c)所示,可以看出HS-MoS2/rGO 电极在所有电流密度下均表现出更低的极化值,表明MoS2/rGO 能够提高多硫化物的氧化还原反应动力学,从而有效降低电极极化。

图11 HS-MoS2/rGO和HS-rGO电极的倍率性能Fig.11 Rate performance of HS-MoS2/rGO and HS-rGO electrodes
2.2.4 电池的长循环性能测试 HS-MoS2/rGO 电极优异的电化学性能通过长循环测试进一步验证。如图12 所示,HS-MoS2/rGO 电极表现出更高的放电比容量,其在1 C 倍率下初始比容量为921.9 mA·h·g-1,而HS-rGO 电极的初始比容量为856.8 mA·h·g-1。此外,HS-MoS2/rGO 电极还具有良好的循环稳定性,经过150 次循环后仍可以保持743.9 mA·h·g-1的可逆比容量,同时库仑效率接近100%。HSMoS2/rGO 电极优异的循环稳定性表明了MoS2/rGO能够有效抑制多硫化物的穿梭,提高了活性物质硫的利用率。此外,相比于以中空硫球作活性物质的HS-MoS2/rGO 电极,以硫粉为活性物质的S-MoS2/rGO 电极的初始比容量仅为744.7 mA·h·g-1,并且容量衰减较快,同时库仑效率显著降低,这表明以均匀分散的中空硫球作为活性物质能够提高硫的利用率并保持电池的循环稳定性。

图12 HS-MoS2/rGO、HS-rGO和S-MoS2/rGO电极的长循环性能Fig.12 Long-term cycling performance of HS-MoS2/rGO,HS-rGO and S-MoS2/rGO electrodes
2.3 循环后正极的SEM表征
图13是循环后正极表面的SEM 图,显示出HSMoS2/rGO 正极的表面比较平整[图13(a)],而HS-rGO正极表面上可以观察到大量团聚的“死硫”[图13(b)],表明MoS2/rGO可以促进放电产物Li2S/Li2S2的沉积,从而提高了硫的利用率。与HS-MoS2/rGO相比,当以硫粉为活性物质时,S-MoS2/rGO 表面存在大块的“死硫”[图13(c)],表明中空硫球由于具有内部空间能够容纳多硫化物同时缓解体积膨胀,从而避免大量硫团聚并保持正极结构完整。

图13 HS-MoS2/rGO、HS-rGO和S-MoS2/rGO在1 C下经过50次循环后的SEM图Fig.13 SEM images of HS-MoS2/rGO,HS-rGO and S-MoS2/rGO electrodes after 50 cycles at 1 C
3 结 论
本文利用低温液相法合成了HS,随后将水热法制备的MoS2纳米花/rGO 复合材料包覆在HS 表面得到HS-MoS2/rGO正极材料并应用到锂硫电池中。单分散的中空硫球有利于缓解体积膨胀,并维持正极结构稳定。通过Li2S6吸附实验和对称电池测试表明MoS2/rGO 能够有效吸附多硫化物并催化多硫化物的转化。同时,EIS 测试表明在MoS2/rGO 表面能够实现更快的电荷转移。此外,循环后的SEM 图揭示了MoS2/rGO 能够促进放电产物Li2S/Li2S2在电极表面均匀地沉积。因此,HS-MoS2/rGO 电极表现出较高的放电比容量、优异的倍率性能和良好的循环稳定性。在1 C倍率下,HS-MoS2/rGO电极初始比容量达到921.9 mA·h·g-1,经过150 次循环后比容量仍可保持在743.9 mA·h·g-1。此外,HS-MoS2/rGO 正极在3 C 倍率下,放电比容量能够达到822.2 mA·h·g-1。该研究表明HS-MoS2/rGO电极具有优异的电化学性能,为正极材料的设计提供了新的思路。
