合成气生物发酵法制乙醇的研究进展
2022-09-13王悦琳晁伟蓝晓程莫志朋佟淑环王铁峰
王悦琳,晁伟,蓝晓程,莫志朋,佟淑环,王铁峰
(1 清华大学化学工程系,北京 100084; 2 北京首钢朗泽科技股份有限公司,北京 100043)
引 言
当前,我国能源供应主要依赖于化石能源。随着能源短缺、环境污染、气候变化等全球性问题日益严峻,我国能源安全面临着诸多不确定因素。因此,开发高效、绿色、可再生的替代燃料,减少对石油等化石能源的消耗,逐渐成为世界关注的焦点。乙醇是一种不含硫及灰分的清洁燃料,在比热容、辛烷值等方面都优于汽油,可以作为现有汽柴油的替代品。目前以玉米、小麦等粮食为原料的第1 代燃料乙醇及以木薯、甜高粱等为原料的第1.5 代燃料乙醇生产均存在“与人争粮、与粮争地”的问题,在我国难以持续大规模发展;而以纤维素为代表的第2 代燃料乙醇技术受限于秸秆的收集处理效率低、预处理费用和纤维素酶成本高等问题,其发展受到严重制约[1-2]。创新燃料乙醇来源,开发非粮乙醇生产新工艺成为国内外研究热点,而以富含CO或CO/H2的合成气为原料生产乙醇是目前非粮乙醇的主要研究方向。合成气来源广泛,既可以由工业尾气产生,也可以通过对木质纤维素等生物质气化转化得到,再由化学催化法(F-T 合成)或生物发酵法转化为乙醇。化学催化法需要高温高压条件,且选择性低、耐毒性差、对合成气成分比例敏感[3]。利用合成气生物发酵法生产乙醇是一种具有前景的乙醇生产新型工艺。对比F-T 合成法,合成气生物发酵法具有以下优势:(1)反应条件温和,可在环境温度和常压下进行,能耗较低;(2)产物选择性高,副产物少;(3)细菌对不同CO∶H2比例的合成气适应性强,不需要从气体中除去CO2[4];(4)相比于化学催化剂,微生物耐杂质性较强;(5)原料来源广泛。
我国钢铁、铁合金、电石、石油炼化、煤化工、黄磷等行业生产过程中副产大量富含CO 和H2的工业尾气。其中,钢铁行业每年会产生含CO 工业尾气达(1×1012)~(1.5×1012)m3,炼焦产生的焦炉煤气总量为(6×1010)~(8×1010)m3,约合(2.5×1010)~(3.5×1010)m3天然气,超过西气东输的总气量;炭黑行业年产2.4×1010m3炭黑尾气[5]。这些工业尾气蕴含了大量的化学能和热能,直接排放造成资源浪费和环境污染,工业尾气燃烧加热或发电也会带来大量的温室气体CO2排放。随着我国“碳达峰”和“碳中和”战略的提出,工业尾气的化学利用受到重视。减少尾气中CO 燃烧带来的CO2排放,将尾气中的CO 和H2转化成更高价值的化工产品受到广泛关注。利用工业尾气中的CO 进行合成气生物发酵是实现工业尾气转化利用的一种重要方式,其主要产物为乙醇,同时联产菌体蛋白。据测算利用10%的工业尾气每年即可产生燃料乙醇超过1000 万吨[6],市场前景广阔。乙醇与汽柴油按一定比例混合作为车用燃料,能够有效减少汽车尾气中PM2.5、CO 和碳氢化合物等污染物的排放。与此同时,乙醇作为基础化工原料可深加工成多元化工新材料,如乙烯、聚乙烯、聚氯乙烯等聚酯材料,从而减少化石能源消耗,为工业尾气低碳化利用开辟了一条新的路径,助力实现“碳达峰”和“碳中和”目标。
合成气生物发酵法制乙醇也存在一些局限性,如生产效率低、气体底物在液相中的溶解度差、传质性能不佳等。这些局限性阻碍了合成气发酵技术的大规模商业化。本文对合成气生物发酵制乙醇的研究进展进行了综述,总结了该工艺机理、典型微生物种类、影响因素以及强化手段,明确了未来的研究方向。
1 合成气生物发酵制乙醇的技术原理
1.1 合成气发酵法用微生物
1987 年,一种新的梭状芽孢杆菌Clostridium ljungdahlii被发现[7],它能够将CO 和H2转化为乙醇和乙酸。随后,合成气发酵法制乙醇研究取得了重大进展,特别是在过程微生物学方面,科研人员陆续从农场土壤、动物粪便、污泥沉积物等物质中发现了数十种能够利用合成气厌氧发酵生产乙醇的微生物,如表1所示。目前,这些菌种中研究较多的是Clostridium ljungdahlii、Clostridium carboxidivoransP7等[26]。

表1 合成气发酵法用微生物Table 1 Microorganisms for syngas fermentation
1.2 合成气发酵法制乙醇代谢途径
到目前为止,已经发现至少六种菌种可以以CO为唯一碳源生产乙醇,包括Clostridium ljungdahlii、Clostridiumcarboxidivorans、Clostridium autoethanogenum、Butyribacterium methylotrophicum、Clostridium ragsdaleiP11和Alkalibaculum bacchi。这些细菌通过一种被称为乙酰辅酶A 途径(Wood-Ljungdahl 途径)的代谢途径发酵生成乙酸和乙醇,如图1所示。CO 和H2作为电子源,分别在一氧化碳脱氢酶(CODH)和氢化酶(H2ase)的作用下发生氧化反应释放电子[28],同时,CO和CO2作为碳源。该代谢途径包含两条支路:甲基支路和羰基支路[29-31]。对于甲基支路,CO2可直接进入该支路,CO 则需要进一步通过CODH 的作用被催化氧化为CO2,同时产生电子。CO2在甲酸脱氢酶的催化作用下生成甲酸。在ATP 的参与下,甲酸转化为甲酰基四氢叶酸(HCO-THF),再被连续还原为甲基四氢叶酸(CH3-THF)。甲基四氢叶酸又在甲基转移酶的催化下,将其甲基转移给类咕啉铁硫蛋白,形成甲基类咕啉铁硫蛋白(CH3-CoFeSP)。对于羰基支路,CO 可以直接进入,CO2则需要在一氧化碳脱氢酶/乙酰辅酶A合成酶(CODH/ACS)的作用下转化为CO。CO 接着在乙酰辅酶A 合成酶的作用下生成羰基。最后,来自CO 或CO2还原得到的羰基、由CO2三步还原得到的甲基类咕啉铁硫蛋白中的甲基和辅酶A形成乙酰辅酶A(Acetyl-CoA)[32-33]。乙酰辅酶A 可以转化为乙酸、乙醇或其他有机酸和醇。

图1 Wood-Ljungdahl途径(乙酰辅酶A途径)[27]Fig.1 Acetyl-CoA“Wood-Ljungdahl”pathway[27]
该途径的简要总反应式如下所示[34]:

式中自由能数据是在pH = 7.0 下测得的[35],1 cal=4.18 J。
1.3 原料气来源
生物发酵制乙醇工艺原料气来源广泛,既有化石燃料气化产生的合成气,如煤燃烧气化、天然气蒸汽转化等,又有生物质如木质纤维素气化转化得到的合成气。典型合成气的来源及对应组分如表2所示。随着我国“碳达峰”和“碳中和”战略的提出,富含CO 或CO/H2的工业尾气也逐渐成为生物发酵制乙醇工艺的重要原料。典型工业过程的工业尾气组成如表3 所示,其主要组成包括H2、CO 和CO2,其中H2和CO提供还原力,CO和CO2提供碳源。

表2 典型合成气来源及组分Table 2 Sources and components of typical syngas

表3 典型工业过程的尾气组分[5,39-44]Table 3 Tail gas components of typical industrial processes[5,39-44]
工业尾气发酵制乙醇从成本和产品价值两方面显示出了突出的经济性。与玉米和木薯等粮食制燃料乙醇相比,工业尾气制乙醇的综合成本降低约20%。将10000 m3原料气发酵可制得1.2 t燃料乙醇,相比于燃烧发电获得的产品价值高一倍,能源利用效率也达到60%[6]。
2 影响合成气发酵的因素
2.1 合成气组成
典型工业尾气的气体成分基本相同,但H2、CO和CO2的比例不同。Orgill[45]研究了H2和CO 两种电子源对C.ragsdalei菌种生长和产物形成的影响。结果表明,乙酰辅酶A 形成后,H2仅用于产物形成,而不用于菌体生长。CO 的电子利用率要高于H2,这意味着提供电子的CO 增多,而形成产物的CO 减小,从而降低了碳转化效率。Heiskanen 等[46]通过实验观察到,在CO 被消耗之前,Butyribacterium methylotrophicum菌种对H2的利用受到抑制,这表明CO 抑制了氢化酶。而Skidmore 等[47]的研究表明,增加H2的分压可以显著提高氢化酶活性。Liu 等[9]利用生物质合成气和CO 分压更高的煤气化工业合成气研究了合成气发酵制乙醇的过程,发现与生物质合成气相比,煤气化工业合成气可获得更高的细胞生长率和乙醇收率。Hurst 等[48]研究了CO 分压对Clostridium carboxidivoransP7 菌株发酵乙醇产量的影响,表明随着CO 分压从0.35 atm(1 atm=101325 Pa)增加至2.0 atm,最大细胞浓度增加了440%,乙醇发酵从非生长相关过程转变为菌体生长相关过程,同时乙酸产量降低,这可能是发生了菌体吸收乙酸并转化为乙醇的过程[22,48-49],并证明了CO 分压(PCO)或CO 分压/ CO2分压(PCO/PCO2)会影响菌体代谢。Chen 等[50]基于C.ljungdahlii基因组尺度代谢重建的稳态和动态通量平衡分析,建立了鼓泡床反应器时空代谢模型,计算得到当CO 摩尔分数为0.45 时,乙醇收率最大。Esquivel-Elizondo 等[51]研究了CO2分子对细胞消耗CO 和H2的影响,表明CO2抑制Pleomorphomonas菌株对CO 的氧化作用,降低Acetobacterium菌株发酵制得乙醇的收率;而H2分子不会抑制Pleomorphomonas和Acetobacterium生产乙醇的过程,但会导致CO的消耗速率小幅降低。
合成气通常含有的一些如甲烷、焦油以及含硫和氮的气体等杂质成分也可能影响菌体增长和产物分布[52-53]。在Ramachandriya 等[54]使用Clostridium ragsdaleiP11 的研究中,甲烷浓度达到5%时也不会影响产物分布或细胞生长。Ahmed 等[55]发现,在Clostridium carboxidivorans发酵过程中,合成气中存在的焦油会导致菌体休眠,增加产乙醇的比例并减少乙酸比例。这种影响可以通过引入0.025 μm 过滤器去除焦油的方法克服。Ahmed 等[56]还发现,合成气中的NO 可以抑制氢化酶,阻止Clostridium carboxidivoransP7 利用H2,并且增加了细胞的乙醇产量。然而,由于NO 抑制了氢化酶的活性,因此生成乙醇的电子必须来自CO 而不是H2,这将降低发酵过程的碳转换效率。NO 浓度低于40×10-6时,对发酵过程没有影响。合成气发酵菌种对甲烷的利用 鲜 有 报 道。 Klasson 等[57]研 究 了H2S 对C.ljungdahlii菌种发酵过程的影响,发现当H2S 浓度高达5.2% (体积)时,C.ljungdahlii的生长没有受到显著影响,证明其相比于化学催化剂具有良好的耐硫性。
2.2 操作条件(pH和温度)
pH是影响微生物催化剂活性的一个重要参数。培养基的pH 影响乙酸生成和乙醇生成之间的转换[58]。不同合成气发酵微生物的最佳pH 在4.5~7.5之间。对于C.carboxidivorans,在不调节pH 的情况下,连续供气间歇实验的发酵产生有机酸,随后转化为醇,这说明不同的pH 可能会影响菌种的代谢路径[59]。Richter 等[60]建立了一个热力学调节而非遗传调节的模型来描述合成气发酵过程中溶剂生成的建立机制。结果表明,未解离的乙酸累积达到热力学阈值时,导致了菌种代谢从乙酸生成(acidogenesis) 阶 段 转 变 为 乙 醇 生 成(solventogenesis)阶段,pH 升高,而在此过程没有观察到蛋白质组对中枢代谢途径的调控。Abubackar等[61]观察到,在控制pH 为4.5的合成气发酵过程中,C.autoethanogenum发酵没有积累乙酸。然而,当pH 为6.0 时,发酵积累了等量的乙酸和乙醇。这表明较低的pH 有利于乙醇的生产。其他不同菌种条件下,如在C.autoethanogenum[62]、C.carboxidivorans[63]、C.ljungdahlii[64]和C.ragsdalei[65]这几种菌种下的研究也都表明,pH4.5~5.0 触发了脂肪酸转化为醇,而pH5.0~6.0有利于与细胞生长相关的乙酸生成。
发酵温度是影响合成气发酵工艺中微生物生长和代谢的另一个关键参数。Kundiyana 等[66]的研究结果表明,在不添加任何缓冲液的情况下,使用C.ragsdalei菌种在32~37℃下进行合成气发酵是可行的,37℃以上的温度大大降低了C.ragsdalei细胞生长和性能,导致乙醇产量显著降低。在Shen 等[67]的实验结果中,较高的温度(33℃和37℃)促进菌种快速生长,但导致细胞团聚,较低的温度(25℃和29℃)避免团聚,但导致细胞生长缓慢,发酵性能低。使用37~25℃和37~29℃的两步温度培养(two-step temperature,简称TST 培养)可以解决这一问题,实现高醇产量。Huhnke 等[20]表明,C.ragsdalei生长的适宜温度为30~40℃,37℃为最适温度。Liou 等[17]报道了C.carboxidivorans生长的适宜温度为24~42℃,37~40℃为最适温度。然而,适宜生长的温度和与生长相关的有机酸积累可能并不适合乙醇的生产。Ramió -Pujol 等[68]的 报 道 表 明,25℃对C.carboxidivorans发酵产乙醇更有利,并且可避免“酸崩溃”效应(有机酸的快速积累导致溶剂生成阶段提前终止,仅产生少量乙醇[69])。
2.3 气–液传质
细菌摄取气体基质经过的传质过程包括气体基质进入气液界面的输运、在液态培养基中的输运、混合气体进入细菌周围的静止液体层的输运以及基质扩散进微生物几个步骤。由于CO 和H2在液体介质中的溶解度低(37℃、100 kPa 条件下,水中CO 或H2的饱和浓度均小于10-3mol/L[70]),气液界面传质是合成气发酵工艺的限速步骤[57]。因此,确定合成气发酵反应器的传质特性对指导和提高合成气发酵制乙醇的效率至关重要。体积传质系数kLa是描述生物反应器中气相向液相传质强度的重要指标。对于微溶气体基质,单位反应器体积的底物转移速率等于从气相到液相的传质速率[71]:


式中,qm为最大比吸收速率,1/h;W′为抑制常数,atm;为饱和常数,atm;X为细菌浓度,mg/L。结合式(5)、式(6)可知,避免基底毒性的一种方法是在增加压力的同时增加细菌浓度[73]。
2.4 培养基
为了更大限度地提高发酵效率,生物反应器内须达到较高的细胞质量浓度。培养基为微生物生长提供必需的营养物质,包括氮、磷、矿物质、维生素和还原剂,以促进微生物最大限度地生长[4]。培养基的选择要根据菌种和目标产品来确定。例如,C.ljungdahlii常用的是PETC 培养基。在合成气发酵研究中观察到,营养丰富的培养基会显著刺激细胞生长并同时形成乙酸。相反,营养有限的条件会促进乙醇的生成,减少乙酸的生成。由于合成气发酵制乙醇是由厌氧产酸细菌进行的,因此,培养基中还需要加入一些还原剂来提供更多的电子,使乙酰辅酶A 转化为乙醇,将微生物的新陈代谢转变为溶剂生成过程,较为常用的还原剂如盐酸半胱氨酸或九水硫酸钠(Na2SO4·9H2O)。Klasson 等[74]研究了不同浓度的还原剂(如硫代乙醇酸钠、抗坏血酸、甲基紫精和苄基紫精)对C.ljungdahlii体系中乙醇浓度和产物比例的影响。研究发现,即使菌群生长停止,在最低实验浓度30×10-6的苄基紫精中也有较高的乙醇产量(3.7 mmol/L)。然而,由于还原剂会抑制产酸从而阻碍了生长所需的ATP 产生,所以一定程度上抑制了细胞的生长。因此,超过一定浓度的还原剂可能对连续发酵产生负面作用[75]。
一些无机离子对菌种生长和Wood-Ljungdahl代谢途径中的关键酶也有重要的影响。比如Na+会对含有Na+依赖性易位ATP 酶的菌种生长和菌种密度产生显著影响,大多数培养基中含有约35 mmol/L Na+[76]。目前也已经研究了Co2+、Cu2+、Fe2+、Mn2+、Mo6+、Ni2+、Zn2+、和等无机离子对发酵过程的影响[77]。这些无机离子分别影响着不同关键酶的活性,如Zn2+会影响一氧化碳脱氢酶和氢化酶的活性,和会影响甲酸脱氢酶FDH的活性。所以,应根据不同菌种与目标产物分布优化培养基中微量金属的浓度。
培养基的经济性也是重要因素。目前已经研究了玉米浆(CSL)和棉花籽提取物(CSE)取代酵母提取物(YE)的可行性,两者成本分别为YE的2%和0.5%[75,78]。Maddipati 等[58]的研究表明,使用玉米浆(CSL)代替酵母提取物(YE)可将培养基成本降低27%,乙醇产量提高78%。Guo 等[15]也采用玉米浆替代酵母膏和维生素,替代后乙醇产量明显上升,乙酸产量也有所增加。然而,也有一些研究表明,使用CSL 可能会对菌种生长和菌种密度造成不利影响[79-80]。
3 反应器类型与传质强化
3.1 典型反应器传质性能比较
搅拌槽反应器(STR)是目前合成气发酵中最常用的生物反应器,可在间歇式、半间歇式或连续模式下运行,也可在一些两阶段研究中与其他生物反应器类型(如鼓泡床反应器)耦合[81-82]。STR 内传质的改善是通过挡板来增加气泡破碎、通过提高叶轮转速和使用微气泡喷射器来实现的[83-84]。当气泡尺寸减小时,传质气液界面面积增加。然而,这种方式会导致高能耗。此外,泡沫的形成和强混合产生的剪切力可能对微生物细胞产生不利影响[83]。
体积传质系数取决于许多因素,包括反应器类型、气体流量、搅拌速度和气液分散形式等。根据式(7),采用动态法测定液相中氧浓度随时间的变化,可以测定反应器对于O2的kLa值,再根据溶质渗透理论可导出CO和H2的kLa[85]。
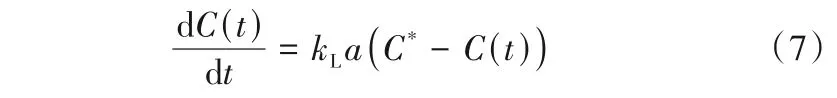
文献已经研究了几种典型反应器的体积传质系数,如连续搅拌槽反应器(CSTR)[85]、鼓泡床反应器(BCR)[23]、气升式反应器(GLR)[86]、滴流床反应器(TBR)[87]。此外,新型膜生物反应器也逐渐应用到发酵工程中,如单片膜生物反应器(MBR)[88]、中空纤维膜反应器(HFMR)[89]和水平旋转填料床膜生物反应器[90]。这些反应器没有机械运动部件,从而降低了功率输入。与搅拌槽反应器相比,鼓泡床反应器(BCR)界面面积大,具有更优的传质效果[91]。在BCR 和GLR 中,采用微气泡扩散器进行气体分散,可以大大提高传质效果;然而,这类反应器的缺点是剪切力大导致细胞生长密度有限等问题。在膜生物反应器中,提高液流速率可以显著改善传质。此外,MBR 是保持高细菌密度的理想反应器,可以进一步提高发酵效率。因此,当反应器在相似条件下运行时,MBR 比BCR 和GLR 具有更高的合成气利用效率和更快的产物生成速度[88]。然而,长期运行后可能会出现生物淤积问题,这是这类反应器的缺点之一[92]。气液体积传质系数kLa可作为比较不同反应器之间有效传质速率的重要参数。表4提供了文献所研究过的合成气发酵过程中典型反应器的kLa值。由表4 可知,与传统反应器相比,膜生物反应器在改善传质方面效果突出。此外,膜生物反应器内可以达到更大的细菌浓度,从而提高产品产量。
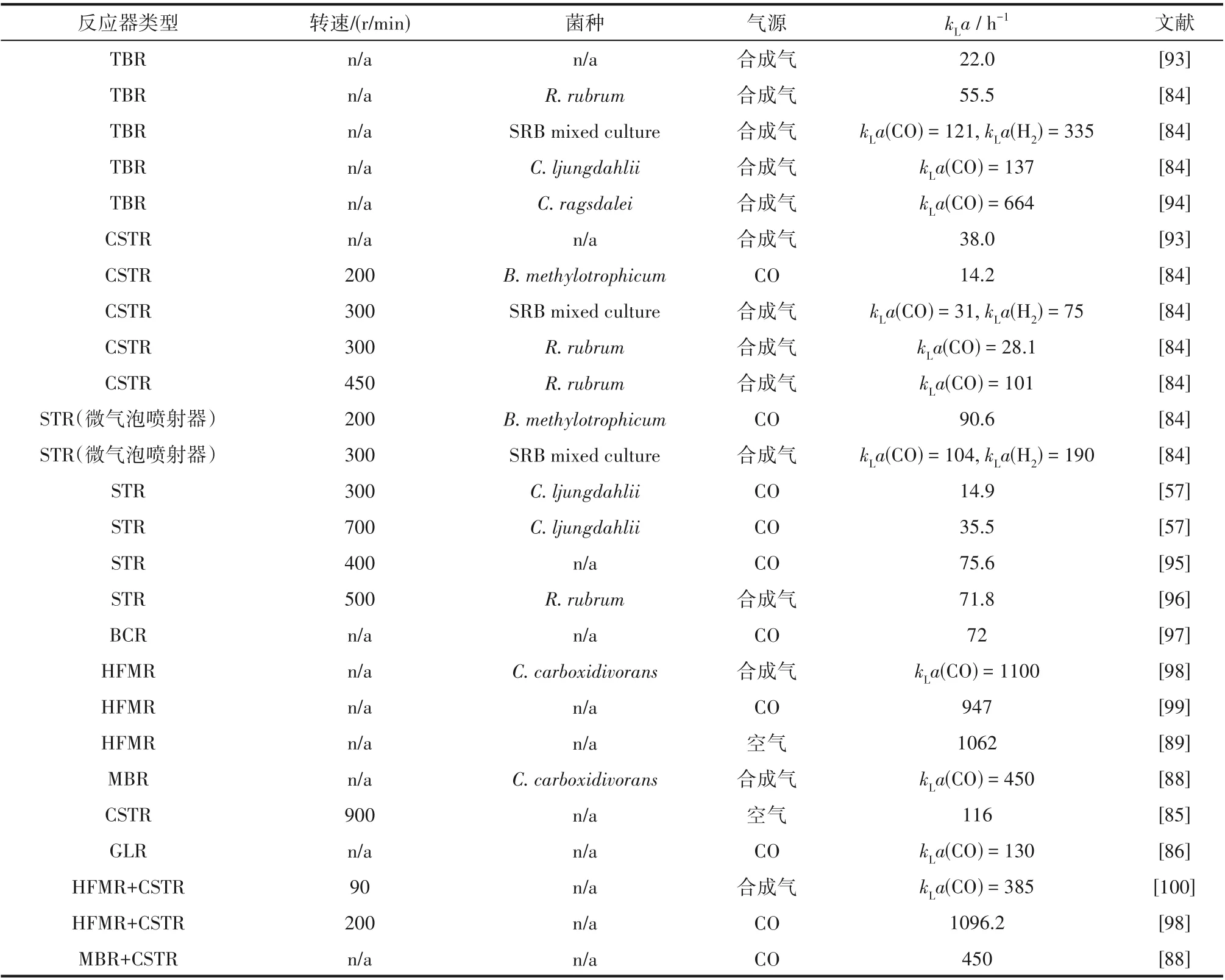
表4 合成气发酵过程中典型反应器kLa值Table 4 kLa value of typical reactors in syngas fermentation
目前,文献中报道了在不同反应器中进行的合成气发酵实验,结果总结在表5 中。综合比较发酵条件的影响可以看出,膜生物反应器由于具有突出的传质效果,与传统反应器相比可以提高乙醇产率。

表5 不同反应器类型及发酵条件下产物结果总结Table 5 Summary of products under different reactor configurations and fermentation conditions
3.2 传质强化方法
(1)添加微米和纳米颗粒。将纳米粒子添加到液相可以通过加强气液边界层混合、抑制气泡聚并和加强穿梭效应来强化传质[104]。Kim 等[105]使用CoFe2O4@SiO2-CH3纳米颗粒提高了发酵产量,与传统反应器相比,乙醇产量提高了213.5%。另外,可以通过添加包含对CO 有亲和力的官能团的纳米颗粒来增加CO 向细胞转移[106-107]。将MCM41 纳米颗粒加入到深红螺菌(Rhodospirillum rubrum)CO 发酵中,CO 传质提高了137%以上;添加含有5%硫基的颗粒,CO 传质可提高201%。Atiyeh 等[108]的专利表明,在合成气发酵培养基中添加活性炭也可以改善气体的溶解度,增强产物的生成。在3 L CSTR 中,向发酵培养基中添加活性炭(7 μm),提高了C.ragsdalei菌种转化CO和H2的能力,使乙醇产量提高了19倍。
(2)在液相中加入电解质。Zhu 等[109]在液体介质中加入电解质后,由于气泡聚并效应减少,气液界面面积增加,CO在水中的传质系数增加了4.7倍。这种作用取决于电解质的类型,阴离子对CO 传递的影响比阳离子更强,测试中最有效的电解质是CuSO4(5%(质量))。然而,这种方法只能应用于电解质不会对微生物的酶活性产生负面影响的发酵过程。
(3)设置微孔分散装置。微孔分散产生微气泡,气液传质相界面积增大。此外,由于表面张力的作用,气泡内的气体压力高于气泡外的气体压力。对于微气泡,这种附加压力更大。由于气体的溶解度与其压力成正比,附加压力下气体基质的溶解度增大,传质驱动力增大,从而使kLa和产品收率也相应增加[110]。Bredwell 等[83]研究了微气泡分散对传质的影响。结果表明,微气泡分散使体系的kLa值显著提高,约是传统分散体系的6倍。
(4)适当提高操作压力。Munasinghe 等[99]基于复合中空纤维膜生物反应器(CHF)研究了操作压力对CO 传质系数的影响。结果表明,当操作压力由5 psi(1 psi=6894.76 Pa)增大至15 psi时,不同液体循环流量下kLa均增大了2~4 倍。Stoll 等[111]详细报道了提高压力对乙醇产率的影响机理。Takors 等[112]报道,合成气发酵操作在4~5 bar(1 bar=105Pa)时经济上最适合。
4 合成气发酵法制乙醇工业化进展
自1992年以来,合成气发酵的研究和发明不断增加,这项工艺也在世界范围内受到广泛关注。目前世界上从事合成气乙醇发酵工艺规模较大的三家公司分别是新西兰的LanzaTech 公司、瑞士的INEOS Bio 公司和美国的Coskata 公司,美国的Genomatica 公司和美国的Kiverdi 公司也在寻求合成气发酵工艺的商业化[113]。然而,受限于运营和财务等困难,INEOS Bio 公司和Coskata 公司目前已经停止业务。LanzaTech 是目前在该领域工业化最成功的企业。LanzaTech报道了独有的菌种,能转化不含H2的CO 尾气,也能转化100%浓度的CO 气体。2005 年,LanzaTech 在新西兰启动了小试试验,以处理合成气和富含CO 的工业废气,用于生产乙醇和2,3-丁二醇[114]。2015 年,LanzaTech、ArcelorMittal 和Primetals Technologies 宣布在比利时根特建立一个工业规模的生物燃料生产装置,预计2022 年底建成。LanzaTech 与美国能源-太平洋西北国家实验室合作,将合成气发酵制成乙醇后再通过催化转化为新一代的可持续航空燃料,该项目于2018年取得重大进展。2011 年,北京首钢朗泽科技股份有限公司(简称首钢朗泽)利用LanzaTech 发酵技术开展工业化应用的可行性研究,并于2012年底在河北曹妃甸首钢京唐公司建成300 t/a 工业尾气发酵制乙醇全流程中试示范装置,发酵乙醇浓度达到50 g/L,CO单程转化率为85%,连续稳定运行周期超过3 个月。2018 年5 月,首钢朗泽在河北曹妃甸首钢京唐公司建设了全球首套4.5万吨/年钢铁工业尾气生物发酵法制燃料乙醇工业化示范项目,实现了从中试到工业化的突破[110]。同时,每生产1 t 乙醇联产约0.12 t菌体蛋白,粗蛋白含量大于80%,是一种优质的蛋白饲料原料,可代替鱼粉和豆粕。该项目成功实现了以工业尾气为原料工业化生产蛋白饲料,为中国蛋白饲料来源开辟了新途径,对减少大豆、鱼粉进口依赖度,保障饲料和粮食安全具有重要意义。2021 年5 月,首钢朗泽在宁夏平罗县建成全球首套4.5 万吨/年铁合金矿热炉尾气生物发酵制燃料乙醇工业化装置,跨领域应用成功,目前在贵州、宁夏等地陆续开展大规模项目的建设。
5 结论与展望
合成气生物发酵制燃料乙醇满足了生产可持续能源和降低碳排放的双重要求。与其他气体转化为燃料的方法(如F-T 合成法)相比,合成气生物发酵法操作温度和压力较低,不仅能源消耗低,而且在原料组成方面具有更大的灵活性,可利用多种工业尾气作为原料。此外,相比金属催化剂,生物催化剂对合成气中的杂质成分耐受性更好。首钢朗泽已经成功地实现了钢铁冶金行业的富含CO 工业尾气生物发酵制乙醇的技术产业化,成为该领域最大的生产企业。菌种基于Wood-Ljungdahl 途径将合成气组分(CO、H2和CO2)转化为乙醇。合成气的组成及压力、液相pH 及温度、培养基组分和气-液传质是影响合成气发酵效率、产物产率和产物分布的主要因素。如何改善气液传质限制和提高产量是合成气发酵工艺面临的关键问题。与传质特性密切相关的反应器设计是近年来研究的热点课题。本文综述了文献中典型反应器的传质性能研究和传质强化的方法,这些结果可以指导合成气发酵技术工业化的进一步改进和提高。合成气发酵工艺未来还需要在以下方面深入研究:
(1)不断优化菌株,筛选出高耐受、宽适宜环境范围的菌株;
(2)开发新型生物反应器、优化反应器设计,提高反应器传质性能与发酵产能。
