应用EP7-A2 文件探讨3 种常用中药注射液对凝血检测项目的干扰
2022-09-06齐迅捷张婧熊远辉彭梅
齐迅捷,张婧,熊远辉,彭梅
(萍乡市中医院检验科,江西 萍乡 337000)
干扰是指在临床实验中被检测物浓度因样品特性或其他成分的影响而出现的临床显著性偏差[1]。 这种影响可见于检测系统的非特异性、指示反应响应不佳、被测物活性抑制等情况.在临床实际工作中病人结果与真值间的偏离主要有三个原因,包括系统偏差、不精密度和干扰.在某种程度上由一个干扰物引起的未预料作用可使临床检验结果具有显著误差[2]。 近年来随着祖国对中医药的扶持和研究力度加大, 使得中医药领域呈现蓬勃发展趋势.更多的中医药被用于临床.有研究显示部分中药成分对血小板的凝集有抑制作用, 对凝血时间(CT)、血浆凝血酶原时间(PT)及活化部分凝血酶原时间(APTT)的检验结果均可产生干扰[3]。本研究探讨3 种中药注射液是否对凝血检测存在干扰,参照EP7-A2 文件,先采用“配对-差异”实验方案确定引起干扰的干扰物和此干扰物干扰的凝血检测项目。 再通过“剂量-效应”实验,确定干扰物浓度和干扰程度之间的关系。
1 材料与方法
1.1 仪器与试剂 Sysmex CA-7000 全自动凝血分析仪,定期进行校准。 试剂购置武汉中太生产的凝血酶原时间(PT)批号:221043;活化部分凝血活酶时间(APTT)批号:320091;凝血酶时间(TT)批号:521041;纤维蛋白酶原(FIB)批号:620101。
1.2 基础样本 收集健康体检者血浆,近期未服用任何药物、无饮酒且不吸烟的健康体检者,静脉采血后离心提取血浆混合为基础样本备用。
1.3 实验药物 对照组空白干扰物为缓冲液,干扰药物为金陵药业股份有限公司的脉络宁注射液,批号20200312; 天津天士力之骄药业有限公司的注射用丹参多酚酸(冻干粉),批号20211103;和昆明龙津药业股份有限公司的注射用灯盏花素(冻干粉),批号20210105-2。
1.4 方法
1.4.1 “配对-差异”实验方案 根据CLSI EP7-2A文件的实验方法,脉络宁注射液使用原液,注射用丹参多酚酸和注射用灯盏花素每支均用2 mL 注射用水溶解。 对照组样本使用基础血浆3.8 mL 加入空白干扰剂缓冲液0.2 mL 进行20 倍稀释;实验组样本使用基础血浆3.8 mL 分别加入药物0.2 mL进行20 倍稀释。 稀释后脉络宁注射液浓度为50 μL/mL; 注射用丹参多酚酸浓度为2.5 mg/mL,注射用灯盏花素浓度为0.25 mg/mL。计算dobs即干扰组样本均值与对照组样本均值的差计算cut-off 值dC(双侧检验)dC=如果dobs>dC,说明存在干扰。
1.4.2 计算“配对-差异”方案的实验次数 首先计算最大允许干扰值dmax/ 批内标准差S 的比值。S 由基础样本重复测定10 次计算后得出。 dmax为最大允许干扰值, 参照卫生部室间质评临床可接受范围。 得出dmax/S 比值后,查表得出n=3。 见表1。
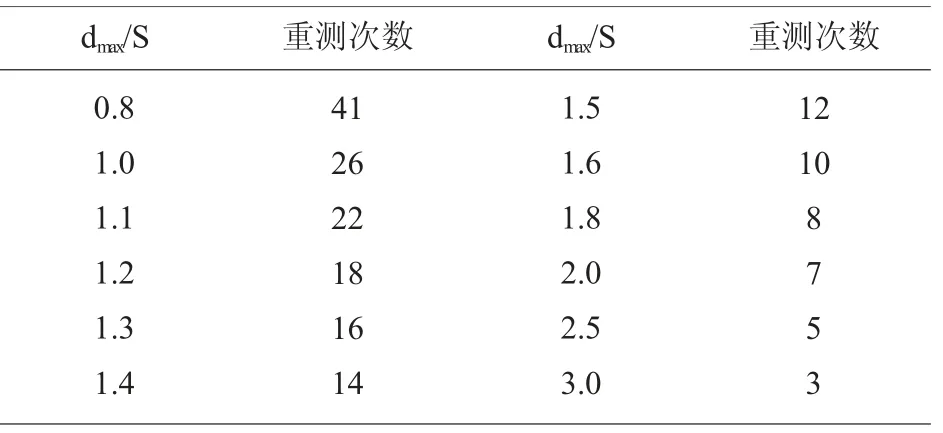
表1 dmax/S 与重测次数对应情况
1.4.3 “剂量-效应”实验方案 根据CLSI EP7-2A文件的要求确定最高浓度和最低浓度.实验过程中尽可能小的稀释测试样本,最好不超过5%,也就是原液稀释20 倍,同“配对-差异”实验所用药物浓度相同.将此浓度确定为最高浓度分别为脉络宁注射液浓度为50 μL/mL; 注射用丹参多酚酸浓度为2.5 mg/mL。 最低浓度本实验确定为 “配对-差异”实验所用对照组样本浓度为0.确定最高和最低浓度样本后, 将低浓度和高浓度样本等体积混匀,配成中间浓度样本。 将低浓度和中间浓度样本等体积混匀,配成25%浓度的样本。 将中间浓度和高浓度样本等体积混匀,配成75%浓度的样本,见表2。做剂量效应曲线时在每个测试浓度水平上重复测试3 次。 在同一种干扰药物分析批内测定5个样本,为了平均系统漂移影响,测定顺序第一次按照升序测定,第二次按照降序测定,第三次按照升序测定。
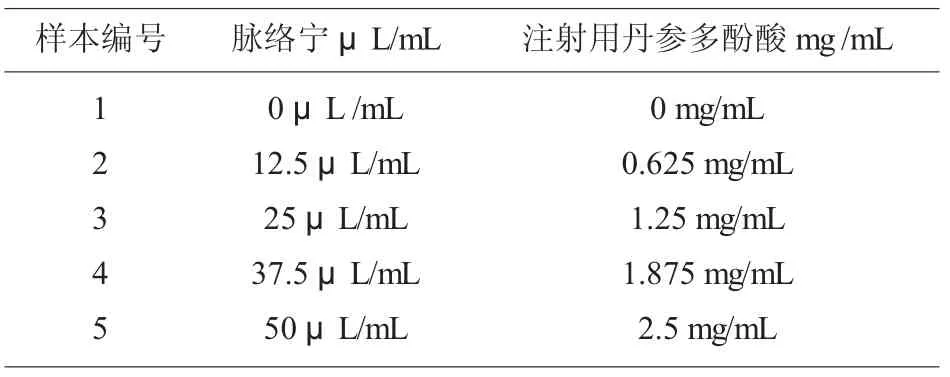
表2 两种中药注射液的5 个浓度梯度的浓度值
1.5 统计学分析 应用SPSS 22.0 软件计算dmax/S、dobs、dC值、药物浓度与干扰效应的线性方程和相关系数。
2 结果
2.1 “配对-差异”实验结果 根据3 种中药注射液“配对-差异” 实验的对照组和干扰组的PT、FIB、TT、APTT 的检测数据计算dobs和dC,根据dobs和dC分析每种药物对凝血检测项目是否存在干扰.干扰物 为 脉 络 宁 注 射 液 的 样 本PT、FIB、TT、APTT 的dobs>dC,均存在干扰。 并且TT、APTT 是负干扰,PT、FIB 是正干扰,见表3。 干扰物为注射用灯盏花素的样本PT、FIB、TT、APTT 的dobs≤dC都不存在干扰现象,见表4。 干扰物为注射用丹参多酚酸的样本PT、FIB、TT、APTT 的dobs>dC,均存在干扰。 并且TT是负干扰,PT、FIB、APTT 是正干扰,见表5。
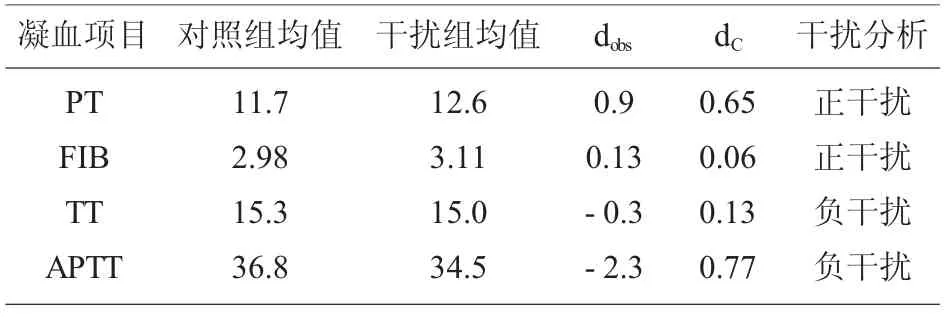
表3 脉络宁注射液对凝血功能检测的干扰
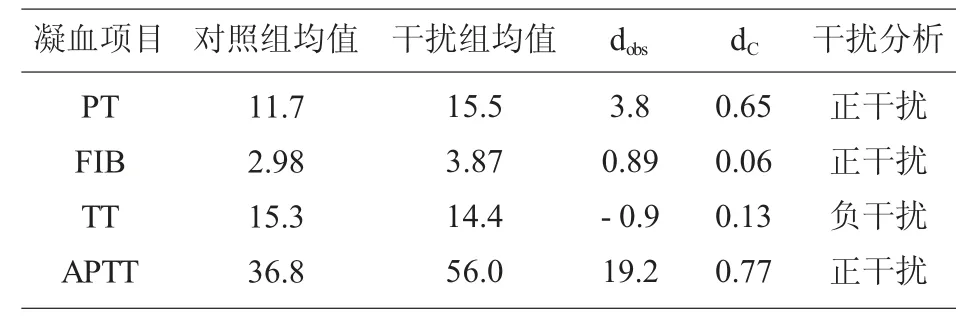
表5 注射用丹参多酚酸对凝血功能检测的干扰
2.2 “剂量-效应”实验结果 脉络宁注射液和注射用丹参多酚酸对凝血检测项目PT、FIB、TT、APTT测定的干扰剂量-效应实验均呈线性关系,脉络宁对PT 和FIB 的干扰为正相关。 对TT 和APTT 的干扰为负相关。 注射用丹参多酚酸对PT、FIB、APTT 的干扰为正相关,对TT 的干扰为负相关,见表6。

表6 两种中药注射液干扰剂量- 效应的相关系数和回归方程
3 讨论
患者在临床治疗过程中, 会使用大量或多量品种不同的治疗药物, 这些药物对临床医学检验结果的准确性会造成影响.而临床检验结果对临床疾病的诊断和疗效观察等越来越重要[4-7]。 了解药物对检验结果的影响, 不但可以合理地分析判断检验结果, 而且可以通过适当的检验方法克服这种影响[8-10]。目前,有研究显示西药抗生素对凝血检测项目有较大的干扰[11-12]。2005 年美国临床实验室标准化协会(CLSI)通过了EP7-A2 文件,使干扰研究有了标准化的实验方案。 有学者运用此文件研究了乳糜标本对D-二聚体检测项目的干扰[13]。 本研究运用EP7-A2 文件对脉络宁注射液、注射用丹参多酚酸、 注射用灯盏花素3 种中药注射液是否对凝血检测项目产生干扰进行系统性的研究。 先通过“配对-差异”实验筛选出对凝血检测项目存在干扰的脉络宁注射液和注射用丹参多酚酸,并且脉络宁对PT 和FIB 的干扰为正干扰, 对TT 和APTT 的干扰为负干扰。 注射用丹参多酚酸对PT、FIB、APTT 的干扰为正干扰, 对TT 的干扰为负干扰。 由于按照“配对-差异”实验的要求采用的药物干扰浓度为单瓶药物剂量的20 倍稀释后的浓度,注射用灯盏花素临床用药剂量是每次2~5 瓶静脉输注, 而脉络宁注射液和注射用丹参多酚酸则是每次1 瓶剂量静脉输注, 因此灯盏花素可能由于剂量小的原因没有出现干扰现象。 运用“剂量-效应” 实验对上述2 种筛选出产生干扰的中药注射液进行浓度与凝血检测干扰效应之间的关系进行研究。 脉络宁注射液和注射用丹参多酚酸对凝血检测项目PT、FIB、TT、APTT 测定的干扰剂量-效应实验均呈线性关系。
但是,EP7-A2 文件推荐的“配对-差异”实验方案和“剂量-效应”实验方案也存在局限性[14],干扰筛选的“配对-差异”实验是体外加入的干扰物,干扰物的浓度应该尽量接近临床治疗状态下的最高血药浓度[15],实际上加入的干扰物并不等同于在人体内的循环状态下存在的药物的状态和浓度。并且对样本产生干扰的可能不是药物本身而是药物的代谢产物。 “剂量-效应”实验方案中的最高浓度和最低浓度的设定也不能真实反应用药前后的人体内出现的最高浓度和最低浓度。 而第三种“利用患者样本作偏倚分析” 实验方案是目前看起来最能够检测药物或者药物代谢产物干扰的方法,但是实验的可控操作性不强。 例如,患者可能服用多种药物和其他食物等, 不能确定哪种药物或食物产生的干扰。 另外药物在病人体内的代谢速度也是存在一定的个体差异的。
本研究的3 种中药注射液均为活血化瘀类药物, 由于此类药物对凝血系统的作用不同于西药作用于特定的凝血因子或者凝血过程中特定的靶点,而是多成分、多靶点、多维度的作用,作用机制较复杂[16]。具体干扰凝血检测的原理有待进一步检测某些凝血因子, 另外结合血栓弹力图和血液流变学的结果进行综合分析。 本研究由于条件有限仅只进行前期的干扰试验。 在临床实际工作中,当凝血检测结果与患者临床症状不相符并且未出现其他并发症,且在室内质控合格的前提下,排除采血、标本运送、温度、离心等因素外,应该考虑患者是否运用了对凝血检验结果造成干扰的药物。 并且不应该只关注西药类的影响, 还应重视活血化瘀类中药的临床使用剂量是否会对凝血检测结果产生影响。 综合分析检测报告与临床实际的症状和病情的发生发展。
