血清尿酸内部参考方法的建立及常规测量系统正确度评价
2022-09-06李文娟王珊黄婷婷梁海港薛绍礼
李文娟,王珊,黄婷婷,梁海港,薛绍礼
(1 安徽伊普诺康生物技术股份有限公司;2 安徽医科大学生物工程系, 安徽 合肥 230000)
人体尿酸(Uric acid, UA)是嘌呤代谢的终产物,为三氧基嘌呤,又称2,4,6-三羟基嘌呤。越来越多的研究表明,人体尿酸含量升高与肾功能减退、血脂升高、心血管疾病和急性痛风性关节炎[1-10]等息息相关。 尿酸检测是临床常规测量项目之一,目前尿酸的检测方法主要有液相色谱法、 磷钨酸法和尿酸酶法等[10-18]。其中同位素稀释液相色谱/质谱法,是具有最高计量学溯源性的方法,但是该方法运行成本高,仪器设备操作复杂,在常规实验室难以实现[17-18]。 磷钨酸法是根据尿酸在碱性溶液中被磷钨酸氧化生成尿囊素及二氧化碳, 磷钨酸则被还原生成钨蓝,可利用比色法根据660 nm 处吸光度的变化来测定尿酸的含量。 该方法由于存在特异性不强、 测定线性范围窄以及受其他还原试剂影响等局限性,目前已经很少使用[13]。 尿酸酶法的反应原理为尿酸酶催化尿酸生成尿囊素和过氧化氢, 根据尿酸于293 nm 处的特征吸收来测定尿酸的含量。 该方法由于具有准确度高、精密度好、抗干扰能力强等优点而成为目前检测尿酸应用最为广泛的方法[14-16],美国临床化学协会标准委员会(American Association for Clinical Chemistry, AACC) 于1973 年提出将尿酸酶法作为候选参考方法。 笔者在1982 年Patricia Duncan 等[19-20]工作的基础上,建立了人血清尿酸内部参考方法, 研究了其准确度、精密度,并通过方法学比对来评价常规测量系统的准确性,以用于尿酸的量值溯源和标准化。
1 材料与方法
1.1 仪器 日本岛津UV2700 型紫外可见分光光度计、瑞士梅特勒XSE205DU 型分析天平、瑞士梅特勒型S220 pH 计、德国Eppendorf 移液器、盐城凯特离心机、日本ASONE 容量瓶。
1.2 试剂 Tris-Base、Tris-HCl、三氯乙酸均购自美国Sigma 公司;尿酸酶购自瑞士Sorachim 公司。 有证标准物质SRM 913b 和SRM 909c 均购自美国国家标准与技术研究院(NIST);2018 年UA 国际参考实验室室间比对样本RELA A 和RELA B 由IFCC 提供。
1.3 方法
1.3.1 尿酸一级标准贮备液的配制及适用性实验根据参考文献[1]配制浓度为100 mg/dL 的尿酸一级标准贮备液,并将其稀释100 倍,于293 nm 处检测其吸光度,若超过0.750±0.010 A,则需重新配制。
1.3.2 尿酸工作标准液的配制及适用性实验 用验证合格的100 mg/dL 的尿酸一级标准贮备液按照要求制备梯度工作标准液,见表1。
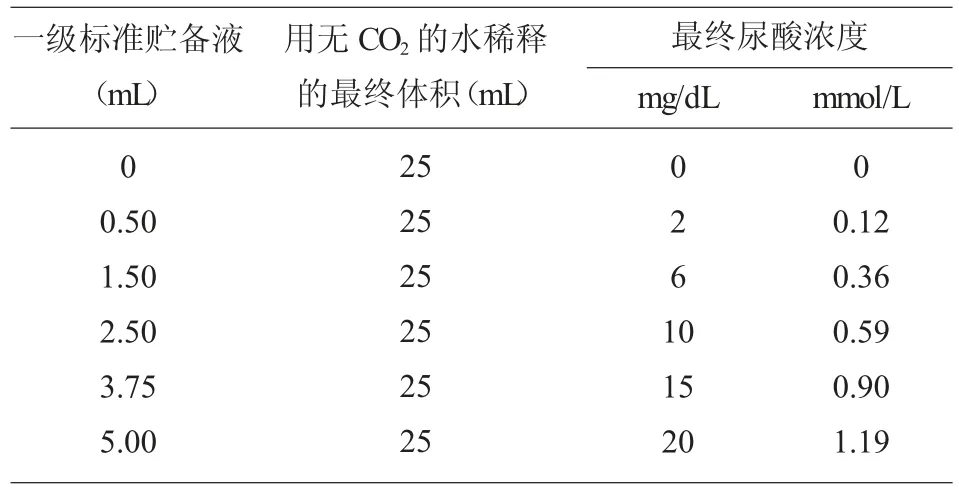
表1 尿酸标准梯度工作标准液配制
用无CO2的水将上述尿酸梯度工作标准液稀释10 倍,于293 nm 处,用无CO2的水调零,测定各梯度工作标准液稀释液的吸光度, 每个梯度稀释液平行测定2 次。 要求各梯度工作标准液稀释液的实测吸光度均值与理论吸光度之比在99%~101%之间, 且每次实测吸光度与与实测吸光度均值之比在98%~102%之间。
1.3.3 尿酸酶活性检测37℃时尿酸酶活性检测步骤,见表2。 后将空白溶液转移至参比池和反应池,于293 nm 处调零;同时将反应溶液A 和反应溶液B 置于37±1 ℃温浴30 min 后, 再将反应溶液B 加到反应溶液A 中,混匀,于37 ℃,293 nm处连续监测5 min。 并依据公式尿酸酶贮备液的酶活μmol/min/mL, 计算尿酸酶贮备液的酶活性。尿酸的摩尔消光系数= 1.2418×104(0.1 mol/L Tris Buffer, pH = 8.5 at 37 ℃)。

表2 尿酸酶活性检测
1.3.4 尿酸含量的测定 根据对测定样本进行处理后, 轻轻混匀室温静置45 min 后于1400 xg 离心40 min,取上清液于293 nm 处检测吸光度,见表3。

表3 尿酸样本含量检测
1.3.5 结果计算 标准曲线的绘制 以梯度工作标准液浓度值为横坐标(x),对应的测定校正吸光度均值为纵坐标(y),根据最小二乘法进行回归作图,得到回归方程,吸光度A(Y)=b×浓度(X)+a,其斜率(b)、截距(a)。 其中每个梯度工作标准液和未知样本的空白吸光度减去实验吸光度, 即可得到其对应的校正吸光度。
1.3.6 精密度验证实验 取2018 年RELA A、2018年RELA B、朗道生化校准血清,在同一天平行测定8 次,分别计算3 份样本的测定不精密度。
1.3.7 准确度验证实验 通过测定2018 年RELA A、2018 年RELA B 和SRM 909c,计算实测值与参考值之间的相对偏倚。
1.3.8 常规测量系统正确度评价实验 通过采用内部参考方法和常规测量系统同时测定40 例不同浓度梯度的血清样本, 以内部参考方法测定值为横坐标,常规测量系统测定值为纵坐标作图,根据线性方程的斜率和相关系数来判断常规测量系统的正确度。
2 结果
2.1 尿酸标准贮备液吸光度验证 尿酸一级标准贮备液稀释100 倍后实测吸光度均值为0.759,在0.750±0.010 A 范围内。
2.2 尿酸梯度工作标准液吸光度验证 根据1.3.2所述方法测定梯度工作标准液,见表4。 从表中可以看出各梯度工作标准液稀释液的实测吸光度均值与理论吸光度之比在99%~101%之间,且每次实测吸光度与与实测吸光度均值之比在98%~102%之间。
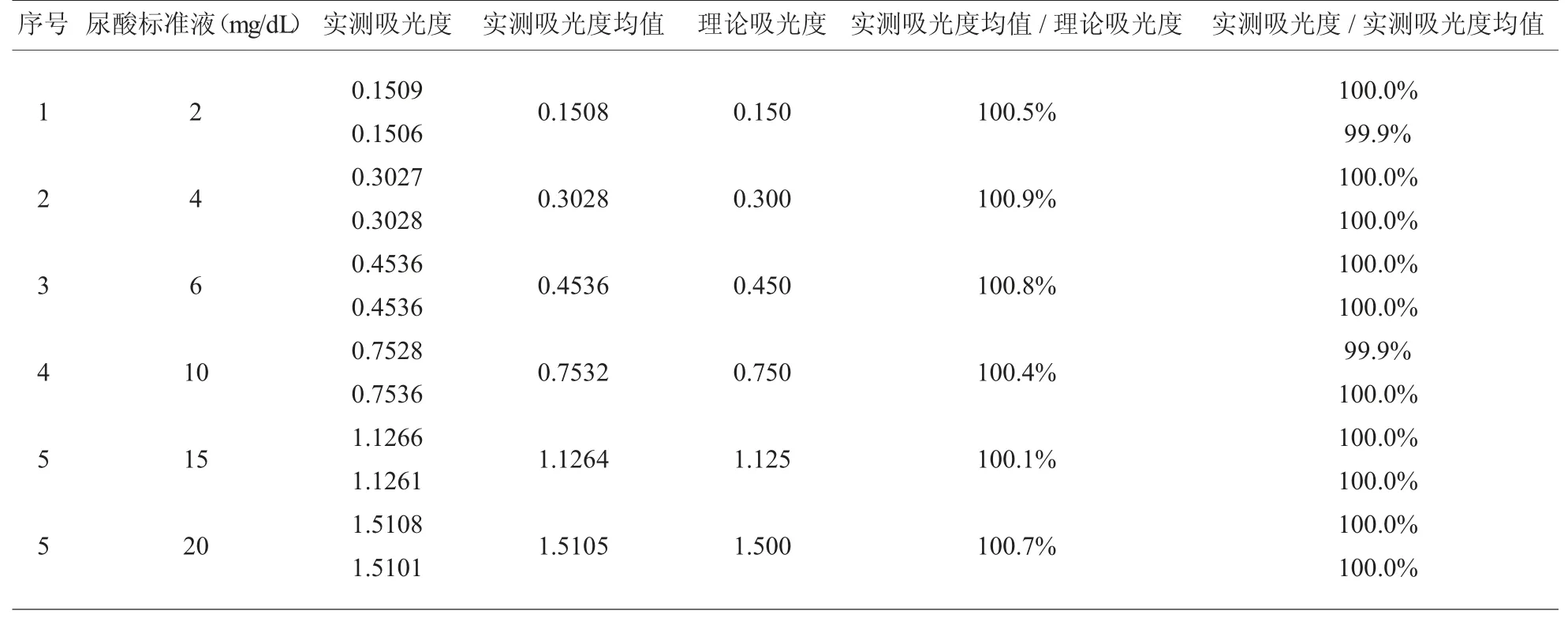
表4 尿酸各梯度工作标准液稀释液测定结果
2.3 线性验证 根据1.3.4 所述方法测定梯度工作标准液,见表5。从表中可以看出,各梯度工作标准液实测浓度与理论浓度的差值均小于±0.15 mg/L,符合要求。 以梯度工作标准液理论浓度值为横坐标(x),对应的实测吸光度均值为纵坐标(y)作图,见图1。 标准曲线的线性方程为 Y=0.0590X+0.0003,R2=1.0000,斜率b 为0.0590,截距a 为0.0003,斜率应该在0.058±0.003 范围内[16],截距应该在0.000 ± 0.005 范围内[16],相关系数不小于0.9995的要求。

表5 尿酸标准曲线测定结果
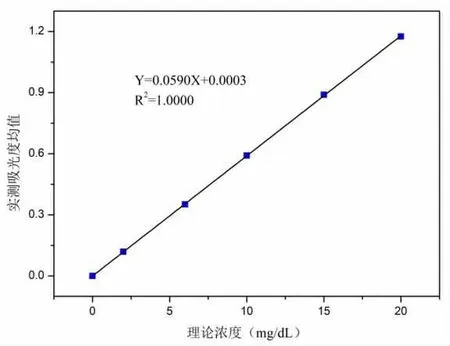
图1 参考方法测定尿酸浓度标准曲线图
2.4 精密度验证 取2018 年RELA A、2018 年RELA B、朗道生化校准血清,在同一天平行测定8次,3 份样本的不精密度(CV)均小于1.0%,见表6,说明该方法具有良好的精密度。
2.5 准确度验证 2018 年RELA A、2018 年RELA B 和SRM 909c 的实测结果以及与参考值的相对偏倚,见表6。从表中可以看出该方法准确度良好。

表6 准确度验证结果
2.6 常规测量系统正确度评价 通过采用内部参考方法和常规测量系统同时测定40 例不同浓度梯度的血清样本, 以内部参考方法测定值为横坐标,常规测量系统测定值为纵坐标作图,见图2。从图中可以看出,线性方程的斜率为0.9686,且相关系数R2为0.9874, 说明内部参考方法和常规测量系统一致性良好。

图2 厂家选定测量方法和常规方法体系相关图
3 讨论
本研究建立的内部血清尿酸参考方法是基于尿酸酶法, 采用紫外可见分光光度计进行测定的方法。 其反应原理为尿酸在尿酸酶催化下,生成尿囊素、 过氧化氢和二氧化碳, 由于尿酸在293 nm处有特征紫外吸收,尿囊素则无,因此,可根据293 nm 处反应前后溶液吸光度的变化来定量测定样本中尿酸的含量。 相较于同位素稀释液相色谱/质谱法,该方法对仪器设备要求较低,更易在常规实验室实现。
参考方法的性能评价主要是指精密度和准确度,目前国际上尚无统一规定,但基本原则是参考方法的精密度和准确度要优于常规方法。 精密度是方法可靠的前提之一, 本研究通过测定朗道生化校准血清以及国际参考实验室能力验证(RELA)样本来评估本方法的精密度,其不精密度均<1%,说明本方法对不同性状及基质成分的样本均表现出良好的精密度。
准确度是方法可靠的关键, 本研究允许偏倚为等效限的1/2。 本研究分析有证参考物质SRM 909c 和国际参考实验室能力验证(RELA)样本偏倚均在允许偏倚范围内, 说明该方法具有良好的准确度。
建立参考方法的最终目的是实现检验结果的溯源性, 故本研究对常规测量系统的正确度开展了评估。 结果表明常规测量系统和参考方法具有良好的一致性, 说明常规测量系统具有良好的正确度,实现了检验结果的溯源性。
综上所述,建立的血清尿酸内部参考方法,精密度和准确度明显优于常规测量系统,且该方法可用于评价常规测量系统的正确度,为血清尿酸常规测量程序检测结果溯源性提供了有效的途径。
