《第5版WHO 造血淋巴肿瘤分类:髓系和组织细胞/树突细胞肿瘤》解读*
2022-09-06叶向军唐海飞卢兴国吴建国浙江大学医学院附属第四医院检验科浙江义乌000兰溪市人民医院检验科浙江兰溪00浙江大学医学院附属第二医院检验科浙江杭州0000
叶向军,唐海飞,卢兴国,吴建国(.浙江大学医学院附属第四医院检验科,浙江义乌 000;.兰溪市人民医院检验科,浙江兰溪 00;.浙江大学医学院附属第二医院检验科,浙江杭州 0000)
2017年WHO造血淋巴肿瘤分类更新之后,肿瘤的基础和临床研究又取得了很多进展,故对分类更新的需求已变得越来越强烈。尤其自2019年开始陆续出版第5 版WHO肿瘤分类系列蓝皮书以来,造血淋巴肿瘤分卷的出版也被提到日程上[1-3]。自2021 年6 月第5 版WHO 造血淋巴肿瘤分类第一次编委会会议后,经过一年时间,基本完成该卷编写,并经国际癌症研究机构(International Agency for Research on Cancer,IARC)的编辑检查和技术编辑后在线上提供测试版,印刷书籍也将在2022年底出版[3]。
根据已经基本确定的第5 版WHO 造血淋巴肿瘤分类蓝皮书,《Leukemia》杂志及时推出介绍文章。本文主要根据该期刊在线发表的这2 篇文章及其所引用的原始文献,以及IARC官网发布的分类初始大纲(目录),解读《第5 版WHO造血淋巴肿瘤分类:髓系和组织细胞/树突细胞肿瘤》[4],对第5版WHO造血淋巴肿瘤分类在基本原理,层次结构,以及各类髓系和组织细胞/树突细胞肿瘤中名称、定义、诊断或分类标准、归属等[4-5]重要变化作介绍。
1 分类基本原理
第5版WHO分类首次在包含全部人类癌症的、围绕增强的层次分类法组织的、统一关系数据库框架内开发。分类(蓝皮书)中的疾病在此新框架内按分类原则和包括过程透明度、书目严谨性和避免偏见等一套规定内容按层次分类[4-5]。尽可能系统地应用3个属性,即:系列+主要临床属性+主要生物学属性定义疾病。系列归属依赖于流式细胞术和/或免疫组织化学染色的免疫表型分析。主要临床属性是未治疗疾病的一般特征,包括诸如急性、慢性、血细胞减少(骨髓增生异常)和细胞增多(骨髓增殖)等描述。大多数生物学属性包括基因融合、重排和突变。当融合的2个牵连基因共同作为诊断标准(如PML:RARA)时,基因融合作为类型/亚型名称的一部分。重排则是某个生物学显性基因(如KMT2A)存在多个融合伙伴基因,这一基因作为类型/亚型名称的一部分。
新版分类依旧应用基于整合形态学(细胞学和组织学)、免疫表型、分子和细胞遗传学数据来确定分类。由于分子机制认识的积累,增加了许多分子定义的疾病类型和亚型。为了促进实用的诊断方法,同时也鼓励在需要时采用分子检测,每个实体的“基本”和“理想”诊断标准以分层方式定义。“基本标准”是允许尽可能普遍地诊断实体的最低标准,尽管某些实体不可避免地包括分子标准。“理想标准”是那些有助于确认和完善诊断的标准,通常需要应用先进的分子技术。分类还遵循人类基因组组织基因命名委员会的书写建议,包括使用双冒号(∷)标记融合基因[4]。计量单位也将统一使用国际单位[3]。
2 层次结构
新分类顺序依然先根据细胞系列分出大类。由于认识到组织细胞/树突细胞肿瘤源自产生单核细胞/组织细胞/树突细胞系列的普通髓系祖细胞,故这一类肿瘤现紧跟在髓系肿瘤之后。在相同细胞系列中,一般按先从良性(肿瘤前病变或肿瘤样病变)到恶性,先遗传学特征明确的,其次遗传学特征不明确的等顺序。在按细胞分化定义的急性髓系白血病类型中则仍沿袭传统次序。为了防止对淋巴瘤的过度诊断和提高对临床病理学不同实体的识别,模拟淋巴瘤或代表重要鉴别诊断的非肿瘤疾病也首次被纳入分类。分类的层次大致提供到类别(例如,成熟B细胞淋巴瘤)、家族/种类(例如,大B细胞淋巴瘤)、实体/类型(例如,弥漫大B细胞淋巴瘤,非特定型)和亚型(例如,弥漫大B 细胞淋巴瘤,非特定型,生发中心B细胞样)4个等级。有些包括变异型,它们一般只有明显的形态学特征,缺乏分子生物学特征。
3 各类髓系和组织细胞/树突细胞肿瘤中名称、定义、诊断或分类标准、归属等重要变化
3.1 髓系肿瘤部分
3.1.1 克隆性造血 克隆性造血(clonal haematopoiesis,CH)由具有起始驱动突变的细胞扩增引起的,可能是造血系统老化的一个方面[6]。CH 包括不确定潜能的克隆性造血(clonal haematopoiesis of indeterminate potential,CHIP)和意义未明克隆性血细胞减少(clonal cytopenia of undetermined significance,CCUS),前者无血细胞减少,后者有持续性血细胞减少。CCUS、骨髓增生异常肿瘤(myelodysplastic neoplasms,MDS)和骨髓增生异常/骨髓增殖性肿瘤(myelodysplastic/myeloproliferative neoplasms,MDS/MPN)对血细胞减少的定义进行了协调。男性Hb<130 g/L,女性<120 g/L为贫血,中性粒细胞绝对计数<1.8×109/L为白细胞减少,血小板<150×109/L为血小板减少。
3.1.2 骨髓增殖性肿瘤 骨髓增殖性肿瘤(myeloproliferative neoplasms,MPN)中慢性粒细胞白血病(chronic myeloid leukaemia,CML)的加速期,因意义不明显,这一分期被废弃。在真性红细胞增多症(polycythaemia vera,PV)诊断中,由于用51Cr标记红细胞来确定红细胞量增加在常规临床实践中少用,不再作为诊断标准。慢性嗜酸性粒细胞白血病(chronic eosinophilic leukaemia,CEL)的诊断标准作了以下修改:(1)定义嗜酸性粒细胞持续性增多的时间从6 个月减至4周;(2)增加对克隆性和异常骨髓形态的要求(如巨核细胞或红系病态造血);(3)取消原始细胞增加(外周血≥2%或骨髓5%~19%)作为判断克隆性的替代方法。这些标准提高了CEL与特发性嗜酸性粒细胞增多综合征和意义未明嗜酸性粒细胞增多症等实体之间的区别,因此原来的“CEL,非特定类型”(CEL,not otherwise specified)改称CEL。幼年型粒单核细胞白血病(juvenile myelomonocytic leukaemia,JMML)认为是儿童早期MPN,与胚系致病基因变异频繁相关。实际上无MDS特征,故从原来的MDS/MPN归入MPN。诊断标准的更新包括:(1)排除KMT2A 重排;(2)消除作为细胞遗传学标准的7号染色体单体;(3)强调诊断性分子研究,特别是RAS通路激活的研究的重要性。
3.1.3 肥大细胞增多症 肥大细胞增多症中系统性肥大细胞增多症(systemic mastocytosis,SM)的诊断标准中表达CD30和存在任何导致非配体依赖性激活的KIT突变已被作为次要诊断标准。基础血清类胰蛋白酶水平>20 ng/mL 这条次要标准,在遗传性α-色氨酸血症的情况下应进行调整,即将基础类胰蛋白酶水平除以1加上α类胰蛋白酶基因的额外拷贝数。例如,当类胰蛋白酶水平为30 ng/mL,且患遗传性α-色氨酸血症患者中发现2个额外的α类胰蛋白酶基因拷贝,校正的类胰蛋白酶水平为30/(1+2)=10,因此未达到这条次要标准[7]。
3.1.4 骨髓增生异常肿瘤 骨髓增生异常综合征改称骨髓增生异常肿瘤(缩写仍为MDS)。这些克隆性造血肿瘤由血细胞减少和形态发育异常定义。血细胞减少定义同CCUS。所有系列的病态造血阈值都推荐为10%。MDS首先分为伴定义遗传学异常的实体和形态学定义的实体(表1)。

表1 MDS分类和定义特征
MDS伴低原始细胞和SF3B1突变作为一种独特的疾病类型,需要有SF3B1突变[8]。野生型SF3B1 的环形铁粒幼细胞≥15%的低原始细胞MDS,仍然可以称伴低原始细胞和环形铁粒幼细胞MDS作为替代名称,这些病例可包含其他RNA剪接组件中的驱动突变。
TP53双等位基因(biTP53)改变可包括多重突变或者突变同时伴另一个等位基因的缺失,突变导致肿瘤克隆缺乏任何残留的野生型p53蛋白。
低增生MDS(MDS-h)作为新的独特的MDS类型,被认为与T细胞介导的对造血干细胞和祖细胞的免疫攻击以及过度产生γ-IFN和/或α-TNF的CD8+细胞毒性T细胞的寡克隆扩增有关。
MDS中病态造血的系列数通常是动态过程,代表克隆进展的临床和表型表现——而不是本身定义特定的MDS类型,现在被认单系和多系病态造血之间的区别是可选的。因为更新的MDS分类方案以及在分类中加入CCUS,不能分类型MDS现已淘汰。
第5 版分类中定义AML 的20%原始细胞切点值被保留,但普遍认为MDS-IB2 治疗上和适当的临床试验设计的角度与AML意义等同。
儿童期MDS中伴低原始细胞儿童MDS取代之前“儿童难治性血细胞减少症”,并包括2 个亚型:伴低原始细胞儿童MDS,增生减低和伴低原始细胞儿童MDS,NOS。伴原始细胞增多儿童MDS和伴低原始细胞儿童MDS 的遗传图谱相似,都不同于成人MDS。
3.1.5 骨髓增生异常/骨髓增殖性肿瘤 MDS/MPN类型现包括4种类型:慢性粒单核细胞白血病(chronic myelomonocytic leukaemia,CMML),伴 中 性 粒 细 胞 增 多MDS/MPN,伴SF3B1突变和血小板增多MDS/MPN,以及MDS/MPN,NOS。
修订后的CMML诊断标准中,单核细胞绝对增多的切点从1.0×109/L 降低到0.5×109/L。并正式认可根据WBC区分的2 种CMML 亚型:骨髓增生异常型(WBC <13×109/L)和骨髓增殖型(WBC≥13×109/L)。上一版中增加的CMML-0亚组(血液中原始细胞<2%和骨髓中<5%)又被废弃。见表2。

表2 慢性粒单核细胞白血病的诊断标准
不典型慢性粒细胞白血病更名为MDS/MPN 伴中性粒细胞增多,MDS/MPN伴环形铁粒幼细胞和血小板增多新命名为MDS/MPN 伴SF3B1 突变和血小板增多。MDS/MPN伴环形铁粒幼细胞和血小板增多一词被保留为可接受的术语,用于野生型SF3B1 且环形铁粒幼细胞≥15%的病例。不可分类型MDS/MPN现在称为MDS/MPN,非特定类型。
3.1.6 急性髓系白血病 急性髓系白血病(acute myeloid leukaemia,AML)现主要分为AML 伴定义遗传学异常与AML,由细胞分化定义(见表3)。AML 伴定义遗传学异常类型中,除AML伴BCR∷ABL1融合和AML伴CEBPA突变外,不再要求原始细胞≥20%(AML 伴CEBPA 突变预后良好,而BCR∷ABL1 中原始细胞则对CML 有区别意义)。AML伴CEBPA突变的定义包括双等位基因(biCEBPA)以及位于碱性亮氨酸拉链(bZIP)区域的单突变(smbZIP-CEBPA)。

表3 急性髓系白血病分类
之前AML伴骨髓增生异常相关改变,现称为“AML,骨髓增生异常相关(AML-MR)”。这一AML类型被定义为表达髓系免疫表型的原始细胞≥20%并具有与MDS相关的特定细胞遗传学和分子异常的肿瘤,新发或继发于MDS 或MDS/MPN之后。主要变化包括:(1)取消形态学单独作为诊断AML-MR的诊断前提;(2)更新定义细胞遗传学标准;(3)引入基于一组8 个基因作为基因突变的定义,在MDS或MDS/MPN 后出现的AML 中有>95%特异性。诊断AML-MR需要存在表4 中列出的一种或多种细胞遗传学或分子异常和/或MDS 或MDS/MPN 病史。由分化定义的急性髓系白血病类型的细胞分化标志物及标准见表5。
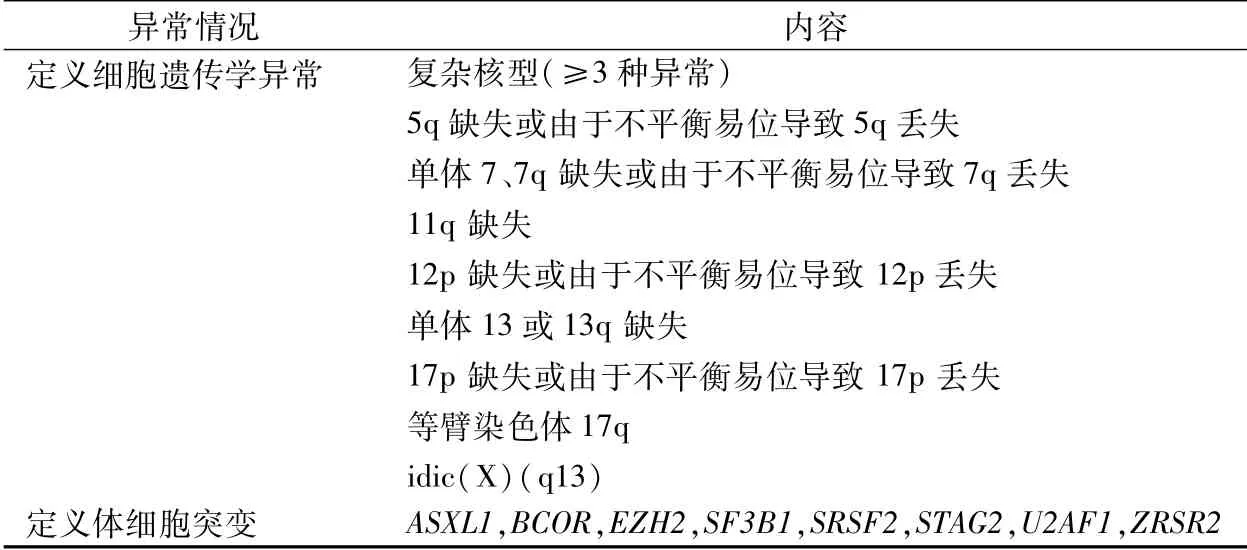
表4 定义急性髓系白血病的骨髓增生异常相关细胞遗传学和分子学异常

表5 由分化定义的急性髓系白血病类型的细胞分化标志物及标准
急性红系白血病(acute erythroid leukaemia,AEL)是一种以伴成熟停滞和高频率TP53基因双等位改变的红系细胞肿瘤性增殖为特征的独特AML类型。新分类强调了TP53双等位基因突变在这种侵袭性AML类型中的核心作用。
3.1.7 继发性髓系肿瘤 继发于细胞毒治疗或胚系易感性的髓系肿瘤被归入此类。MPN的AML转化保留在MPN类别中,而MDS和MDS/MPN的AML转化则在AML-MR下。治疗相关髓系肿瘤改称细胞毒治疗后髓系肿瘤(myeloid neoplasms post cytotoxic therapy,MN-pCT)。诊断尽可能详细说明髓系肿瘤的类型,并附上附录“细胞毒治疗后”,例如细胞毒治疗后CMML。PARP1抑制剂暴露被作为MN-pCT的合格标准。
伴胚系易感性相关髓系肿瘤的诊断框架按照可适应未来改进和发现的可扩展模型进行了重组。现分为伴胚系易感性无先前血小板疾病或器官功能障碍髓系肿瘤,伴胚系易感性和先前血小板疾病髓系肿瘤和伴胚系易感性和潜在器官功能障碍髓系肿瘤3种。
3.1.8 髓系/淋系肿瘤伴嗜酸性粒细胞增多和酪氨酸激酶基因融合 髓系/淋系肿瘤伴嗜酸性粒细胞增多和酪氨酸激酶基因融合(MLN-TK)名称与修订第4版不同,基因也有所增加或修改。承认伴JAK2 重排、FLT3 重排和ETV6∷ABL1融合新类型,并引入伴其他明确的酪氨酸激酶融合MLN-TK新的可扩展的遗传学框架。
3.1.9 混合或不明系列急性白血病 不明系列急性白血病(acute leukemia of ambiguous lineage,ALAL)和混合表型急性白血病(mixedphenotype acute leukaemia,MPAL)也增加了分子分类的框架,新分类见表6。
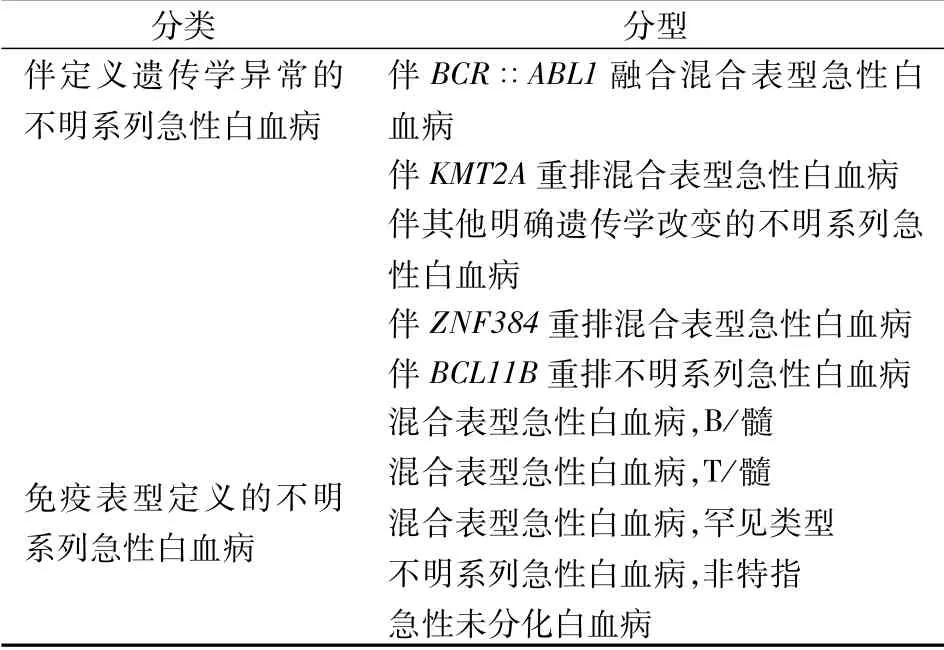
表6 不明系列急性白血病分类
通过免疫表型分析确定系列取决于每种抗原与被评估系列之间的关联强度。作为一般原则,某一抗原的表达强度和/或模式越接近最相似的正常细胞群,就越能保证反映该系列。例如,与均一的弱表达髓过氧化物酶相比,髓过氧化物酶表达强度和模式不一反而与早期髓系成熟中所见更相似,与髓系系列更强烈相关。此外,证明来自同一系列的多个抗原的协调表达模式进一步提高了这些抗原在系列归属中的特异性。鉴于这些原则,在单一系列不明显的情况下用于系列归属的免疫表型标准进行了修订,见表7。
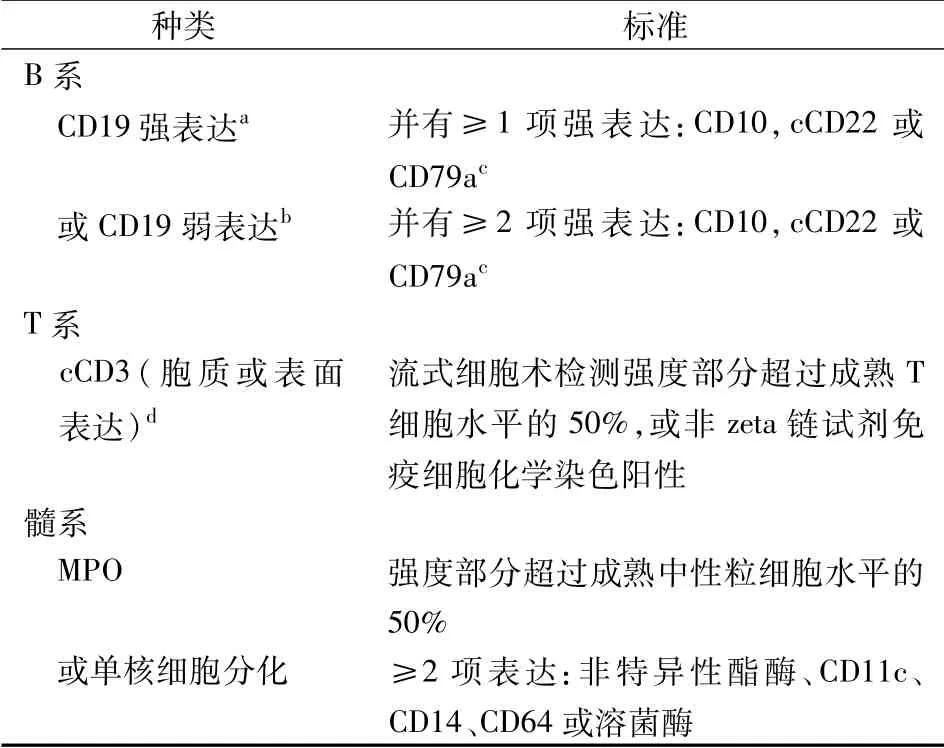
表7 混合表型急性白血病的系列归属标准
3.2 组织细胞/树突细胞肿瘤 这些肿瘤在分类结构(章节安排)上紧随髓系肿瘤之后,以识别它们源自产生单核细胞/组织细胞/树突细胞系列的普通髓系祖细胞。新分类将克隆性浆细胞样树突细胞疾病纳入该类别,将滤泡树突细胞肉瘤和成纤维细胞网状细胞瘤单独分类,并新增Rosai-Dorfman病和ALK阳性组织细胞增多症类型。
3.2.1 浆细胞样树突细胞肿瘤 重新定义成熟浆细胞样树突细胞增殖(mature plasmacytoid dendritic cell proliferation,MPDCP),强调最近的数据表明与潜在的髓系肿瘤具有共同的克隆性。原始浆细胞样树突细胞肿瘤的诊断框架基本相同,重点是免疫表型诊断标准,见表8。

表8 原始浆细胞样树突细胞肿瘤的免疫表型诊断标准
3.2.2 树突和组织细胞肿瘤 近年来,人们发现组织细胞肿瘤通常表现出MAPK通路基因的突变,例如BRAF、ARAF、MAP2K1、NRAS和KRAS。第5版中新增实体ALK阳性组织细胞增多症则进一步集中在MAPK 通路上,这是介导ALK激活的信号通路之一。
