全自动凝血分析仪检测2种诱导剂诱导的血小板聚集试验参考区间的建立
2022-09-06寿玮龄陈倩徐雯马超超吴卫中国医学科学院北京协和医学院北京协和医院检验科北京00730新乡医学院第三附属医院检验科河南新乡453000
寿玮龄,陈倩,徐雯,马超超,吴卫(.中国医学科学院 北京协和医学院 北京协和医院检验科,北京 00730;.新乡医学院第三附属医院检验科,河南 新乡 453000)
血小板聚集试验(platelet aggregation test, PAgT)是评估机体血小板功能、监测抗血小板治疗效果等的重要指标。PAgT 光学法(light transmission aggregometry,LTA)的检测原理为通过在富血小板血浆(platelet rich plasma,PRP)中加入不同种类、不同浓度诱导剂,使血小板聚集,导致PRP 浊度变化,透光率增加,检测系统将浊度变化转变为电信号,连续记录血小板聚集曲线,从而得到血小板最大聚集率(maximum platelet aggregation rate,MPAR)等参数。LTA 与临床事件相关性较好,临床应用广泛,被称为血小板聚集功能检测的“金标准”[1-2]。二 磷酸 腺 苷(adenonisine disphosphate,ADP)和花生四烯酸(arachidonic acid,AA)是常用的2种诱导剂。根据美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)H58-A指南、国际血栓与止血学会(International Society on Thrombosis and Haemostasis,ISTH)共识等推荐,ADP 诱导剂常用终浓度为2、5和10 μmol/L,AA诱导剂常用终浓度为0.5 和1.0 mmol/L[3-6]。Sysmex公司CN系列和CS系列全自动凝血分析仪进行LTA,可减少手工加样误差,同时可使用多种诱导剂,检测用量少,一定程度上可减少患者采血负担。目前国内外尚无CN3000 及CS5100 全自动凝血分析仪的PAgT参考区间的报道。本研究按照CLSI EP28-A3c 文件要求[7],通过募集表观健康成年人,采用CN3000 和CS5100 全自动凝血分析仪进行不同终浓度ADP、AA 诱导的PAgT,用非参数法(non-parametric method)建立上述诱导剂诱导PAgT的MPAR值的表观健康人群参考区间。
1 对象与方法
1.1 研究对象 自2021年5月至12月,募集年龄18~70 岁表观健康人共134 例,按照18 ~30 岁、31~40岁、41~50岁、>50 岁分为4 个年龄段,男女比例分布均匀。入选标准:(1)体质指数(BMI)在参考区间18.0 ~28.0 kg/m2内;(2)女性未处于妊娠期及哺乳期(1年内);(3)无皮肤黏膜出血史及相关家族史;(4)未服用抗血小板药物及其他导致血小板功能异常的药物,包括吲哚美辛、酚妥拉明、双嘧达莫、青霉素类药物、肝素等;(5)近3 个月内未服用中药制剂;(6)无主要器官系统严重疾病,3个月内体检结果提示肝肾功能正常;(7)近2 周内无发热感冒等症状,近3个月未献血;(8)吸烟量每日不超过5支;(9)每日饮酒量小于100 mL;(10)近1个月内作息正常。
通过调查问卷了解研究对象姓名、年龄、BMI、饮食、医疗记录等基本信息;签署知情同意书后入组。排除标准:(1)入组至标本采集前不满足上述表观健康入选标准;(2)采血前24 h 摄入咖啡因,吸烟、饮酒及参加剧烈运动;(3)自愿退出;(4)标本采集处理后不满足LTA检测要求。
本研究已通过中国医学科学院北京协和医院伦理委员会批准(伦理审查批件编号:HS-2459)。
1.2 仪器与试剂 CN3000 全自动凝血分析仪、CS5100全自动凝血分析仪、XS-800i 全自动血细胞分析仪及配套血小板聚集功能ADP 检测试剂盒(批号:F1903231)、AA检测试剂盒(批号:FA0578)由日本Sysmex公司提供。试剂配制及分装、保存按照试剂说明书要求进行,ADP 终浓度分别为2、5和10 μmol/L,AA终浓度分别为0.5和1.0 mmol/L。
1.3 标本采集与处理 清晨采集研究对象空腹静脉血,0.109 mol/L 枸橼酸钠与静脉血按1 ∶9 比例混匀。采集标本时在针插入血管见回血后应立即释放止血带;采血过程不超过1 min。标本采集后室温静置30 min,以200×g离心10 min获得PRP,后将剩余标本以1 500×g 离心10 min 获取乏血小板血浆(platelet poor plasma,PPP)。离心后标本无黄疸、乳糜及溶血。
1.4 标本检测 计数PRP 中血小板数,剔除PRP血小板计数小于150×109/L的标本,PRP 血小板计数增高时不进行调整。20 μL 0.9%NaCl 溶液添加到140 μL PPP 中,660 nm波长下设置为透光强度基线;20 μL 诱导剂添加到140 μL PRP 中,测定660 nm波长下透光度的变化,计算MPAR。标本采集后4 h内完成检测。
1.5 重复性 检测10 个不同终浓度诱导剂诱导的MPAR,各取正常水平临床标本1 人份,每份标本重复检测11次,计算后10次检测结果的算术平均值、标准差和变异系数(CV)。
1.6 统计学分析 采用Excel、JMP Trail 16、SPSS 21.0软件和R语言4.0.5(reference intervals 1.2.0版本)进行数据分析。按照CLSI EP28-A3c 文件,首先进行数据正态性分布检验,对非正态分布数据进行“Box-Cox”正态转换后,使用Turkey 法对数据进行离群值剔除(低限,Q1-1.5×IQR;高限,Q3+1.5×IQR:IQR =Q3-Q1)。独立样本多组间比较采用Kruskal-Wallis H 检验,两组之间的比较用Mann-Whitney U检验;配对样本间比较采用Wilcoxon 符号秩检验,P<0.05 表示差异有统计学意义。按非参数方法计算参考区间,取数据分布的第2.5 百分位数和第97.5百分位数作为参考下限(lower reference limit,LL)和参考上限(upper reference limit,UL),并计算90%置信区间(confidence intervals,CI)。
2 结果
2.1 重复性 不同终浓度ADP 和AA诱导的MPAR的不精密度,以CV表示,均小于5.00%。见表1。
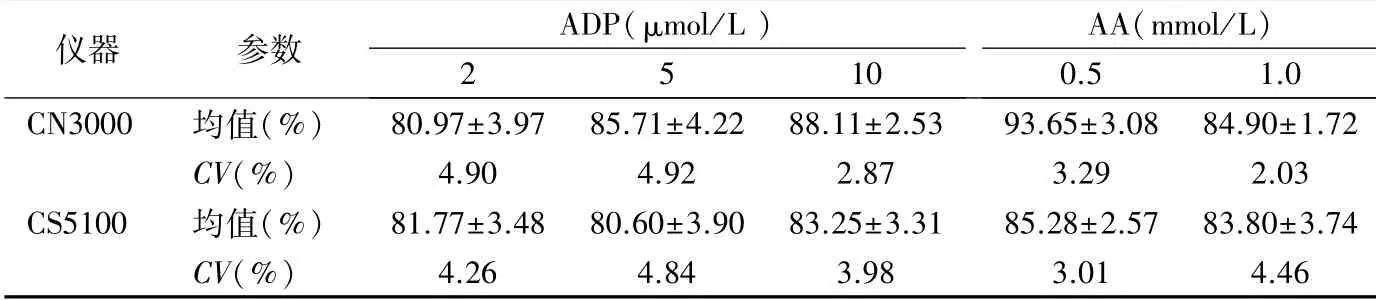
表1 不同终浓度ADP 和AA诱导的MPAR重复性
2.2 表观健康人ADP 和AA诱导的MPAR生物参考区间建立
2.2.1 数据分布 134 例入选者中男性69 例,女性65例,18 ~30 岁30 例,31 ~40 岁32 例,41 ~50岁36 例,>50 岁36 例;男女比例在各年龄段均匀分布。CN3000 和CS5100 系统上AA 终浓度0.5 mmol/L诱导的MPAR 分别剔除离群值3 个和4个,其他终浓度诱导剂诱导的MPAR各剔除离群值1个。PRP 血小板计数为(306.9±71.8)×109/L,所有PRP 血小板计数均大于150×109/L。
2.2.2 不同性别及年龄段间MPAR 比较 根据非参数秩和检验结果提示,2 个检测系统检测不同终浓度ADP、AA诱导的MPAR 在男女之间差异均无统计学意义(P均>0.05),见表2。2个检测系统检测不同终浓度ADP、AA诱导的MPAR在4 个年龄段间差异均无统计学意义(P均>0.05),见表3。

表2 不同性别间ADP 和AA诱导的MPAR(%)

表3 不同年龄段间ADP 和AA诱导的MPAR(%)
2.2.3 同系统不同终浓度诱导剂间MPAR 及不同检测系统间MPAR比较 2 个检测系统ADP 终浓度2、5 μmol/L(CN 系列Z =-2.634,P =0.001;CS系列Z =-4.996,P =0.000),CS 系列AA 终浓度0.5、1.0 mmol/L(Z =-3.361,P =0.008)之间MPAR差异有统计学意义。根据Wilcoxon 符号秩检验分析,除外AA 终浓度1.0 mmol/L(Z =-2.319,P =0.020),其他不同种类不同终浓度诱导剂诱导的MPAR在CN3000和CS5100 两系统间差异均无统计学意义(P均>0.05)。
2.2.4 ADP 和AA 诱导的MPAR 参考区间建立 取数据分布第2.5 百分位数和第97.5 百分位数作为LL和UL,表观健康人不同终浓度ADP、AA诱导的MPAR参考区间及90%CI结果见表4。

表4 表观健康人ADP、AA诱导的MPAR的参考区间
3 讨论
本研究中2 个检测系统不同终浓度ADP 和AA诱导的MPAR 重复性分别为2.87%~4.92%和2.03%~4.46%,与文献报道[8]基本一致,远低于试剂说明书正常标本最大聚集率的CV%≤20%的标准,满足临床检测需求。
与Platton 等[9]纳入42 例表观健康人在Sysmex CS2X00系统上采用第2.5和第97.5百分位数的结果相比较,本研究ADP 终浓度2 μmol/L 参考区间与其接近,但文献中ADP 终浓度5 μmol/L 和10 μmol/L 时生物参考区间分别是44%~98%和48%~106%,与本研究结果存在差异,本研究中AA 2个终浓度生物参考区间结果与该文献相比也存在差异;但本研究中AA 终浓度1.0 mmol/L 则与Stratmann等[10]在CS2100 系统上结果接近。王佳等[11]建立的ADP 终浓度2 μmol/L 手工法参考区间为(60.83±4.29)%,高于本研究中仪器法结果。试剂 说 明 书 ADP 终 浓 度 2 μmol/L 和 AA 1.0 mmol/L生物参考区间分别为59.1%~98.3%和63.2%~100%,其下限均与本研究结果存在差异。同时,本研究结果显示,AA 终浓度1.0 mmol/L 时MPAR在CN3000和CS5100 两系统间差异有统计学意义,提示不同检测系统参考区间存在差异,实验室建立或验证本实验室检测系统不同浓度诱导剂诱导的MPAR参考区间则十分重要。
CLSI H58-A文件显示,在不同年龄组间MPAR参考区间差异无统计学意义[3]。邓新立等[12]研究提示60 ~80 岁以上高龄人群中ADP 终浓度5 μmol/L诱导的MPAR结果差异无统计学意义,建议AA终浓度0.25 mmol/L诱导的MPAR在60~69岁人群参考区间为37.12%~88.47%,70 ~90 岁人群参考区间为37.45%~88.97%。本研究局限之处在于募集志愿者年龄20 ~66 岁范围内不同终浓度ADP 和AA诱导的MPAR 在年龄间差异无统计学意义,缺乏在低龄和高龄人群中PAgT 检测结果的参考区间的建立及验证。
