氨燃料及应用技术研究进展
2022-09-06许焕焕任霄汉朱子霖马春元
许焕焕,葛 一,李 强,任霄汉,朱子霖,马春元
(1.山东大学能源与动力工程学院,山东 济南 250061;2.山东大学热科学中心,山东 济南 250061;3.中国石油大学(华东)新能源学院,山东 青岛 266580)
随着现代化的高速建设,能源危机以及环境恶化日益加剧,能源结构低碳化已成为各国能源战略的共同选择,发展可替代煤、石油等化石燃料的可再生能源及其高效清洁燃烧技术迫在眉睫.长期以来,氢气被视为最有前景的可再生燃料之一,但氢气储存、运输等问题一直是制约氢气利用的技术瓶颈.氨(NH3)具有相对较高的氢含量,被认为是更安全经济的氢储运手段,逐渐受到人们越来越多的关注.此外,氨的体积能量密度与压缩天然气、甲醇等相近,且完全燃烧时,理想产物仅为水和氮气,是一种清洁的可再生替代燃烧,氨燃烧技术具有极大的应用前景.
在国际范围内倡导碳中和的今天,众多国家纷纷出台了将氨作为未来能源发展方向的战略布局.日本、美国、韩国、芬兰、澳大利亚等相继出台了船舶氨燃料报告,且日本已开启了一系列的氨燃料汽车研发工作,旨在加速氨燃料在航运业的能源比重.在电厂发电方面,日本在其第六版《能源战略计划》中提及到利用氨与天然气或煤粉混烧发电,日本电力巨头JERA的氨能混烧火电厂示范项目于2021年10月首次点火启动.此外,利用氨进行风电、光电等新能源储能,合成“绿氨”,并结合燃气轮机等火电站重新发电,不仅能够提升新能源的消纳,而且有利于实现火电深度灵活调峰,符合我国国家发展改革委与国家能源局2021年所提的“风光火(储)一体化”能源布局.
目前,氨被广泛应用于化工、农业等领域,相比之下,氨燃烧应用不是很成熟,对氨燃烧机理的认识仍需进一步研究.关于氨燃烧的研究大多集中于基础燃烧特性方面,除日本对内燃机、燃气轮机以及锅炉等燃烧装置中的氨燃烧展开了全面的工业探索和技术开发外,大部分的氨应用燃烧仍处于理论和实验室研究水平.相较于国外对氨燃烧研究,国内对氨燃烧研究起步较晚,清华、西交等开展了相关技术研究工作,但未见工业应用相关报道.本文从氨燃料的物化特性、燃烧特性、反应机理以及实际燃烧应用技术等方面阐述了氨燃料的研究进展,以期为氨燃料的后续研究提供参考.
1 氨的概述
1.1 物理特性
氨呈碱性、无色、气味较强.常温常压下呈气态,室温下压力升高至8~9个大气压即可被液化.氨的密度比空气轻,大气条件下可以很快扩散,这大大降低了泄露时发生爆炸与火灾的风险.单位质量NH3中含氢17.6%,可作为氢载体进行氢能的存储和输运.此外,液氨的体积能量密度相对较高,11.2 MJ/L,高于液氢(8.49 MJ/L)和压缩氢气(25 ℃,69 MPa时为4.5 MJ/L)[1].大气温度时氨气的相对毒性比汽油和甲醇高三个数量级左右,浓度超过300 ppm时即会危害人体健康,因此,氨的密封存储至关重要.此外,由于氨被归类为有毒化学品,因此必须进行规范化管理,以减轻其对人类和环境的危险.
工业上,氨主要通过哈勃-博施(Haber-Bosch)工艺在450 ℃~500 ℃、20 MPa的高温高压条件下合成,该生产工艺中,反应物为来自于煤、石油或天然气中的氢气和从空气中提取的氮气[2].与汽油、天然气、液化石油气、甲醇和氢气等常规燃料相比,氨成本最低[3].Wang等[4]提出可以利用太阳能等再生能源合成氨,该方法可以避免二氧化碳等温室气体的排放,借助N循环进行NH3化学能的转化利用,可取代化石燃料转化利用的C循环,最终避免能源利用过程中的碳排放.
1.2 氨的储存与运输
氨通常以液体的形式进行储存与运输,液氨密度较高,液态条件下储存氨通常采用两种方法:一是将温度保持在环境水平下逐渐增加其压力,例如在25 ℃下加压至0.99 MPa;另一种是将压力保持在大气水平的同时降低温度,即在大气压力下将氨冷却至-33.4 ℃,这种较为温和的条件允许在其体积密度保持不变的情况下采用轻质低成本的储罐.同时,液氨的特性与丙烷相似,用于丙烷储存运输的基础设施也可以用于液氨,因此氨储存的经济性较好.考虑到氨对部分金属,如铜、铜合金、镍浓度大于6%的合金的腐蚀危害,实际应用时可采用带聚乙烯内衬套的不锈钢或碳纤维储罐和管路[5].表1比较了氨与一些常规燃料的储存方式和成本[6].由表1可以看出,在所列燃料中,汽油的能量密度最高,而相应的单位能量成本也较高.氨的能量密度与压缩天然气、液化石油气和甲醇相比较为接近,而在单位能量成本上有着较大的优势.

表1 不同燃料储存方式及成本比较[6]
为了改善储存与运输的安全问题,研究人员不断研发新型储氨技术,如固体形式的氨储存方法[2,7-9].这种方法基本通过结合金属胺络合物(M(NH3)n)Xm,例如Mg(NH3)6Cl2,Ca(NH3)8Cl2等中的氨来进行.在Mg(NH3)6Cl2的情况下,发生的反应为
Mg(NH3)6Cl2→MgCl2+6NH3.
(1)
使用金属胺来储存氨的另一个好处是它们的毒性非常低,和汽油甲醇相当.在金属氨络合物中,氨的吸附和解吸过程是完全可逆的.只有在350 ℃或更高的温度下氨才会从多孔介质中释放,因此有效解决了氨的毒性问题,这同时也导致了氨释放成本的增加.
1.3 氨的利用方向
目前,氨的主要利用方向有以下两种:
(1)氢载体.如上所述,氢气在储存运输时的单位体积能量低并且存在复杂的安全问题.而氨的储存运输成本较低,安全性较高,并且单位体积氢原子含量高,在20 ℃和8.6 bar的条件下1 mol氨中含有1.5 mol的氢,储氢容量高达17.7(wt)%[10],这比当前最先进的金属氢化物储存方法高4倍,因而氨通常被用作携氢载体.
(2)作为化石燃料的替代能源.氨具有传统燃料的众多优点,如便于储运、高热值、高辛烷值、低污染等,其完全燃烧的产物是氮气和水,不含温室气体和其他碳类有害污染物.与氢气相比,氨燃料的最大优点是能量密度大、易液化、便于存储及携带;与汽油相比,其热值虽然稍低,但辛烷值远高于汽油,因而有利于增大压缩比来提高内燃机的热效率.
2 氨的燃烧特性
2.1 NH3的基本燃烧特性
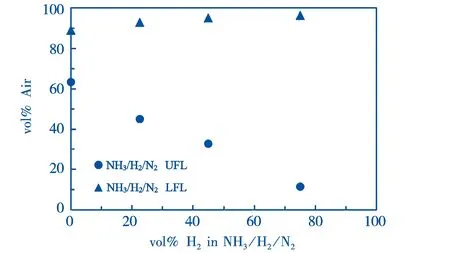
图1 400 ℃、1 atm下空气中NH3/H2/N2混合气可燃极限[11],UFL:富燃极限,LFL:贫燃极限
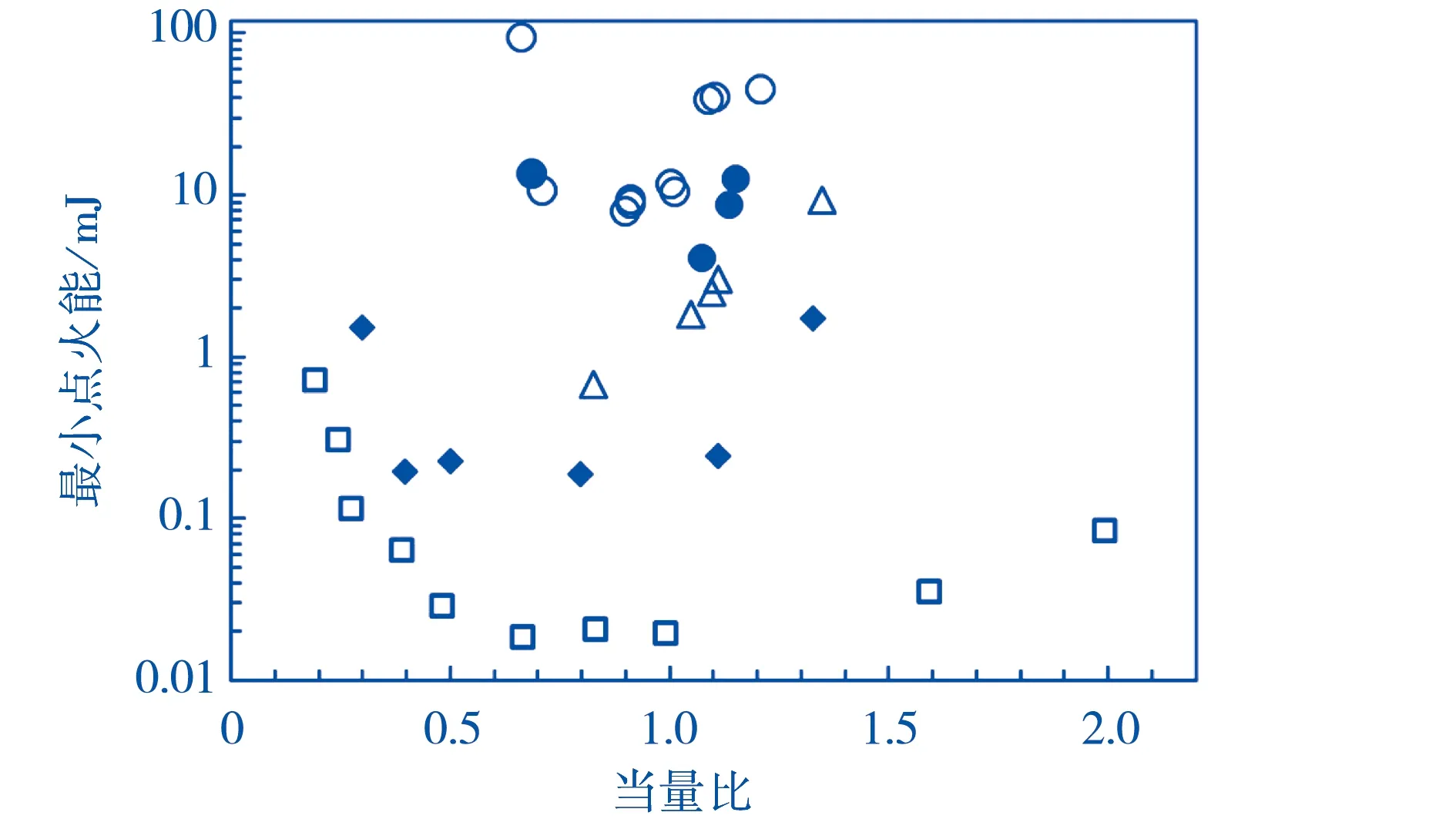
□:H2;○:NH3;●:NH3/H2/N2(8 vol% H2,2.8 vol% N2);△:NH3/H2/N2(18.5 vol%H2,6.1 vol% N2);◆:NH3/H2/N2(32.8 vol% H2,11 vol% N2)图2 环境温度和大气压力下空气中NH3、H2和部分NH3混合物的最小点火能[12,13]
本节通过整理文献报道的NH3燃烧数据,讨论了NH3的点火和燃烧特性,包括可燃极限、最小点火能、自燃温度以及层流火焰速度.纯氨可燃极限范围较窄,在大气压力下,400 ℃时空气中NH3/H2/N2的可燃极限随空气体积百分比和燃料混合物中氢气体积浓度的变化规律[11],如图1所示.从图1中可以看出,随着H2的加入,燃料混合物中H2的含量越高,燃烧极限越宽.氨燃料点火特性较差,氨燃烧往往比其他燃料需要更高的点火能.
Verkamp等[12]在较大范围内研究了在环境温度和大气压力下空气中NH3和NH3/H2/N2的最小点火能.空气中NH3、H2和NH3/H2/N2的最小点火能[12,13],如图2所示.从图2中可以看出,H2的最小点火能明显低于NH3,且增加NH3/H2/N2混气中H2的浓度可以降低最小点火能,且混合燃料可以在更大的范围内点燃.
层流火焰传播速度是一个重要燃烧特性参数,常被用于表征燃烧强度.在较大范围内比较了在室温和大气压力下空气中NH3、NH3/H2/N2和CH4的层流火焰速度[1],如图3所示.从图3中可以看出,H2的火焰传播速度最高,CH4的火焰传播速度次之,NH3火焰传播速度最小.增加NH3/H2混合物中的H2浓度可以显著提高火焰速度,Li等[14]认为这是因为H2浓度的增加提高了重要自由基(如OH、H和O)的生成速率,从而加快了NH3的燃烧反应速率.
2.2 NH3的化学反应机理及燃烧动力学
为了开发基于燃烧的氨利用技术,有必要通过氨燃烧现象深入了解详细的化学过程.早在20世纪60年代,人们就开始研究含氨火焰中的化学反应.1989年,Miller等[15]在对NH3/O2和NH3/H2/O2火焰在低压条件下(2.6 kPa和19.6 kPa)进行数值模拟和实验研究的基础上,首次完整描述了NH3燃烧的详细反应机理,主要反应途径如图4所示.理论动力学模型和实验数据之间的比较表明,在一定的温度、和压力范围内,Miller等的机理可以合理预测NH3的火焰结构,然而,该机理还没有在大气压或高压下进行验证.此外,研究发现,该机理不能准确预测在贫燃和富燃情况下NH3火焰中重要自由基(如OH、O、H和HNO)的形成,特别是在低压条件下[16,17].
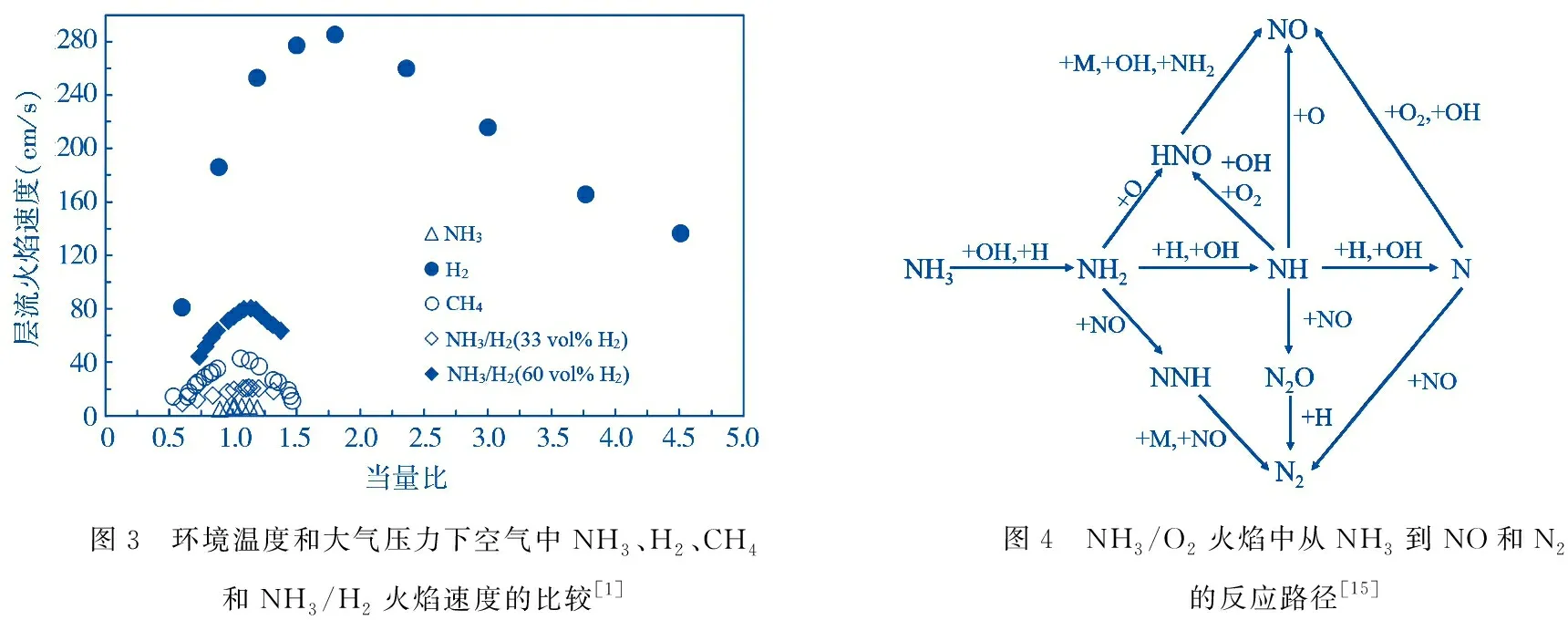
图3 环境温度和大气压力下空气中NH3、H2、CH4和NH3/H2火焰速度的比较[1]图4 NH3/O2火焰中从NH3到NO和N2的反应路径[15]
研究人员在图4所示的机理的基础上尝试了许多修改完善.例如,Bian等[16]修改了涉及NH2和NH基团的反应速率常数.Konnov等[18]开发了一种结合N2H3和N2H4反应的机制,以改进对低压(4.6 kPa)和贫燃(NH3/O2)火焰的火焰结构的预测.Lindstedt等[17]通过合并反应NH2+O来预测在更大的化学计量范围内的NH3/H2/O2和NH3/O2的火焰结构以及在低压下的火焰温度.上述的NH3氧化机制都是在低压下发展起来的,不能很好的预测在内燃机中遇到的高压条件下NH3点火延迟时间和层流火焰速度.最近,一些动力学机制被开发出来,试图预测高压下NH3的点火和燃烧特性[19].基于HCN氧化过程中迅速生成NO的机理[20],Mathieu等[19]通过激波管实验研究了氨在高温(1 560 K~2 445 K)和高压(约0.14 MPa、1.1 MPa和3.0 MPa)条件下的氧化,对涉及OH和N2O基团的基本反应进行了修改,结果显示能够更好的预测高压下NH2基团形成.Song等[21]在Miller机理的基础上,改进了包含NNH、NH2、OH、HO2和H2NO基团的基本反应,建立了一个新的机制.研究表明,氨在高压下氧化的主要途径为
(2)
终止链的主要步骤是NH2+NO=N2+H2O和NH2+NO2=N2O+H2O.Otomo等[22]通过修改NH2、NHO和N2H2基团的基本反应动力学常数,进一步改进了Song等的机理,可以很好的预测高压下NH3的点火延迟时间和层流火焰速度.

图5 在1.4 atm~30 atm压力和当量比为1的条件下,NH3/空气燃烧点火延迟时间的模拟和实验结果的比较[1]

图6 不同温度和压力下NH3/空气层流火焰速度的模拟和实验结果比较[1]
Lesmana等[1]计算了不同机理下NH3在不同温度和压力下的着火延迟和层流火焰速度,并与文献中现有的实验数据进行了比较,如图5和图6所示.从图中可以看出,Otomo机理[22]比其他的机理更好的预测了点火延迟时间和火焰速度,然而,Otomo机理在与内燃机应用相关的大范围温度和压力条件下的表现仍不尽人意.目前,氨燃烧的化学动力学模型仍有待进一步优化,已有的反应模型只能在特定的条件下较准确的预测氨火焰的速度和结构等特征.这些化学动力学模型为氨的燃烧提供了基础理论库,并对氨燃烧设备的开发和优化提供了理论指导.
2.3 氨燃烧NOx排放
尽管氨燃烧不造成CO2排放,却会带来严重的NOx问题.在其排放所有的污染物中,NO是导致光化学污染的主要产物,对生态环境和人体健康都有严重影响.其次,N2O是另一主要污染物,且N2O的温室效应比CO2高298倍[23].研究表明,氨燃烧的NOx排放不同于H2和常规碳氢燃料,在氨燃烧过程中,热力型NO不再占主要地位,燃料型NO成为主要来源[24].
为阐明氨燃烧过程中NOx排放特性和机理,国内外学者做了大量研究.西安交通大学Zhang等[25]实验研究了NH3/CH4/空气在预混旋流燃烧器上的NO排放特性,结果表明,当混合燃料中NH3的热值比率为0.5时,NOx排放量最高,并指出,为降低NOx排放,应该尽量在富燃且远离NH3掺混量=0.5的条件下燃烧.Glarborg等[26]发现,由于O、H和OH等促进NH2和NH通过HNO反应路径向NO的转化,含氨燃料燃烧时NOx排放随火焰中O/H自由基浓度的升高而增加.Okafor等[27]指出,在当量比0.8~1.1范围内,单级燃烧时NH3/CH4/空气NOx排放量超过5 000 ppmv,约为已报道的NH3/空气NOx排放量的两倍;而富燃-贫燃模式时,CH4/NH3/空气的NOx排放显著低于NH3/空气,这是因为NH3/CH4/空气混合物的火焰速度较高,保证了贫燃燃烧区内较低的NOx产量.清华大学Li等[28]对燃气轮机工作条件下NH3/CH4空气分级燃烧进行了化学反应器网络(CRN)数值模拟,结果表明,CH4中NH3的加入主要通过促进HNO途径使主反应区NOx排放急剧增加,由于氧气能够明显抑制HNO型NOx的生成,故通过改变当量比可实现NOx排放的有效调控,同时,他们指出,在富燃料条件下,通过HNO途径生成的NOx可与通过NHi等途径还原的NOx抵消,从而导致NOx总排放较低,这也给氨的富燃-贫燃技术提供了理论依据.
由此可见,分级燃烧技术及降低氨燃料NOx排放的有效手段,然而,富燃-贫燃技术也有弊端,富燃区伴随着不完全燃烧,如若在后续贫燃区内没有适当的燃烧组织,NOx排放达标也存在困难[28].故烟气脱硝技术仍会是氨燃烧NOx控制的最后一道技术保障.
2.4 氨与其他燃料的比较
为了更合理的利用氨燃料,有必要了解氨与传统燃料在燃烧方面的差异及其优缺点,以便能够针对更换燃料所带来的燃烧特性差异问题提出相应的改进方法.氨、氢气、乙醇、二甲醚、汽油和柴油等燃料的一些关键特性[1],如表2所示.

表2 氨、氢、乙醇、二甲醚、汽油和柴油燃料的热力学和燃烧特性[1]
具体地,NH3与其他燃料相比的优缺点可总结如下:
(1)优点
①能量密度高:NH3的体积能量密度与甲醇和二甲醚相当,比液氢的体积能量密度高33%;
②基于化学计量空燃比的热值相对较高:从上表中可以看出,每单位质量的化学计量混合物中NH3有着与汽油相当的低热值和高热值;
③高辛烷值:NH3的辛烷值非常高,具有良好的抗爆性能,是内燃机的良好燃料;
④易于储存和运输:液态NH3由于蒸汽压低、沸点高,相对于液态H2来说,其储存和运输容易得多;
⑤无碳燃烧:NH3燃烧产物不含含碳有害污染物,如CO2、CO、HCs、SOx和烃类燃料燃烧时不可避免地产生颗粒物.
(2)缺点
①气化潜热高:表1所示的燃料中,NH3汽化潜热最高,达1 370 kJ/kg.如果NH3以液体的形式注入发动机气缸,其将吸收大量的热量并蒸发.结果会导致明显的温降,降低燃烧温度;
②火焰传播速度低:NH3在大气压力和环境温度下的火焰速度相对较低,仅为7 cm/s,是表1所列的各燃料中最低的一种.汽油的火焰速度大约是NH3的6倍,这意味着当NH3应用于发动机时,很容易出现燃烧效率低和不完全燃烧的情况;
③最小点火能高:在所有燃料中,NH3最小点火能最高.因此,发动机点火需要较高的火花能量;
④点火温度高:NH3的点火温度高于其他燃料.因此,在依赖燃料自燃的情况下,NH3在发动机中点火是困难的;
⑤可燃极限窄:与H2相比,NH3的可燃极限要窄得多,在贫燃或富燃的条件下可能会导致失火;
⑥潜在的高NOx排放:与传统的汽油发动机相比,NH3燃料产生的NOx排放较高.
3 氨燃烧应用技术
目前,氨主要用作于农业肥料(约80%),其余20%用于食品生产、工业材料、制冷剂和添加剂[29].而氨的燃烧应用研究还尚显不足,需要进一步的研究.本节整理了近年氨在内燃机、燃气轮机以及燃料电池等方面的应用,简要介绍了氨与碳基燃料、氢气的掺混燃烧研究现状.
3.1 内燃机
与乙醇、甲醇、氢气和汽油/柴油混合燃料等其他替代燃料类似,氨具有较高的辛烷值(约为120),可以改善燃烧性能,减少诸如爆震等不良影响[30],因此以氨为燃料可以增加发动机的压缩比以提高输出功率,也可通过与碳基燃料或者氢气等燃料进行掺混燃料来改善氨的燃烧特性.
氨作为内燃机用燃料最早可以追溯到1882年,Gurney[31]开发了一种氨气作为燃料的驱动小型火车头的发动机.20世纪60年代中期,人们对氨作为内燃机燃料的应用进行了深入的研究[32,33].1970年-1980年在这一领域几乎没有进行研究和开发,关于这一时期的氨基发动机发展的文献很少.20世纪90年代,这一理念又被重新提起,自2004年在美国召开的第一次关于氨的会议开始,氨的研究再次掀起热潮.
文献研究表明,NH3可以通过三种方式作为内燃机的燃料,即(1)NH3作为单一燃料进行燃烧[34];(2)NH3在双燃料系统中与碳基燃料掺混燃烧[35,36];(3)NH3在进入内燃机燃烧之前先部分分解成H2和N2[34,35,37,38].然而,使用单一NH3燃料的火花点火式内燃机性能较差[34],而双燃料系统中产生大量的氮氧化物、一氧化碳和未燃烧的碳氢化合物排放[35,36].NH3分解燃烧法被认为是改善NH3燃料内燃机性能的最有效的方法.研究表明,为了获得良好的性能,氨需要至少裂解4w%~5w%的氢气.
基于热力学性能、系统效能、行驶里程、油箱紧凑性和行驶成本等因素,Zamfifirescu等[3,39]对氨作为内燃机可持续燃料的可行性进行了分析.研究表明,因为氨的火焰速度低,抗自燃性强,氨需要与其他燃料混合作为助燃剂.这与先前通常采用双燃料方法在内燃机发动机中进行氨燃烧[40,41]的研究相吻合.卡特彼勒公司参考了1937年以前的氨的专利,在2008年提交了一项以氨为燃料的发动机专利[42].在该专利中,氨作为主燃料,同时采用电力来补充机械动力,从而驱动一种新的动力系统,该系统能够提供良好的燃烧效率.
3.1.1 氨与碳基燃料掺混燃烧
如前文所述,将氨与其他燃料掺混燃烧是改善内燃机中氨燃烧的解决方案之一.研究发现,当氨与碳基燃料混合后,火焰速度、热释放速率与辐射强度都得到提高,且二氧化碳排放量也明显低于碳基燃料[43].因此,氨与碳基燃料的掺混燃烧对向无碳燃烧的过渡具有深远意义.
Grannell等[44,45]在研究中已经证明,使用氨掺混汽油燃料可以获得较高的综合性能.Reiter等[46]对现有的柴油发动机进行改进,采用氨掺混柴油作为燃料,取得了良好的效果.此外,掺混氨燃料的燃烧有较低的NOx排放,低于纯NH3燃烧的60%[47].科研人员还尝试了汽油/氨、乙醇/氨、硝酸铵/氨以及氨在纯氧中的燃烧,研究结果表明,这些掺混燃料能够在稳定条件下提供较高的输出功率,然而在实际应用中受到燃烧过程中的产物NOx的影响.
韩国能源研究所(KIER)开发的AmVeh是氨燃料发动机技术中十分有趣的新概念之一,如图7所示.研究人员通过增加一个控制系统以及去除氨可以腐蚀的含铜合金(尤其被称为“黄色金属”的高锌黄铜),对液化石油气-汽油装置进行了改造.该技术将现有的车辆改装,燃烧70%NH3和30%汽油的混合燃料[48].如果将该技术应用于韩国20%的车辆中,则每年可减少1 000万吨二氧化碳排放,这将极大有利于他们减缓气候变暖目标的实现.

图7 韩国运输用氨基发动机[48]
为了确定最佳运行参数,研究人员还对氨燃烧往复式发动机进行了数值模拟.Zhong等[49]采用CFD分析,建立了氨气和正庚烷的压缩比、进气特性和空气/燃料比的模型.结果表明:当压缩比为16∶1,入口空气温度为800 K时,氨混合燃料可以通过压缩着火.此外,随着正庚烷的增加,所需的点火温度从800 K降到360 K.Dincer等[50]总结了涉及综合余热回收、制氢和减排系统的柴油车用氨混合燃料的数据,文献中还考虑了相应的经济因素(例如碳税税率和燃料成本),并将其与传统的柴油电力机车在能源效率、热力学效率、燃油消耗、能耗和环境影响等方面进行了比较.结果表明,掺混50%氨的混合燃料能提高余热回收,并且能源效率和热力学效率都有一定的提高.此外,污染物(氮氧化物、CO、颗粒物、碳氢化合物)排放较少,温室气体排放量也显著减少了53%.
对于所有燃烧系统,尾气排放一直是研究人员关注的热点,也是制约燃烧系统发展的关键因素之一,掺氨燃烧系统也不例外.Ryu等[51]的研究描述了火花点火发动机中汽油-氨掺混燃烧的燃烧特性和直接喷射的尾气排放.研究发现,由于氨分子含氮量高,一氧化碳的排放量较少,而一氧化氮和碳氢化合物的排放量较高.尽管在排放方面存在较大的挑战,但是直接将氨与含碳燃料混合使用已被广大研究者证明在发动机燃烧中是可行的.
3.1.2 氨与氢气掺混燃烧
氢气具有燃烧速度高、扩散性好、点火能量低等特点,在氨中添加氢气能有效改善燃烧、提高燃烧速度以及拓宽可燃极限.而且NH3和H2掺混燃烧和纯NH3燃烧一样不会产生碳排放,因此,氨与氢气掺混燃烧是强化氨火焰以及无碳燃烧的有效途径.近年来,研究人员对氨与氢气掺混燃料的燃烧特性进行了大量的研究.
1967年,Starkman等[52]对氨燃料的重整进行了研究,发现氨氢气掺混燃烧中氢气的质量浓度必须在4%~5%以上,才能使氨燃料在内燃机中达到较好的性能,这一结论对氨氢气掺混燃烧的研究具有一定的指导意义.Frigo等[53]开发了一种新型装置,该装置能够将氨裂解成发动机所需浓度的氢气和氨气,研究证实了在氨燃料中加入氢气可以加快其燃烧速度.
在氨燃料发动机系统中,氢气可以通过催化重整装置从氨中获取,如图8所示[54].Ryu等[55]的研究表明,氨催化分解后产生的氢气与氨掺混燃烧,这不仅使得氨发动机的燃烧特性得到了较好的改善,还降低了废气排放,而且提高了发动机的功率,降低了气耗量.Comotti等[56]设计了一种制氢系统,该系统利用氨作为原料在钌基催化剂下分解得到氢气,再与氨混合在发动机中燃烧,结果表明,该系统能提供高达1.4 Nm3/h的氢气,且发动机运行性能较好.

图8 将NH3转化为H2的系统概念图[54]
Ezzat等[57]研发了一种新型的氨氢混合动力汽车,并评价了混合系统的可行性.研究结果表明,利用氨裂解(即氢气)回收的相当可观,分别为ICE和ICE-PEM系统的16.4%和13.1%.
在污染物排放方面,Westlye等[58]比较了使用NH3/H2混合燃料与纯汽油燃料时发动机的NOx排放情况.结果表明,燃用NH3/H2混合燃料时NO2排放比燃用汽油高,但NOx总排放量低3%~4%.他们提出可以借助未燃氨的裂缝机理和选择性催化还原(SCR)技术来控制NOx的排放.
3.2 燃气轮机
将氨用于燃气轮机的想法始于20世纪60年代中期,Solar公司和加州大学伯克利分校研究了一种250马力的T350单缸氨涡轮燃烧器[59],研究人员发现使用NH3蒸汽的发动机的性能与使用JP-4的发动机相似.
SPG Advanced Propulsion公司和Energy公司[59,60]是少数几家声称即将开发商用系统的公司之一,其提出的商用氨系统如图9所示.在一系列的研究基础上,对研制一种可靠氨燃烧技术所面临的主要挑战进行了总结:(1)较低的火焰回火性质和较慢的NH3动力学;(2)燃烧不稳定;(3)提高效率需要有良好的氨蒸发作保证;(4)提高火焰速度和燃烧速率所需的燃料裂解.

图9 SPG高级推力和能量试验台[59]
旋流器和火焰稳定器具有稳定燃烧,提高效率,减少氮氧化物排放的作用.爱荷华大学的Meyer等[61]对带有喷嘴、涡流稳定器和自维持热交换器的40 kW燃烧器中氨与其他分子的涡流稳定化燃烧进行了分析研究.发现使用旋流器可以实现不同浓度的氨、氢气和甲烷的燃烧稳定.在将氨和氢氧根混合的实验中,发现使用火焰稳定器不仅可提高燃烧效率,还可明显降低NOx排放,这可能是物质二次反应(NOx和未燃烧氨)的结果.
日本福岛可再生能源研究所开发了一种燃料柔性平台[62],如图10所示.用于燃烧可再生能源(如风能和太阳能)生产的液态氨,并将其与煤油结合在一个50 kW的微型燃气轮机中.该装置已被应用于原型副燃料燃烧室,并证明该装置燃用不同浓度氨煤油混合物的可行性.

图10 NH3/空气和NH3/CH4/空气燃气轮机发电实验装置[62]
在用氨取代煤油启动燃气轮机的研究中,研究人员发现当用NH3代替煤油的比例为38%和30%时,输出功率分别为17 kW和21 kW.然而,产生的NOx随着氨注入量的增加而显著增加,达到了600 ppmv的水平.目前,最好的解决方案是使用选择性催化转化器(SCR),可以将微型燃气轮机产生的NOx排放降低到10 ppmv[62-64].
Kurata等[65]比较了纯NH3和NH3/CH4混合气作为燃料的两种燃气轮机发电机组的性能及排放特性.结果表明,添加甲烷促进了氨的燃烧强度,提高了燃烧效率和热效率;随NH3燃料比例的增加,NO排放呈现先增加后降低的趋势,降低趋势这可能是由于残留的NH3会还原部分NO导致.Okafor等[66]采用先富燃后贫燃的方法来降低NH3/CH4微型燃气轮机的污染物排放,结果表明,燃气轮机在0.25 MPa条件下燃烧效率高达99.8%,NOx和CO排放分别低至49 ppmv和2 ppmv,N2O、HCN和NH3的排放浓度几乎为零.
Xiao等还提供了数据来确定使用氨/甲烷[67]和氨/氢气[68]混合燃料发电的潜力.结果表明,在工业装置中使用高压氨可以通过增加物质重组和压实火焰前缘来减缓NOx的产生.NUON等公司也开始了关于氨燃烧的计划,NUON与代尔夫特理工大学、质子风险投资公司、OCI Nitrogen公司、AkzoNobel公司、ISPT公司和特恩特大学合作,展开了“能源-氨”项目[69,70].2013年正式启用的Magnum-plant项目将燃煤电厂改造为绿色氨燃料设施,从而大幅减少二氧化碳的排放[71,72].西门子等跨国公司也已经制定了氨研发路线图,将可再生能源生产的绿色氨和水力发电定位为未来的能源载体,将其用于运输、加工或大功率发电.
2017年7月,Chugoku电力公司在水岛电厂进行了一系列试验[73],以450 kg/h的速度向155 MW的燃煤电厂添加氨.结果表明氨水的加入没有导致工厂的电力效率下降.按能量含量计算,氨的添加量占总燃料的0.6%~0.8%.在这个比率下,二氧化碳排放量明显减少.
3.3 燃料电池
最近,研究人员提出通过将氨注入氢燃料电池汽车中来使其更容易运行并降低成本.Wojcik等[74]首次将氨作为燃料电池(SOFC)的单一燃料进行分析,报告中表明,他们的试验可以在800 ℃是达到50 MW/cm2的功率密度.在最近的ARPA-E峰会上,Soloveichik对未来交通提出了的混合动力汽车的设想,这种混合动力汽车将插电式电池和燃料电池结合在一起.他介绍了各种可持续燃料的不同使用范围,强调了氨燃料利用的可能性.就行驶里程而言,60.6 L的氨气油箱可行驶756公里,几乎是相同体积的液氢(417 km)的两倍,相同体积的压缩氢(254 km)的三倍[75].此外,氨燃料电池还可用于从低温工艺流程中回收废气能量.Zhu等[76]报道,利用氨再生电池可以将低品位的热能转化为电能.同时和其他燃料电池一样,使用堆叠电池可以增加电流,这表明该技术可能是未来废物回收的一个很有前途的选择.
4 氨燃料面临的挑战及解决方案
内燃机、燃气轮机等是目前碳氢燃料大规模应用的主要燃烧装置,也应是低碳转型的重点实施对象.由于氨燃料的较低反应活性,其在上述燃烧设备上的全面应用仍面临巨大挑战,可总结为(1)氨较低的能量密度要求在保证相同的功率输出下消耗更多的燃料量;(2)低火焰传播速度大大削弱燃烧稳定性;(3)氨燃烧过程具有较大的NOx排放潜值.
为了解决氨燃料面临的挑战(1)和挑战(2),提高氨的燃烧稳定性和着火性能,常见的助燃措施有:将氨与其他燃料掺混燃烧,例如氢气[24,77],甲烷[67,78-82];提高初始燃烧温度[83];以及在富氧条件下燃烧[82,84].掺混燃烧也是现有内燃机、燃气轮机逐步实现由化石燃料向碳中和燃料转变的有效方法.通过以上方法,可以克服纯氨燃烧的低放热率、较差的火焰稳定特性和低燃烧效率等不足.
研究报道显示,NOx排放量随NH3燃料的添加发生变化,且当量比对NH3燃烧NOx排放影响显著.Kobayashi等[85]的研究表明,分级燃烧有助于实现NH3/空气非预混燃烧中的低NOx排放,并且大量研究证实了富燃-贫燃技术(Rich-Lean Two Stage Combustion)在氨燃烧中的低氮排放优势.利用富燃-贫燃分级燃烧模式,Okafor等[27]实现了NH3/CH4用于燃气轮机十分理想的燃烧特性(NOx排放49 ppmv,CO排放2 ppmv,N2O、HCN和NH3近乎零排放,以及高达99.8%的燃烧效率).富燃-贫燃技术即在第一燃烧区富燃以降低NOx生成以及提高燃烧稳定性,利用第二燃烧区的过量空气调节燃烧温度并保证燃烧完全.此外,研究人员还开发了新的燃烧策略,如轻度燃烧,即在低氧浓度和高强度湍流混合条件下的燃烧模式,可以实现高效燃烧和低排放[84].在极端工况和高污染物排放要求时,可以通过加装选择性催化还原(SCR)装置来控制NOx排放.如何提高现有的氨高效清洁燃烧技术在不同条件下的可靠性,以及实现该些技术的实际工程应用,是未来氨燃料广泛应用的重点研究方向之一.
5 结 语
可再生能源在应对当今全球面临的环境问题和能源危机等挑战时发挥着至关重要的作用.氨作为一种清洁的可再生替代燃料,具有能量密度高、安全可靠、存储方便和成本低廉等特点.本文综述了氨作为可持续燃料的可能性和优缺点,目前氨的燃烧是氨作为能源利用的最有效的方法之一.目前,国内外学者已对氨的基本燃烧特性包括火焰结构、点火性能和火焰传播速度以及污染物排放等展开了深入的研究,为氨燃料实际工程应用奠定了坚实基础.然而,与其他替代燃料相比,关于氨高效清洁燃烧技术的研究仍十分有限,且研究仍处于理论分析及实验室水平研究,实际工程应用有待进一步的推广验证和完善.另外,氨燃料的燃烧机理仍未完全理清,开发合适的氨燃烧化学动力学模型以及寻求最优的氨燃烧方式将很可能是未来研究的重点,氨燃料的研究任重道远.
