黔北麻羊毛色差异主要调控基因及其通路分析
2022-09-05孙宝盛肖贵榜杨玉能杨泓涛李世春邓位喜
孙宝盛,张 颜,肖贵榜,杨玉能*,杨泓涛,李世春,邓位喜*
(1遵义职业技术学院,贵州遵义 563006;2习水县富兴牧业有限公司,贵州遵义 563006)
0 引言
【研究意义】毛色是毛用、绒用和皮用畜禽品种的重要经济性状之一。毛色也是一种可利用的遗传标记(孟浩浩等,2014),是认定品种的主要条件之一(李晓锋等,2012;宋宇宁,2017;Saleh et al.,2021)。因此,探讨动物不同毛色的形成机制对于改善毛皮动物的经济性状和遗传育种等均具有重要意义。【前人研究进展】针对动物毛色形成机制的探索,目前已引起越来越多学者的广泛关注。哺乳动物的毛色是由黑色素细胞产生的2种不同类型黑色素,即真黑色素和褐黑色素的分布和比例所决定(鲍加荣等,2015;郭跃跃等,2017;刘海霞等,2021)。黑色素细胞产生的黑素小体是合成黑色素的唯一溶酶体细胞器(郑会芹,2010;杜站宇等,2016b),黑素小体经过一系列酶学反应最终生成黑色素。黑色素的生成可分为4个阶段,包括黑素细胞转移和成熟、黑素体形成、黑素颗粒转运及黑色素排出(李溯和丁劲松,2013)。黑色素合成后沉积于黑素小体内,形成均匀一致的成熟黑素颗粒,沿微管、微丝运输至黑素细胞的树突上,再通过细胞吞噬等作用转运至相邻的角质细胞(陈旭等,2020;刘海霞等,2021),随后被胞内的溶酶体降解,随表皮细胞脱落而排出(孟舒等,2006;杜站宇等,2016a)。黑色素的合成过程主要涉及3种酶,即酪氨酸酶(Tyrosinase,TYR)、酪氨酸酶相关蛋白1(Tyrosinase-related protein-1,TYRP-1)和酪氨酸酶相关蛋白2(Tyrosinase-related protein-2,TYRP-2)(宋康康,2007)。其中,TYR是黑色素合成的关键酶。黑色素生物合成是一个由TYR催化体内酪氨酸羟化而成的过程(陈清西和宋康康,2006)。黑色素小体内TYR活性较强时,酪氨酸被TYR羟化为多巴,多巴再被氧化成多巴醌(郑会芹,2010),经过一系列反应最终生成黑色素(郭跃跃等,2017),从而使畜禽的皮毛呈褐色或黑色(Peng et al.,2017);当TYR活性较低导致黑色素生成减少或缺乏时,皮毛则呈现白色(岳丹等,2021)。高莉等(2011)研究表明,棕色羊驼的基因表达量明显高于白色羊驼。除基因外,-和基因也是影响黑色素生成的重要候选基因(李丽莎等,2016)。黑素皮质素受体1(Melanocortin 1 receptor,MC1R)又被称为促黑素细胞激素受体(Melanocyte stimulating hormone,MSHR),属于G蛋白受体,当其与促黑色素细胞激素如α-促黑激素(α-melanocyte stimulating hormone,α-MSH)结合时,能激活膜上的环腺苷酸酶系统产生cAMP激活TYR,促进真黑色素的合成及黑色素细胞的增殖,进而调控毛色(FitzGerald et al.,2006;陈伟等,2012),即基因也是调控动物黑色素合成的重要基因。此外,α-MSH可通过激活黑色素生成的主要调节因子——小眼畸形相关转录因子(Microphthalmia-associated transcription factor,MITF),而提高酪氨酸活性,促进真黑色素合成(孟浩浩等,2014;Kumaris et al.,2018)。黑色素合成的关键信号通路包括MC1R/α-MSH、丝裂原活化蛋白激酶(Mitogen-activated protein kinase,MAPK)、磷脂酰肌醇-3-激酶/蛋白激酶B(Phosphatidylinositol 3-kinase/Akt,PI3K/Akt)及Wnt/β-连环蛋白(Wnt/βcatenin)等通路(赵美娟等,2019)。【本研究切入点】黔北麻羊是贵州省的三大优良地方山羊品种之一,受农业农村部农产品地理标志登记保护(翁吉梅等,2018;周志楠等,2020)。黔北麻羊具有肩部羊毛为黑色、腹部为白色的独特特征(罗卫星等,2010),因此分析黔北麻羊毛色特征形成的分子机制,可为探究动物毛色的形成机理提供参考依据,但至今对于贵州地方品种黔北麻羊毛色差异分子机制的研究很少,调控其毛色的主要基因和通路也有待进一步挖掘。【拟解决的关键问题】选取黔北麻羊肩部黑色羊毛和腹部白色羊毛的皮肤组织进行转录组测序分析,以期获得调控其毛色差异的候选基因和通路,为揭示黔北麻羊特征毛色的形成机制提供理论依据。
1 材料与方法
1.1 试验材料
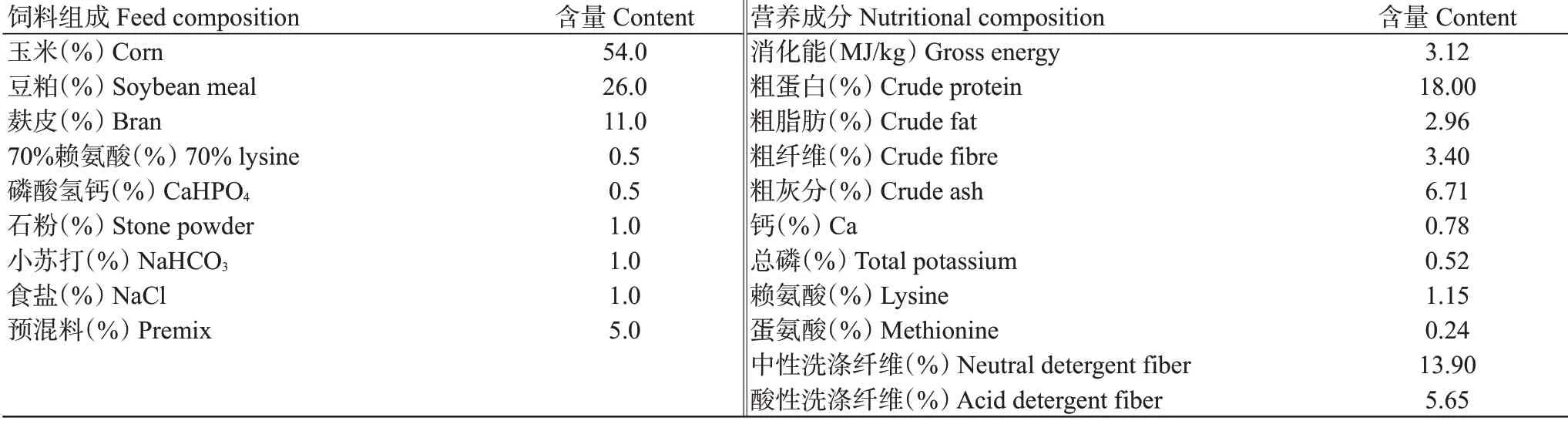
选取习水县富兴牧业有限公司的1岁黔北麻羊公羊(图1),共3只,体状相近。每只羊取肩部黑色羊毛下的皮肤组织块,每块皮肤组织为1个重复,共3个重复(Black-1、Black-2和Black-3),作为试验组;每只羊再取腹部白色羊毛下的皮肤组织块,共3个重复(White-1、White-2和White-3),作为对照组。黔北麻羊饲料由富兴牧业有限公司提供,其饲料组成及营养水平见表1。

1.2 饲养管理
黔北麻羊的日常饲养管理参照NY 5032—2006《无公害食品 畜禽饲料和饲料添加剂使用准则》。
1.3 样品采集
在3只黔北麻羊肩部黑色羊毛区各取1小块皮肤组织(刮毛),同样在腹部白色羊毛区各取1小块皮肤组织(刮毛),装入冻存管经液氮速冻后置于-80 ℃冰箱保存备用。为避免基因表达受扰乱,取样时不对皮肤进行局部麻醉。
1.4 转录组测序
转录组测序流程包括RNA提取、样品质检、文库构建和质控及上机测序等。(1)从-80 ℃冰箱取出皮肤组织提取RNA,并对样品RNA进行质检。(2)构建文库。以带有Oligo(dT)的磁珠富集组织mRNA,加 入Fragmentation Buffer 将mRNA 随 机 打 断,以mRNA 为 模 板,采 用 引 物Random Hexamers 合 成cDNA第一链;再加入缓冲液、dNTPs和DNA合成酶I合成cDNA第二链;利用AMPure XP Beads纯化双链cDNA,并进行末端修复、加ploy(A)尾和连接测序接头,以AMPure XP Beads选择片段大小;通过PCR富集构建cDNA文库。(3)文库质控。对cDNA文库的插入片段长度和有效浓度进行质控。(4)最后通过Illumina HiSeq4000测序平台进行测序。
1.5 生物信息学分析
(1)对测序数据进行质控,与参考基因组比对后进行基因表达水平分析。(2)使用主成分分析(Principal component analysis,PCA)评估组间的差异及组内样本生物学重复性。(3)然后进行基因表达差异分析。采用DESeq2进行差异表达基因(Differentially expressed genes,DEGs)筛选,筛选标准为表达差异倍数logFold Change>1、校正后的<0.05,绘制差异表达基因火山图;然后对差异表达基因进行GO功能注释分析:分别从生物学过程(Biological process)、细胞组分(Cellular component)和分子功能(Molecular function)三大功能对差异表达基因进行GO功能注释分析,并通过Fisher精确检验出差异表达基因与参考物种基因组的差异显著性,找到所有差异表达蛋白富集的功能类别。最后对差异表达基因进行KEGG信号通路富集分析:一是基于KEGG数据库对差异表达基因进行注释;二是以KEGG信号通路为单位和参考基因组为背景进行富集分析,以确定受到显著影响的代谢和信号转导途径。
2 结果与分析
2.1 黔北麻羊毛色样本主成分分析结果
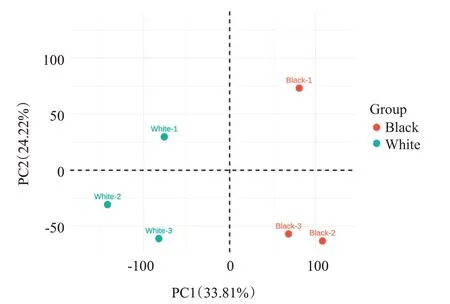
黔北麻羊不同毛色样本间的主成分分析结果显示,图2右侧的黑色羊毛试验组(Black)和左侧的白色羊毛对照组(White)间的样本明显分散,表明组间差异明显;但组内样本明显聚类,表明样品表达模式的相似度很高。可见,黔北麻羊不同毛色样本选择合理、可靠性高。
2.2 黔北麻羊毛色差异表达基因火山图
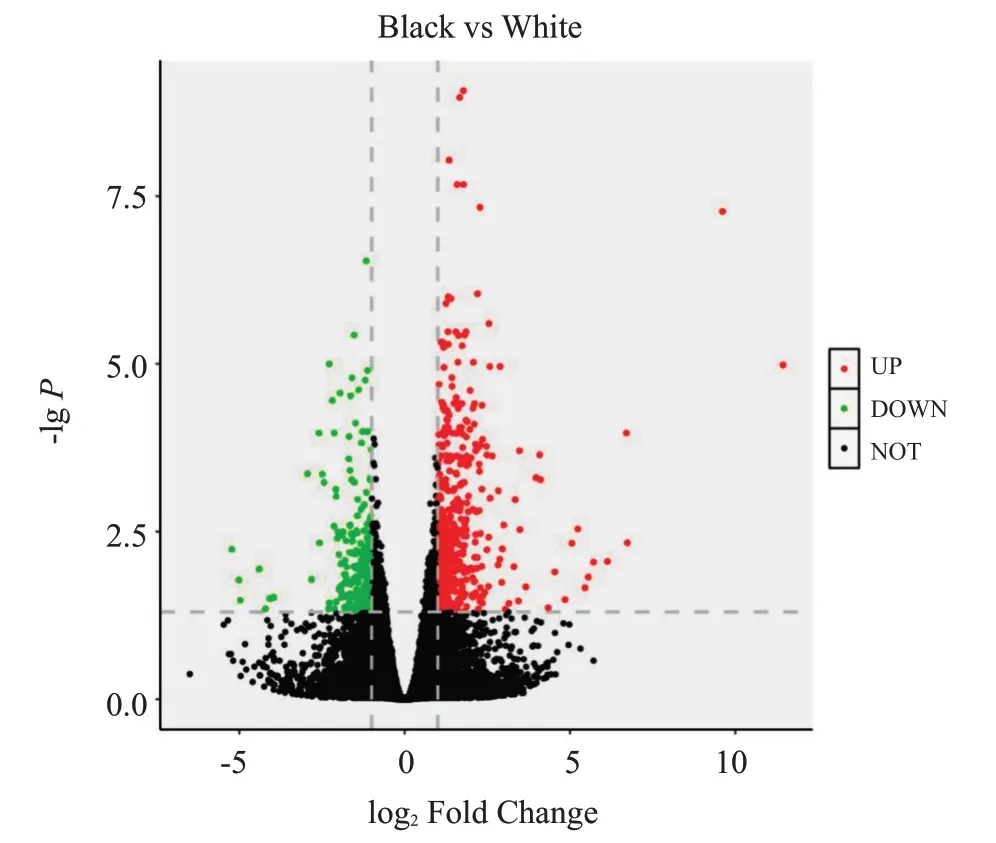
如图3所示,黔北麻羊毛色差异表达基因火山图能直观展示2个毛色组样品中差异表达基因的分布情况及其表达趋势。与白色羊毛对照组相比,黑色羊毛试验组存在509个显著上调表达基因(红色圆点)、195个显著下调表达基因(绿色圆点),其余基因表达差异不显著(黑色圆点)。
2.3 黔北麻羊黑白毛色组间与黑色素相关的显著差异表达基因
与白色羊毛对照组相比,在黑色羊毛试验组的509个显著上调基因中筛选获得5个与黑色素生成相关且表达差异显著(表达差异倍数logFold Change>1,校正后的<0.05)的基因,分别是基因、基因、基因、角蛋白19基因()和角蛋白79基因()(表2)。TYR和TYRP1催化酪氨酸合成黑色素;MC1R可与α-MSH结合,激活酪氨酸激酶形成黑色素,合成的黑色素转运至角质形成细胞进行存储,角质形成细胞进一步分化形成角蛋白。因此,黑色羊毛试验组、、、和等基因表达上调,意味着黑色素生成呈增长趋势。

2.4 显著差异表达基因GO功能注释分析结果
显著差异表达基因在生物学过程、分子功能和细胞组分三大GO功能中共注释到6081条功能条目。其中,生物学过程注释到4671条GO功能条目,有554条为显著富集;分子功能注释到881条GO功能条目,有145条为显著富集;细胞组分注释到529条GO功能条目,有69条为显著富集。相对于白色羊毛对照组,在黑色羊毛试验组显著富集的前30条GO功能条目(图4)中色素代谢过程(Pigment metabolic process)与黑色素合成代谢密切相关。
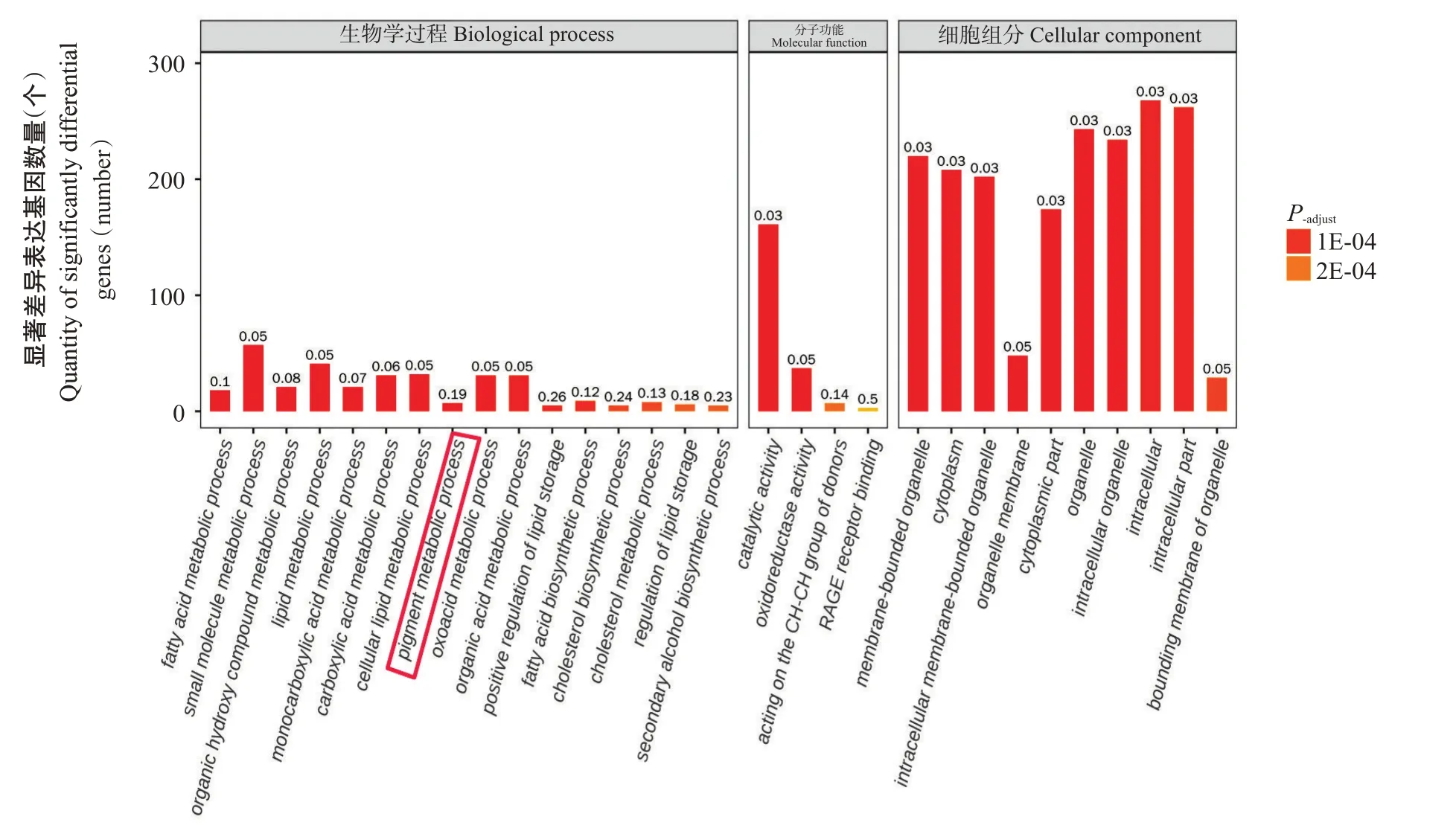
显著差异表达基因的GO功能注释分析还发现,在显著差异表达基因参与的生物学过程、分子功能和细胞组分三大GO功能注释分类中,除了上述色素代谢过程外,黑色羊毛试验组还显著富集于色素沉着(Pigmentation)、色素生物合成过程(Pigment biosynthetic process)、色素颗粒组织(Pigment granule organization)、色素颗粒膜(Pigment granule membrane)、黑素小体(Melanosome)、黑素小体膜(Melanosome membrane)、黑素小体组织(Melanosome organization)、黑色素生物合成过程(Melanin biosynthetic process)、黑色素代谢过程(Melanin metabolic process)、黑素细胞刺激素受体活性(Melanocytestimulating hormone receptor activity)、角质形成细胞分化(Keratinocyte differentiation)、角质形成细胞分化调节(Regulation of keratinocyte differentiation)等与黑色素形成相关的GO功能条目(表3)上,与黑色羊毛试验组中生成黑色素相关基因、和等显著上调的结果相对应。

2.5 显著差异表达基因KEGG信号通路富集分析结果
显著差异表达基因的KEGG信号通路富集分析结果表明,相对于白色羊毛对照组,黑色羊毛试验组显著富集在25条通路上,排名前20(图5)的KEGG信号通路分别是酒精中毒(Alcoholism)、甘氨酸/丝氨酸/苏氨酸代谢(Glycine,serine and threonine metabolism)、甘油酯代谢(Glycerolipid metabolism)、核黄素代谢(Riboflavin metabolism)、丙酮酸代谢(Pyruvate metabolism)、甘油磷脂代谢(Glycerophospholipid metabolism)、AMPK信号通路(AMPK signaling pathway)、ABC转运蛋白(ABC transporters)、丙酸代谢(Propanoate metabolism)、乙醛酸和二羧酸代谢(Glyoxylate and dicarboxylate metabolism)、丁酸代谢(Butanoate metabolism)、脂肪酸延伸(Fatty acid elongation)、过氧化物酶体(Peroxisome)、酪氨酸代谢(Tyrosine metabolism)、PPAR信号通路(PPAR signaling pathway)、缬氨酸/亮氨酸/异亮氨酸降解(Valine,leucine and isoleucine degradation)、脂肪酸降解(Fatty acid degradation)、脂肪酸代谢(Fatty acid metabolism)、脂肪酸生物合成(Fatty acid biosynthesis)及代谢途径(Metabolic pathways),以代谢途径(红色气泡)富集到的显著差异表达基因最多。值得注意的是,在黑色羊毛试验组显著差异表达基因富集的KEGG信号通路中,与黑色素生成密切相关的是酪氨酸代谢通路(红色框)。

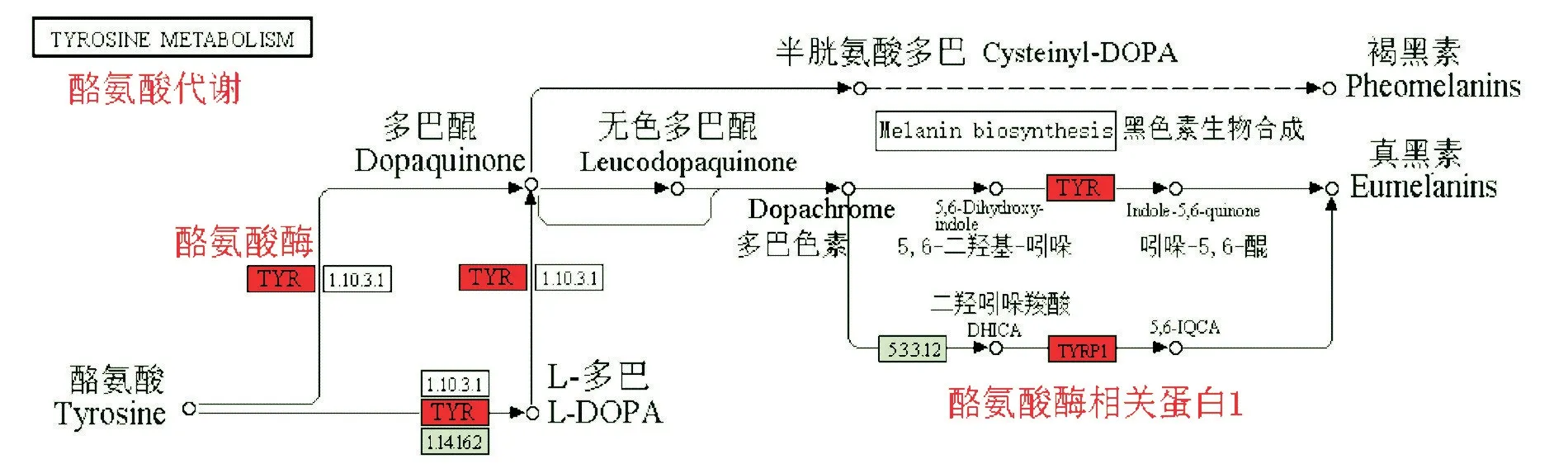
将显著差异表达基因标注到酪氨酸代谢通路(图6)中发现,TYR可催化酪氨酸→半胱氨酸多巴→褐黑素,也可催化酪氨酸→多巴醌→无色多巴醌→多巴色素,然后一条途径是生成5,6-二羟基-吲哚→酪氨酸酶催化生成吲哚-5,6-醌→真黑素,另一条途径是生成二羟基吲哚羧酸,再被TYRP1催化生成真黑素。相对于白色羊毛对照组,黑色羊毛试验组中参与黑色素生成通路的基因和基因表达显著上调(红色框),意味着黑色素生成增加。
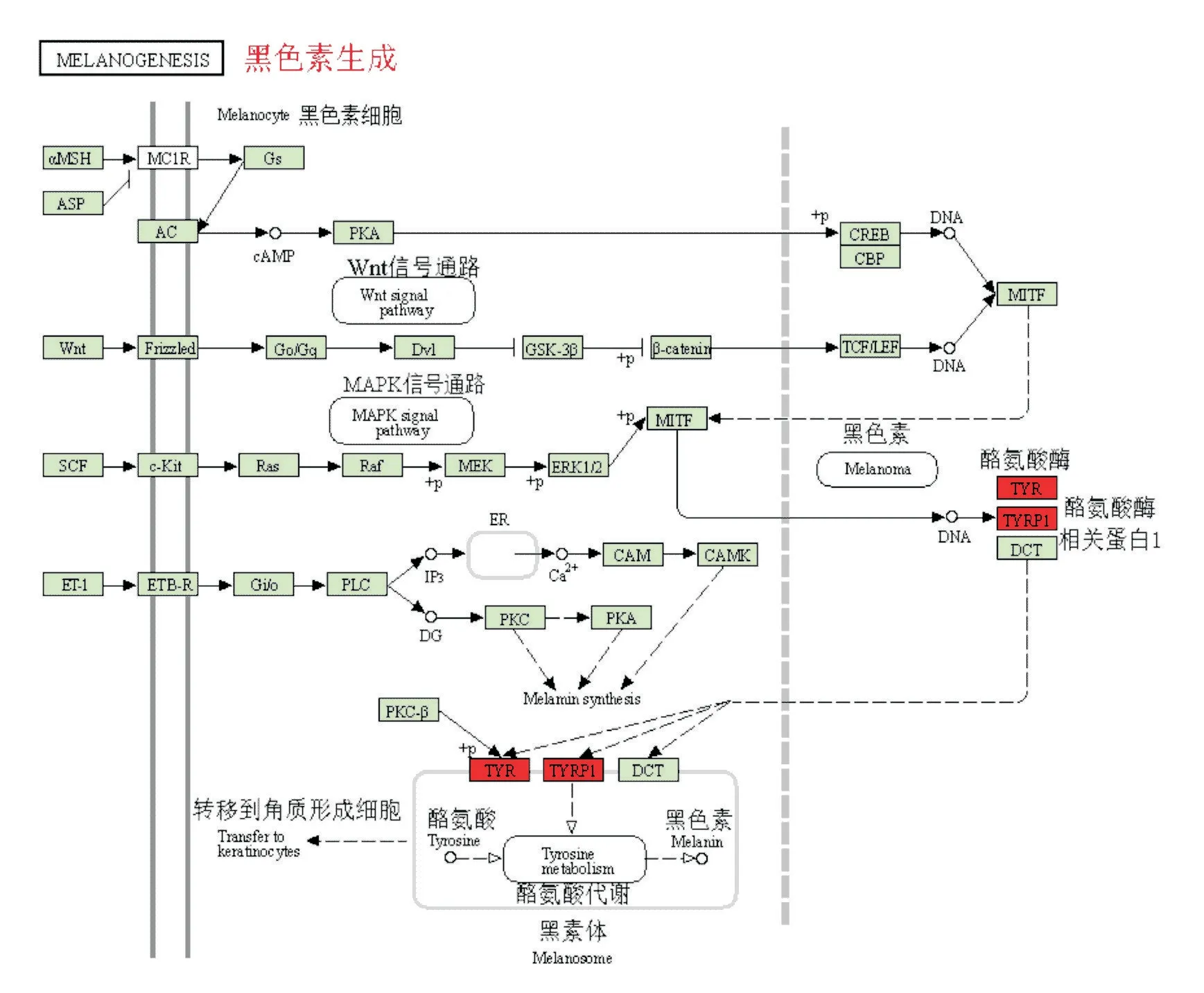
相对于白色羊毛对照组,黑色羊毛试验组中参与黑色素生成通路中的基因和基因上调(红色),但两组间参与黑色素生成(Melanogenesis)通路的Wnt/β-catenin、MAPK等信号通路富集程度均无显著差异,PI3K/Akt和MC1R/α-MSH等其他与黑色素生成相关的信号通路也不存在显著差异(图7)。说明Wnt/β-catenin、MAPK、PI3K/Akt 和MC1R/α-MSH等经典的黑色素生成信号通路并不是黔北麻羊生成黑色素的主要通路,而是酪氨酸代谢通路。
3 讨论
TYR是黑色素合成过程中的关键限速酶。黑色素的生物合成是由TYR催化体内酪氨酸羟化而启动一系列生化反应的过程(郑会芹,2010)。酪氨酸可通过膜的主动运输进入黑色素细胞内完成黑色素合成(李文等,2007),第一阶段是酪氨酸被TYR催化形成L-多巴,继而氧化生成多巴醌;第二阶段是多巴醌从2个不同途径生成真黑素和褐黑素(陈清西和宋康康,2006)。本研究中,黑色羊毛试验组的基因表达显著上调,催化酪氨酸合成多巴醌,增加黑色素生成。因此,基因应是黔北麻羊肩、腹部存在黑白毛色差异的主要调控基因之一。除TYR外,黑色素生成通路的关键酶还包括TYRP-1和TYRP-2等。基因是第一个被克隆获得的色素基因,对黑色素合成及黑色素细胞的发育、生存与功能均发挥重要调节作用(李丽莎等,2016),是影响羊驼黑色素生成的重要候选基因之一(高莉等,2010)。本研究结果也表明,相对于白色羊毛对照组,黑色羊毛试验组中的基因表达明显上调,进而加速催化二羟吲哚羧酸(DHICA)生成5,6-IQCA,最终增加真黑素生成。因此,基因也是影响黔北麻羊黑白毛色差异的重要基因。
基因是控制毛色形成的主要候选功能基因之一,与黑色素细胞的生成密切相关(付冬丽,2013)。MC1R与α-MSH的亲和力最高,MC1R/α-MSH是黑色素细胞接受机体激素调控的主要信号通路,对动物毛色形成起重要作用(任玉红等,2012)。α-MSH激活黑色素细胞膜上的MC1R和腺苷酸环化酶系统,ATP转变为cAMP,激活酪氨酸激酶,活化在糙面内质网及游离核糖体上合成的TYR(杨永升等,2004),而TYR催化黑素细胞从血液中摄取酪氨酸,经高尔基复合体变成多巴,多巴在黑素体内聚积到一定量后即释放黑色素(李秋玲等,2008)。本研究结果表明,与白色羊毛对照组相比,黑色羊毛试验组中的基因表达也显著上调,从而导致黑色素生成增加,即基因也是形成黔北麻羊黑白毛色差异的重要基因。
黑素细胞在黑素小体中合成黑色素并转运至周围的角质形成细胞进行存储,黑色素停留在这些角质形成细胞的细胞核上能发挥保护作用。在黑色素的生成过程中,角质形成细胞接受紫外线照射后释放的促黑激素(MSH)作用于黑素细胞表面的MSH受体,从而上调基因、基因和基因的表达(王秋枫,2003)。在本研究中,与白色羊毛对照组相比,黑色羊毛试验组的基因和基因呈上调表达,而角质形成细胞在分化过程中形成角蛋白,表明生成角蛋白的角质形成细胞及其黑色素明显增加,进而造成黔北麻羊肩、腹部的黑白毛色差异,与崔玉琮等(2017)研究发现角蛋白可激活羊驼皮肤黑色素细胞黑色素合成相关信号通路即促进黑色素合成的结论一致。
羊毛的毛色主要取决于黑色素的组成、数量和分布情况(郭跃跃等,2017),黑色素是在黑素小体中合成及贮存。本研究的GO功能注释分析结果表明,黑色羊毛试验组中的显著差异表达基因主要富集于黑素小体、色素沉着、色素生物合成过程、黑色素生物合成过程及角质形成细胞等与黑色素形成相关的GO功能条目上。黑色素的生成涉及以下KEGG信号通路:MC1R/α-MSH、PI3K/Akt、MAPK、Wnt/βcatenin及NO等(赵美娟等,2019;王歆悦等,2020;刘海霞等,2021;罗晓君等,2021)。但在本研究中,Wnt/β-catenin、MAPK、PI3K/Akt和MC1R/α-MSH等经典的黑色素生成信号通路及其参与的Melanogenesis通路在黑色羊毛试验组与白色羊毛对照组间的富集程度并无显著差异。值得注意的是,相对于白色羊毛对照组,黑色羊毛试验组中生成黑色素的酪氨酸代谢通路却明显富集,说明酪氨酸代谢应是黔北麻羊生成黑色素的主要通路,而非Wnt/β-catenin、MAPK等经典的黑色素生成信号通路。
4 结论
、、和等是调控黔北麻羊毛色的主要基因,酪氨酸代谢通路是调控黔北麻羊毛色的主要通路。、、和等基因的局部上调表达,激活酪氨酸代谢等信号通路而促使黑色素生成增加,是黔北麻羊肩部黑色羊毛和腹部白色羊毛存在差异的主要原因。
