老年CKD患者25(OH)D、SOST水平与OSP和跌倒风险的关系
2022-09-03张丽赵倩贾英杰毛慧辇皓然韩雪蒋晗微张秀娟
张丽 赵倩★ 贾英杰 毛慧 辇皓然 韩雪 蒋晗微 张秀娟
慢性肾脏病(chronic kidney diseases,CKD)是一种以肾脏结构和功能障碍为主要特征的慢性进展代谢性疾病,具有较高的患病率与死亡率[1]。有研究表明,增龄是CKD 发病的主要危险因素之一,其发病率随年龄增高而逐渐增加[2]。老年CKD 患者常因长期肾损伤及心血管疾病、心功能不全、高血压、糖尿病等多种合并症而引起骨代谢异常,导致骨转换、矿化异常,最终造成骨质疏松症(osteoporosis,OSP)[3]。维生素D(vitamin D,VitD)是体内调节钙平衡的主要激素,可经肝脏、肾脏酶的羟化作用形成25 羟维生素D[25⁃hy⁃droxy vitamin D,25(OH)D],可维持神经肌肉的协调作用,有助于降低跌倒风险[4]。骨密度(Bone mass density,BMD)是目前临床诊断和预测患者OSP 的常见方法,既往有研究显示,25(OH)D 水平与BMD 存在相关性[5]。骨硬化蛋白(Sclerostin,SOST)对骨形成具有负调节作用,参与调节骨重建过程[5]。本研究通过检测老年CKD 患者血清25(OH)D、骨硬化蛋白水平,分析其与OSP 和跌倒风险的相关性。
1 资料与方法
1.1 一般资料
选取2019年1月至2020年12月在承德市中心医院确诊的120 例CKD 患者,根据是否发生OSP 将患者分为OSP 组(n=33)和非OSP 组(n=87)。纳入标准:年龄≥65 岁,符合CKD 诊断标准[6];患者及家属了解知情并签署知情同意书。排除标准:合并严重心、肝、肾等脏器功能不全及其它免疫性相关性疾病;合并高血压、糖尿病或其他内分泌疾病者;妊娠期、哺乳期或长期服用避孕药者;近3 个月内服用过VitD;合并恶性肿瘤或心理、精神疾病者。本研究经医院伦理委员会通过。
1.2 研究方法
于入组次日清晨,采集所有入选者空腹静脉血5 mL,采用全自动生化分析仪(Hitachi 7600,日本日立公司)检验血钙(Ca)、血磷(P)、碱性磷酸酶(Alkaline phosphatase,ALP)、血清血肌酐(serum creatinine,SCr)、尿素氮(blood urea nitrogen,BUN)、白蛋白(albumin,ALB)水平;采用酶联免疫法(试剂盒由江西艾博因生物科技有限公司生产)检测25(OH)D、SOST 水平;采用全自动电化学发光仪检测血清全段甲状旁腺素(intact parathyroid hormone,iPTH)水平;采用美国双能X 线骨密度仪检测所有受试者L1~4、股骨颈、大转子部位;采用Morse 跌倒评估量表(Morse Fall Scale,MFS)对CKD 组患者跌倒风险进行评估。
1.3 观察指标
比较OSP 组与非OSP 组年龄、体质量指数(body mass index,BMI)等一般资料及不同部位BMD(L1~4、股骨颈、大转子)、血清25⁃(OH)⁃D、SOST水平,分析老年CKD 患者发生OSP 的影响因素。
OSP 评判标准[7]:参照中国老年学学会骨质疏松委员会(Osteoporosis committee of Chinese geron⁃tology society,OCCGS)中OSP 的标准,以BMD 下降25%为OSP。
跌倒风险评估[8]:采用MFS 量表,通过跌倒史、医学疾病诊断、行走辅助、静脉输液治疗、步行姿态和认知状态等6 个条目进行评分,以MFS 评分≥25 分为具有跌倒风险。
1.4 统计学处理
采用SPSS 18.0 统计学软件进行数据分析,满足正态分布且方差齐的计量资料采用()表示,采用两样本独立t检验,计数资料采用n(%)表示,采用χ2检验,采用Logistic 回归分析影响老年CKD患者OSP 和跌倒发生的危险因素;采用ROC 曲线分析血清25⁃(OH)⁃D、SOST 水平诊断老年CKD患者OSP 的价值;采用Pearson 相关性分析血清25(OH)D、SOST 水平与OSP、跌倒风险之间的相关性,P<0.05 提示有统计学意义。
2 结果
2.1 老年CKD 患者发生OSP 的单因素分析
OSP 组患者合并糖尿病发生率和血清SOST水平明显高于对照组,不同部位BMD 和血清25⁃(OH)⁃D 均显著低于对照组,差异有统计学意义(P<0.05)。见表1。
表1 老年CKD 患者发生OSP 的单因素分析[n(%),±s]Table 1 Univariate analysis of OSP in elderly patients with CKD[n(%),±s]
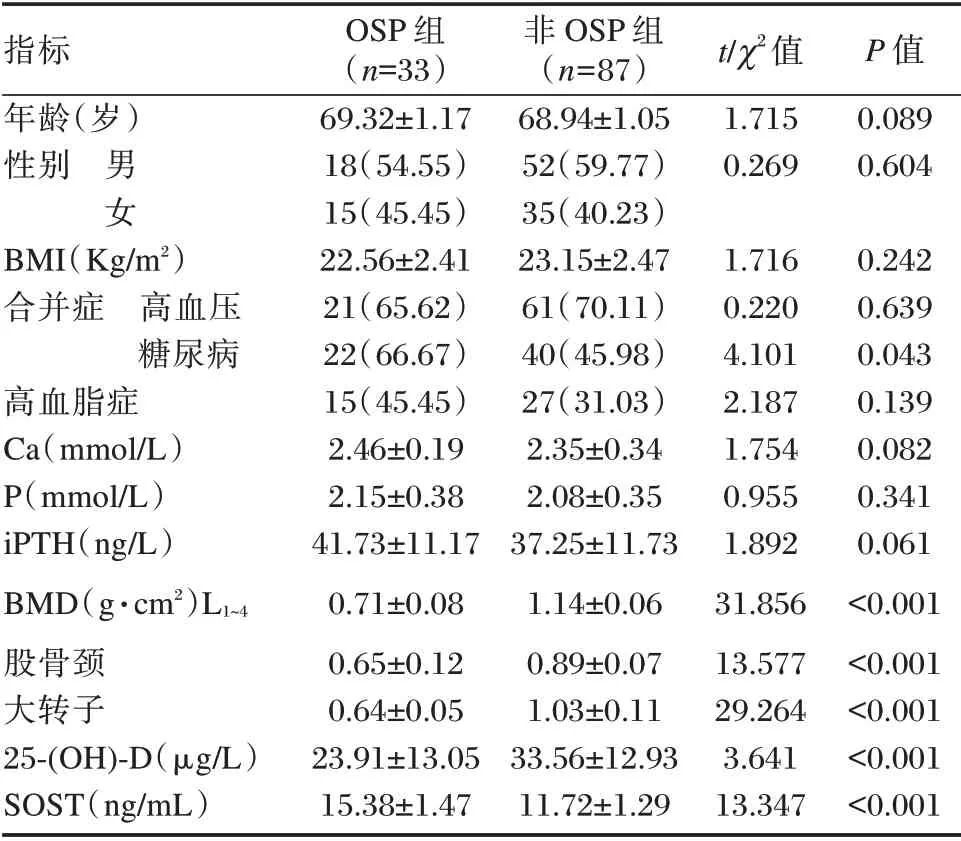
表1 老年CKD 患者发生OSP 的单因素分析[n(%),±s]Table 1 Univariate analysis of OSP in elderly patients with CKD[n(%),±s]
指标年龄(岁)性别 男女BMI(Kg/m2)合并症 高血压糖尿病高血脂症Ca(mmol/L)P(mmol/L)iPTH(ng/L)BMD(g·cm2)L1~4股骨颈大转子25⁃(OH)⁃D(μg/L)SOST(ng/mL)OSP 组(n=33)69.32±1.17 18(54.55)15(45.45)22.56±2.41 21(65.62)22(66.67)15(45.45)2.46±0.19 2.15±0.38 41.73±11.17 0.71±0.08 0.65±0.12 0.64±0.05 23.91±13.05 15.38±1.47非OSP 组(n=87)68.94±1.05 52(59.77)35(40.23)23.15±2.47 61(70.11)40(45.98)27(31.03)2.35±0.34 2.08±0.35 37.25±11.73 1.14±0.06 0.89±0.07 1.03±0.11 33.56±12.93 11.72±1.29 t/χ2值1.715 0.269 P 值0.089 0.604 1.716 0.220 4.101 2.187 1.754 0.955 1.892 31.856 13.577 29.264 3.641 13.347 0.242 0.639 0.043 0.139 0.082 0.341 0.061<0.001<0.001<0.001<0.001<0.001
2.2 老年CKD 患者发生OSP 的多因素分析
采用差异变量赋值,非OSP 组=0,OSP 组=1;无糖尿病=0,合并糖尿病=1。采用中位数法对Ca、BMD、25⁃(OH)⁃D、SOST 进行变量赋值,<中位数= 0,≥中位数= 1。经二分类Logistic 分析,血清25⁃(OH)⁃D 水平降低、SOST 水平升高均为老年CKD 患者并发OSP 诊断的独立因素(P<0.05)。见表2。
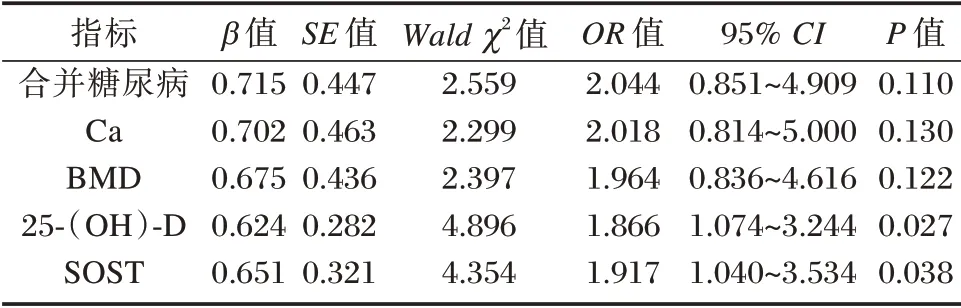
表2 老年CKD 患者发生OSP 的多因素分析Table 2 Multivariate analysis of OSP in elderly patients with CKD
2.3 血清25⁃(OH)⁃D、SOST 水平诊断老年CKD患者OSP 的ROC 分析
血清25⁃(OH)⁃D、SOST 水平联合预测老年CKD患者发生OSP 的曲线下面积(Area Under Curve,AUC)为0.870,敏感度为75.758%,特异度为89.655%,具有最好诊断价值(P<0.05)。见表3、图1。
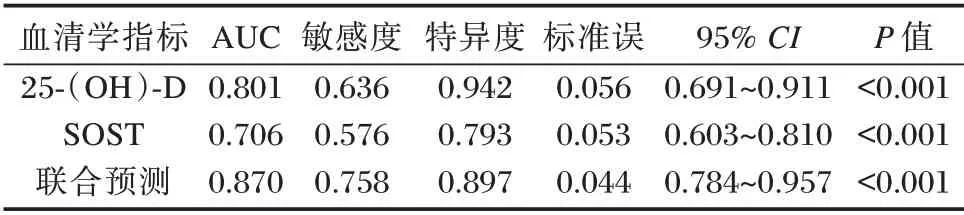
表3 血清25⁃(OH)⁃D、SOST 水平诊断老年CKD 患者OSP 的ROC 特征Table 3 ROC characteristics of serum 25⁃(OH)⁃D and SOST levels in the diagnosis of OSP in elderly patients with CKD

图1 血清25⁃(OH)⁃D、SOST 水平诊断老年CKD 患者OSP 的ROC 分析曲线Figure 1 ROC curves of serum 25⁃(OH)⁃D and SOST levels in the diagnosis of OSP in elderly patients with CKD
2.4 老年CKD 患者的跌倒风险
OSP 组MFS 评分为(65.13±3.24)分,明显高于非OSP 组的(41.05±2.98)分,差异有统计学意义(P<0.05)。
2.5 老年CKD 患者MFS 评分与血清25⁃(OH)⁃D、SOST 水平的相关性分析
老年CKD 患者MFS 评分与血清25⁃(OH)⁃D水平呈显著正相关(r=0.512,P<0.05),与血清SOST 水平呈显著负相关(r=-0.327,P<0.05)。
3 讨论
随着年龄增长,老年CKD 患者骨质形成减少、流失增加,伴VitD 生成不足,易导致患者并发OSP,进而引起患者肌肉反应能力减退,增加其跌倒风险[9⁃10]。既往研究显示,25⁃(OH)⁃D 可参与骨质代谢,影响BMD 和骨质结构,对OSP 的发生发展过程具有促进作用,而SOST 参与骨重建过程,在CKD 患者中呈现高表达状态[11]。
本研究结果显示,老年CKD 患者OSP 的发生与合并糖尿病、BMD、25⁃(OH)⁃D 及SOST 水平有关,二分类Logistic 分析结构显示,25⁃(OH)⁃D 水平降低、SOST 水平升高为老年CKD 患者并发OSP 诊断的独立因素,且ROC 分析显示血清25⁃(OH)⁃D、SOST 水平联合预测老年CKD 患者发生OSP 具有最好诊断价值。方纪林等人[12]研究显示,血清25⁃(OH)⁃D 水平可随CKD 病情进展而呈现降低趋势,且与骨代谢异常密切相关,血清25⁃(OH)⁃D 水平检测可作为CKD 患者并发OSP 的诊断参考。25⁃(OH)⁃D 是VitD 在肝脏特殊羟化酶催化作用下形成,是VitD 在体内的主要存储形式,在Ca、P 平衡和骨代谢中具有重要作用。SOST 可有效抑制骨代谢调节信号通路,在骨形成及代谢中发挥重要作用。赵敏等人[13]研究显示,血清25⁃(OH)⁃D 和骨代谢指标水平与OSP 的发生关系密切,且对其有较高的检测价值。本研究结果与以上研究结论基本一致,提示临床应重点关注血清25⁃(OH)⁃D、SOST 水平异常表达的老年CKD 患者,并积极采取有效干预措施,评估其OSP 发生的风险,指导临床治疗方案的调整。
本研究采用MFS 评分对老年CKD 患者的跌倒风险进行评价,结果显示OSP 组MFS 评分明显高于非OSP 组。Pearson 相关性分析结果显示,老年CKD患者MFS 评分与血清25⁃(OH)⁃D 水平呈显著正相关,与血清SOST 水平呈显著负相关。吴旭等[14]研究发现,血清25⁃(OH)⁃D 可促进骨生成,其水平值降低可引起骨质生成速度降低,同时加快骨质吸收速度,从而导致老年CKD 患者出现OSP,并增加其跌倒风险。Goto、Conley 等[15⁃16]研究发现,SOST 可抑制BMD,其血清含量升高提示机体BMD 明显降低,从而加速骨量丢失,促进骨质疏松症形成,增加患者跌倒风险。老年OSP 患者肾功能恶化时,低血清25⁃(OH)⁃D 水平可导致患者跌倒风险显著增加。本研究结果与上述研究基本一致,提示临床可通过检测老年CKD 患者血清25⁃(OH)⁃D、SOST 水平变化评估其病情进展情况,评估跌倒风险并采取措施帮助老年患者减少跌倒发生,降低OSP 性骨折风险,提高其生活质量。另外,临床可通过补充VitD 含量、降低SOST 水平从而达到促进患者病情改善的目的。
综上所述,老年CKD 患者血清25⁃(OH)⁃D、SOST 水平呈异常表达状态,血清25⁃(OH)⁃D 水平降低、SOST 水平升高均为老年CKD 患者并发OSP 的独立危险因素。
