基于网络药理学探讨黄芪、丹参治疗冠状动脉痉挛的活性成分与分子机制
2022-09-02曲信彦冯汝丽靳嘉麟徐江林曲文白
曲信彦,高 群,潘 熠,冯汝丽,谢 龙,靳嘉麟,徐江林,曲文白,马 征,林 谦
冠状动脉痉挛(coronary artery spasm,CAS)[1]是指由于冠状动脉舒缩功能异常而导致血管张力增加,出现部分或完全闭塞的病理生理状态,为多种缺血性心脏疾病的重要病理生理基础。冠状动脉痉挛可作为诱发心肌缺血的独立因素,冠心病病人合并冠状动脉痉挛时缺血症状进一步加重,多中心大型调查研究结果显示,缺血性心脏病病人麦角新碱激发试验阳性率达43%[2],提示冠状动脉痉挛这一机制广泛存在于缺血性心脏病人群中。冠状动脉痉挛多以心绞痛为主要表现,可归属于中医学“胸痹”范畴,其基本病机为气虚血瘀,临床上益气活血法治疗胸痹有较好疗效[3],黄芪(HQ)、丹参(DS)分别为益气、活血代表药物。
网络药理学是在系统生物学理论基础上,对生物系统进行网络分析,强调对信号通路的多途径调节,具有整体性、系统性的特点,与中医理论的整体观念具有较强趋同性[4]。本研究拟通过网络药理学,预测黄芪、丹参治疗冠状动脉痉挛的物质基础与作用靶点,从整体分析黄芪、丹参治疗冠状动脉痉挛的分子机制,为后续基础研究提供参考依据。
1 资料与方法
1.1 黄芪、丹参有效成分及相关靶点筛选 从中药系统药理学数据库与分析平台(TCMSP,https://tcmspw.com/tcmsp.php)[5]中检索黄芪、丹参有效成分,并设定口服生物利用度(oral bioavailability,OB)≥30%、药物相似性(drug-likeness,DL)≥0.18为阈值进行初步筛选,筛选所得有效成分通过化源网数据库(https://www.chemsrc.com)及PubChem数据库(https://pubchem.ncbi.nlm.nih.gov)校正名称,靶点结果通过UniProt数据库(https://www.uniprot.org)校正靶点信息,将有效成分、靶点导入CytoScape 3.8.2构建药物-有效成分-靶点网络图,使用其内置Network Analyzer工具对有效成分的网络拓扑参数(Degree为连接度,Betweenness为介度,closenesss为紧密度等)进行分析,依据分析结果筛选出主要有效成分。
1.2 冠状动脉痉挛相关靶点筛选 以“coronary artery spasm”为关键词,通过基因名片(GeneCards,https://www.genecards.org)数据库筛选治疗冠状动脉痉挛的相关靶点,并于在线人类孟德尔遗传数据库(OMIM,https://www.omim.org)及DRUGBANK数据库(https://www.drugbank.com)中检索相关靶点予以补充,合并3个数据库靶点后删除重复值。
1.3 黄芪、丹参-冠状动脉痉挛靶点核心靶蛋白相互作用(PPI)网络构建 将黄芪、丹参作用相关靶点及冠状动脉痉挛相关靶点导入在线作图工具VENNY 2.1(https://bioinfogp.cnb.csic.es/tools/venny/index.html)绘制Venn图并得到交集靶点,将交集靶点导入STRING平台(Version 11.0,https://string-db.org),生物种类选择“Homo sapiens”,以高置信度(high confidence)>0.700进行筛选,其余选项默认,得到PPI网络模型,将其以Tsv文件格式下载后导入CytoScape 3.8.2中进一步处理得到最终PPI网络模型,使用内置Network Analyzer工具对节点的网络拓扑参数进行分析并筛选出主要作用靶点。
1.4 黄芪、丹参-冠状动脉痉挛靶点功能与通路的富集分析 将筛选出的主要作用靶点导入Metascape平台(http://www.metascape.org/gp/index.html)[6],设置P<0.01,分析其基因本体功能及代谢通路并进一步进行富集分析。
1.5 分子对接 从TCMSP数据库下载主要有效成分的化合物结构,从PDB数据库(https://www.rcsb.org)下载核心靶点的蛋白质结构,使用Pymol 2.2.0软件和AutoDock Tools 1.5.6软件对化合物、蛋白质进行处理,使用AutoDock Vina软件对主要有效成分与核心靶点进行分子对接,通过得到的对接亲和力反映结合稳固性。
2 结 果
2.1 黄芪、丹参有效成分及相关靶点筛选 检索后初步获得黄芪化学成分87种、丹参202种,经OB、DL筛选并剔除无靶点化学成分后最终得到黄芪有效成分17个、作用靶点206个,得到丹参有效成分59个、作用靶点130个,删除重复值后得到有效成分76个、靶点239个详见表1。将有效成分、靶点导入CytoScape 3.8.2构建药物-有效成分-靶点网络图,结果见图1;使用其内置Network Analyzer工具对其网络拓扑参数进行分析,依据连接度值筛选出主要有效成分为槲皮素、山奈酚、木犀草素等,详见表2。

表1 黄芪、丹参有效成分

(续表)

(续表)

图1 药物-有效成分-靶点网络图

表2 主要有效成分
2.2 冠状动脉痉挛相关靶点 检索GeneCards数据库、OMIM数据库、DRUGBANK数据库并筛选、去除重复值后共获得冠状动脉痉挛相关靶点2 153个。
2.3 黄芪、丹参-冠状动脉痉挛靶点PPI网络构建 将筛选得到的黄芪、丹参作用靶点与冠状动脉痉挛疾病靶点导入在线作图工具VENNY 2.1后得到黄芪、丹参-冠状动脉痉挛共同靶点144个,进一步将靶点导入STRING平台,得到黄芪、丹参-冠状动脉痉挛靶点PPI网络模型,将其以Tsv文件格式下载后导入CytoScape 3.8.2中进一步处理,结果见图2,节点颜色及大小反映该靶点Degree值,依据Degree≥22(2倍中位数)筛选出主要靶点,包括蛋白激酶B1(AKT1)、肿瘤抑制蛋白P53(TP53)、白细胞介素6(IL6)等,详见表3。

图2 黄芪、丹参-冠状动脉痉挛靶点PPI网络图

表3 黄芪、丹参-冠状动脉痉挛主要作用靶点

(续表)
2.4 黄芪、丹参-冠状动脉痉挛靶点功能与通路的富集分析 将主要作用靶点导入Metascape平台,设置P<0.01,分析其基因本体GO(gene ontology,GO)功能及代谢通路并进一步富集分析,在GO注释分析结果中,其参与的生物学过程主要为血管生成(angiogenesis)等,分布的细胞组件主要为膜筏(membrane raft)等,参与的分子生物学功能主要为细胞因子受体结合(cytokine receptor binding)等,详见图3、表4~表6;京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)通路富集分析结果主要为晚期糖基化终末产物(AGE)-糖基化终末产物受体(RAGE)信号通路(AGE-RAGE signaling pathway in diabetic complications)及流体剪切应力与动脉粥样硬化(fluid shear stress and atherosclerosis)等,详见图4、表7。

图3 GO注释柱状图

表4 主要生物学过程

表5 主要细胞学组分
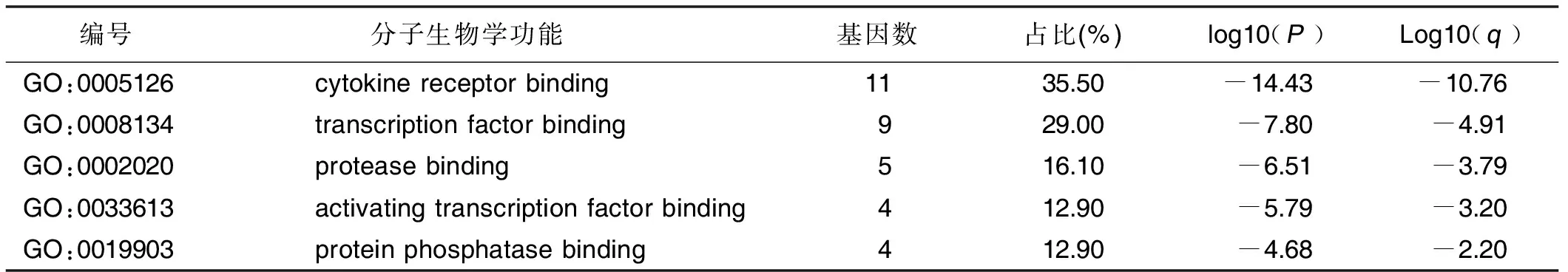
表6 主要分子生物学功能

图4 KEGG主要富集通路气泡图

表7 主要富集通路
2.5 分子对接 将主要有效成分槲皮素、山奈酚、木犀草素与核心靶点AKT1、TP53、IL6分别进行分子对接,得出平均对接亲和力为-32.604 kJ/mol,提示主要有效成分与核心靶点间具有较强的结合力。详见表8。

表8 分子对接结果
3 讨 论
冠状动脉痉挛是由于冠状动脉舒缩功能异常而导致血管张力增加,进而使冠状动脉血管出现部分或完全闭塞的病理生理状态,其作为单一因素诱发的各类心绞痛、心肌梗死及无症状性心肌缺血等称为冠状动脉痉挛综合征[7],而合并冠状动脉固有狭窄时可进一步加重缺血症状[2],是各类缺血性心脏病不可忽视的病理生理基础。研究显示,冠状动脉痉挛的主要发病机制包括血管内皮细胞功能障碍及血管平滑肌细胞的收缩敏感性升高等[8],其中血管内皮细胞功能障碍主要与一氧化氮(NO)、内皮素(ET)、血栓素A2(TXA2)及前列环素I2(PGI2)等血管舒缩物质的合成与分泌障碍相关[9],而血管平滑肌细胞的收缩敏感性升高主要与蛋白激酶C(PKC)[10-11]和Rho激酶(ROCK)[12]相关,但其具体调控机制仍有待进一步研究。
临床上冠状动脉痉挛发作时多以心绞痛为主要表现,属中医“胸痹”范畴,其病机多属本虚标实,本虚以心气亏虚为主,标实多见血瘀,兼有寒凝、痰阻等,临床上以益气活血法治疗胸痹心痛常有较好疗效[13],黄芪、丹参作为常用益气活血药,其治疗冠心病所致胸痹心痛机制研究相对较多[14],但通过干预冠状动脉痉挛进而改善缺血机制尚不确切。
本研究通过网络药理学筛选出黄芪、丹参治疗冠状动脉痉挛可能的主要有效成分为槲皮素、山奈酚、木犀草素等。槲皮素为常见黄酮类化合物,具有舒张血管[15]、降压[16]、抗心肌缺血[17]、改善缺血再灌注损伤[18]等心血管保护作用;研究发现,槲皮素可通过激活蛋白激酶B(AKT),上调内皮型一氧化氮合酶(eNOS)表达,进而释放更多的NO使冠状动脉舒张[19];亦有研究认为其可通过抑制冠状动脉平滑肌L型钙通道从而舒张冠状动脉[20]。山奈酚、木犀草素等亦有舒张冠状动脉的作用[21-22]。
涉及的核心靶点为AKT1、TP53、IL6等,AKT1为重要的信号转导枢纽,在心血管疾病中发挥重要作用[23],AKT1的激活可介导eNOS合成更多的NO进而使冠状动脉舒张[24],其对血管内皮细胞及平滑肌细胞的增殖、迁移等方面亦有重要影响[25];TP53的过表达可抑制血管内皮功能[26],亦有研究认为内源性TP53对血管平滑肌细胞具有保护作用[27],其影响冠状动脉痉挛机制有待进一步研究; IL6为重要炎性因子,可对血管内皮细胞功能产生不利影响[28]。
涉及的主要通路为AGE-RAGE信号通路,晚期糖基化终末产物(advanced glycation end products,AGEs)为持续高血糖状态下一系列糖基化反应的最终产物,其与RAGE结合后激活一系列下游通路,调控eNOS、PKC等,对血管内皮细胞及平滑肌细胞功能造成影响[29-31]。流体剪切应力与动脉粥样硬化亦为重要通路,AKT在其中通过调控内皮细胞eNOS活性对平滑肌细胞舒缩产生重要影响[32-34]。
分子对接结果提示,主要有效成分与核心靶点间具有较好的对接亲和力,进一步验证了黄芪、丹参对冠状动脉痉挛的调控作用。
综上所述,本研究通过网络药理学初步确定了黄芪、丹参治疗冠状动脉痉挛的主要有效成分为槲皮素、山奈酚、木犀草素等,核心靶点为AKT1、TP53、IL6等,涉及的主要通路为AGE-RAGE信号通路及流体剪切应力与动脉粥样硬化通路等,为后续的基础研究提供了指导。
